食物过敏是指过敏原蛋白引起的异常或过强的免疫反应,从免疫学机制而言,可以将食物过敏反应分为4 种类型,即:免疫球蛋白(immunoglobulin,Ig)E介导的I型超敏反应、II型细胞毒性超敏反应、III型免疫复合型超敏反应以及T细胞介导的迟发性超敏反应。目前可以从广义的角度将食物过敏分为IgE介导和非IgE介导两大类,其中以IgE介导的食物过敏反应最为常见。IgE介导的过敏反应是指过敏原与特异性抗体形成复合物后,与细胞(如肥大细胞、嗜碱性细胞)相结合,随后细胞释放组胺、5-羟色胺及白三烯等大量活性介质[1],这些物质作用于组织与器官,引起局部或者全身性的过敏反应。诱发非IgE介导的食物过敏所需食物量较大,临床表现为一系列 胃肠道紊乱,如过敏蛋白刺激产生的结肠炎、乳糜泻等主要由非IgE介导的过敏反应引起[2]。据统计,食物过敏的患病率在成人中约为5%,儿童由于自身免疫器官发育尚未成熟,过敏性疾病的患病率约为8%[3]。虽然一些儿童过敏患者随着年龄增长可自愈,但大部分过敏反应会伴随患者终身[4]。食物过敏原是指能使机体产生过敏反应的抗原分子,一般为蛋白质或者糖蛋白。过敏原蛋白主要通过食物摄入,少数过敏原蛋白气化后由呼吸道吸入[5]。 大多数食物过敏原具有极高的稳定性,不仅耐高温高压,同时耐水解、耐消化[6]。例如鸡蛋中的主要过敏原卵白蛋白经过烘烤和煮沸后,近紫外光谱学检测结果显示其三级结构未发生明显变化[7],原因在于其含有较多二硫键,形成的高度稳定性结构不容易被降解以及失去活性[8]。采取恰当的方法可以部分降低过敏原的致敏性,目前食品过敏原的消减技术主要有化学法、物理法和微生物发酵法[9-10],由于微生物发酵法对食品风味、质地破坏程度小而得到了更多关注,但目前相关的微生物资源还十分有限,同时微生物的分子机制和菌株特异性以及临床试验效果方面还需要进一步阐述。因此目前避免食用过敏原仍然是保护过敏人群健康的唯一有效手段[11], 国外一些发达国家要求对食品生产过程中的潜在过敏原进行标识,例如美国、日本以及欧盟等国家对致敏物质清单和食物过敏原标识方式管理等方面都有详细的 说明[12-14]。而我国对食物过敏原的标签法规和标准要求还在起步阶段,对过敏原的标识也没有采取强制的规定[15]。 事实上,食品标签难以对食品在生产、运输和存储过程中由于交叉污染产生的过敏原进行标注[16],此外食品行业过度使用预防标签会限制消费者对商品的自由选择,因此利用适当的检测技术来验证过敏原标签的准确性,并评估食物过敏的潜在风险具有重要意义。
本综述介绍了8 类常见致敏食品中主要过敏原的结构与致敏特点,对常用的食物过敏原方法以及现阶段一些新兴的检测技术进行了综述,并对检测方法未来的发展方向进行展望,期望能对促进食物过敏原检测方法的开发提供参考。
1 食品中常见过敏原
含有过敏原的食品高达170余种,其中最主要的食品有8 种,分别为大豆、小麦、坚果、花生、牛奶、鸡蛋、鱼类、甲壳及贝类,引起约90%的过敏反应[17]。食品中过敏原结构与致敏特性的明确有助于过敏原检测技术的开发,从而有助于推动过敏原的标识及相关法规的建立。常见食品中的主要过敏原的结构与致敏特性如表1所示。
表1 食品中主要过敏原及致敏特性
Table 1 Major food allergens and allergic symptoms caused by their ingestion
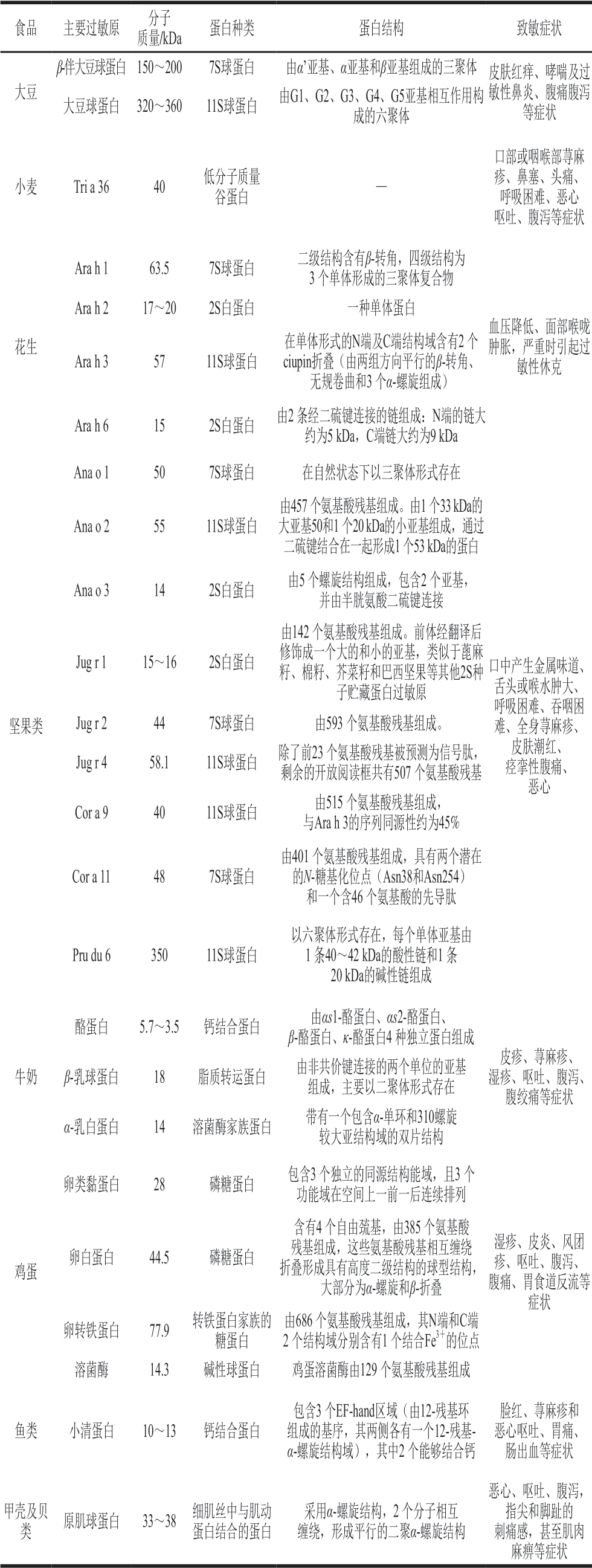
注:—.无相关报道。
食品 主要过敏原 分子质量/kDa 蛋白种类 蛋白结构 致敏症状大豆β-伴大豆球蛋白 150~200 7S球蛋白 由α’亚基、α亚基和β亚基组成的三聚体 皮肤红痒、哮喘及过敏性鼻炎、腹痛腹泻等症状大豆球蛋白 320~360 11S球蛋白 由G1、G2、G3、G4、G5亚基相互作用构成的六聚体小麦 Tri a 36 40 低分子质量谷蛋白 —口部或咽喉部荨麻疹、鼻塞、头痛、呼吸困难、恶心呕吐、腹泻等症状Ara h 1 63.5 7S球蛋白 二级结构含有β-转角,四级结构为 3 个单体形成的三聚体复合物Ara h 2 17~20 2S白蛋白 一种单体蛋白花生 在单体形式的N端及C端结构域含有2 个ciupin折叠(由两组方向平行的β-转角、无规卷曲和3 个α-螺旋组成)Ara h 6 15 2S白蛋白 由2 条经二硫键连接的链组成:N端的链大约为5 kDa,C端链大约为9 kDa Ara h 3 57 11S球蛋白血压降低、面部喉咙肿胀,严重时引起过敏性休克Ana o 1 50 7S球蛋白 在自然状态下以三聚体形式存在由457 个氨基酸残基组成。由1 个33 kDa的大亚基50和1 个20 kDa的小亚基组成,通过二硫键结合在一起形成1 个53 kDa的蛋白Ana o 3 14 2S白蛋白 由5 个螺旋结构组成,包含2 个亚基,并由半胱氨酸二硫键连接Ana o 2 55 11S球蛋白由142 个氨基酸残基组成。前体经翻译后修饰成一个大的和小的亚基,类似于蓖麻籽、棉籽、芥菜籽和巴西坚果等其他2S种子贮藏蛋白过敏原Jug r 2 44 7S球蛋白 由593 个氨基酸残基组成。Jug r 4 58.1 11S球蛋白 除了前23 个氨基酸残基被预测为信号肽,剩余的开放阅读框共有507 个氨基酸残基Cor a 9 40 11S球蛋白 由515 个氨基酸残基组成,与Ara h 3的序列同源性约为45%Jug r 1 15~16 2S白蛋白坚果类口中产生金属味道、舌头或喉水肿大、呼吸困难、吞咽困难、全身荨麻疹、皮肤潮红、痉挛性腹痛、恶心Cor a 11 48 7S球蛋白由401 个氨基酸残基组成,具有两个潜在的N-糖基化位点(Asn38和Asn254)和一个含46 个氨基酸的先导肽Pru du 6 350 11S球蛋白以六聚体形式存在,每个单体亚基由1 条40~42 kDa的酸性链和1 条20 kDa的碱性链组成酪蛋白 5.7~3.5 钙结合蛋白 由αs1-酪蛋白、αs2-酪蛋白、β-酪蛋白、κ-酪蛋白4 种独立蛋白组成牛奶 β-乳球蛋白 18 脂质转运蛋白 由非共价键连接的两个单位的亚基组成,主要以二聚体形式存在α-乳白蛋白 14 溶菌酶家族蛋白 带有一个包含α-单环和310螺旋较大亚结构域的双片结构皮疹、荨麻疹、 湿疹、呕吐、腹泻、腹绞痛等症状卵类黏蛋白 28 磷糖蛋白 包含3 个独立的同源结构能域,且3 个功能域在空间上一前一后连续排列鸡蛋含有4 个自由巯基,由385 个氨基酸残基组成,这些氨基酸残基相互缠绕折叠形成具有高度二级结构的球型结构,大部分为α-螺旋和β-折叠卵转铁蛋白 77.9 转铁蛋白家族的糖蛋白卵白蛋白 44.5 磷糖蛋白湿疹、皮炎、风团疹、呕吐、腹泻、腹痛、胃食道反流等症状由686 个氨基酸残基组成,其N端和C端 2 个结构域分别含有1 个结合Fe3+的位点溶菌酶 14.3 碱性球蛋白 鸡蛋溶菌酶由129 个氨基酸残基组成鱼类 小清蛋白 10~13 钙结合蛋白包含3 个EF-hand区域(由12-残基环组成的基序,其两侧各有一个12-残基-α-螺旋结构域),其中2 个能够结合钙脸红、荨麻疹和恶心呕吐、胃痛、肠出血等症状甲壳及贝类 原肌球蛋白 33~38 细肌丝中与肌动蛋白结合的蛋白采用α-螺旋结构,2 个分子相互缠绕,形成平行的二聚α-螺旋结构恶心、呕吐、腹泻,指尖和脚趾的刺痛感,甚至肌肉麻痹等症状
1.1 大豆
大豆引发的过敏为IgE抗体介导的速发型过敏反应,会损害患者的皮肤系统、呼吸系统以及消化系统,引发荨麻疹和皮疹等皮肤病,呼吸障碍、呼吸急促、哮喘等呼吸道疾病,腹痛、腹泻等消化道症状,甚至会导致过敏人群发生过敏性休克[18]。世界过敏原数据库收录数据显示,引起过敏反应的大豆过敏原43 种,但大多数过敏反应由两种主要过敏原蛋白引起,即大豆球蛋白和β-伴大豆球蛋白。β-伴大豆球蛋白是由α’亚基、α亚基和β亚基组成的三聚体,大豆球蛋白是由包括G1、G2、G3、G4、G5在内的5 个亚基组成的六聚体,组成这两种过敏蛋白的各亚基具有免疫原性且蛋白结构稳定,在自然状态下难以被破坏[19]。
1.2 小麦
小麦中蛋白含量占10%~15%,按其在不同溶剂中的溶解度不同主要分为4 类:清蛋白、球蛋白、醇溶蛋白和麦谷蛋白,这些蛋白成分是小麦中的重要营养物质,同时也是小麦过敏原的主要来源[20]。与小麦过敏相关的疾病主要有小麦运动激发过敏症、接触性荨麻疹、特异性皮炎、面包师哮喘症、恶心呕吐以及腹泻等[21],大多数小麦过敏涉及的是轻度反应,在某些特殊情况下也会导致生命危险。世界卫生组织/国际免疫学会联合会过敏原命名小组分委员会已经提供了13 种小麦过敏原,包括Tri a 14、Tri a 18、Tri a 19、Tri a 20、Tri a 25、Tri a 26、Tri a 36、Tri a 37、Tri a 41~Tri a 45[11]。其中,Tri a 14是一种非特异性脂转移蛋白,是引起面包师哮喘症和鼻炎的主要过敏原;Tri a 19 被认为是主要的小麦过敏原,是导致小麦运动激发过敏症的主要过敏蛋白[22];Tri a 25是一种硫氧化蛋白,有研究表明硫氧化蛋白可以缓解过敏反应,因此对于Tri a 25是否为过敏原尚存争议;Tri a 36是引起食物过敏的主要蛋白,是一种低分子质量的麦谷蛋白,有研究表明重组Tri a 36比 Tri a 19在小麦食物过敏诊断中具有更高的敏感性[23]。
1.3 坚果类
能够引起过敏反应的坚果类食物主要包括杏仁、腰果、核桃、榛子、开心果、巴西坚果等,过敏人群食用后,会出现胸闷、咽喉痛,呼吸困难以及恶心、胃痉挛,呕吐腹泻等症状。坚果一般作为植物的种子或者果实,因此大多数坚果蛋白属于3 种保守的种子贮藏蛋白,包括2S白蛋白、7S豆球蛋白和11S豆球蛋白[24]。 2S白蛋白属于醇溶蛋白超家族,此家族中的植物源性过敏原具有低分子质量和序列中含有多个半胱氨酸残基的特征。通常,8 个半胱氨酸参与建立4 条链内的二硫键,构成蛋白质三维结构所必需的α-螺旋。醇溶蛋白超家族的大多数过敏原由于其结构小而紧凑,对热、pH值和胃肠道酶具有高度耐受性。多种坚果中的蛋白成分属于2S白蛋白,如巴西坚果(Ber e 1)、 核桃(Jug r 1)、榛子(Cor a 14)、腰果(Ana o 3)、开心果(Pis v 1)。另外两种种子贮藏蛋白7S豆球蛋白和11S豆球蛋白属于Cupin超家族。7S球蛋白通常为三聚体蛋白,其亚基分子质量为40~80 kDa,7S球蛋白的氨基酸序列不包含半胱氨酸,因此缺乏二硫键,蛋白的稳定性较弱。11S球蛋白是成熟的三聚体蛋白,每个亚基由分子质量在30~40 kDa之间的酸性亚基和20 kDa左右的碱性亚基组成,两个亚基都由二硫键连接。属于这两类蛋白的坚果过敏成分有核桃(7S球蛋白Jug r 2、11S球蛋白Jug r 4)、腰果(7S球蛋白Ana o 1、11S球蛋白Ana o 2)、榛子(7S球蛋白Cor a 11、11S球蛋白Cor a 9)。此外,其他坚果类中的主要过敏原也经常引起人体过敏反应,如杏仁过敏原Pru du 6、山核桃过敏原Car i 4、榛子果仁过敏原Cor a 9、巴西坚果过敏原Ber e 2、腰果过敏原Ana o 2、开心果过敏原Pis v 2/5、核桃过敏原Jug n/r 4等[25]。由于坚果类食物众多,新的坚果类食物过敏原可能还会被持续发现。
1.4 花生
花生常引起食物过敏反应,过敏症状包括血管性水肿、低血压、腹痛到危及生命的哮喘和过敏性休克等[26]。 目前花生中已鉴定出16 种蛋白质过敏原,并将其命名为Ara h 1~17,由于Ara h 4与Ara h 3的序列重复率大于90%,因此2012年Ara h 4被重新命名为Ara h 3.0201,将其与Ara h 3作为相同的过敏原[27]。50%以上过敏患者血清IgE检测结果表明,最常见的花生过敏原为Ara h 1~3和Ara h 6。这4 种过敏原都是种子贮藏蛋白,Ara h 1属于种子贮藏蛋白中的7S球蛋白,Ara h 3属于11S球蛋白,而Ara h 2和Ara h 6都属于2S白蛋白。研究表明Ara h 2和 Ara h 6比Ara h 1和Ara h 3更耐高温和蛋白酶,可能是由于存在较多二硫键,导致了过敏反应的持久性[28-30],花生过敏被多数国家认定为最严重的食物过敏之一。
1.5 牛奶
牛奶含有丰富的蛋白质,主要包括酪蛋白和乳清蛋白两类,分别占乳蛋白总量的80%和20%。乳蛋白是主要的食物过敏原,常引起婴幼儿过敏性疾病。牛奶过敏通常表现为湿疹、特异性皮肤炎等皮肤症状以及恶心、呕吐、腹痛、腹泻和大便干燥等消化道症状。牛奶中的过敏原主要有3 种,分别是酪蛋白以及乳清蛋白中的α-乳白蛋白、β-乳球蛋白[31]。酪蛋白分为4 个亚型:α-S1酪蛋白、α-S2酪蛋白、β-酪蛋白和κ-酪蛋白,它们的结构特征为存在一个中心疏水部分和亲水层的磷酸化位点。其中α-S1酪蛋白是4 个亚型中致敏性最强的,有近70%的无序结构,只有少量的二级结构,如 α-螺旋或β-折叠;α-乳白蛋白属于c-型溶菌酶/α-乳白蛋白家族,是一种参与乳糖合成的钙结合蛋白,侧链结构由大量α-螺旋以及β-折叠组成,稳定性高,保护其内部不受 溶剂的破坏[32];β-乳球蛋白是脂质转载蛋白家族的一员,作为脂质、激素、类固醇等的转运体,存在于反刍动物的乳清蛋白中,由6 个不同的短肽链片段组成,主要位于β链,在过敏原表面形成一个平坦区域[33]。由于α-乳白蛋白、β-乳球蛋白和酪蛋白这3 种主要的牛奶过敏原在牛奶中的含量丰富,因此导致较高的牛奶过敏发生率。
1.6 鸡蛋
鸡蛋也是引起食物过敏的主要食品之一,过敏症状主要表现为湿疹、皮炎和风团疹,消化道出现呕吐、腹泻、胃食道反流等。鸡蛋中的主要过敏原有6 种,蛋黄中存在2 种,分别是α-卵黄蛋白和卵黄糖蛋白;蛋清中有4 种,分别是卵类黏蛋白、卵白蛋白、卵转铁蛋白和溶菌酶,这4 种蛋白分别占蛋清蛋白总量的11%、54%、12%和3.5%[34]。卵类黏蛋白的分子质量约为28 kDa,由186 个氨基酸残基组成,含有9 个二硫键,分子结构比较稳定,因此其对热加工以及胰蛋白酶酶解处理均具有很好的耐受性。卵白蛋白在蛋清蛋白中的含量最丰富,致敏能力较强,分子质量约为44.5 kDa,由385 个氨基酸残基组成,含有一个二硫键和多个巯基基团。卵转铁蛋白是一种易溶解的非结晶蛋白,致敏性也比较强,分子质量约为77.9 kDa,由686 个氨基酸残基组成,分子内含有15 个二硫键,卵转铁蛋白是蛋清蛋白中唯一一个转铁蛋白家族的糖蛋白,含有一个可以与Fe3+结合的位点,此位点赋予了其很多生物活性,同时与金属离子相结合后结构更加稳定。溶菌酶是一种较弱的过敏原,目前对溶菌酶更多的研究是在其抑菌性质上,实际上溶菌酶也具有潜在的致敏性,溶菌酶分子质量约14.3 kDa,由198 个氨基酸残基组成,分子内含有4 个二硫键,结构非常稳定,但作为一种酶,其稳定性会受到pH值的影响,pH值越低越不稳定。
1.7 鱼类
鱼类肉质鲜嫩且营养价值高,但是鱼类常引起过敏人群发生食物过敏反应。过敏症状主要表现为脸红、荨麻疹、恶心呕吐、腹泻、体温逆转、视力模糊等神经系统症状以及血压下降、心传导阻滞等心血管症状[35]。鱼类主要过敏原为小清蛋白、醛缩酶和烯醇化酶。小清蛋白具有保守蛋白结构,分子质量为10~13 kDa,属于食物过敏原中最大的蛋白质家族之一的钙结合蛋白。小清蛋白的热稳定性极高,对食品加工和酶消化的耐受能力极强,不容易通过物理化学方法去除,因此小清蛋白是导致70%以上的鱼及鱼类产品引起过敏反应的原因[36]。其次,醛缩酶和β-烯醇化酶也是重要的鱼类过敏原,分子质量分别为40 kDa和47~50 kDa。醛缩酶和烯醇化酶对热处理敏感,对食品加工的耐受度低于小清蛋白,因此过敏反应的发生概率也低于小清蛋白。其中2013年的一项调查显示,不同鱼类中的致敏作用有13%~37%来自醛缩酶A,14%~56%来自β-烯醇化酶[37]。另一种鱼类过敏原原肌球蛋白在贝类中作为重要的过敏原存在,但在鱼类中引起的过敏反应相对较少。在世界卫生组织/国际免疫学联合会仅有一种鱼类过敏原被注册,即莫桑比克罗非鱼[38]。目前对于鱼类中的原肌球蛋白研究甚少,尚需进一步确定其他鱼类中的原肌球蛋白是否会引起过敏反应。此外,由于鱼类产品种类繁多,除了上述过敏原外,仍不断有其他潜在的鱼类过敏原被发现,包括醛磷酸脱氢酶、磷酸三脂异构酶、甘油醛-3-磷酸脱氢酶和肌酸激酶等,然而这些分子的致敏特性仍有待确定。
1.8 甲壳及贝类
甲壳及贝类食品味道鲜美且营养丰富,然而因含有过敏原常引起过敏人群发生海鲜过敏反应。过敏症状表现为恶心呕吐、腹泻腹痛的胃肠道症状,也会导致指尖和脚趾的刺痛感,甚至出现肌肉麻痹。甲壳及贝类过敏原主要存在于肉的可食用部分,其主要过敏原包括原肌球蛋白和精氨酸激酶[39]。原肌球蛋白被认为是所有的可食用甲壳类动物中都存在的无脊椎动物泛变应原,参与脊椎动物和无脊椎动物的肌肉收缩。原肌球蛋白是由 α-螺旋盘绕而成的同源二聚体蛋白质,其螺旋结构是由7 个氨基酸组成的重复序列,在整个蛋白质的长度上与每个位于第一和第四位的疏水氨基酸的相互作用,这种二级和三级结构赋予原肌球蛋白结构稳定性,因此能够经受高温和高压处理保持其致敏性[40]。另一种主要过敏原精氨酸激酶(arginine kinase,AK)广泛分布于无脊椎动物中,通常作为单体存在,但也观察到一些二聚体。AK分子质量为38~45 kDa,是一种热不稳定蛋白,有研究证实在经过热处理后其IgE反应活性丧失,并且经过热处理和酸处理后致敏性降低[41]。除了上述两种主要过敏原,还发现了一些其他能够引起过敏反应的甲壳及贝类过敏原,例如肌球蛋白轻链、肌质钙结合蛋白和肌钙蛋白,这3 种过敏原能够引起轻微的过敏反应,过敏反应频率在15%~50%之间。此外还有许多未知的蛋白质会引起甲壳类动物的过敏反应,这些蛋白质的致敏特性尚不明确,还需进一步的研究。
2 食物过敏原常用检测技术
目前食物过敏原的常用检测技术主要为:基于蛋白水平的免疫学检测技术,包括酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)法、免疫层析技术、免疫印迹技术以及生物传感器技术;基于蛋白水平的非免疫学检测技术质谱技术;以及基因水平的分子生物学检测方法,包括实时荧光定量聚合酶链式反应(polymerase chain reation,PCR)、环介导等温扩增检测(loop mediate isothermal amplification,LAMP)。同时,仍不断有新的检测技术被开发,用于准确检测食品中隐藏的过敏原以及降低生产过程中的交叉污染带来的风险[42],从而更好地保证过敏人群的生命健康。
2.1 基于蛋白水平的免疫学检测技术
2.1.1 酶联免疫吸附试验法
ELISA法基于免疫酶的特点对待测物质进行免疫测定,检测结果可根据底物与酶反应后的产物颜色对抗原进行定性或定量分析。ELISA法根据检测原理以及检测对象的不同分为多种类型,用于食物过敏原检测的主要是夹心法和竞争法[43]。Orcajo等[44]开发了一种标准化的竞争性ELISA法用于检测牛奶中主要过敏原β-乳球蛋白,通过优化检测条件、IgE与β-乳球蛋白比例和试剂浓度,确定了最佳检测参数,最后β-乳球蛋白的检测限低于0.2 mg/mL,提高了检测方法的灵敏度。张洁琼等[45]分别制备了兔和鼠多克隆抗体,建立了双抗体夹心ELSIA法检测中国甜杏仁过敏原蛋白苦杏仁球蛋白。结果表明,中国苦杏仁及美国大杏仁中苦杏仁球蛋白的检测限分别为(12.11±1.70)μg/L和(18.95±1.52)μg/L,且与常见的14 种植物性蛋白没有交叉反应,表明该方法具有良好的特异性。ELISA法是目前在食物过敏原的检测中应用最广泛的一种方法[46],特异性强、灵敏度高,现阶段多采用成品化的试剂盒进行样品检测。ELISA法检测结果的准确性依赖于抗体对致敏蛋白的识别,但由于食品加工过程中蛋白结构的改变使抗体无法准确识别结合部位,导致检测灵敏度下降 [47-48],容易产生假阳性结果。虽然ELISA法存在一定局限性,但其仍是主要的食品过敏原定量方法,尤其是在检测花生、大豆和鸡蛋等过敏食物中的致敏组分应用较广。
2.1.2 免疫层析技术
免疫层析技术是酶联免疫吸附技术原理的扩展应用,层析时,标记物与待测物之间形成的复合物被相应的配体捕获而聚集到硝化纤维膜上的检测线上,之后复合物在膜上呈现出标记物所带有的颜色,最后可通过纤维膜上显色条的有无、颜色的深浅和反射光线强弱等实现定性或定量检测[49]。免疫层析技术多应用于花生、榛子等坚果的过敏原检测,也有研究人员将其应用到鱼类过敏原的检测中。李梦银[50]建立了金磁免疫层析检测方法对鱼类及其制品中的小清蛋白进行检测,结果表明所制备的金磁免疫层析试纸条检测特异性及检测稳定性良好,最低检测质量浓度为4 ng/mL,为检测鱼类中的小清蛋白提供了一种有效方法。免疫层析技术是将色谱层析和免疫技术相结合的一种快速分析方法,检测的关键在于着色标记物的灵敏度,随着近代纳米材料科学的发展,发现了一些新型的纳米材料如胶体金、胶体银、超顺磁性纳米微球作为标记物可以显著提高检测灵敏度,实现食品中痕量水平过敏原的检测同时,基于其原理制备快速 检测试纸,可以实现现场快速检测。因此应用免疫层析检测技术结合新型纳米材料作为标记物,优化层析体系,提高检测效率将是未来研究的热点。
2.1.3 免疫印迹技术
免疫印迹技术,又称蛋白质印迹技术。该法首先利用凝胶电泳根据蛋白质分子质量的不同将样品分离,随后将凝胶上的蛋白质样品转移至硝酸纤维素膜上,使用放射性物质或者酶标记抗体来进行样品的检测与分析。免疫印迹技术主要用于食物过敏原的鉴定以及半定量分析,Willison等[51]利用小鼠单克隆抗体4C10对杏仁主要过敏原Pru du 6的构象表位进行定位,免疫印迹实验的分析中,该单克隆抗体与非还原性的Pru du 6发生反应,证明了该过敏原构象表位识别的准确性。Harish Babu等[52] 从浓缩的茄子皮以及层析物中获得了茄子蛋白样品,使用十二烷基硫酸钠-聚丙烯酰胺凝胶电泳将蛋白样品分离后进行免疫印迹分析,最后将茄子中重要的多酚氧化酶识别为重要过敏原。对于蛋白成分比较复杂的样品,可以采用双向免疫印迹技术实现蛋白样品更高的分离程度,Lu Mei等[53]利用4 例大豆过敏者血清和6 例大豆致敏者血浆的双向凝胶电泳免疫印迹法鉴定大豆IgE结合蛋白,并结合四极杆-飞行时间串联质谱从染色凝胶中分离出相应的斑点,并对其进行消化和分析。结果表明β-伴大豆球蛋白和大豆球蛋白为大豆中主要的过敏原。免疫印迹技术实现了凝胶电泳的高分辨率与固相免疫分析的结合,只需少量试剂即可实现蛋白质的快速、高灵敏度分析。但免疫印迹技术在样品分析时花费的时间过长,同时食品基质的复杂性将会影响分析的准确度。
2.1.4 生物传感器技术
生物传感器主要由生物识别元件和信号转换元件两大部分组成,通过将目标分析物与识别元件进行特异性结合后将产生的物理、化学信号转化为可以检测的光、电信号以达到检测目的[54]。目前用于食物过敏原检测的传感器主要为免疫传感器,根据测定原理的不同可进一步分为电化学免疫传感器、场效应生物传感器和表面等离子体共振(surface plasmon resonance,SPR)传感器等。Ruiz-Valdepeñas等[55]报道了一个敏感的磁力免疫传感器来检测β-乳球蛋白,最低检测限可达0.8 ng/mL,将该方法应用于不同类型乳制品中β-乳球蛋白的检测时,其检测结果与商业ELISA方法提供的结果完全一致,因此有望成为一个可靠的替代方法。生物传感器的识别元件有多种形式,开发新的识别方法并与其他技术联用可以实现不同样品的检测。蒋栋磊[56]以食物过敏原作为 研究对象,将免疫系统中的RBL-2H3肥大细胞作为识别元件,结合电化学传感、荧光质粒转染、磁纳米粒子标记、微流控芯片等技术构建了一系列快速、灵敏、新颖的细胞传感器,为食品安全检测研究提供了一条崭新的途径。近年来SPR生物传感器得到了较多关注,Pollet等[57] 报道了一种具有纳米信号增强的光纤SPR生物传感器检测复杂食品基质中的花生过敏原,采用磁铁矿纳米颗粒作为辅助标记,将SPR生物测定Ara h 1的检出限提高了两个数量级,从9 μg/mL提高到0.09 μg/mL,同时SPR纤维可以很容易地再生,一根纤维可以重复使用35 次而不丧失敏感性。生物传感器技术是一种快速检测技术,具有灵敏度高、检测成本低、检测仪器微型化的优势,在开发生物传感器技术时,需要充分考虑制备材料的性能,选择合适的制备材料可以提高传感器的检测灵敏度。利用磁珠开发电化学免疫传感器已被证明是一个有用的工具,可以提高其灵敏度,缩短分析时间,并降低基质效应。但目前生物传感器技术仪器的制备复杂,对样品预处理的要求高,这些在一定程度上限制了其实现商业化、标准化。利用研制新型的纳米材料来将其应用到生物传感器,可以实现样品的快速优化处理,将是免疫传感器技术未来的发展趋势。
2.2 基于基因水平的分子生物学检测技术
2.2.1 实时荧光定量PCR技术
实时荧光定量PCR技术在体外模拟体内的DNA复制,利用扩增后的核酸产物来进行样品检测。通过在PCR体系中加入荧光基团,利用荧光基团产生的荧光信号变化来动态监测整个反应过程的实时荧光定量PCR技术在食物过敏原的检测中应用更加广泛。传统PCR技术主要对样品进行定性检测,而实时荧光定量PCR可以实现多种复杂食品中过敏原的定性定量分析以及物种的鉴定。Sanchiz等[58] 首次建立了一种以Cas s 9过敏原编码基因为靶点的实时荧光定量PCR方法,在板栗与小麦的二元混合物中最低检测限为100 mg/kg。此外,实时荧光定量PCR还适用于食品中痕量蛋白的检测,Villa等[59]建立了一种实时荧光定量PCR技术筛选用于复杂肉制品中的牛奶成分,结果显示筛选出来的两个线粒体基因(cytb和12S rRNA)以及两个核基因(β-乳球蛋白和β-酪蛋白),在生肉以及金华火腿的样品中牛奶浓缩蛋白的最低检测限为500 mg/kg。 PCR技术与毛细管电泳技术的结合可以实现多种过敏原的同时检测,有效提高了食物过敏原的检测效率。Cheng Fang等[60]采用十重PCR技术结合毛细管电泳技术,同时检测了榛子、开心果、燕麦、芝麻、花生、腰果、大麦、小麦、大豆和山核桃中的10 种常见食物过敏原。该方法的绝对检测限在2~20 个单倍体基因组之间,在随后的20 种商业食品的应用中也验证了该方法的可靠性。 Suh等[61]利用多重PCR技术扩增出4 种软体动物的特异性扩增子和一个通用真核引物扩增子,并与毛细管电泳技术相结合,建立了牡蛎、贻贝、鲍鱼、蛤蜊原肌球蛋白基因和真核生物18S rRNA基因的多重PCR检测方法,DNA的检测限为16 pg,可以广泛应用于海鲜类食物 过敏原的检测。实时定量PCR是在食品过敏原检测中应用最广的一项基因水平检测技术,相比于常规PCR,特异性更强,灵敏度更高,实现了定性到定量的飞跃,适用于复杂食物中多重过敏原的同时定量分析。在食品基质中,过敏原作为蛋白质会在检测过程中更加容易降解,DNA相较于蛋白质降解速度要慢得多,因此,这也是基因水平检测方法的优势。然而实时PCR技术在检测过程中容易造成样品的污染以及假阳性的结果,造成检测误差。
2.2.2 环介导等温扩增检测技术
LAMP是近些年发展起来的一种新型的核酸扩增技术,通过设计4~6 条特异性引物,使用具有链置换活性的DNA聚合酶,在等温条件下每小时将目标基因扩增9~10 倍[62]。由于其操作简单、检测时间短,目前已经应用于食品微生物检测、转基因食品检测以及过敏原成分检测等多个方面。张懿翔等[63]设计并筛选出了LAMP特异性扩增产物,建立了LAMP技术对28 种牡蛎阳性样品、阴性样品以及相关食品进行检测,结果表明该方法可以检测出样品中质量分数仅为0.1%的牡蛎成分,以及DNA质量浓度为0.01 ng/μL的样品,同时反应可在25~45 min内完成,提高了检测效率。刘津等[64]设计并筛选了食物过敏原澳洲坚果LAMP引物,并对反应体系以及反应条件进行优化,建立的LAMP技术能够特异性、灵敏、稳定地检测食品中澳洲坚果成分,检测限为0.5%。研究人员采用相同的实验流程建立了巴西坚果的LAMP技术,同样取得了可靠的检测结果[65]。乳制品中的商业欺诈现象十分常见,建立可靠的检测技术具有重要意义。Kim等[66]开发了一种可以同时检测牛奶和山羊奶的双重LAMP,缩短了检测时间,检出限可达2%。LAMP技术相比于与普通核酸扩增技术,对实验器材的要求大大降低,无需类似于热循环仪的昴贵实验仪器,优化了实验流程,缩短了检测时间,同时检测结果可以直接通过肉眼观察是否生成白色浑浊或者绿色荧光来判断,适用于食物过敏原的快速现场检测。尽管在引物设计上难度较大,但LAMP技术在食品安全检测领域仍具有广阔的发展前景。
2.3 质谱技术
近年来,随着质谱技术的不断成熟与完善,在食品过敏原检测中的应用得到了越来越多的关注[67]。使用质谱法检测食物过敏原时多与高效分离纯化技术如液相色谱、毛细管电泳等相结合,最常用的检测方法为 液相色谱-串联质谱法(liquid chromatography-tandem mass spectrometry,LC-MS/MS),在选择合适的样品预处理方式和稳定的特征肽段的前提下,可以提高检测的灵敏度和准确性。Ma Χiuli等[68]为了对加工食品中的芝麻过敏原进行全面定量,优化了7 种芝麻过敏原蛋白的提取和胰蛋白酶消化条件,并分别对其进行了标记和绝对 定量(absolute quantitative,AQUA)肽的筛选。结果显示7 个芝麻过敏原AQUA肽的检测限和定量限的测定范围分别为0.1~140.0 fmol/μL和0.4~400 fmol/μL,在多个实验中的总体变异系数小于5%,证明所建立的LC-MS/MS检测方法在提高芝麻加工食品的安全性的潜在价值。由于LC-MS/MS法受食品基质的影响较小,因此在复杂食品基质中检测食物过敏原的应用十分广泛,Planque等[69] 基于超高效液相色谱-串联质谱技术建立了检测复杂食品(巧克力、冰淇淋)和加工食品(曲奇、酱料)中10 种过敏原的方法,该检测方法达到了多重过敏原检测的最低定量限:牛奶蛋白0.5 mg/kg,花生、腰果、榛子和开心果蛋白2.5 mg/kg,鸡蛋蛋白3.0 mg/kg,大豆蛋白5 mg/kg,核桃蛋白5 mg/kg,山核桃蛋白5 mg/kg, 适用于实验中4 种不同的基质。此外该实验中通过标记的内部标准进行校正,将牛奶酪蛋白肽的相对标准偏差从30.9%降低到10.3%。此外,液相色谱-质谱法可以检测痕量级别的食物过敏原,Inman等[70]建立了一种液质色谱-质谱方法用于检测孜然和红辣椒两种香料中被杏仁和杏花过敏原污染的情况,结果表明该方法可以用于鉴别香料中百万分之一的杏仁坚果污染物。尽管质谱法在应用时需要昴贵的仪器以及专业的技术人员,但质谱法具有快速、高特异性、高通量的优势,可以克服免疫学方法存在的通量低和交叉干扰的弊端,也克服了 PCR技术不能直接检测致敏蛋白质的缺点,具有较好的开发潜力[71]。
3 新型食物过敏原检测技术
生物芯片包括基因芯片和蛋白芯片两种,是食物过敏原检测的一种新型、有效的检测工具,因其高特异性、高灵敏度和高通量的特点成为近年来人们研究的热点[72]。张轶群[73]首次对三维芯片载体的基片进行处理,得到了具有良好固定效果的三维芯片载体,并在此基础上,建立并完善了海产品过敏原的检测方法,为海产品过敏原的控制提供了必要的技术储备。目前生物芯片在食物过敏原检测领域应用并不广泛,但由于其高效快速检测的特点,具有很大的发展前景。此外,为了能够更好地区分致敏蛋白与非致敏蛋白,提高食物过敏原检测的高效准确性,Lu Wenzhe等[16]开发了一种基于物理化学特性基序来区分过敏原和非过敏原同源物的方法,并定量估计查询序列的潜在过敏原性。该方法可对蛋白家族中已知的致敏蛋白进行表征,然后从8万 个随机选择的非过敏原序列中分离出的过敏原序列进行评分,证明了过敏原特异性基序的平均评分与非过敏原的平均评分存在显著差异。这种评分方法也能将那些具有显著总体相似性的序列辨别出来,为以后应用蛋白质序列检测食品中过敏原提供了依据。
综上所述,每种食物过敏原检测技术都兼具优缺点,没有一种单独的方法能够将所有优点结合起来,对所有相关的过敏性食品成分进行经济、可靠、快速和明确的识别和定量(图1)。对于一些复杂的分析样品,可能需要使用一种以上的技术来进行全面的检测。

图1 食物过敏原检测技术基本原理及优缺点
Fig.1 Basic principles as well as advantages and disadvantages of food allergen detection technologies
4 结 语
目前在世界范围内,过敏性疾病的发生率仍呈现不断上升的趋势,明确食品中的过敏原并建立相关的检测技术对于预防食物过敏的发生至关重要。在目前的食物过敏原检测技术中,基于蛋白水平的ELISA检测技术和基于核酸水平的实时荧光定量PCR技术应用最为广泛,已经逐渐商业化、标准化。蛋白质容易在加工过程中发生变性、聚集等现象,导致其线性表位以及构象表位发生改变,给过敏原的检测带来困难,因此更容易造成检测误差,出现假阳性以及假阴性结果。相比之下,核酸检测更不易于受到外界条件影响,但由于是间接性检测,无法检测到蛋白质谱引起的过敏反应。而质谱法既可以改善免疫学方法中存在的检测通量低和交叉干扰的影响,同时避免了核酸检测技术不能直接检测致敏蛋白的缺点,能够对蛋白质和多肽进行明确鉴定,并且可以同时检测多种过敏原。但昴贵的仪器成本以及对检测人员的高素质要求在一定程度上限制了其进一步的发展。为了减少过敏性疾病的发生,未来的主要发展方向有两点:一方面,开发有效的过敏原减除技术,如通过热加工、高压及微生物发酵降解等方式降解过敏原蛋白从而降低致敏性;另一方面,开发便捷、快速、高效的过敏原检测技术,以帮助消费者更好地避免摄入过敏原。
[1]ALBA P T, DANIEL L O, ELENA M, et al.Assessment of the allergenic potential of the main egg white proteins in BALB/c mice[J].Journal of Agricultural and Food Chemistry, 2018, 66(11): 2970-2976.DOI:10.1021/acs.jafc.8b00402.
[2]LIU Guangyu, MEI Xuejiao, HU Mengjun, et al.Analysis of the allergenic epitopes of tropomyosin from mud crab using phage display and site-directed mutagenesis[J].Journal of Agricultural and Food Chemistry, 2018, 66(34): 9127-9137.DOI:10.1021/acs.jafc.8b03466.
[3]JIN T C, WANG C, ZHANG C Y, et al.Crystal structure of cocosin, a potential food allergen from coconut (Cocos nucifera)[J].Journal of Agricultural and Food Chemistry, 2017, 65(34): 7560-7568.DOI:10.1021/acs.jafc.7b02252.
[4]ZHANG Y Z, DU W X, FAN Y T, et al.Purification and characterization of a black walnut (Juglans nigra) allergen, Jug n 4[J].Journal of Agricultural and Food Chemistry, 2017, 65(2): 454-462.DOI:10.1021/acs.jafc.6b04387.
[5]YOUCE S, MARYAM D.Plant food allergy: influence of chemicals on plant allergens[J].Food and Chemical Toxicology, 2018, 115: 365-374.DOI:10.1016/j.fct.2018.03.032.
[6]CABANILLAS B, MALEKI S J, RODRÍGUEZ J, et al.Allergenic properties and differential response of walnut subjected to processing treatments[J].Food Chemistry, 2014, 157: 141-147.DOI:10.1016/j.foodchem.2014.02.025.
[7]GOMAA A, BOYE J.Impact of irradiation and thermal processing on the immunochemical detection of milk and egg allergens in foods[J].Food Research International, 2015, 74: 275-283.DOI:10.1016/j.foodres.2015.05.023.
[8]ABDEL RAHMAN A M, GAGNÉ S, HELLEUR R J.Simultaneous determination of two major snow crab aeroallergens in processing plants by use of isotopic dilution tandem mass spectrometry[J].Analytical and Bioanalytical Chemistry, 2012, 403(3): 821-831.DOI:10.1007/s00216-012-5873-2.
[9]LI J, ZHOU R L, REN Z Q, et al.Improvement of protein quality and degradation of allergen in soybean meal fermented by Neurospora crassa[J].LWT-Food Science and Technology, 2019, 101: 220-228.DOI:10.1016/j.lwt.2018.10.089.
[10]FU W H, RAO H, TIAN Y, et al.Bacterial composition in sourdoughs from different regions in China and the microbial potential to reduce wheat allergens[J].LWT-Food Science and Technology, 2020, 117: 108669.DOI:10.1016/j.lwt.2019.108669.
[11]周晓.论食品企业中的过敏原控制[J].科技视界, 2019(14): 80-81.DOI:10.19694/j.cnki.issn2095-2457.2019.14.037.
[12]赵海军, 鲁超, 殷杰, 等.美国过敏原新规对出口食品的影响及应对[J].检验检疫学刊, 2018, 28(1): 21-28.
[13]郑颖, 陈曙光, 叶钰, 等.日本食物过敏原的管理及对我国的启示[J].食品科学, 2016, 37(3): 253-257.DOI:10.7506/spkx1002-6630-201603044.
[14]王梦娟, 李江华, 郭林宇, 等.欧盟食品中过敏原标识的管理及对我国的启示[J].食品科学, 2014, 35(1): 261-265.DOI:10.7506/spkx1002-6630-201401052.
[15]王敏峰, 夏强, 王攀.中国食物过敏原标签标注研究[J].食品工业, 2013, 34(12): 189-191.
[16]LU Wenzhe, NEGI S S, SCHEIN C, et al.Distinguishing allergens from non-allergenic homologues using Physical-Chemical Property (PCP) motifs[J].Molecular Immunology, 2018, 99: 1-8.DOI:10.1016/j.molimm.2018.03.022.
[17]KHUDA S, SLATE A, PEREIRA M, et al.Effect of processing on recovery and variability associated with immunochemical analytical methods for multiple allergens in a single matrix: sugar cookies[J].Journal of Agricultural and Food Chemistry, 2012, 60(17): 4195-4203.DOI:10.1021/jf3001839.
[18]胡晓利, 布冠好, 张晓旭.大豆蛋白过敏原及常见脱敏方法研究进展[C]//中国食品科学技术学会第十五届年会论文摘要集.北京: 中国食品科学技术学会, 2018: 331.
[19]李丽芳, 黄文胜, 张九凯, 等.超高效液相色谱-串联质谱法检测大豆主要过敏原蛋白[J].食品科学, 2020, 41(24): 316-324.DOI:10.7506/spkx1002-6630-20190923-278.
[20]李玺, 薛文通.小麦致敏蛋白及其过敏病症研究进展[J].食品科技, 2016, 41(8): 147-152.DOI:10.13684/j.cnki.spkj.2016.08.037.
[21]姚亚亚, 张迪, 田博宇, 等.小麦过敏原检测技术的研究进展[J].粮食与油脂, 2019, 32(4): 16-18.DOI:10.3969/j.issn.1008-9578.2019.04.006.
[22]BAAR A, PAHR S, CONSTANTIN C, et al.Specific IgE reactivity to Tri a 36 in children with wheat food allergy[J].The Journal of Allergy and Clinical Immunology, 2014, 133(2): 585-587.DOI:10.1016/j.jaci.2013.10.044.
[23]BAAR A, PAHR S, CONSTANTIN C, et al.Evidence for higher sensitivity of recombinant Tri a 36 compared to omega-5-gliadin for diagnosis of wheat food allergy[J].Clinical and Translational Allergy, 2013, 3(Suppl 3): 171.DOI:10.1186/2045-7022-3-S3-P171.
[24]OFFERMANN L R, BUBLIN M, PERDUE M L, et al.Structural and functional characterization of the hazelnut allergen Cor a 8[J].Journal of Agricultural and Food Chemistry, 2015, 63(41): 9150-9158.DOI:10.1021/acs.jafc.5b03534.
[25]MATTISON C P, MALVEIRA CAVALCANTE J, IZABEL GALLÃO M, et al.Effects of industrial cashew nut processing on anacardic acid content and allergen recognition by IgE[J].Food Chemistry, 2018, 240: 370-376.DOI:10.1016/j.foodchem.2017.07.146.
[26]WANG Y, FU T J, HOWARD A, et al.Crystal structure of peanut (arachis hypogaea) allergen Ara h 5[J].Journal of Agricultural and Food Chemistry, 2013, 61(7): 1573-1578.DOI:10.1021/jf303861p.
[27]POMÉS A, DAVIES J M, GADERMAIER G, et al.WHO/IUIS allergen nomenclature: providing a common language[J].Molecular Immunology, 2018, 100: 3-13.DOI:10.1016/j.molimm.2018.03.003.
[28]MONTSERRAT M, MAYAYO C, SÁNCHEZ L, et al.Study of the thermoresistance of the allergenic Ara h1 protein from peanut (Arachis hypogaea)[J].Journal of Agricultural and Food Chemistry, 2013, 61(13): 3335-3340.DOI:10.1021/jf305450s.
[29]VAN BOXTEL E L, KOPPELMAN S J, VAN DEN BROEK L A M, et al.Determination of pepsin-susceptible and pepsin-resistant epitopes in native and heat-treated peanut allergen Ara h 1[J].Journal of Agricultural and Food Chemistry, 2008, 56(6): 2223-2230.DOI:10.1021/jf072907n.
[30]DE JONG G A H, JAYASENA S, JOHNSON P, et al.Purification and characterization of naturally occurring post-translationally cleaved Ara h 6, an allergen that contributes substantially to the allergenic potency of peanut[J].Journal of Agricultural and Food Chemistry, 2018, 66(41): 10855-10863.DOI:10.1021/acs.jafc.8b03140.
[31]黄美佳.钙离子对牛乳α-乳白蛋白结构与致敏性的影响[D].南昌: 南昌大学, 2018: 15-17.
[32]QI K L, LIU T, YANG Y J, et al.A rapid immobilized trypsin digestion combined with liquid chromatography-tandem mass spectrometry for the detection of milk allergens in baked food[J].Food Control, 2019, 102: 179-187.DOI:10.1016/j.foodcont.2019.03.017.
[33]D’AURIA E, MAMELI C, PIRAS C, et al.Precision medicine in cow’s milk allergy: proteomics perspectives from allergens to patients[J].Journal of Proteomics, 2018, 188: 173-180.DOI:10.1016/j.jprot.2018.01.018.
[34]刘珂, 熊丽姬, 高金燕, 等.热加工对鸡蛋中4 种主要过敏原结构的影响[J].食品科学, 2017, 38(23): 51-58.DOI:10.7506/spkx1002-6630-201723009.
[35]JIANG D L, JIANG H, JI J, et al.Mast-cell-based fluorescence biosensor for rapid detection of major fish allergen parvalbumin[J].Journal of Agricultural and Food Chemistry, 2014, 62(27): 6473-6480.DOI:10.1021/jf501382t.
[36]SHARP M F, STEPHEN J N, KRAFT L, et al.Immunological crossreactivity between four distant parvalbumins-impact on allergen detection and diagnostics[J].Molecular Immunology, 2015, 63(2): 437-448.DOI:10.1016/j.molimm.2014.09.019.
[37]KUEHN A, HILGER C, LEHNERS-WEBER C, et al.Identification of enolases and aldolases as important fish allergens in cod, salmon and tuna: component resolved diagnosis using parvalbumin and the new allergens[J].Clinical & Experimental Allergy, 2013, 43(7): 811-822.DOI:10.1111/cea.12117.
[38]LIU R, HOLCK A L, YANG E, et al.Tropomyosin from tilapia (Oreochromis mossambicus) as an allergen[J].Clinical and Experimental Allergy, 2013, 43(3): 365-377.DOI:10.1111/cea.12056.
[39]RUETHERS T, TAKI A C, JOHNSTON E B, et al.Seafood allergy: a comprehensive review of fish and shellfish allergens[J].Molecular Immunology, 2018, 100: 28-57.DOI:10.1016/j.molimm.2018.04.008.
[40]KAMATH S D, RAHMAN A M A, KOMODA T, et al.Impact of heat processing on the detection of the major shellfish allergen tropomyosin in crustaceans and molluscs using specific monoclonal antibodies[J].Food Chemistry, 2013, 141(4): 4031-4039.DOI:10.1016/j.foodchem.2013.06.105.
[41]KAMATH S D, RAHMAN A M A, VOSKAMP A, et al.Effect of heat processing on antibody reactivity to allergen variants and fragments of black tiger prawn: a comprehensive allergenomic approach[J].Molecular Nutrition and Food Research, 2014, 58(5): 1144-1155.DOI:10.1002/mnfr.201300584.
[42]CHEN M X, YANG H, MA Y N, et al.Absolute quantification of allergen Glb33 in rice by liquid chromatography-mass spectrometry using two isotope-labeled standard peptides[J].Journal of Agricultural and Food Chemistry, 2019, 67(17): 5026-5032.DOI:10.1021/acs.jafc.8b06738.
[43]侯瑾, 李迎秋.酶联免疫吸附技术在食品安全检测中的应用[J].中国调味品, 2017, 42(6): 165-169.DOI:10.3969/j.issn.1000-9973.2017.06.036.
[44]ORCAJO J, LAVILLA M, MARTÍNEZ DE MARAÑÓN I.Specific and sensitive ELISA for measurement of IgE-binding variations of milk allergen β-lactoglobulin in processed foods[J].Analytica Chimica Acta, 2019, 1052: 163-169.DOI:10.1016/j.aca.2018.11.048.
[45]张洁琼, 高淑霞, 生威, 等.双抗体夹心酶联免疫吸附法检测杏仁过敏原苦杏仁球蛋白[J].食品科学, 2013, 34(16): 173-177.
[46]梁玉博.食品检测中酶联免疫吸附试验的应用[J].现代食品, 2018(7): 125-127.DOI:10.16736/j.cnki.cn41-1434/ts.2018.07.042.
[47]PARKER C H, KHUDA S E, PEREIRA M, et al.Multi-allergen quantitation and the impact of thermal treatment in industry-processed baked goods by ELISA and liquid chromatography-tandem mass spectrometry[J].Journal of Agricultural and Food Chemistry, 2015, 63(49): 10669-10680.DOI:10.1021/acs.jafc.5b04287.
[48]GOMAA A, BOYE J.Simultaneous detection of multi-allergens in an incurred food matrix using ELISA, multiplex flow cytometry and liquid chromatography mass spectrometry (LC-MS)[J].Food Chemistry, 2015, 175: 585-592.DOI:10.1016/j.foodchem.2014.12.017.
[49]唐瑞莉.浅析食品过敏原检测中免疫学技术的应用[J].技术与市场, 2016, 23(4): 126.DOI:10.3969/j.issn.1006-8554.2016.04.073.
[50]李梦银.鱼类主要过敏原小清蛋白金磁免疫层析试纸条的研制[D].上海: 上海师范大学, 2019: 33-35.
[51]WILLISON L N, ZHANG Qian, SU Mengna, et al.Conformational epitope mapping of Pru du 6, a major allergen from almond nut[J].Molecular Immunology, 2013, 55(3/4): 253-263.DOI:10.1016/j.molimm.2013.02.004.
[52]HARISH BABU B N, WILFRED A, VENKATESH Y P.Emerging food allergens: identification of polyphenol oxidase as an important allergen in eggplant (Solanum melongena L.)[J].Immunobiology, 2017, 222(2): 155-163.DOI:10.1016/j.imbio.2016.10.009.
[53]LU Mei, JIN Yuan, CERNY R, et al.Combining 2-DE immunoblots and mass spectrometry to identify putative soybean (Glycine max) allergens[J].Food and Chemical Toxicology, 2018, 116 (Part B): 207-215.DOI:10.1016/j.fct.2018.04.032.
[54]叶璟, 周海鹰.生物传感器检测食物过敏原的研究进展[J].科技 通报, 2017, 33(11): 6-10.DOI:10.13774/j.cnki.kjtb.2017.11.002.
[55]RUIZ-VALDEPEÑAS MONTIEL V, CAMPUZALO S, CONZUEIO F, et al.Electrochemical magnetoimmunosensing platform for determination of the milk allergen β-lactoglobulin[J].Talanta, 2015, 131: 156-162.DOI:10.1016/j.talanta.2014.07.076.
[56]蒋栋磊.基于肥大细胞传感器检测食物过敏原蛋白技术研究[D].无锡: 江南大学, 2015: 20-23.
[57]POLLET J, DELPORT F, JANSSEN K P F, et al.Fast and accurate peanut allergen detection with nanobead enhanced optical fiber SPR biosensor[J].Talanta, 2011, 83(5): 1436-1441.DOI:10.1016/j.talanta.2010.11.032.
[58]SANCHIZ Á, BALLESTEROS I, LÓPEZ-GARCÍA A, et al.Chestnut allergen detection in complex food products: development and validation of a real-time PCR method[J].LWT-Food Science and Technology, 2020, 123.DOI:10.1016/j.lwt.2020.109067.
[59]VILLA C, COSTA J, OLIVEIRA M, et al.Cow’s milk allergens: Screening gene markers for the detection of milk ingredients in complex meat products[J].Food Control, 2020, 108: 106823.DOI:10.1016/j.foodcont.2019.106823.
[60]CHENG Fang, WU Jiajie, ZHANG Jin, et al.Development and interlaboratory transfer of a decaplex polymerase chain reaction assay combined with capillary electrophoresis for the simultaneous detection of ten food allergens[J].Food Chemistry, 2016, 199: 799-808.DOI:/10.1016/j.foodchem.2015.12.058.
[61]SUH S M, KIM M J, KIM H I, et al.A multiplex PCR assay combined with capillary electrophoresis for the simultaneous detection of tropomyosin allergens from oyster, mussel, abalone, and clam mollusk species[J].Food Chemistry, 2020, 317: 126451.DOI:10.1016/j.foodchem.2020.126451.
[62]范安妮, 佘之蕴, 张娟, 等.环介导等温扩增技术在食品安全检测领域的应用研究进展[J].食品工业科技, 2018, 39(10): 330-334.DOI:10.13386/j.issn1002-0306.2018.10.061.
[63]张懿翔, 于媛媛, 宋春宏, 等.环介导等温扩增技术快速检测食物过敏原牡蛎成分[J].食品安全质量检测学报, 2019, 10(7): 1804-1810.
[64]刘津, 张隽, 李婷, 等.食物过敏原澳洲坚果环介导等温扩增检测方法的建立与应用[J].食品科学, 2014, 35(22): 226-232.DOI:10.7506/spkx1002-6630-201422044.
[65]刘津, 陈源树, 凌莉, 等.食物过敏原巴西坚果环介导等温扩增检测方法的建立与应用[J].食品工业科技, 2014, 35(14): 76-80.DOI:10.13386/j.issn1002-0306.2014.14.007.
[66]KIM M J, KIM H Y.Direct duplex real-time loop mediated isothermal amplification assay for the simultaneous detection of cow and goat species origin of milk and yogurt products for field use[J].Food Chemistry, 2018, 246: 26-31.DOI:10.1016/j.foodchem.2017.11.014.
[67]PILOLLI R, DE ANGELIS E, MONACI L.Streamlining the analytical workflow for multiplex MS/MS allergen detection in processed foods[J].Food Chemistry, 2017, 221: 1747-1753.DOI:10.1016/j.foodchem.2016.10.110.
[68]MA Xiuli, LI Hong, ZHANG Jiukai, et al.Comprehensive quantification of sesame allergens in processed food using liquid chromatography-tandem mass spectrometry[J].Food Control, 2020, 107.DOI:10.1016/j.foodcont.2019.106744.
[69]PLANQUE M, ARNOULD T, DIEU M, et al.Liquid chromatography coupled to tandem mass spectrometry for detecting ten allergens in complex and incurred foodstuffs[J].Journal of Chromatography A, 2017, 1530: 138-151.DOI:10.1016/j.chroma.2017.11.039.
[70]INMAN S E, GROVES K, MCCULLOUGH B, et al.Development of a LC-MS method for the discrimination between trace level prunus contaminants of spices[J].Food Chemistry, 2018, 245: 289-296.DOI:10.1016/j.foodchem.2017.10.101.
[71]古淑青, 赵超敏, 程甲, 等.基于质谱技术的食品过敏原检测方法研究进展[J].色谱, 2016, 34(7): 639-646.DOI:10.3724/SP.J.1123.2016.03005.
[72]雷洪波, 张娟, 吴炜亮.食物过敏原及其生物芯片检测技术的研究进展[J].食品工业, 2014, 35(6): 227-230.
[73]张轶群.海产品过敏原免疫芯片检测方法的研究[D].青岛: 中国海洋大学, 2009: 16-58.