核桃,又称胡桃、羌桃,是胡桃科植物,与扁桃、腰果、榛子并称为世界著名的“四大干果”,是我国重要经济树种之一。核桃仁含油65%~70%,并含有大量的多不饱和脂肪酸(61.8%~75.3%),其中含亚油酸62.2%、亚麻酸13.5%,同时还含有多种维生素及矿物元素,具有细胞修复、消炎、抗病毒、抗血栓等功效,宜长期食用[1-2]。
气味是植物油风味的典型特征之一,是判断植物油的品质及质量优劣的重要指标。油脂挥发性物质是其气味产生的基础物质,其形成与制备工艺有着密切关联[3]。核桃油常见制备方法主要包括压榨法、有机溶剂浸提法、水酶法和超临界萃取法[4]等,本实验选择适合大规模工业生产的压榨法和有机溶剂浸提法进行研究,其中压榨法是当前生产核桃油的主要方法[5],包括冷榨法和热榨法,该方法是利用机械压榨的方式将核桃仁中的油脂通过螺杆挤压挤出,冷榨核桃油的品质较高,营养成分保留较好,但是气味清淡,热榨核桃油具有典型的烘烤坚果味,气味浓郁,但是在高温烘烤过程中会造成部分营养成分的损失;有机溶剂浸提法是利用萃取原理,选用某种能溶解油脂的有机溶剂,经与适度破碎核桃仁的接触(浸泡或喷淋),使核桃仁中的油脂被有机溶剂萃取出来的一种方式,该方法提取率较高,适合大规模生产,但可能存在一定的溶剂残留,易导致蛋白质变性[6],且风味较差,缺乏核桃油本身独特的风味。目前已有研究表明[7-13],不同工艺制备核桃油的挥发性物质构成存在不同,但是,仍鲜见基于挥发性物质构成对不同工艺制备的核桃油进行区分的相关报道,而利用挥发性物质构成差异可为核桃油制备工艺的区分判别提供参考。
食用油的风味物质分析通常先采用蒸馏法、顶空法、吸附法等技术对风味组分进行提取富集,然后经气相色谱-质谱联用仪进行分析检测[14],其中静态顶空分析法是将食用油置于密闭容器中加热,待食用油与上层空气达到热力学平衡后,直接取顶空气体进样,此法制备简便,不使用溶剂,不混入干扰物,进样的气体与人能嗅到的香气近似[15]。
本研究通过冷榨、热榨(不同烘烤温度和时间)、有机溶剂浸提法(索氏抽提法)制备核桃油,对不同样品进行挥发性物质测定,利用顶空气相色谱-质谱分析,结合相对气味活度值(relative odor activity value,ROAV)、主成分分析(principal component analysis,PCA)和聚类热图,对不同制备工艺核桃油样品的挥发性物质进行分析,以期确定不同工艺制备核桃油的关键香气成分,并探索基于挥发性物质对不同工艺核桃油进行有效区分的可行性,为核桃油生产加工及品质控制提供理论依据。
1 材料与方法
1.1 材料与试剂
核桃购于新疆维吾尔自治区石河子市农贸市场,品种为温185。正己烷(分析纯) 德国Meker公司。
1.2 仪器与设备
7890B/5977A顶空气相色谱-质谱联用仪、HP-5色谱柱(30 m×0.25 mm,0.25 µm) 美国安捷伦科技有限公司;ZY-22A螺杆榨油机 中国温州宏阔科技有限公司;K1H烤箱 中国广东格兰仕电器制造有限公司。
1.3 方法
1.3.1 冷榨核桃油的制备
将300 g核桃仁置于螺杆榨油机中,调节温度为30 ℃,压榨得到毛油,于4 ℃、10 000 r/min离心15 min,取上层清液得到冷榨核桃油样品[16]。
1.3.2 热榨核桃油的制备
各取300 g核桃仁于120、150 ℃和180 ℃分别烘烤10、20 min和30 min[17],取烘烤后的核桃仁迅速冷却至室温,置于螺杆榨油机中,调节温度为30 ℃,压榨得到毛油,于4 ℃、10 000 r/min离心15 min,取上层清液得到热榨核桃油样品。
1.3.3 有机溶剂浸提核桃油的制备
采用索氏抽提法[18],提前将核桃仁粉碎,选用正己烷作为有机溶剂萃取,于70 ℃回流提取4 h,后经70 ℃旋转蒸发,回收正己烷,剩余即为有机溶剂提取样品。
1.3.4 顶空条件
加热箱80 ℃,时间30 min;进样时间30 s,进样量1 µL;传输线温度100 ℃;定量环温度105 ℃。
1.3.5 色谱条件
根据Tahri等[19]方法进行修改。
HP-5色谱柱(30 m×0.25 mm,0.25 μm);溶剂延迟1.5 min;柱温箱升温程序:40 ℃保持3 min;以2 ℃/min升至80 ℃,保持3 min;以2 ℃/min升至150 ℃,保持4 min;以5 ℃/min升至230 ℃,保持5 min;进样口温度200 ℃;载气(高纯度He)流速1.0 mL/min;分流进样,分流比为10∶1;传输线温度230 ℃。
1.3.6 质谱条件
电子电离源;电子能量70 eV;四极杆温度250 ℃;离子源温度230 ℃;全扫描模式;溶剂延迟3 min;质量扫描范围m/z 35~500。
1.3.7 化合物识别
化合物经过NIST谱库检索定性分析,仅报道匹配度大于80%的化合物,同时以各化合物峰面积占总峰面积的比值表示化合物的相对含量。
1.3.8 ROAV计算
通过计算ROAV[20],确定挥发性物质对样品风味的贡献。一般认为ROAV>1的挥发性物质是样品中的关键风味物质,0.1<ROAV≤1的挥发性物质是对样品的总体风味起修饰作用。选取化合物中对样品风味贡献最大的ROAVstan为100,其余各组分的ROAV按下式计算:
式中:CA为各组分的相对含量/%;TA为各组分的感觉阈值/(mg/kg);Cstan为对整体风味贡献最大的化合物的相对含量/%;Tstan为对整体风味贡献最大的化合物的感觉阈值/(mg/kg)。
1.4 数据处理
采用Origin 2018 Pro、SPSS Statistics 25.0、The Unscrambler 9.7以及MeV 4.90处理。
2 结果与分析
2.1 不同工艺制备核桃油挥发性成分分析
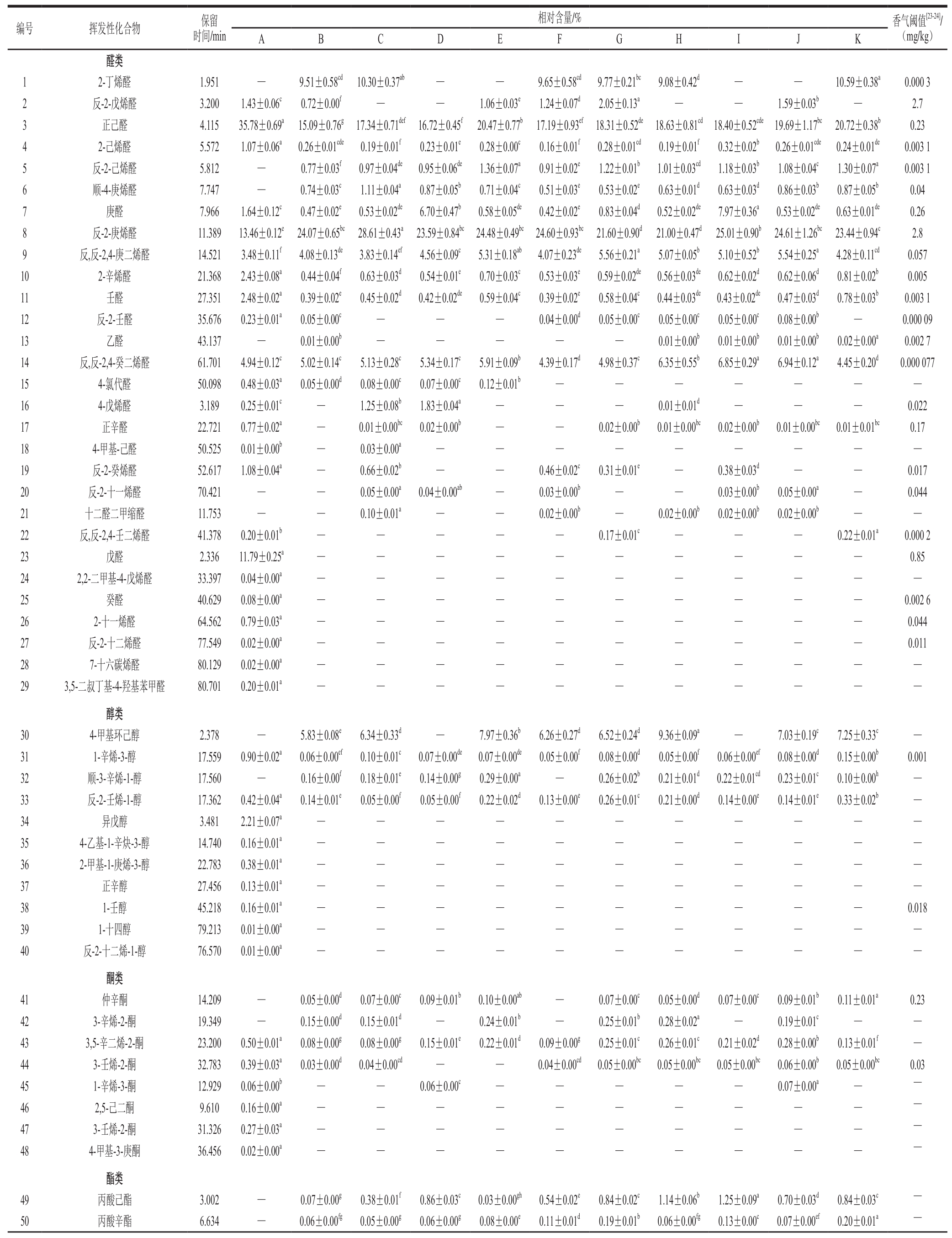
使用顶空气相色谱-质谱对不同工艺核桃油挥发性物质进行测定分析,此方法样品制备简单,不使用溶剂,不存在交叉污染等问题[21-22]。如图1、表1所示,不同工艺核桃油中共检测到92 种挥发性物质,包括29 种醛类、21 种烃类、11 种醇类、8 种酮类、7 种酯类、5 种酸类、4 种含氧杂环、2 种含氮杂环及5 种其他化合物。其中有机溶剂浸提核桃油测得60 种挥发性物质,冷榨样品测得43 种挥发性物质,热榨样品测得62 种挥发性物质,所有样品共有化合物有14 种。对于冷榨和热榨核桃油样品,挥发性物质含量最高的是反-2-庚烯醛,其次为正己醛和顺-2-辛烯;对于有机溶剂浸提得到的核桃油样品,挥发性物质含量最高的为正己醛,其次为反-2-庚烯醛和戊醛。
表1 不同工艺制备核桃油挥发性物质组成及相对含量
Table 1 Composition and contents of volatile substances in walnut oil prepared by different processes
编号 挥发性化合物 保留时间/min相对含量/%A B C D E F G H IJK香气阈值[23-24]/(mg/kg)2-丁烯醛 1.951 — 9.51±0.58cd 10.30±0.37ab — — 9.65±0.58cd 9.77±0.21bc 9.08±0.42d — — 10.59±0.38a 0.000 3 2反-2-戊烯醛 3.200 1.43±0.06c 0.72±0.00f — — 1.06±0.03e 1.24±0.07d 2.05±0.13a — — 1.59±0.03b — 2.7 3正己醛 4.115 35.78±0.69a 15.09±0.76g 17.34±0.71def 16.72±0.45f 20.47±0.77b 17.19±0.93ef 18.31±0.52de 18.63±0.81cd 18.40±0.52cde 19.69±1.17bc 20.72±0.38b 0.23 4 2-己烯醛 5.572 1.07±0.06a 0.26±0.01cde 0.19±0.01f 0.23±0.01e 0.28±0.00c 0.16±0.01f 0.28±0.01cd 0.19±0.01f 0.32±0.02b 0.26±0.01cde 0.24±0.01de 0.003 1 5反-2-己烯醛 5.812 — 0.77±0.03f 0.97±0.04de 0.95±0.06de 1.36±0.07a 0.91±0.02e 1.22±0.01b 1.01±0.03cd 1.18±0.03b 1.08±0.04c 1.30±0.07a 0.003 1 6顺-4-庚烯醛 7.747 — 0.74±0.03c 1.11±0.04a 0.87±0.05b 0.71±0.04c 0.51±0.03e 0.53±0.02e 0.63±0.01d 0.63±0.03d 0.86±0.03b 0.87±0.05b 0.04 7庚醛 7.966 1.64±0.12c 0.47±0.02e 0.53±0.02de 6.70±0.47b 0.58±0.05de 0.42±0.02e 0.83±0.04d 0.52±0.02de 7.97±0.36a 0.53±0.02de 0.63±0.01de 0.26 8反-2-庚烯醛 11.389 13.46±0.12e 24.07±0.65bc 28.61±0.43a 23.59±0.84bc 24.48±0.49bc 24.60±0.93bc 21.60±0.90d 21.00±0.47d 25.01±0.90b 24.61±1.26bc 23.44±0.94c 2.8 9反,反-2,4-庚二烯醛 14.521 3.48±0.11f 4.08±0.13de 3.83±0.14ef 4.56±0.09c 5.31±0.18ab 4.07±0.23de 5.56±0.21a 5.07±0.05b 5.10±0.52b 5.54±0.25a 4.28±0.11cd 0.057 10 2-辛烯醛 21.368 2.43±0.08a 0.44±0.04f 0.63±0.03d 0.54±0.01e 0.70±0.03c 0.53±0.03e 0.59±0.02de 0.56±0.03de 0.62±0.02d 0.62±0.06d 0.81±0.02b 0.005 11 壬醛 27.351 2.48±0.02a 0.39±0.02e 0.45±0.02d 0.42±0.02de 0.59±0.04c 0.39±0.02e 0.58±0.04c 0.44±0.03de 0.43±0.02de 0.47±0.03d 0.78±0.03b 0.003 1 12 反-2-壬醛 35.676 0.23±0.01a 0.05±0.00c — — — 0.04±0.00d 0.05±0.00c 0.05±0.00c 0.05±0.00c 0.08±0.00b — 0.000 09 13 乙醛 43.137 — 0.01±0.00b — — — — — 0.01±0.00b 0.01±0.00b 0.01±0.00b 0.02±0.00a 0.002 7 14 反,反-2,4-癸二烯醛 61.701 4.94±0.12c 5.02±0.14c 5.13±0.28c 5.34±0.17c 5.91±0.09b 4.39±0.17d 4.98±0.37c 6.35±0.55b 6.85±0.29a 6.94±0.12a 4.45±0.20d 0.000 077 15 4-氯代醛 50.098 0.48±0.03a 0.05±0.00d 0.08±0.00c 0.07±0.00c 0.12±0.01b — — — — — — —16 4-戊烯醛 3.189 0.25±0.01c — 1.25±0.08b 1.83±0.04a — — — 0.01±0.01d — — — 0.022 17 正辛醛 22.721 0.77±0.02a — 0.01±0.00bc 0.02±0.00b — — 0.02±0.00b 0.01±0.00bc 0.02±0.00b 0.01±0.00bc 0.01±0.01bc 0.17 18 4-甲基-己醛 50.525 0.01±0.00b — 0.03±0.00a — — — — — — — — —19 反-2-癸烯醛 52.617 1.08±0.04a — 0.66±0.02b — — 0.46±0.02c 0.31±0.01e — 0.38±0.03d — — 0.017 20 反-2-十一烯醛 70.421 — — 0.05±0.00a 0.04±0.00ab — 0.03±0.00b — — 0.03±0.00b 0.05±0.00a — 0.044 21 十二醛二甲缩醛 11.753 — — 0.10±0.01a — — 0.02±0.00b — 0.02±0.00b 0.02±0.00b 0.02±0.00b — —22 反,反-2,4-壬二烯醛 41.378 0.20±0.01b — — — — — 0.17±0.01c — — — 0.22±0.01a 0.000 2 23 戊醛 2.33611.79±0.25a— — — — — — — — — — 0.85 24 2,2-二甲基-4-戊烯醛 33.397 0.04±0.00a — — — — — — — — — — —25 癸醛 40.6290.08±0.00a— — — — — — — — — — 0.002 6 26 2-十一烯醛 64.562 0.79±0.03a — — — — — — — — — — 0.044 27 反-2-十二烯醛 77.549 0.02±0.00a — — — — — — — — — — 0.011 28 7-十六碳烯醛 80.129 0.02±0.00a — — — — — — — — — — —29 3,5-二叔丁基-4-羟基苯甲醛 80.701 0.20±0.01a — — — — — — — — — — —醛类1醇类30 4-甲基环己醇 2.378 — 5.83±0.08e 6.34±0.33d — 7.97±0.36b 6.26±0.27d 6.52±0.24d 9.36±0.09a — 7.03±0.19c 7.25±0.33c —31 1-辛烯-3-醇 17.559 0.90±0.02a 0.06±0.00ef 0.10±0.01c 0.07±0.00de 0.07±0.00de 0.05±0.00f 0.08±0.00d 0.05±0.00f 0.06±0.00ef 0.08±0.00d 0.15±0.00b 0.001 32 顺-3-辛烯-1-醇 17.560 — 0.16±0.00f 0.18±0.01e 0.14±0.00g 0.29±0.00a — 0.26±0.02b 0.21±0.01d 0.22±0.01cd 0.23±0.01c 0.10±0.00h —33 反-2-壬烯-1-醇 17.362 0.42±0.04a 0.14±0.01e 0.05±0.00f 0.05±0.00f 0.22±0.02d 0.13±0.00e 0.26±0.01c 0.21±0.00d 0.14±0.00e 0.14±0.01e 0.33±0.02b —34 异戊醇 3.481 2.21±0.07a — — — — — — — — — — —35 4-乙基-1-辛炔-3-醇 14.740 0.16±0.01a — — — — — — — — — — —36 2-甲基-1-庚烯-3-醇 22.783 0.38±0.01a — — — — — — — — — — —37 正辛醇 27.456 0.13±0.01a — — — — — — — — — — —38 1-壬醇 45.218 0.16±0.01a — — — — — — — — — — 0.018 39 1-十四醇 79.213 0.01±0.00a — — — — — — — — — — —40 反-2-十二烯-1-醇 76.570 0.01±0.00a — — — — — — — — — — —酮类41 仲辛酮 14.209 — 0.05±0.00d 0.07±0.00c 0.09±0.01b 0.10±0.00ab — 0.07±0.00c 0.05±0.00d 0.07±0.00c 0.09±0.01b 0.11±0.01a 0.23 42 3-辛烯-2-酮 19.349 — 0.15±0.00d 0.15±0.01d — 0.24±0.01b — 0.25±0.01b 0.28±0.02a — 0.19±0.01c — —43 3,5-辛二烯-2-酮 23.200 0.50±0.01a 0.08±0.00g 0.08±0.00g 0.15±0.01e 0.22±0.01d 0.09±0.00g 0.25±0.01c 0.26±0.01c 0.21±0.02d 0.28±0.00b 0.13±0.01f —44 3-壬烯-2-酮 32.783 0.39±0.03a 0.03±0.00d 0.04±0.00cd — — 0.04±0.00cd 0.05±0.00bc 0.05±0.00bc 0.05±0.00bc 0.06±0.00b 0.05±0.00bc 0.03 45 1-辛烯-3-酮 12.929 0.06±0.00b — — 0.06±0.00c — — — — — 0.07±0.00a — —46 2,5-己二酮 9.610 0.16±0.00a — — — — — — — — — — —47 3-壬烯-2-酮 31.326 0.27±0.03a — — — — — — — — — — —48 4-甲基-3-庚酮 36.456 0.02±0.00a — — — — — — — — — — —酯类49 丙酸己酯 3.002 — 0.07±0.00g 0.38±0.01f 0.86±0.03c 0.03±0.00gh 0.54±0.02e 0.84±0.02c 1.14±0.06b 1.25±0.09a 0.70±0.03d 0.84±0.03c —50 丙酸辛酯 6.634 — 0.06±0.00fg 0.05±0.00g 0.06±0.00g 0.08±0.00e 0.11±0.01d 0.19±0.01b 0.06±0.00fg 0.13±0.00c 0.07±0.00ef 0.20±0.01a —
续表1
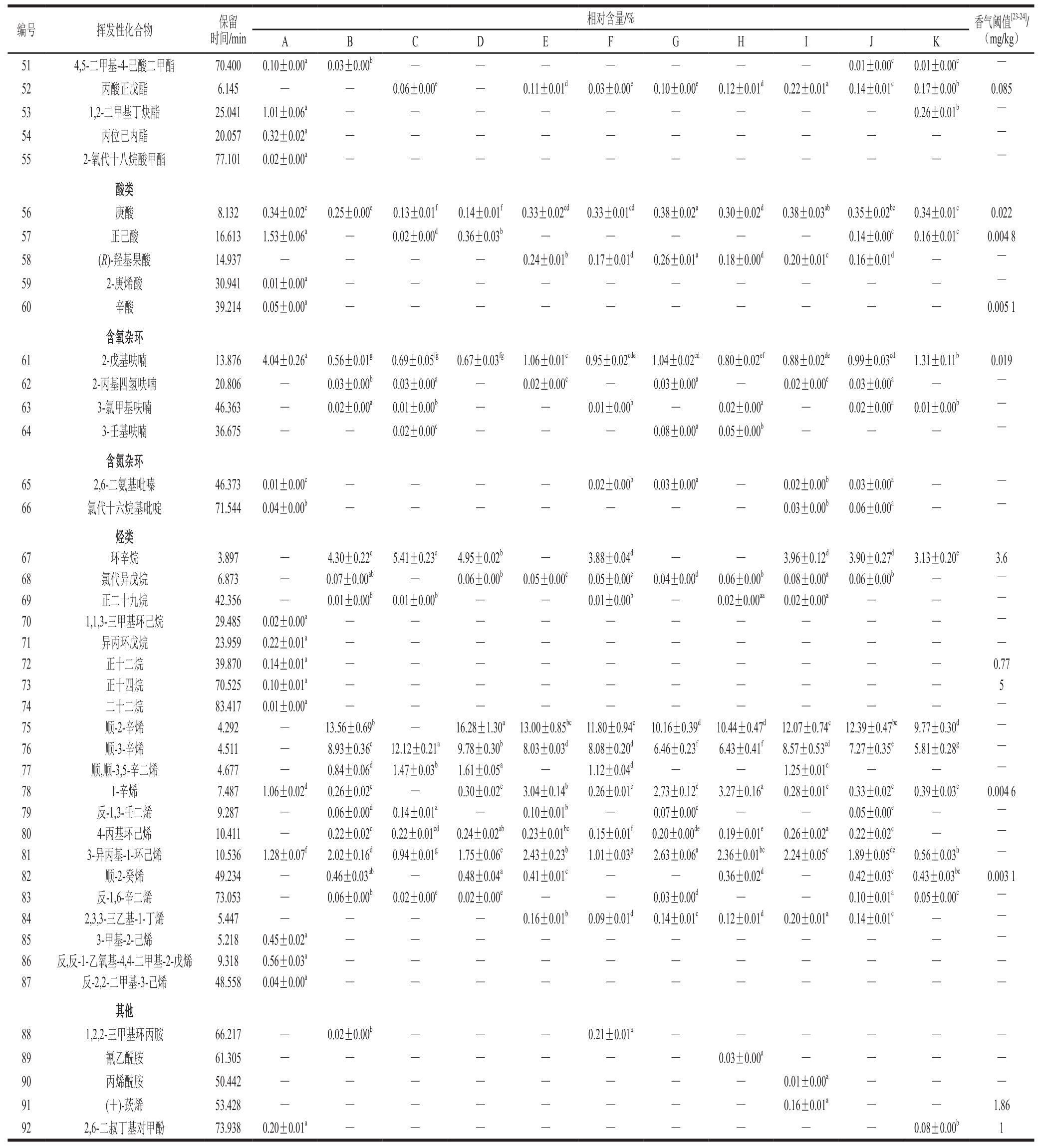
注:—.未检出;下同。同行肩标不同字母表示差异显著(P<0.05)。
编号 挥发性化合物 保留时间/min相对含量/%A B C D E F G H IJK香气阈值[23-24]/(mg/kg)51 4,5-二甲基-4-己酸二甲酯 70.400 0.10±0.00a 0.03±0.00b — — — — — — — 0.01±0.00c 0.01±0.00c —52 丙酸正戊酯 6.145 — — 0.06±0.00e — 0.11±0.01d 0.03±0.00e 0.10±0.00e 0.12±0.01d 0.22±0.01a 0.14±0.01c 0.17±0.00b 0.085 53 1,2-二甲基丁炔酯 25.041 1.01±0.06a — — — — — — — — — 0.26±0.01b —54 丙位己内酯 20.057 0.32±0.02a — — — — — — — — — — —55 2-氧代十八烷酸甲酯 77.101 0.02±0.00a — — — — — — — — — — —酸类56 庚酸 8.132 0.34±0.02c 0.25±0.00e 0.13±0.01f 0.14±0.01f 0.33±0.02cd 0.33±0.01cd 0.38±0.02a 0.30±0.02d 0.38±0.03ab 0.35±0.02bc 0.34±0.01c 0.022 57 正己酸 16.613 1.53±0.06a — 0.02±0.00d 0.36±0.03b — — — — — 0.14±0.00c 0.16±0.01c 0.004 8 58 (R)-羟基果酸 14.937 — — — — 0.24±0.01b 0.17±0.01d 0.26±0.01a 0.18±0.00d 0.20±0.01c 0.16±0.01d — —59 2-庚烯酸 30.941 0.01±0.00a — — — — — — — — — — —60 辛酸 39.2140.05±0.00a— — — — — — — — — — 0.005 1含氧杂环61 2-戊基呋喃 13.876 4.04±0.26a 0.56±0.01g 0.69±0.05fg 0.67±0.03fg 1.06±0.01c 0.95±0.02cde 1.04±0.02cd 0.80±0.02ef 0.88±0.02de 0.99±0.03cd 1.31±0.11b 0.019 62 2-丙基四氢呋喃 20.806 — 0.03±0.00b 0.03±0.00a — 0.02±0.00c — 0.03±0.00a — 0.02±0.00c 0.03±0.00a — —63 3-氯甲基呋喃 46.363 — 0.02±0.00a 0.01±0.00b — — 0.01±0.00b — 0.02±0.00a — 0.02±0.00a 0.01±0.00b —64 3-壬基呋喃 36.675 — — 0.02±0.00c — — — 0.08±0.00a 0.05±0.00b — — — —含氮杂环65 2,6-二氨基吡嗪 46.373 0.01±0.00c — — — — 0.02±0.00b 0.03±0.00a — 0.02±0.00b 0.03±0.00a — —66 氯代十六烷基吡啶 71.544 0.04±0.00b — — — — — — — 0.03±0.00b 0.06±0.00a — —烃类67 环辛烷 3.897 — 4.30±0.22c 5.41±0.23a 4.95±0.02b — 3.88±0.04d — — 3.96±0.12d 3.90±0.27d 3.13±0.20e 3.6 68 氯代异戊烷 6.873 — 0.07±0.00ab — 0.06±0.00b 0.05±0.00c 0.05±0.00c 0.04±0.00d 0.06±0.00b 0.08±0.00a 0.06±0.00b — —69 正二十九烷 42.356 — 0.01±0.00b 0.01±0.00b — — 0.01±0.00b — 0.02±0.00aa 0.02±0.00a — — —70 1,1,3-三甲基环己烷 29.485 0.02±0.00a — — — — — — — — — — —71 异丙环戊烷 23.959 0.22±0.01a — — — — — — — — — — —72 正十二烷 39.870 0.14±0.01a — — — — — — — — — — 0.77 73 正十四烷 70.525 0.10±0.01a — — — — — — — — — — 5 74 二十二烷 83.417 0.01±0.00a — — — — — — — — — — —75 顺-2-辛烯 4.292 — 13.56±0.69b — 16.28±1.30a 13.00±0.85bc 11.80±0.94c 10.16±0.39d 10.44±0.47d 12.07±0.74c 12.39±0.47bc 9.77±0.30d —76 顺-3-辛烯 4.511 — 8.93±0.36c 12.12±0.21a 9.78±0.30b 8.03±0.03d 8.08±0.20d 6.46±0.23f 6.43±0.41f 8.57±0.53cd 7.27±0.35e 5.81±0.28g —77 顺,顺-3,5-辛二烯 4.677 — 0.84±0.06d 1.47±0.03b 1.61±0.05a — 1.12±0.04d — — 1.25±0.01c — — —78 1-辛烯 7.487 1.06±0.02d 0.26±0.02e — 0.30±0.02e 3.04±0.14b 0.26±0.01e 2.73±0.12c 3.27±0.16a 0.28±0.01e 0.33±0.02e 0.39±0.03e 0.004 6 79 反-1,3-壬二烯 9.287 — 0.06±0.00d 0.14±0.01a — 0.10±0.01b — 0.07±0.00c — — 0.05±0.00e — —80 4-丙基环己烯 10.411 — 0.22±0.02c 0.22±0.01cd 0.24±0.02ab 0.23±0.01bc 0.15±0.01f 0.20±0.00de 0.19±0.01e 0.26±0.02a 0.22±0.02c — —81 3-异丙基-1-环己烯 10.536 1.28±0.07f 2.02±0.16d 0.94±0.01g 1.75±0.06e 2.43±0.23b 1.01±0.03g 2.63±0.06a 2.36±0.01bc 2.24±0.05c 1.89±0.05de 0.56±0.03h —82 顺-2-癸烯 49.234 — 0.46±0.03ab — 0.48±0.04a 0.41±0.01c — — 0.36±0.02d — 0.42±0.03c 0.43±0.03bc 0.003 1 83 反-1,6-辛二烯 73.053 — 0.06±0.00b 0.02±0.00e 0.02±0.00e — — 0.03±0.00d — — 0.10±0.01a 0.05±0.00c —84 2,3,3-三乙基-1-丁烯 5.447 — — — — 0.16±0.01b 0.09±0.01d 0.14±0.01c 0.12±0.01d 0.20±0.01a 0.14±0.01c — —85 3-甲基-2-己烯 5.218 0.45±0.02a — — — — — — — — — — —86 反,反-1-乙氧基-4,4-二甲基-2-戊烯 9.318 0.56±0.03a — — — — — — — — — — —87 反-2,2-二甲基-3-己烯 48.558 0.04±0.00a — — — — — — — — — — —其他88 1,2,2-三甲基环丙胺 66.217 — 0.02±0.00b — — — 0.21±0.01a — — — — — —89 氰乙酰胺 61.305 — — — — — — — 0.03±0.00a — — — —90 丙烯酰胺 50.442 — — — — — — — — 0.01±0.00a — — —91 (+)-莰烯 53.428 — — — — — — — — 0.16±0.01a — — 1.86 92 2,6-二叔丁基对甲酚 73.938 0.20±0.01a — — — — — — — — — 0.08±0.00b 1
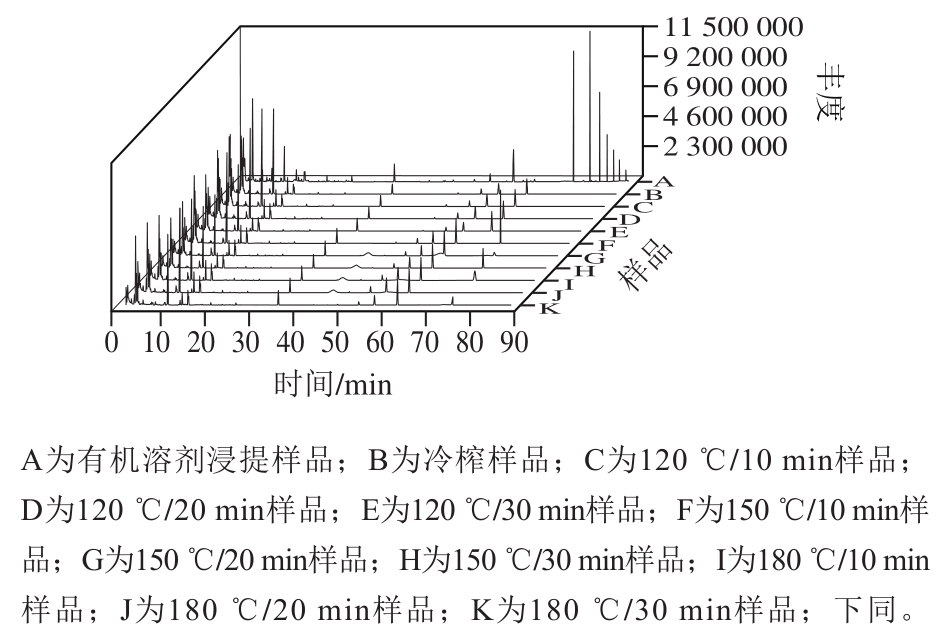
图1 不同工艺制备核桃油总离子流图
Fig. 1 Total ion current chromatograms of volatile substances in walnut oil prepared by different processes
由以上分析可知,不同制备工艺所得核桃油样品的挥发性物质构成存在显著差异(P<0.05),有机溶剂浸提法所得样品与压榨法的挥发性物质存在一定差异性,由于溶剂热萃取的作用以及萃取过程对脂肪酸有更大的分解作用[25],部分挥发性物质只在有机溶剂浸提样品中检测到,包括反,反-2,4-壬二烯醛、戊醛、异戊醇、正辛醇、1-辛烯-3-酮、2,5-己二酮、3-壬烯-2-酮、1,2-二甲基丁炔酯、丙位己内酯、2-庚烯酸、辛酸、3-甲基-2-己烯、反-2,2-二甲基-3-己烯等,但是由于这些物质感觉阈值较高,含量较低,因此对整体风味贡献不大。
如图2所示,核桃油样品中醛类占比最高,为61.57%~82.67%,其次为烃类(3.88%~35.47%)、醇类(0.26%~9.83%)、含氧杂环(0.61%~4.04%),其余几类物质含量占比较低,其中有机溶剂浸提样品中的醛类物质占比最高,烃类物质占比最低。
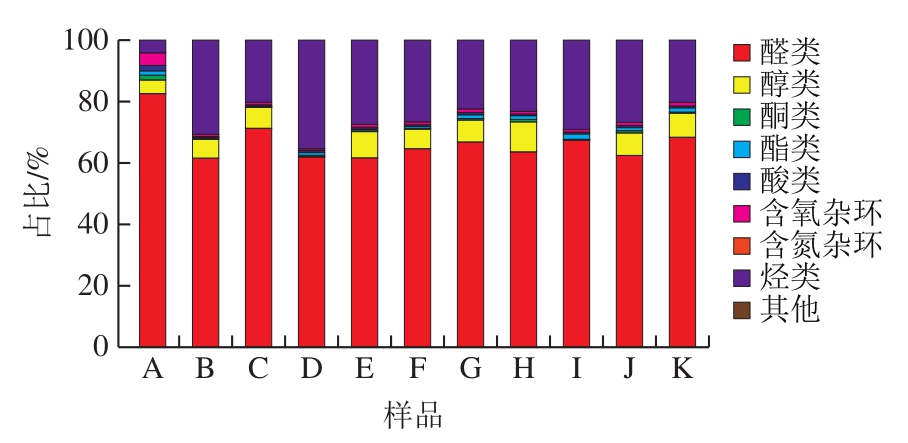
图2 不同工艺制备核桃油挥发性物质占比
Fig. 2 Proportions of volatile substances in walnut oil prepared by different processes
醛类物质中,有机溶剂浸提核桃油中相对含量最高的为正己醛(35.78%),其次为反-2-庚烯醛(13.46%);冷榨核桃油和热榨核桃油中相对含量最高的是反-2-庚烯醛(21.00%~28.61%),其次为正己醛(15.09%~20.72%)。醛类物质主要来自于脂质分子的自由基的裂解。脂质自动氧化生成的过氧化物在超过150 ℃时易分解,生成烷氧基自由基和羟自由基,烷氧基自由基进一步裂解形成挥发性的醛、烯和醇等有机化合物[26]。醛类物质具有清香、果香、脂肪香等香气特征,其检出浓度较高且香气阈值较低,是核桃油的主要呈香物质。
烃类物质中,有机溶剂浸提核桃油中相对含量最高的为3-异丙基-1-环己烯(1.28%),其次为1-辛烯(1.06%);冷榨核桃油中相对含量最高的是顺-2-辛烯(13.56%),其次为顺-3-辛烯(8.93%);120 ℃/10 min热榨核桃油中相对含量最高的是顺-3-辛烯(12.12%),其次为环辛烷(5.41%),其余热榨核桃油中相对含量最高的是顺-2-辛烯(9.77%~16.28%),其次为顺-3-辛烯(5.81%~9.78%)。烃类物质在所有样品中均有检出,包括饱和烃和不饱和烃,不饱和烃阈值较低,饱和烃阈值较高,主要来自于脂肪酸烷氧基的裂解,对风味贡献不大[27]。
醇类物质中,有机溶剂浸提核桃油中相对含量最高的为异戊醇(2.21%),其次为1-辛烯-3-醇(0.90%);冷榨核桃油和热榨核桃油中主要挥发性物质为4-甲基环己醇(5.83%~9.36%)、反-2-壬烯-1-醇(0.05%~0.33%)、顺-3-辛烯-1-醇(0.10%~0.29%)和1-辛烯-3-醇(0.05%~0.15%)。饱和醇类阈值较高,高浓度下才会对核桃油风味有贡献作用。不饱和醇类阈值相对较低,对核桃油风味有较大贡献作用[28],如1-辛烯-3-醇。
2-戊基呋喃是核桃油挥发性物质含氧杂环中相对含量最高的物质,为0.56%~4.04%,一般为碳水化合物或不饱和脂肪酸氧化产生[29],表现为绿豆、黄油味,但其含量较低,对核桃油风味贡献不大。
2.2 不同工艺核桃油关键香气成分分析
核桃油的总体风味是由其挥发性成分的相对含量及感觉阈值共同决定的。只有部分化合物对核桃油总体风味起到显著贡献,这些化合物即为样品的关键风味物质。在衡量挥发性物质对风味的贡献时,仅以物质的相对含量进行判断不够全面和准确。研究样品往往包含几十甚至上百种挥发性化合物,气味活度值的绝对定量非常繁琐且成本较高,因此为进一步分析各挥发性物质对核桃油风味的贡献程度,采用计算ROAV进行分析[30-31]。
根据文献查阅得到的感觉阈值计算出核桃油挥发性物质构成中ROAV大于0.1的挥发性物质[23-24],结果如表2所示,其中反,反-2,4-癸二烯醛是核桃油中风味贡献最大的物质。在有机溶剂浸提样品中,反,反-2,4-癸二烯醛、反式-2-壬醛、反,反-2,4-壬二烯醛、1-辛烯-3-醇和壬醛是关键香气成分;在冷榨样品、120 ℃/10 min样品、150 ℃/10 min样品、150 ℃/30 min样品中,反,反-2,4-癸二烯醛和2-丁烯醛是关键香气成分;在120 ℃/20 min样品、120 ℃/20 min样品、180 ℃/10 min样品和180 ℃/20 min样品中,反,反-2,4-癸二烯醛是关键香气成分;在150 ℃/20 min样品、180 ℃/30 min样品中,反,反-2,4-癸二烯醛、2-丁烯醛和反,反-2,4-壬二烯醛是关键香气成分,其余物质对核桃油的风味起修饰作用。王勇[32]利用顶空固相微萃取-气相色谱-质谱结合ROAV法对市售核桃油的香气成分进行了分析,测出9 种关键挥发性香气成分,分别为反,反-2,4-癸二烯醛、1-辛烯-3-醇、己醛、壬醛、2-辛烯醛、辛醛、反-2-癸烯醛、反-2-庚烯醛、2-戊基呋喃,与本研究结果相似。何金鑫[33]利用ROAV法计算分析出了山核桃的关键风味物质,包括己醛、庚醛、辛醛、壬醛、2-辛烯醛、1-辛烯-3-醇、庚醇、2-壬烯醛、2-癸烯醛,与本研究结果有所差异的原因可能是核桃的品种不一致,以及在制油过程中部分挥发性物质未进入油相,残留在核桃蛋白粕里。
表2 不同工艺制备核桃油挥发性物质的ROAV
Table 2 ROAV values of volatile substances in walnut oil prepared by different processes
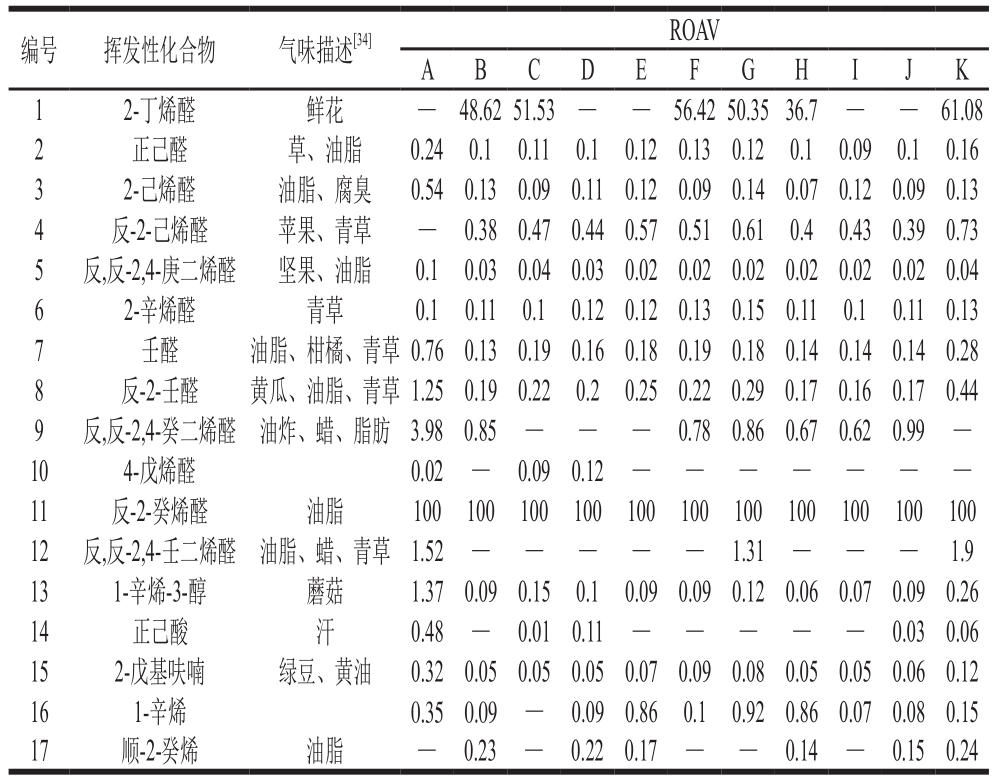
编号 挥发性化合物 气味描述[34]ROAV A B C D E F G H I J K 1 2-丁烯醛 鲜花 — 48.6251.53— — 56.4250.3536.7 — — 61.08 2 正己醛 草、油脂 0.24 0.1 0.11 0.1 0.120.130.12 0.1 0.09 0.1 0.16 3 2-己烯醛 油脂、腐臭 0.540.130.09 0.11 0.120.090.140.070.120.090.13 4 反-2-己烯醛 苹果、青草 — 0.380.470.440.570.510.61 0.4 0.430.390.73 5 反,反-2,4-庚二烯醛 坚果、油脂 0.1 0.030.040.030.020.020.020.020.020.020.04 6 2-辛烯醛 青草 0.1 0.11 0.1 0.120.120.130.15 0.11 0.1 0.110.13 7 壬醛 油脂、柑橘、青草 0.760.130.190.160.180.190.18 0.140.14 0.140.28 8 反-2-壬醛 黄瓜、油脂、青草 1.250.190.22 0.2 0.250.220.290.170.160.170.44 9 反,反-2,4-癸二烯醛 油炸、蜡、脂肪 3.980.85 — — — 0.780.860.670.620.99 —10 4-戊烯醛 0.02 — 0.090.12 — — — — — — —11 反-2-癸烯醛 油脂 100 100 100 100 100 100 100 100 100 100 100 12 反,反-2,4-壬二烯醛 油脂、蜡、青草 1.52 — — — — — 1.31 — — — 1.9 13 1-辛烯-3-醇 蘑菇 1.370.090.15 0.1 0.090.090.12 0.060.07 0.090.26 14 正己酸 汗 0.48—0.010.11— — — — — 0.030.06 15 2-戊基呋喃 绿豆、黄油 0.320.050.050.050.070.090.080.050.050.060.12 16 1-辛烯 0.350.09 — 0.090.86 0.1 0.920.860.070.080.15 17 顺-2-癸烯 油脂 — 0.23— 0.220.17— — 0.14— 0.150.24
2.3 不同工艺核桃油关键香气成分PCA
PCA是采取降维的方法,找出对样品贡献最大和最主要的因子,利用PCA空间分布图可以在最大程度上体现因子间的差异性[35]。对表2中的17 种挥发性物质进行PCA,如图3所示。共提取到2 个PC,PC1(66%)和PC2(29%),累计方差贡献率为95%(大于85%),可以较好反映原始数据的绝大部分信息,完全符合PCA要求[36]。
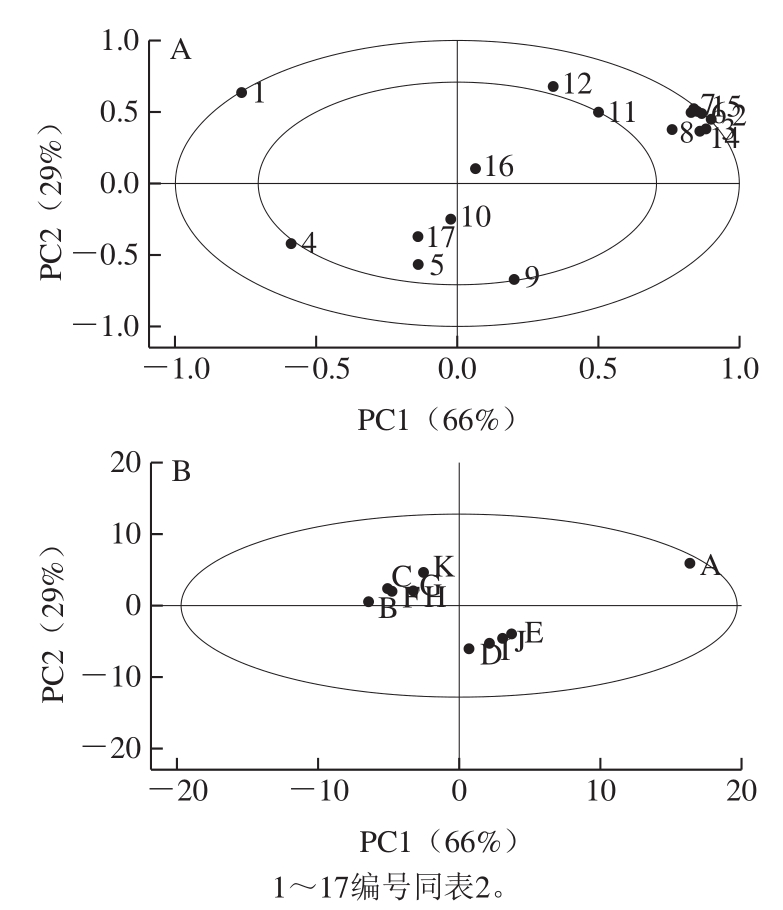
图3 PCA得分图(A)和载荷图(B)
Fig. 3 PCA scores (A) and correlation loadings (B) plots
图3A结果表明,正己醛(2)、2-己烯醛(3)、2-辛烯醛(6)、壬醛(7)、反-2-壬醛(8)、1-辛烯-3-醇(13)、正己酸(14)和2-戊基呋喃(15)与PC1显示出较强的正相关,2-丁烯醛(1)与PC1显示出较强的负相关;PC2与2-丁烯醛(1)、反,反-2,4-壬二烯醛(12)显示出较强的正相关,与反,反-2,4-癸二烯醛(9)显示出较强的负相关。结合ROAV可得,壬醛(7)、反-2-壬醛(8)、反,反-2,4-癸二烯醛(9)和1-辛烯-3-醇(12)为核桃油中的关键香气成分。壬醛为油脂、柑橘和青草味,反-2-壬醛为黄瓜、油脂和青草味,反,反-2,4-癸二烯醛为油炸、蜡、油脂味,1-辛烯-3-醇为蘑菇味,共同构成了核桃油的整体风味。Mu Honglei等[37]研究了氧化过程中的核桃油挥发性物质,PCA结果显示2-辛烯醛、己醛、2-庚醛、1-辛烯-3-醇、己酸和壬醛是主要的风味物质,与本研究相似,均分析认为1-辛烯-3-醇和壬醛是核桃油中的关键香气成分。
图3B可以很明显区分不同工艺核桃油样品。样品A与其他样品距离较远,说明样品A与其他样品风味具有明显差异,即可以通过挥发性物质将有机溶剂浸提所得核桃油与压榨所得核桃油区分开。其中150 ℃/10 min样品(F)、150 ℃/20 min样品(G)和150 ℃/30 min样品(H)聚在一起,说明这些样品的挥发性成分具有相似性,其余样品分布无规律。
2.4 不同工艺核桃油热图分析
图4中每种成分平均值的差值大小用不同颜色深浅表示,颜色越深含量越多,颜色越浅含量越少,最深色为不同样品间特有成分[38]。从图4可以看出,有机溶剂浸提样品与压榨所得样品色差较大,说明2 类样品挥发性香气物质差异性明显。从样品聚类结果进行分析,主要分为了两大类,一类是有机溶剂浸提样品,另一类是压榨所得样品,可得到相同结论。对于a区域的挥发性物质来说,有机溶剂浸提所得样品的含量均高于压榨所得样品。对于b区域挥发性物质,有机溶剂浸提所得样品的含量均小于压榨所得样品。对于其他区域挥发性物质,样品的挥发性物质含量呈现无规律变化。因此可通过a和b区域的化合物对核桃油的制备工艺进行区分。

图4 挥发性物质聚类热图
Fig. 4 Clustering heat map of volatile substances in walnut oil prepared by different processes
3 结 论
通过分析不同工艺制备的11 个核桃油样品挥发性香气物质,并通过ROAV和PCA法确定样品中的关键香气成分。结果表明,11 个核桃油样品中共鉴定出92 种挥发性香气物质,其中有29 种醛类、21 种烃类、11 种醇类、8 种酮类、7 种酯类、5 种酸类、4 种含氧杂环、2 种含氮杂环以及5 种其他化合物。不同提取工艺得到的样品挥发性香气物质构成不同,有机溶剂浸提法所得样品与压榨样品的挥发性香气物质存在一定差异,对于压榨核桃油样品,包括冷榨和热榨,挥发性香气物质含量较高的是反-2-庚烯醛、正己醛和顺-2-辛烯;对于有机溶剂浸提核桃油样品,挥发性香气物质含量较高的是正己醛、反-2-庚烯醛和戊醛。结合ROAV和PCA,确定了壬醛、反-2-壬醛、反,反-2,4-癸二烯醛和1-辛烯-3-醇是核桃油中的关键香气成分。通过挥发性成分聚类热图分析,不同工艺制备的样品之间色差较大,表明挥发性物质可作为区分不同工艺制备核桃油的判别方式。
[1]BAKKALBASI E. Oxidative stability of enriched walnut oil with phenolic extracts from walnut press-cake under accelerated oxidation conditions and the effect of ultrasound treatment[J]. Journal of Food Measurement and Characterization, 2019, 13(1): 43-50. DOI:10.1007/s11694-018-9917-y.
[2]万本屹, 董海洲, 李宏, 等. 核桃油的特性及营养价值的研究[J]. 西部粮油科技, 2001(5): 18-20. DOI:10.3969/j.issn.1007-6395.2001.05.006.
[3]黄江艳, 李秀娟, 潘思轶. 固相微萃取技术在食品风味分析中的应用[J]. 食品科学, 2012, 33(7): 289-298.
[4]王丁丁, 赵见军, 张润光, 等. 核桃油研究进展[J]. 食品工业科技,2013, 34(16): 383-387.
[5]代增英, 高克栋, 冯建岭, 等. 核桃油的研究进展[J]. 江苏调味副食品, 2014(1): 6-8. DOI:10.3969/j.issn.1006-8481.2014.01.003.
[6]管伟举, 陈钊, 谷克仁. 核桃油研究进展[J]. 粮食与油脂, 2010(5):39-41. DOI:10.3969/j.issn.1008-9578.2010.05.013.
[7]杨春英, 刘学铭, 王思远, 等. SPME-GC/MS分析植物油挥发性风味成分[J]. 中国粮油学报, 2015, 30(10): 127-134. DOI:10.3969/j.issn.1003-0174.2015.10.024.
[8]周晔, 樊玮, 张俊佩, 等. 压榨和精炼核桃油挥发性成分的比较及其电子鼻判别[J]. 中国油脂, 2017, 42(2): 130-134; 140. DOI:10.3969/j.issn.1003-7969.2017.02.030.
[9]罗凡, 费学谦, 戚雨婷, 等. 加热温度对核桃油理化品质的影响规律研究[J]. 中国粮油学报, 2018, 33(6): 51-58. DOI:10.3969/j.issn.1003-0174.2018.06.010.
[10]杨朝晖, 马磊, 孟阿会, 等. 固相微萃取GC/MS法测定氧化核桃油中挥发性成分[J]. 农业机械, 2011(26): 59-60.
[11]宋婉瑶, 刘玉亮, 姚雷. 有机溶剂萃取与SPME提取的玫瑰水挥发性成分对比分析[J]. 上海交通大学学报(农业科学版), 2016, 34(4):57-64. DOI:10.3969/j.issn.1671-9964.2016.04.010.
[12]焦曌. 浙江山核桃油脂品质与香气的研究[D]. 长沙: 中南林业科技大学, 2010.
[13]ZHOU Y, FAN W, CHU F X, et al. Improvement of the flavor and oxidative stability of walnut oil by microwave pretreatment[J]. Journal of the American Oil Chemists’ Society, 2016, 93(11): 1563-1572.DOI:10.1007/s11746-016-2891-9.
[14]钟海雁, 黄永辉, 龙奇志, 等. 食用油气味的研究方法及展望[J]. 食品科技, 2007, 32(9): 8-11. DOI:10.3969/j.issn.1005-9989.2007.09.006.
[15]郭凯, 芮汉明. 食品中挥发性风味成分的分离、分析技术和评价方法研究进展[J]. 食品与发酵工业, 2007, 33(4): 110-115.DOI:10.3321/j.issn:0253-990X.2007.04.028.
[16]闫圣坤, 杨嘉鹏, 王庆惠, 等. 低温冷榨核桃油工艺及主要压榨参数优化[J]. 农业工程, 2020, 10(1): 48-52. DOI:10.3969/j.issn.2095-1795.2020.01.014.
[17]罗凡, 费学谦, 郭少海, 等. 不同干燥方式对核桃仁及核桃油理化品质的影响[J]. 中国油脂, 2019, 44(2): 8-13. DOI:10.3969/j.issn.1003-7969.2019.02.003.
[18]刘雪芳, 郝利平, 常月梅. 索氏抽提法提取核桃油工艺的优化[J]. 山西农业科学, 2017, 45(1): 34-36. DOI:10.3969/j.issn.1002-2481.2017.01.09.
[19]TAHRI K, DUARTE A A, CARVALHO G, et al. Distinguishment,identification and aroma compound quantification of Portuguese olive oils based on physicochemical attributes, HS-GC/MS analysis and voltammetric electronic tongue[J]. Journal of the Science of Food and Agriculture, 2018, 98(2): 681-690. DOI:10.1002/jsfa,8515.
[20]陈卓. 新疆红花籽油特征挥发性香气分析在品控中的应用[D].石河子: 石河子大学, 2018.
[21]谢诚, 欧昌荣, 汤海青, 等. 食品中挥发性风味成分提取技术研究进展[J]. 核农学报, 2015, 29(12): 2366-2374. DOI:10.11869/j.issn.100-8551.2015.12.2366.
[22]栗维志. 静态顶空进样器污染处理办法及避免进样交叉污染[J]. 河北化工, 2010, 33(6): 66-67; 77. DOI:10.3969/j.issn.1003-5059.2010.06.028.
[23]VAN GEMERT L J. Odour thresholds[M]. The Netherlands: Oliemans Punter & Partners BV, 2011.
[24]里奥·范海默特. 化合物嗅觉阈值汇编[M]. 北京: 中国科学技术出版社, 2018: 5.
[25]MORENO A O, DORANTES L, GALINDEZ J, et al. Effect of different extraction methods on fatty acids, volatile compounds, and physical and chemical properties of avocado (Persea americana Mill.)oil[J]. Journal of Agricultural and Food Chemistry, 2003, 51(8): 2216-2221. DOI:10.1021/jf0207934.
[26]文志勇, 孙宝国, 梁梦兰, 等. 脂质氧化产生香味物质[J]. 中国油脂,2004, 29(9): 41-44. DOI:10.3321/j.issn:1003-7969.2004.09.012.
[27]李翠翠, 侯利霞, 汪学德, 等. 炒籽温度及初始水分含量对葵花籽酱挥发性风味成分的影响[J]. 食品科学, 2020, 41(14): 278-285.DOI:10.7506/spkx1002-6630-20190731-432.
[28]唐春红, 陈旭华, 张春晖, 等. 不同卤制方法对鸡腿肉中挥发性风味化合物的影响[J]. 食品科学, 2014, 35(14): 123-129. DOI:10.7506/spkx1002-6630-201414024.
[29]刘源, 周光宏, 徐幸莲, 等. 南京盐水鸭挥发性风味化合物的研究[J]. 食品科学, 2006, 27(1): 166-171. DOI:10.3321/j.issn:1002-6630.2006.01.038.
[30]刘登勇, 周光宏, 徐幸莲. 确定食品关键风味化合物的一种新方法:“ROAV”法[J]. 食品科学, 2008, 29(7): 370-374.
[31]孙灵霞, 李苗云, 靳春杰, 等. 基于电子鼻和气质联用技术分析不同品牌道口烧鸡的香气差异性[J]. 食品与发酵工业, 2020, 46(6): 238-243.
[32]王勇. HS-SPME-GC-MS结合ROAV法对市售核桃油香气成分的研究[J]. 粮食与油脂, 2020, 33(6): 63-66. DOI:10.3969/j.issn.1008-9578.2020.06.017.
[33]何金鑫. 山核桃氧化过程中挥发性产物和品质变化的研究[D].合肥: 安徽农业大学, 2017.
[34]WEI C Q, LIU W Y, XI W P, et al. Comparison of volatile compounds of hot-pressed, cold-pressed and solvent-extracted flaxseed oils analyzed by SPME-GC/MS combined with electronic nose: major volatiles can be used as markers to distinguish differently processed oils[J]. European Journal of Lipid Science and Technology, 2015,117(3): 320-330. DOI:10.1002/ejlt.201400244.
[35]MELUCCI D, BENDINI A, TESINI F, et al. Rapid direct analysis to discriminate geographic origin of extra virgin olive oils by flash gas chromatography electronic nose and chemometrics[J]. Food Chemistry,2016, 204(8): 263-273. DOI:10.1016/j.foodchem.2016.02.131.
[36]陈恺, 李琼, 周彤, 等. 不同干制方式对新疆哈密大枣香气成分的影响[J]. 食品科学, 2017, 38(14): 158-163. DOI:10.7506/spkx1002-6630-201714024.
[37]MU H L, GAO H Y, CHEN H J, et al. Study on the volatile oxidation compound and quantitative prediction of oxidation parameters in walnut (Carya cathayensis Sarg.) oil[J]. European Journal of Lipid Science and Technology, 2019, 121(6): 1800521. DOI:10.1002/ejlt.201800521.
[38]JAMI E, ISRAEL A, KOTSER A, et al. Exploring the bovine rumen bacterial community from birth to adulthood[J]. The ISME Journal,2013, 7(6): 1069-1079. DOI:10.1038/ismej.2013.2.