地参为唇形科地笋属植物毛叶地笋(Lycopus lucidus Turcz. var. hirtus Regel)的干燥根茎,是一种传统的药食兼用佳品,可炒食、油炸、做酱菜等,堪称蔬菜珍品[1]。地参野生资源广泛分布于我国大部分地区,人工栽培于云南、山东、广西、江苏、江西、重庆、浙江等省(市)[2]。目前有关地参的文献报道主要集中在酚酸类[3-4]和多糖类[5],研究表明,地参酚酸和多糖具有抗氧化、降血脂、降血糖、抗肿瘤、免疫调节等多种生物活性[6-7]。因此,地参备受人们关注,成为近年来保健食品、药品等领域研究开发与应用的热点。但地参除含有酚酸、多糖、萜类与甾体、黄酮类、挥发油、微量元素、粗蛋白外[8-10],还含有丰富的氨基酸类化合物[11-12]。
氨基酸作为蛋白质的基本组成单元和人体的必需营养成分,不仅能判断食品的营养状况,而且作为食品加工或中药炮制过程中参与美拉德反应的底物之一,同样也关联和影响着食品的风味和药物的生理活性[13-14]。早期的研究表明地参中含有丰富的氨基酸成分,总含量可达2.72%,但研究停留在对云南产野生地参的粗略统计[11-12],尚鲜见其深入的研究报道。因此,测定地参中氨基酸含量对地参的质量控制、开发利用具有重要意义。
近几年来,较为普遍的氨基酸测定方法有氨基酸分析仪法[15-17]、液相色谱-质谱串联法[18-19]、高效液相色谱法[20-21],前2 种方法成本较高,普及度不高,高效液相色谱法操作简单,成本较低,应用范围广,常用于实验室常规检测。由于氨基酸的分子质量较小,极性较强,没有发色基团[22],不利于直接检测,虽有报道采用液相色谱-带电气溶胶检测器直接测定氨基酸的含量[23],但该法灵敏度低、重现性差,故通过衍生试剂给氨基酸添加发色基团更有利于检测。目前常用的柱前衍生方法有异硫氰酸苯酯(phenyl isothiocyanate,PITC)法、6-氨基喹啉-N-羟基琥珀酰亚胺活化环氨基甲酸酯(6-aminoquinolyl-N-hydroxysuccinimidyl carbamate,AQC)法[24]、邻苯二醛(o-phthalaldehyde,OPA)法[25]、2,4-二硝基氟苯(2,4-dinitrofluorobenzene,FDNB)法[26]等。但AQC价格昂贵,OPA只能与一级氨基酸发生反应且衍生物质不稳定,FDNB法需要在避光条件下进行且毒性较大[27-28],而PITC可与一、二级氨基酸同时反应,且价格便宜、操作简单、衍生产物单一、稳定,成为柱前衍生化测定氨基酸的首选。
本研究采用PITC对地参氨基酸进行柱前衍生化,即在碱性条件下,氨基酸与PITC相结合生成具有紫外吸收的化合物[29],利用高灵敏度的超高效液相色谱(ultrahigh performance liquid chromatography,UPLC)仪进行分离检测,并通过主成分分析(principal component analysis,PCA)、聚类分析对不同产地地参样品进行差异分析,以期为地参在食品、保健食品以及药品的深入开发利用方面提供参考依据。
1 材料与方法
1.1 材料与试剂
地参自采或委托采集于云南腾冲(S1)、重庆万州(S2)、江苏徐州(S3)、山东菏泽(S4)、广西玉林(S5)、云南大理(S6)6 个地参主要栽培基地,重庆三峡学院生物与食品工程学院鉴定为唇形科地笋属植物毛叶地笋的干燥根茎。
天冬氨酸 成都德思特生物技术有限公司;16 种氨基酸标准品 合肥博美生物科技有限公司;氨基酸信息详见表1。
表1 17 种氨基酸信息
Table 1 Information about 17 amino acids tested in this study
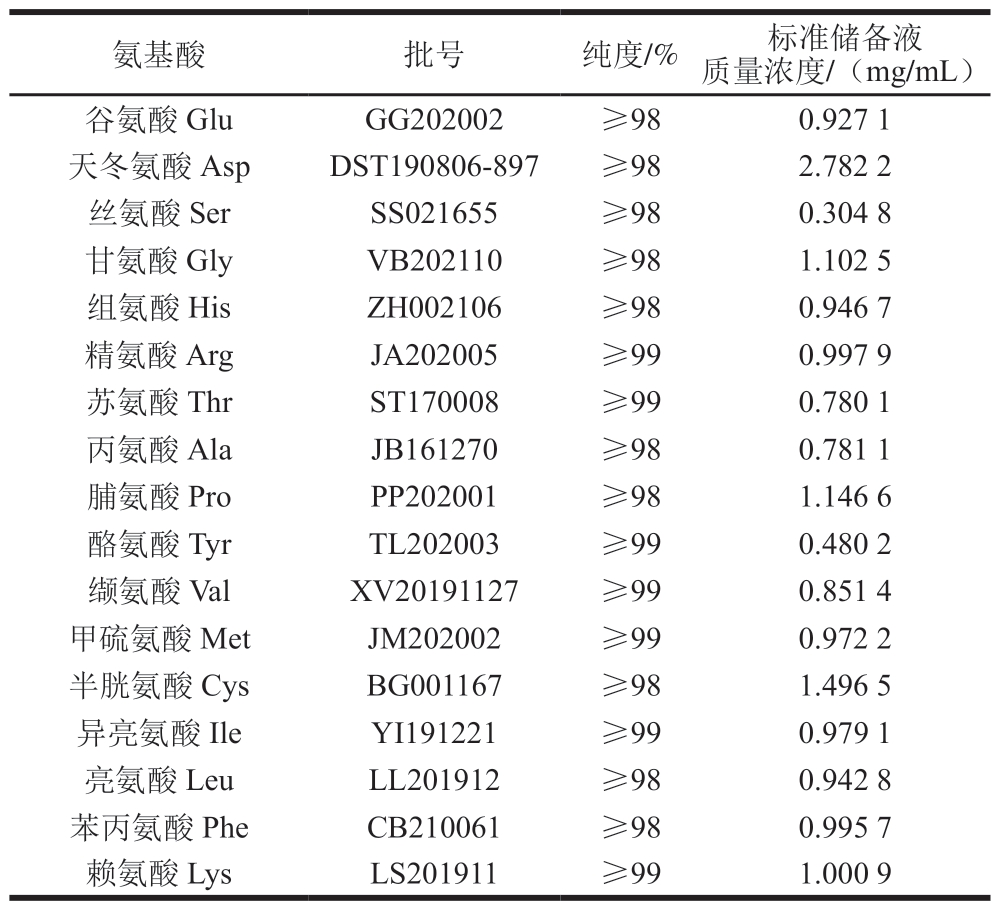
氨基酸 批号 纯度/% 标准储备液质量浓度/(mg/mL)谷氨酸 Glu GG202002 ≥98 0.927 1天冬氨酸 Asp DST190806-897 ≥98 2.782 2丝氨酸 Ser SS021655 ≥98 0.304 8甘氨酸 Gly VB202110 ≥98 1.102 5组氨酸 His ZH002106 ≥98 0.946 7精氨酸 Arg JA202005 ≥99 0.997 9苏氨酸 Thr ST170008 ≥99 0.780 1丙氨酸 Ala JB161270 ≥98 0.781 1脯氨酸 Pro PP202001 ≥98 1.146 6酪氨酸 Tyr TL202003 ≥99 0.480 2缬氨酸 Val XV20191127 ≥99 0.851 4甲硫氨酸 Met JM202002 ≥99 0.972 2半胱氨酸 Cys BG001167 ≥98 1.496 5异亮氨酸 Ile YI191221 ≥99 0.979 1亮氨酸 Leu LL201912 ≥98 0.942 8苯丙氨酸 Phe CB210061 ≥98 0.995 7赖氨酸 Lys LS201911 ≥99 1.000 9
盐酸、三乙胺、苯酚、乙酸钠、冰醋酸(均为分析纯) 成都科龙化工试剂厂;PITC(纯度≥99%,蛋白测序级) 上海麦克林生化科技有限公司;乙腈(色谱纯) 德国默克公司;实验用水为去离子超纯水。
1.2 仪器与设备
ACQUITY UPLC H-Class UPLC仪(配有二极管阵列检测器和Empower色谱工作站) 美国Waters公司;Milli-Q Advantage A10超纯水机(电阻率≥18.2 MΩ·cm)美国Millipore公司;3-30KS型高速离心机 德国Sigma公司;MS3型涡旋混合器 德国IKA公司;SQP万分之一电子天平 德国Sartorius公司;TurboVap LV氮吹仪瑞典Biotage公司;BPG-9240A精密鼓风干燥箱 上海一恒科学仪器有限公司。
1.3 方法
1.3.1 标准溶液的制备
分别称取17 种氨基酸标准品适量,用0.1 mol/L HCl溶液溶解,配制成不同质量浓度的标准品储备液,详见表1。分别吸取各标准储备液适量于6 个10 mL量瓶中,用0.1 mol/L HCl溶液定容至刻度,得不同质量浓度的系列混合标准品溶液,待衍生化操作。
1.3.2 样品溶液的制备
1.3.2.1 地参样品的水解
参照GB 5009.124—2016《食品中氨基酸的测定方法》[30],将地参样品经50 ℃干燥,粉碎过35 目筛,备用。准确称取0.5 g(精确至0.000 1 g)地参粉末于顶空瓶中,加入6 mol/L盐酸溶液10 mL,继续向顶空瓶内加入苯酚3 滴,立即密封。将顶空瓶置于110 ℃的电热鼓风干燥箱内水解22 h后,取出,冷却至室温,滤过,用少量纯水多次冲洗残渣并转移至25 mL量瓶中,加纯水定容至刻度,混匀。取地参水解液0.4 mL于氮吹管中,在50 ℃水浴条件下氮吹至近干,加入0.4 mL纯水复溶备用。
1.3.2.2 氨基酸衍生化
精密移取1.3.2.1节复溶后的水解液0.4 mL于10 mL离心管中,分别加入1.0 mol/L三乙胺-乙腈溶液和0.1 mol/L PITC-乙腈溶液各0.2 mL,混匀,室温静置60 min后,加入正己烷1 mL,涡旋混合器振荡1 min,8 000 r/min冷冻离心5 min,萃取反应过剩的PITC,弃上层正己烷,将下层溶液用纯水定容至2 mL量瓶中,经0.22 µm微孔滤膜过滤,待测。
1.3.3 空白溶液的制备
取0.1 mol/L盐酸溶液0.4 mL于10 mL离心管中,自“分别加入1.0 mol/L三乙胺-乙腈溶液和0.1 mol/L PITC-乙腈溶液各0.2 mL”起照1.3.2.2节方法进行衍生化处理,即得。
1.3.4 色谱条件
A C Q U I T Y U P L C B E H C 1 8 色谱柱(2.1 mm×150 mm,1.7 μm);检测波长254 nm;柱温40 ℃;进样量1 µL;流速0.2 mL/min;流动相:A为0.1 mol/L乙酸钠-乙腈(97∶3,V/V)溶液(冰醋酸调pH 6.5),B为80%乙腈溶液;梯度洗脱:0~1 min,94% A,6% B;1~15 min,94%~65% A,6%~3 5% B;1 5 ~2 2 m i n,6 5%~4 0% A,35%~60% B。
1.4 数据处理
采用Microsoft Excel 2007软件对测定数据进行处理,氨基酸含量以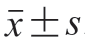 表示。采用SPSS 20.0软件对数据进行PCA和聚类分析。
表示。采用SPSS 20.0软件对数据进行PCA和聚类分析。
2 结果与分析
2.1 衍生试剂用量的优化
氨基酸的衍生反应属于竞争性反应,只有足够的衍生试剂才能保证所有氨基酸充分衍生化。本研究取最高浓度的混合标准溶液0.4 mL,加入1.0 mol/L三乙胺-乙腈溶液0.2 mL,涡旋混匀,分别加入衍生试剂0.1 mol/L PITC-乙腈溶液0.1、0.2、0.3、0.4、0.5 mL进行衍生化反应,通过各氨基酸衍生产物的峰面积确定最佳用量。结果表明:当衍生试剂超过0.2 mL时,峰面积增幅不明显,考虑到过量的PITC会造成色谱柱的损坏[26],故本研究选择衍生试剂用量为0.2 mL。
2.2 水解液酸碱度调节
氨基酸需在碱性条件下(约为pH 9)与PITC发生反应生成具有紫外吸收的氨基酸衍生物[26],故地参水解液pH值的调节尤为重要。本研究比较用NaOH溶液调节pH值至中性和氮吹法除掉HCl溶液2 种方式,结果发现:用NaOH溶液调节pH值的过程中生成了大量的NaCl,当加入三乙胺-乙腈溶液和PITC-乙腈溶液后,出现分层现象,衍生试剂与目标物无法充分接触,造成反应不完全。而采用氮吹法除HCl溶液能完全避免这种现象,保证氨基酸完全衍生。在上述优化后的条件下对标准品和样品进行衍生化处理,按1.3.4节色谱条件注入UPLC仪进行测定,如图1所示,各色谱峰峰形尖锐,分离度良好。
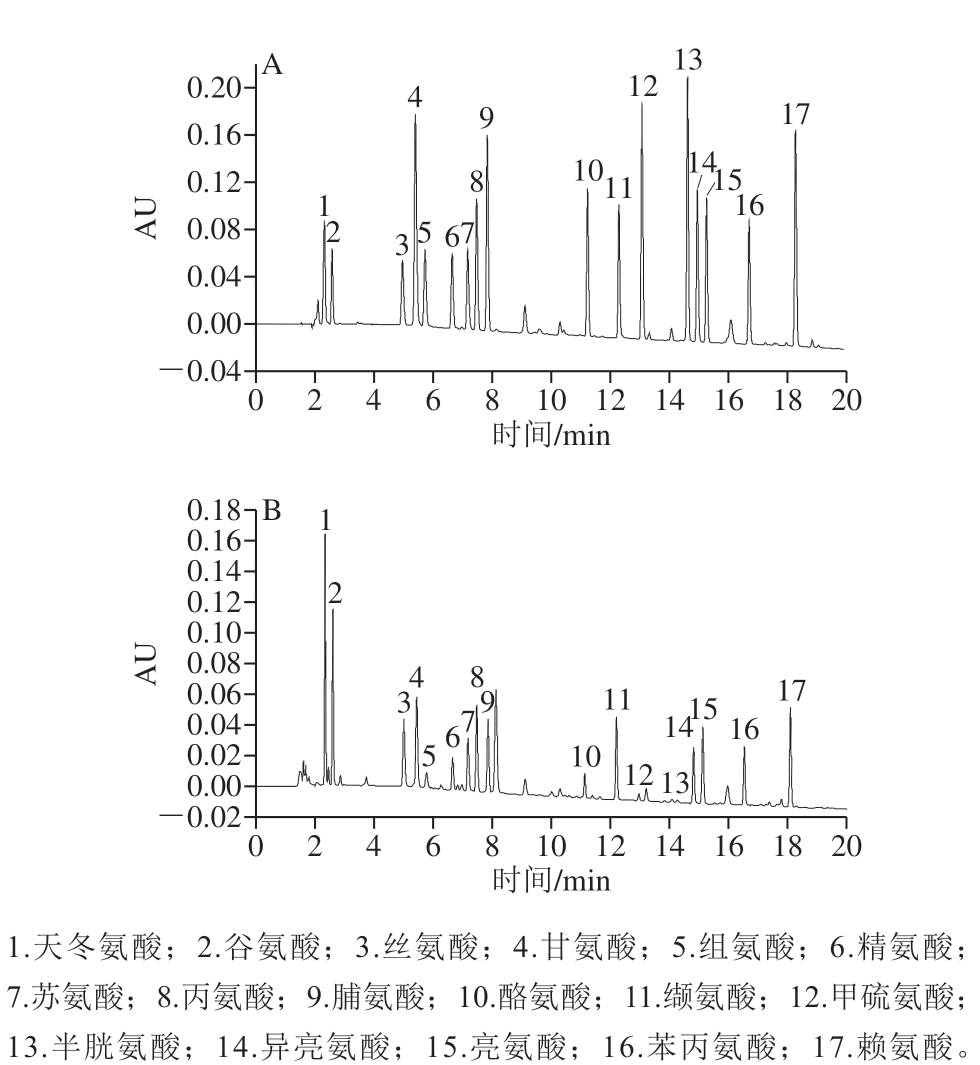
图1 氨基酸标准品(A)与地参样品(B)UPLC图
Fig. 1 UPLC chromatograms of mixture of 17 amino acid standards (A) and amino acids in hydrolysate of L. lucidus Turcz. var. hirtus Regel (B)
2.3 线性关系、检出限结果
表2 17 种氨基酸的标准曲线、线性范围、相关系数、检出限、定量限、仪器精密度和方法重复性
Table 2 Calibration curves, linear ranges, correlation coefficients,limits of detection, limits of quantitation, instrumental precision and method repeatability for amino acids detected by UPLC
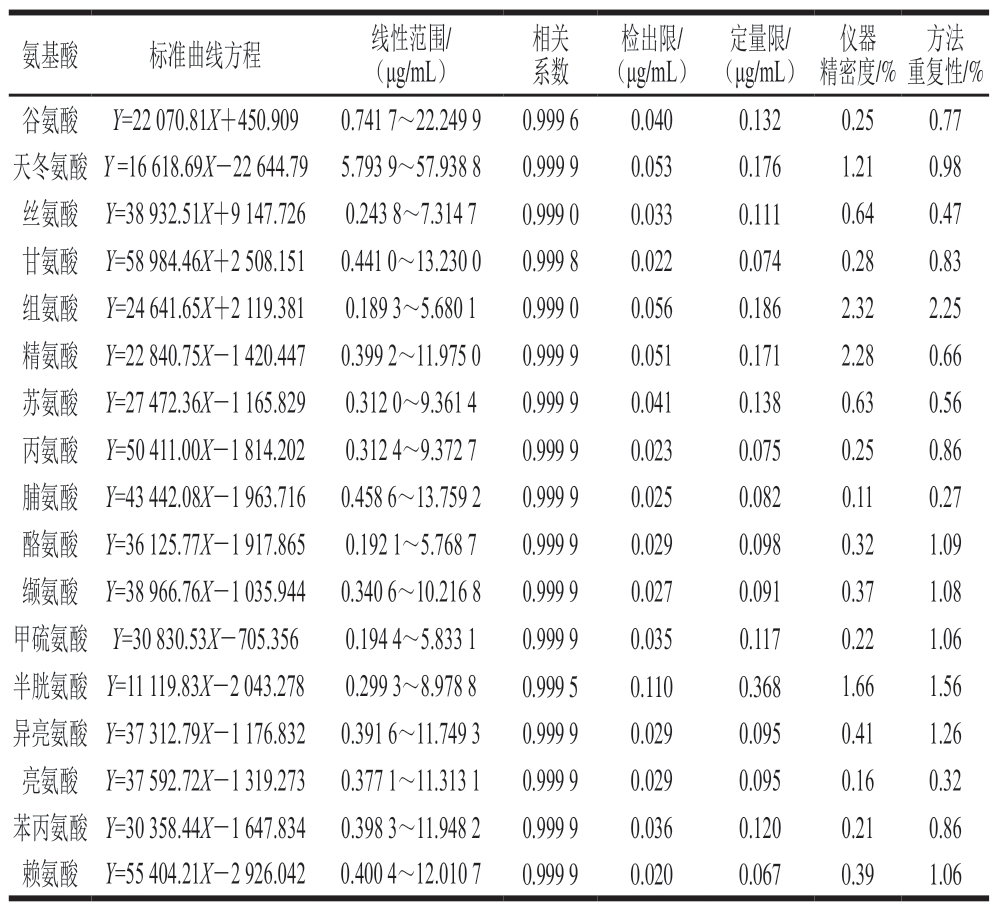
氨基酸 标准曲线方程 线性范围/(μg/mL)方法重复性/%谷氨酸 Y=22 070.81X+450.909 0.741 7~22.249 9 0.999 6 0.040 0.132 0.25 0.77天冬氨酸 Y =16 618.69X-22 644.79 5.793 9~57.938 8 0.999 9 0.053 0.176 1.21 0.98丝氨酸 Y=38 932.51X+9 147.726 0.243 8~7.314 7 0.999 0 0.033 0.111 0.64 0.47甘氨酸 Y=58 984.46X+2 508.151 0.441 0~13.230 0 0.999 8 0.022 0.074 0.28 0.83组氨酸 Y=24 641.65X+2 119.381 0.189 3~5.680 1 0.999 0 0.056 0.186 2.32 2.25精氨酸 Y=22 840.75X-1 420.447 0.399 2~11.975 0 0.999 9 0.051 0.171 2.28 0.66苏氨酸 Y=27 472.36X-1 165.829 0.312 0~9.361 4 0.999 9 0.041 0.138 0.63 0.56丙氨酸 Y=50 411.00X-1 814.202 0.312 4~9.372 7 0.999 9 0.023 0.075 0.25 0.86脯氨酸 Y=43 442.08X-1 963.716 0.458 6~13.759 2 0.999 9 0.025 0.082 0.11 0.27酪氨酸 Y=36 125.77X-1 917.865 0.192 1~5.768 7 0.999 9 0.029 0.098 0.32 1.09缬氨酸 Y=38 966.76X-1 035.944 0.340 6~10.216 8 0.999 9 0.027 0.091 0.37 1.08甲硫氨酸 Y=30 830.53X-705.356 0.194 4~5.833 1 0.999 9 0.035 0.117 0.22 1.06半胱氨酸 Y=11 119.83X-2 043.278 0.299 3~8.978 8 0.999 5 0.110 0.368 1.66 1.56异亮氨酸 Y=37 312.79X-1 176.832 0.391 6~11.749 3 0.999 9 0.029 0.095 0.41 1.26亮氨酸 Y=37 592.72X-1 319.273 0.377 1~11.313 1 0.999 9 0.029 0.095 0.16 0.32苯丙氨酸 Y=30 358.44X-1 647.834 0.398 3~11.948 2 0.999 9 0.036 0.120 0.21 0.86赖氨酸 Y=55 404.21X-2 926.042 0.400 4~12.010 7 0.999 9 0.020 0.067 0.39 1.06相关系数检出限/(μg/mL)定量限/(μg/mL)仪器精密度/%
取1.3.1节的17 种氨基酸混合标准工作液按照1.3.2.2节方法进行衍生化处理,以1.3.4节色谱条件依次进样分析,记录色谱峰峰面积,以各氨基酸标准品的峰面积(Y)与其相应的质量浓度(X)绘制标准曲线,根据信噪比计算检出限(RSN=3)和定量限(RSN=10)。如表2所示,17 种氨基酸的相关系数均大于0.999 0,表明线性关系良好;检出限为0.020~0.110 μg/mL,定量限为0.067~0.368 μg/mL,表明仪器灵敏度高,可检测较低质量浓度的氨基酸。
2.4 仪器精密度结果
取同一混合标准品衍生化溶液按照1.3.4节色谱条件连续进样6 次,记录17 种氨基酸峰面积并计算相对标准偏差(relative standard deviation,RSD),见表2。结果显示:各氨基酸峰面积的RSD在0.11%~2.32%之间,均小于3.00%,表明仪器精密度良好,可进行样品分析。
2.5 方法重复性结果
精密称取样品(S6)0.5 g,平行6 份,按照1.3.2节制备样品溶液,并按1.3.4节色谱条件进样测定,记录17 种氨基酸峰面积并计算RSD,见表2。结果显示:各物质峰面积RSD在0.27%~2.25%之间,表明该方法的重复性良好,可用于地参样品中氨基酸的含量测定。
2.6 衍生产物稳定性结果
取同一混合标准品衍生化溶液,分别在0、2、8、14、20、24、28、32、36 h时间里按照1.3.4节色谱条件进样,结果显示:各衍生产物随着时间的延长,标准品质量浓度呈下降趋势,在32 h内测得17 种氨基酸RSD在0.30%~2.63%之间,均小于3.00%;超过32 h后,部分氨基酸RSD超过3.00%。表明氨基酸衍生产物随着时间的推移发生了降解,为了保证结果的准确性,衍生化处理完毕后保证在32 h内完成检测。
2.7 加标回收实验结果
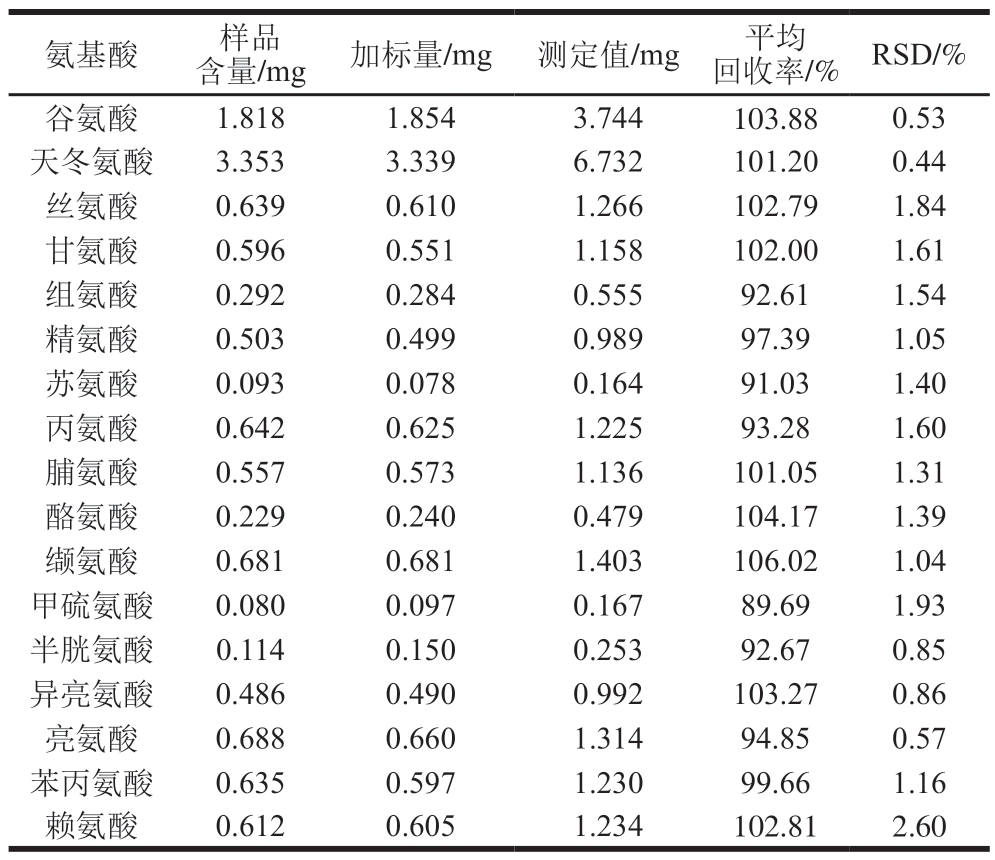
表3 17 种氨基酸回收率结果(n=6)
Table 3 Recoveries of 17 amino acids spiked into sample (n= 6)
含量/mg 加标量/mg 测定值/mg 平均回收率/% RSD/%谷氨酸 1.818 1.854 3.744 103.88 0.53天冬氨酸 3.353 3.339 6.732 101.20 0.44丝氨酸 0.639 0.610 1.266 102.79 1.84甘氨酸 0.596 0.551 1.158 102.00 1.61组氨酸 0.292 0.284 0.555 92.61 1.54精氨酸 0.503 0.499 0.989 97.39 1.05苏氨酸 0.093 0.078 0.164 91.03 1.40丙氨酸 0.642 0.625 1.225 93.28 1.60脯氨酸 0.557 0.573 1.136 101.05 1.31酪氨酸 0.229 0.240 0.479 104.17 1.39缬氨酸 0.681 0.681 1.403 106.02 1.04甲硫氨酸 0.080 0.097 0.167 89.69 1.93半胱氨酸 0.114 0.150 0.253 92.67 0.85异亮氨酸 0.486 0.490 0.992 103.27 0.86亮氨酸 0.688 0.660 1.314 94.85 0.57苯丙氨酸 0.635 0.597 1.230 99.66 1.16赖氨酸 0.612 0.605 1.234 102.81 2.60氨基酸 样品
根据本实验方法,称取已测得氨基酸含量的地参样品(S6)0.25 g各6 份,置于顶空瓶中,分别加入各标准品储备液适量,按照1.3.2节方法制备衍生化溶液,按1.3.4节色谱条件测定峰面积,计算回收率和RSD,以平均值表示,结果见表3。结果表明17 种氨基酸平均回收率为89.69%~106.02%,RSD为0.44%~2.60%,可以满足地参中17 种氨基酸含量测定的要求。
2.8 地参样品中氨基酸的含量测定
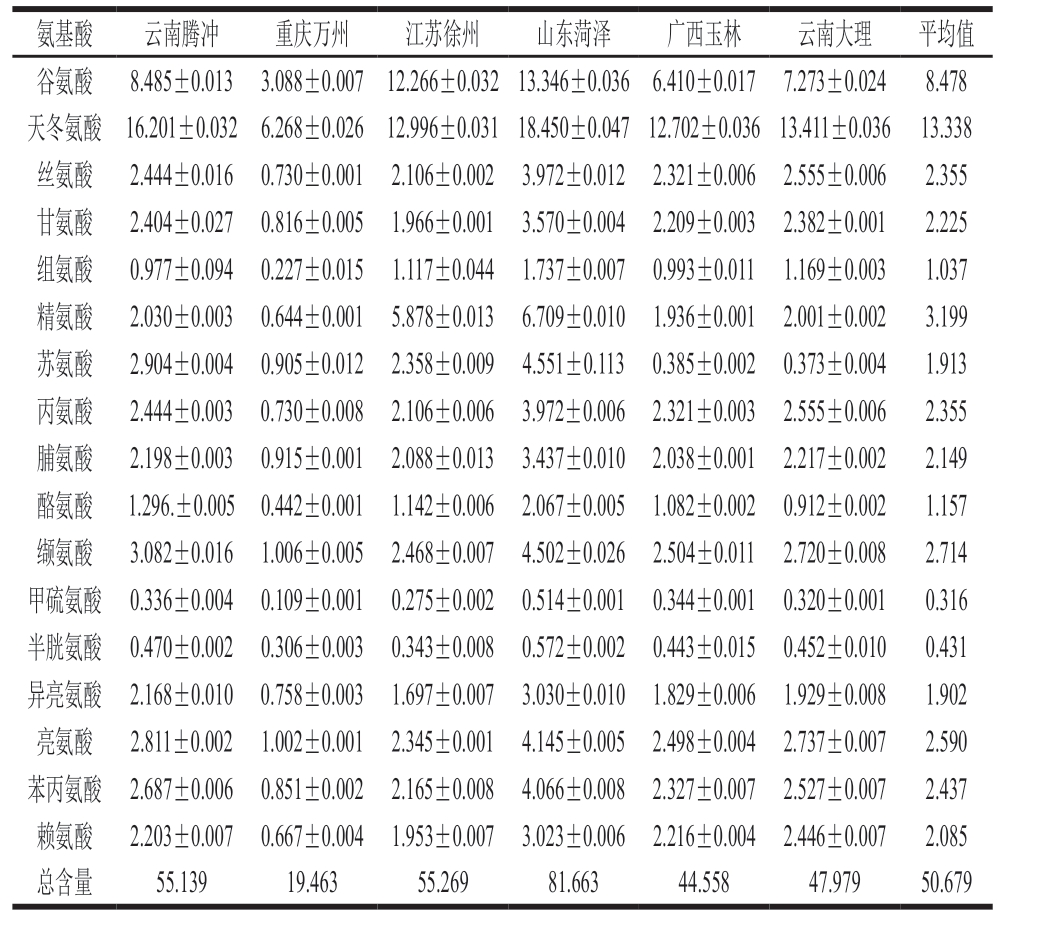
表4 不同产地地参中氨基酸含量(n=3)
Table 4 Amino acid composition of samples collected from six different
habitats (n= 3)mg/g
氨基酸 云南腾冲 重庆万州 江苏徐州 山东菏泽 广西玉林 云南大理 平均值谷氨酸 8.485±0.013 3.088±0.007 12.266±0.032 13.346±0.036 6.410±0.017 7.273±0.024 8.478天冬氨酸 16.201±0.032 6.268±0.026 12.996±0.031 18.450±0.047 12.702±0.036 13.411±0.036 13.338丝氨酸 2.444±0.016 0.730±0.001 2.106±0.002 3.972±0.012 2.321±0.006 2.555±0.006 2.355甘氨酸 2.404±0.027 0.816±0.005 1.966±0.001 3.570±0.004 2.209±0.003 2.382±0.001 2.225组氨酸 0.977±0.094 0.227±0.015 1.117±0.044 1.737±0.007 0.993±0.011 1.169±0.003 1.037精氨酸 2.030±0.003 0.644±0.001 5.878±0.013 6.709±0.010 1.936±0.001 2.001±0.002 3.199苏氨酸 2.904±0.004 0.905±0.012 2.358±0.009 4.551±0.113 0.385±0.002 0.373±0.004 1.913丙氨酸 2.444±0.003 0.730±0.008 2.106±0.006 3.972±0.006 2.321±0.003 2.555±0.006 2.355脯氨酸 2.198±0.003 0.915±0.001 2.088±0.013 3.437±0.010 2.038±0.001 2.217±0.002 2.149酪氨酸 1.296.±0.005 0.442±0.001 1.142±0.006 2.067±0.005 1.082±0.002 0.912±0.002 1.157缬氨酸 3.082±0.016 1.006±0.005 2.468±0.007 4.502±0.026 2.504±0.011 2.720±0.008 2.714甲硫氨酸 0.336±0.004 0.109±0.001 0.275±0.002 0.514±0.001 0.344±0.001 0.320±0.001 0.316半胱氨酸 0.470±0.002 0.306±0.003 0.343±0.008 0.572±0.002 0.443±0.015 0.452±0.010 0.431异亮氨酸 2.168±0.010 0.758±0.003 1.697±0.007 3.030±0.010 1.829±0.006 1.929±0.008 1.902亮氨酸 2.811±0.002 1.002±0.001 2.345±0.001 4.145±0.005 2.498±0.004 2.737±0.007 2.590苯丙氨酸 2.687±0.006 0.851±0.002 2.165±0.008 4.066±0.008 2.327±0.007 2.527±0.007 2.437赖氨酸 2.203±0.007 0.667±0.004 1.953±0.007 3.023±0.006 2.216±0.004 2.446±0.007 2.085总含量 55.139 19.463 55.269 81.663 44.558 47.979 50.679
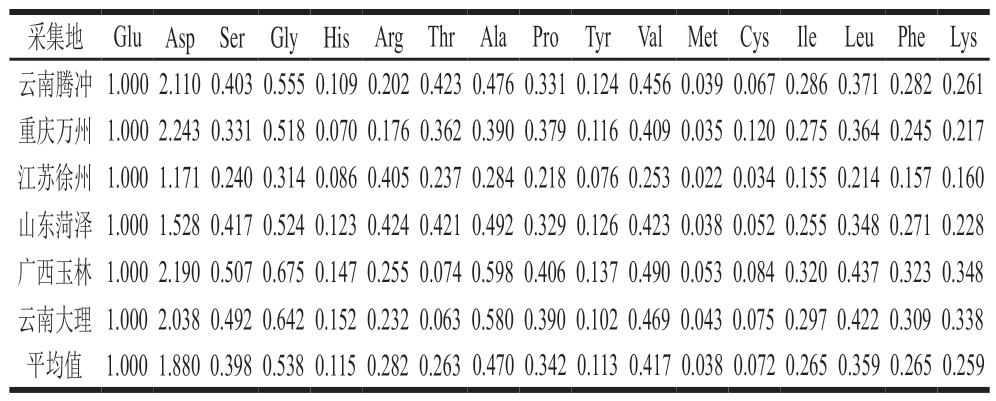
表5 地参氨基酸的物质的量比(n=3)
Table 5 Molar ration of amino acid (n = 3)
采集地 Glu Asp Ser Gly His Arg Thr Ala Pro Tyr Val Met Cys Ile Leu Phe Lys云南腾冲 1.000 2.110 0.403 0.555 0.109 0.202 0.423 0.476 0.331 0.124 0.456 0.039 0.067 0.286 0.371 0.282 0.261重庆万州1.000 2.243 0.331 0.518 0.070 0.176 0.362 0.390 0.379 0.116 0.409 0.035 0.120 0.275 0.364 0.245 0.217江苏徐州1.000 1.171 0.240 0.314 0.086 0.405 0.237 0.284 0.218 0.076 0.253 0.022 0.034 0.155 0.214 0.157 0.160山东菏泽1.000 1.528 0.417 0.524 0.123 0.424 0.421 0.492 0.329 0.126 0.423 0.038 0.052 0.255 0.348 0.271 0.228广西玉林 1.000 2.190 0.507 0.675 0.147 0.255 0.074 0.598 0.406 0.137 0.490 0.053 0.084 0.320 0.437 0.323 0.348云南大理 1.000 2.038 0.492 0.642 0.152 0.232 0.063 0.580 0.390 0.102 0.469 0.043 0.075 0.297 0.422 0.309 0.338平均值 1.000 1.880 0.398 0.538 0.115 0.282 0.263 0.470 0.342 0.113 0.417 0.038 0.072 0.265 0.359 0.265 0.259
取6 个不同产地地参样品按照1.3.2节进行样品溶液的制备,平行3 份,注入UPLC测定氨基酸含量,并计算各氨基酸组分间物质的量比,结果见表4、5。不同产地的地参酸水解液中均检出17 种氨基酸,但氨基酸总量存在差异,介于19.463~81.663 mg/g之间,氨基酸总量为山东菏泽>江苏徐州>云南腾冲>云南大理>广西玉林>重庆万州,平均含量为50.679 mg/g,明显高于紫苏叶与紫苏子[29]、霍山石斛[14]、橄榄[18],与党参[31]含量接近。地参所含氨基酸中含量最高的为天冬氨酸,为6.268~18.450 mg/g,平均含量为13.338 mg/g,其次是谷氨酸,含量为3.088~13.346 mg/g,平均含量为8.478 mg/g,分别占总氨基酸含量的26.32%和16.73%,这与前期对云南地产野生地参的研究[11-12]结果一致;含量较低的氨基酸为甲硫氨酸和半胱氨酸,甲硫氨酸含量为0.109~0.514 mg/g,平均含量为0.316 mg/g,半胱氨酸含量为0.306~0.572 mg/g,平均含量为0.431 mg/g。
从表4可知,6 个产地地参中包括7 种人体必需氨基酸,含量为5.298~23.831 mg/g,平均含量为13.956 mg/g。必需氨基酸含量从高到低依次为缬氨酸、亮氨酸、苯丙氨酸、赖氨酸、苏氨酸、异亮氨酸、甲硫氨酸,含量最高的缬氨酸占氨基酸总量的5.36%,甲硫氨酸含量最低,占总量的0.62%。6 个产地地参按必需氨基酸含量排序为山东菏泽>云南腾冲>江苏徐州>云南大理>广西玉林>重庆万州。不同产地地参必需氨基酸与氨基酸总量的百分比为23.99%~29.36%,平均值为27.35%,必需氨基酸与非必需氨基酸含量的百分比为31.57%~41.57%,平均值为37.73%,与联合国粮食及农业组织/世界卫生组织标准中对氨基酸理想模式的规定必需氨基酸与氨基酸总量比值为40%和必需氨基酸与非必需氨基酸比值为60%[32]有一定差距,表现为地参营养价值不够均衡。
药用氨基酸种类齐全,包括甲硫氨酸、苯丙氨酸、亮氨酸、赖氨酸、酪氨酸、天冬氨酸、谷氨酸、甘氨酸和精氨酸9 种,含量为13.887~55.890 mg/g,平均含量为35.825 mg/g,占总氨基酸的比例为68.44%~74.16%,平均比值为70.96%,高于枸杞[33]、石斛[34]等中药,与党参[31]含量相当。结果显示,尽管不同产地地参的药用氨基酸含量相差较大,但其在总氨基酸中所占比例无明显差异,与王晓媛等[34]对不同品种石斛的研究结果类似。其中天冬氨酸和谷氨酸作为地参中主要的药用氨基酸,分别占药用氨基酸总量的37.23%和23.67%,而谷氨酸和天冬氨酸作为对映体,在人体的氨基酸蛋白质代谢过程中具有重要的作用[35]。研究表明,谷氨酸作为中枢神经中的主要兴奋性神经递质可介导神经信号转导,能改善学习和记忆能力[36];同时谷氨酸被人体吸收后与血氨结合可解氨毒,具有保肝护肝的作用[37]。而天冬氨酸具有增强机体免疫力、消除疲劳、促进肝功能和保护心肌等生物活性,广泛用于食品、保健食品、化妆品及工业原料中,需求量大[38]。在地参中精氨酸含量仅次于天冬氨酸、谷氨酸,达3.199 mg/g,有增强机体免疫功能、改善心脑血管等作用[31]。综上所述,地参中富含各类药用氨基酸为其开发成各种保健食品、药品以及日常食用的药膳提供了一定的抗病物质基础。
由表5可知,地参检出的17 种氨基酸组分间物质的量比存在差异,但广西玉林和云南大理2 个产地之间相似度极高。
2.9 PCA结果
2.9.1 PC筛选及其贡献率利用SPSS 20软件对地参中17 种氨基酸进行PCA。如表6所示,从17 个氨基酸组分中提取出2 个PC(特征值>1),PC1的特征值为15.210,特征贡献率为89.473%,主要影响因子为脯氨酸、缬氨酸和苯丙氨酸;PC2的特征值为1.176,特征贡献率为6.917%,主要影响因子为精氨酸、苏氨酸和谷氨酸;2 个PC的累计贡献率为96.390%。
表6 方差分析
Table 6 Analysis of variance

PC 初始特征值 提取平方和载入合计 方差贡献率/% 累计贡献率/% 合计 方差贡献率/% 累计贡献率/%F1 15.210 89.473 89.473 15.210 89.473 89.473 F2 1.176 6.917 96.390 1.176 6.917 96.390
2.9.2 综合PCA结果
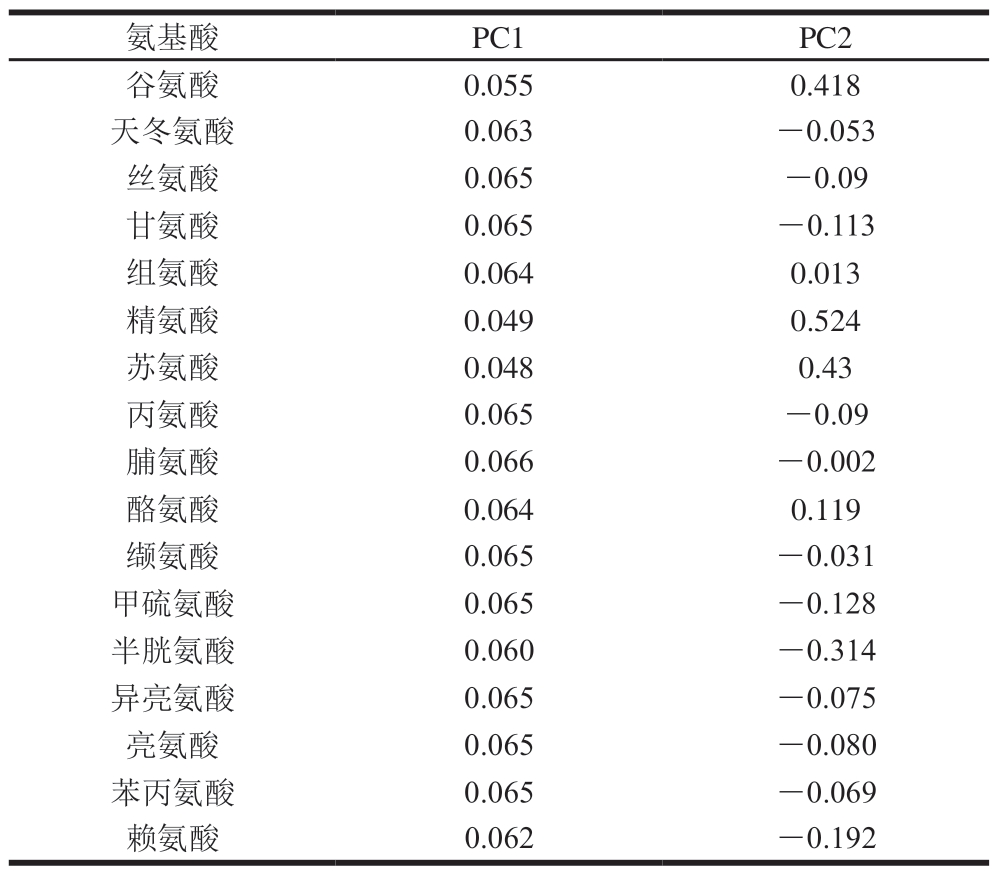
表7 PC系数向量值
Table 7 Vectors of principal components
氨基酸 PC1 PC2谷氨酸 0.055 0.418天冬氨酸 0.063 -0.053丝氨酸 0.065 -0.09甘氨酸 0.065 -0.113组氨酸 0.064 0.013精氨酸 0.049 0.524苏氨酸 0.048 0.43丙氨酸 0.065 -0.09脯氨酸 0.066 -0.002酪氨酸 0.064 0.119缬氨酸 0.065 -0.031甲硫氨酸 0.065 -0.128半胱氨酸 0.060 -0.314异亮氨酸 0.065 -0.075亮氨酸 0.065 -0.080苯丙氨酸 0.065 -0.069赖氨酸 0.062 -0.192
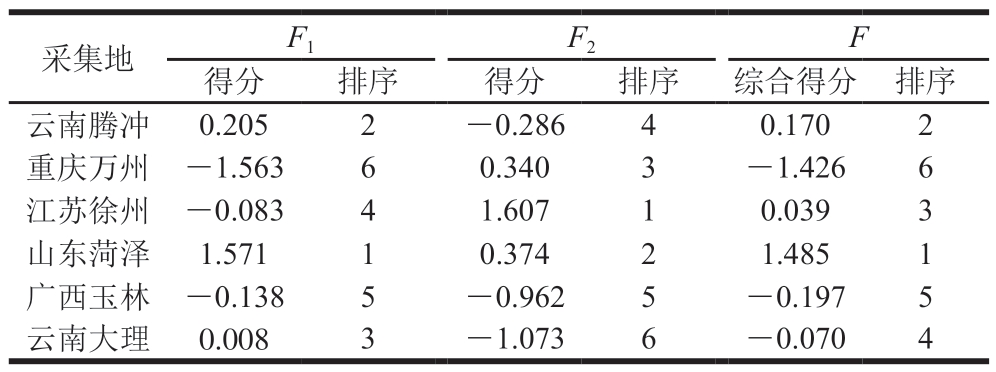
表8 样品PC得分、综合得分及其排序
Table 8 Principal component scores, comprehensive scores and their ranking
采集地 F1 F2 F得分 排序 得分 排序 综合得分 排序云南腾冲 0.205 2 -0.286 4 0.170 2重庆万州 -1.563 6 0.340 3 -1.426 6江苏徐州 -0.083 4 1.607 1 0.039 3山东菏泽 1.571 1 0.374 2 1.485 1广西玉林 -0.138 5 -0.962 5 -0.197 5云南大理 0.008 3 -1.073 6 -0.070 4
将表7中的系数向量值与17 种氨基酸含量标准化后的数据相乘,计算每个PC得分,根据每个PC所对应的特征值占所提取PC总特征值之和的比例作为权重得到综合PC表达式为F=0.928F1+0.072F2,并进行排序。如表8所示,相对于PC1,采自山东菏泽的地参得分最高;相对于对PC2,采自江苏徐州的地参得分最高;综合得分排序由高到低依次为山东菏泽>云南腾冲>江苏徐州>云南大理>广西玉林>重庆万州。不同产地地参的F值为-1.426~1.485,表明不同产地地参间氨基酸含量差异明显。
2.10 聚类分析结果
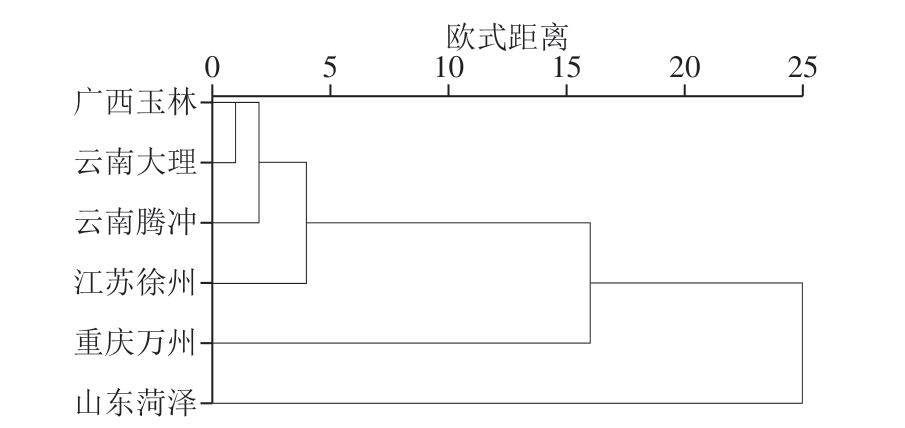
图2 样品聚类分析
Fig. 2 Cluster analysis of samples
采用SPSS 20.0软件对6 份样品进行聚类分析,结果见图2。当欧式距离为15时,全部样品被分成3 大类,其中山东菏泽的为第I类,营养价值最高,其余4 组为第II类,氨基酸品质含量中等,重庆万州为第III类,品质相对较差,与PCA的结果一致。第I类山东菏泽地参为高品质蛋白,可作为地参资源开发与利用的理想资源;第III类为低品质蛋白,氨基酸含量可能与当地生态环境、种质资源等[2]有关。聚类分析结果较好地体现了不同产地间氨基酸含量的差异性,为地参营养价值、药用开发提供理论指导。
3 结 论
本研究采用6 mol/L盐酸溶液在110 ℃条件下对地参样品进行水解,取水解液进行PITC柱前衍生,结合UPLC进行测定,计算得到地参中游离和水解氨基酸的总和。该方法的灵敏度高、分离效果好、精密度、重复性、稳定性和回收率良好,结果稳定可靠。分析地参样品中氨基酸的组成及含量,可以为地参药材质量评价和将其开发为保健品提供理论依据。
地参作为我国传统药食两用的中药材历史悠久,其氨基酸种类丰富且含量较高,本研究中6 个不同产区的地参均含有17 种氨基酸,总含量约占地参质量的5.00%即50 g/kg,极具开发作为补充氨基酸的功能性食品的潜力,丰富市场;检出氨基酸中含有7 种必需氨基酸和9 种药用氨基酸,具有较高的营养价值和药用价值,并通过PCA和聚类分析综合评价,山东菏泽地参氨基酸总含量高,重庆万州的相对较低。因此,建立地参栽培基地时,应充分考虑地参对产地的适应性。由于本实验选择的样品产地仅限于5 个地参栽培省(市)并未包括我国所有地参产地,且样本数量较少并不能完全代表当地地参品质,因此在今后研究中还需扩大采样量和采样范围,调查生长环境和栽培技术,明确环境因素对地参氨基酸营养价值和药用价值的影响,为地参品质评价、产品的深入开发利用提供更多依据。
[1] 国家中医药管理局. 中华本草: 第7卷[M]. 上海: 上海科学技术出版社, 1999: 76-77.
[2] 姜峰, 倪穗, 岑冲锋, 等. 不同种源地参在宁波地区的适应性及多糖含量比较研究[J]. 中国野生植物资源, 2019, 38(5): 20-24. DOI:1006-9690(2019)05-0020-05.
[3] 郭琦, 高春燕. 硬毛地笋酚类化合物对DNA损伤的保护作用[J].食品科学, 2018, 39(23): 54-59. DOI:10.7506/spkx1002-6630-201823009.
[4] LU Y H, HUANG J H, LI Y C, et al. Variation in nutritional compositions, antioxidant activity and microstructure of Lycopus lucidus Turcz. root at different harvest times[J]. Food Chemistry, 2015,183: 91-100. DOI:10.1016/j.foodchem.2015.03.033.
[5] YANG X B, LV Y, TIAN L M, et al. Composition and systemic immune activity of the polysaccharides from an herbal tea (Lycopus lucidus Turcz)[J]. Agriculture and Food Chemistry, 2010, 58: 6075-6080. DOI:10.1021/jf101061y.
[6] LU Y H, TIAN C R, GAO C Y, et al. Protective effect of free phenolics from Lycopus lucidus Turcz. root on carbon tetrachloride-induced liver injury in vivo and in vitro[J]. Food & Nutrition Research, 2018,62(25): 1398-1407. DOI:10.29219/fnr.v62.1398.
[7] 熊伟, 谭德勇, 陈贵元, 等. 地参多糖对小鼠免疫功能影响的实验研究[J]. 时珍国医国药, 2011, 22(1): 11-13. DOI:10.3969/j.issn.1008-0805.201101.005.
[8] 杨保成, 彭涛, 康文艺. 地笋属植物化学成分研究进展[J]. 中国实验方剂学杂志, 2013, 19(4): 346-350. DOI:10.13422/j.cnki.syfjx.2013.04.092.
[9] REN Q, DING L, SUN S S, et al. Chemical identification and quality evaluation of Lycopus lucidus Turcz by UHPLC-Q-TOF-MS and HPLC-MS/MS and hierarchical clustering analysis[J]. Biomedical Chromatography, 2016, 31(5): 3867-3869. DOI:10.1002/bmc.3867.
[10] YU J Q, LEI J C, ZHANG X Q, et al. Anticancer, antioxidant and antimicrobial activities of the essential oil of Lycopus lucidus Turcz.var. hirtus Regel[J]. Food Chemistry, 2011, 126(4): 1593-1598.DOI:10.1016/j.foodchem.2010.12.027.
[11] 许泳吉, 钟惠民, 杨波, 等. 野生植物地参中营养成分的测定[J].光谱实验室, 2003, 20(4): 528-529. DOI:1004-8138(2003)04-0528-02.
[12] 张荣平, 周宁娜, 罗天诰. 地参中氨基酸、粗蛋白和元素分析[J].中医药研究, 1998, 14(5): 54-55.
[13] 陈蓉, 张超, 顾倩, 等. 柱前衍生-HPLC法同时测定不同产地茯苓中18 种氨基酸含量[J]. 药物分析杂志, 2017, 37(2): 297-303.DOI:10.16155/j.0254-1793.2017.02.16.
[14] 郝经文, 王荣花, 徐文冬, 等. 柱前衍生化HPLC同时测定霍山石斛中13 种游离氨基酸含量[J]. 天然产物研究与开发, 2018, 30(11):1849-1857. DOI:10.16333/j.1001-6880.2018.11.001.
[15] 张苏平, 邱伟强, 卢祺, 等. 全自动氨基酸分析仪法测定4 种贝类肌肉中谷胱甘肽和游离氨基酸含量[J]. 食品科学, 2017, 38(4): 170-176. DOI:10.7506/spkx1002-6630-201704027.
[16] 辛丽娜, 刘常凯, 何林飞, 等. 6 种农业特种养殖动物肉中18 种氨基酸含量分析[J]. 肉类研究, 2019, 33(2): 58-63. DOI:10.7506/rlyj1001-8123-20181126-219.
[17] 郭琳仪, 孙慧阳, 马洁, 等. 新疆、内蒙古地区马乳及发酵酸马乳中氨基酸分析与营养评价[J]. 乳业科学与技术, 2019, 42(2): 1-6.DOI:10.15922/j.cnki.jdst.2019.02.001.
[18] 彭真汾, 王威, 叶清华, 等. 高效液相色谱-串联质谱法定量分析橄榄果实氨基酸组分[J]. 食品科学, 2018, 39(24): 231-238. DOI:10.7506/spkx1002-6630-201824035.
[19] SONG C H, ZHANG S J, JI Z Y, et al. Accurate determination of amino acids in serum samples by liquid chromatography-tandem mass spectrometry using a stable isotope labeling strategy[J]. Journal of Chromatographicence, 2015, 53: 1536-1541. DOI:10.1093/chromsci/bmv049.
[20] 芮鸿飞, 张晓瑜, 刘兴泉, 等. PITC柱前衍生-反相高效液相色谱法测定黄酒中游离氨基酸和生物胺[J]. 食品科学, 2016, 37(8): 159-163. DOI:10.7506/spkx1002-6630-201608028.
[21] 唐翎, 魏伟, 赵勇. 柱前衍生高效液相色谱测定猴头菌丝体中15 种游离氨基酸的含量[J]. 中国药学杂志, 2017, 52(21): 1899-1902.DOI:10.11669/cpj.2017.21.006.
[22] 卫阳飞, 宋海, 岳国仁, 等. 6 种葡萄籽中水解氨基酸和游离氨基酸含量测定及比较[J]. 食品与机械, 2018, 34(9): 77-82. DOI:10.13652/j.issn.1003-5788.2018.09.016.
[23] SOCIA A, FOLEY J P. Direct determination of amino acids by hydrophilic interaction liquid chromatography with charged aerosol detection[J]. Journal of Chromatography A, 2016, 1446: 41-49.DOI:10.1016/j.chroma.2016.03.042.
[24] 江东龙, 陈芳, 熊丹丹, 等. 柱前衍生化HPLC法同时测定龟甲胶中14 种水解氨基酸含量[J]. 药物分析杂志, 2015, 35(10): 1790-1795.DOI:10.16155/j.0254-1793.2015.10.16.
[25] 马阳, 侯娅, 邹立思, 等. 不同种质和地域太子参氨基酸柱前衍生-HPLC测定及多元统计分析[J]. 天然产物研究与开发, 2016,28(8): 1192-1198. DOI:10.16333/j.1001-6880.2016.8.004.
[26] 段智红, 黄永梅, 吕应年, 等. 2,4-二硝基氟苯柱前衍生HPLC-UV法测定海稻米中的γ-氨基丁酸含量[J]. 食品工业科技, 2019, 40(2):257-261; 270. DOI:10.13386/j.issn1002-0306.2019.02.044.
[27] 赫欣睿, 武中庸, 叶永丽, 等. 高效液相色谱法测定氨基酸的研究进展[J]. 分析测试学报, 2016, 35(7): 922-928. DOI:10.3969/j.issn.1004-4957.2016.07.026.
[28] 牛国一, 曹志勇, 张新党, 等. 高效液相色谱分析氨基酸的方法研究及优化[J]. 黑龙江畜牧兽医, 2017(7): 279-282. DOI:10.13881/j.cnki.hljxmsy.2017.0643.
[29] 祝洪艳, 张荻, 张力娜, 等. 柱前衍生化HPLC法检测紫苏子和紫苏叶中氨基酸的含量[J]. 药物分析杂志, 2017, 37(10): 1858-1864.DOI:10.16155/j.0254-1793.2017.10.17.
[30] 国家卫生和计划生育委员会, 国家食品药品监督管理总局. 食品中氨基酸的测定: GB 5009.124—2016[S]. 北京: 中国标准出版社, 2016.
[31] 杨鲜, 祝慧凤, 王涛, 等. 重庆巫山等多地党参氨基酸及营养价值比较与分析[J]. 食品科学, 2014, 35(15): 251-257. DOI:10.7506/spkx1002-6630-201415051.
[32] FAO/WHO. Energy and protein requirements[R]. Geneva: World Health Organization, 1973.
[33] 吴有锋, 谭亮, 沈建伟, 等. 柴达木枸杞中17 种氨基酸的测定与分析[J]. 食品工业科技, 2017, 38(1): 281-286. DOI:10.13386/j.issn1002-0306.2017.01.048.
[34] 王晓媛, 王彦兵, 陈玉芹, 等. 6 种石斛属植物氨基酸组成及营养价值评价[J]. 天然产物研究与开发, 2019, 31(4): 601-607.DOI:10.16333/j.1001-6880.2019.4.007.
[35] 潘健, 刘文, 陈文秋, 等. 柱前衍生RP-HPLC法同时测定天花粉中天门冬氨酸与谷氨酸的含量[J]. 中国药房, 2012, 23(35): 3326-3328.DOI:10.6039/j.issn.1001-0408.2012.35.22.
[36] 许凯, 毕晶晶, 张继昊. 天然非蛋白氨基酸的生物活性机制研究进展[J]. 食品科学, 2019, 40(21): 251-259. DOI:10.7506/spkx1002-6630-20181004-004.
[37] CAULI O, RODRIGO R, LLANSOLA M, et al. Glutamatergic and gabaergic neurotransmission and neuronal circuits in hepatic encephalopathy[J]. Metabolic Brain Disease, 2009, 24(1): 69-80.DOI:10.1007/s11011-008-9115-4.
[38] 谭畅, 晁若冰. HPLC测定L-天门冬氨酸中的有关物质[J]. 华西药学杂志, 2006, 21(1): 81-83. DOI:10.13375/j.cnki.wcjps.2006.01.034.