早在几个世纪以前,就有科学家通过显微镜在人的牙菌斑等表面观察到了细菌形成的层膜状结构,这就是细菌的生物膜。生物膜是指依附于有生命或无生命物体表面且被胞外大分子包裹的有组织的细菌群体,也被称为生物被膜[1-2]。生物膜是大多数细菌普遍存在的一种生存方式,其可能存在于医疗器械、病理组织、食品工业原料、食品机械和管道表面等地方。事实上绝大多数细菌都是以生物膜的形式生长,而不是以浮游状态生长[3-4]。生物膜由细菌细胞、胞外聚合物和其他颗粒物的水合混合物构成[5]。生物膜是细菌抵御各种环境胁迫的一种有效方式,当细菌遇到极端环境(温度、pH值、渗透压、金属离子、抗生素和其他微生物等)威胁时就会聚集形成生物膜[6-7]。同时细菌生物膜的细胞之间可以通过群体感应进行化学物质交流,从而调节营养物质的获取和转运、细胞之间的杂交以及细胞的运动和代谢产物的生成,使生物膜成为一个类似多细胞生物的群体[8-9]。
1 乳酸菌生物膜的形成
乳酸菌是一类可发酵碳水化合物产乳酸的无芽孢革兰氏阳性菌,是一种公认的食用安全益生菌,具有降低肠道pH值、调节肠道菌群、抑制有害菌生长、防治乳糖不耐症等多种功效,还是制作酸奶、泡菜等生活中常见发酵食品的重要菌株[10-12]。和大多数细菌一样,乳酸菌在一些环境中也能产生生物膜,但目前关于生物膜的研究主要集中在致病菌方面,而对乳酸菌这样的益生菌生物膜研究较少,但实际上不论是在肠道还是在发酵食品中,乳酸菌大多是以生物膜方式生存,因此加强对乳酸菌生物膜的研究很有必要[13-14]。
1.1 乳酸菌生物膜组成
乳酸菌生物膜的组成成分和其他细菌类似,主要包括菌体和胞外聚合物,而胞外聚合物又由各种生物大分子(蛋白质、胞外多糖、脂质、DNA(eDNA)等)构成[15]。在结构上细胞只占生物膜的小部分空间,通常为5%~35%。而胞外聚合物填充在生物膜细胞之间,占生物膜中的大部分空间。胞外聚合物直接提供了乳酸菌生物膜的胞外环境和生存条件,将细胞与外界环境分隔开,也为生物膜提供了机械稳定性,保护了生物膜中的乳酸菌。这也是形成生物膜后乳酸菌抵御外界不良环境能力增强的原因之一[16]。此外,生物膜的成分,尤其是胞外聚合物和生物膜的代谢表现密不可分。如多糖可以结合大量水分,提高机械稳定性,改善蛋白质和酶的调节作用,促进eDNA与信息交流基因转移。胞外聚合物对细菌与细菌之间以及细菌与外界物质交换也起着重要作用,如海绵状的胞外聚合物可以更高效地吸附捕获营养物质,作为细菌之间的介质可以运送养料、排出代谢废物,为细菌之间及细菌与外界的信息交流提供便利,如基因的转移、信号分子的转移和释放等,这些都是生物膜为了适应不良环境而采取的一些策略。总之生物膜的构成成分和它的各种功能及代谢表现息息相关[17-19]。
1.2 乳酸菌生物膜的形成过程
目前,关于乳酸菌生物膜形成的详细过程还不是十分明确,但是对枯草芽孢杆菌、表皮葡萄球菌、金黄色葡萄球菌等典型革兰氏阳性菌的研究都表明生物膜形成的大致步骤是相同的[20-21]。一般革兰氏阳性菌生物膜的形成过程可以分为4 个阶段[22-24]。第一步是细菌的黏附和定植阶段,细菌在与某些物体表面接触后会黏附在其表面,开始形成生物膜,有鞭毛的细菌是通过鞭毛的运动聚集在一起的,而乳酸菌大多数都没有鞭毛,所以乳酸菌可能是通过沉降等方式聚集黏附在一起。但这时附着的细胞仅有少量的胞外聚合物包裹,还未进入细胞膜的形成过程,而这些黏附的细胞也还可以重新进入浮游状态,此时黏附过程是可逆的。第二个阶段是细菌的生长阶段,随着黏附和定植的细菌数量不断增加,一些与生物膜形成相关的基因开始调整表达,细菌开始大量生长、繁殖并分泌大量胞外聚合物将细菌黏合起来,同时使细菌在物体表面黏合得更加牢固,这个黏附是不可逆的。第三阶段是生物膜的生长成熟阶段,在经历不可逆的黏附阶段之后生物膜进一步生长进入成熟期,通过激光共聚焦显微镜可以观察到成熟的生物膜是由细菌堆积成类似蘑菇状或堆状的微菌落组成,菌落之间有水通道,可以运送养料排出废物。最后一个阶段是细菌的播散阶段,成熟的生物膜通过蔓延、部分脱落或释放出浮游细菌等方式进行扩展。释放出来的浮游细菌可重新定植于物体表面,再次经历这4 个阶段形成新的生物膜。细菌生物膜的形成过程可用图1表示。
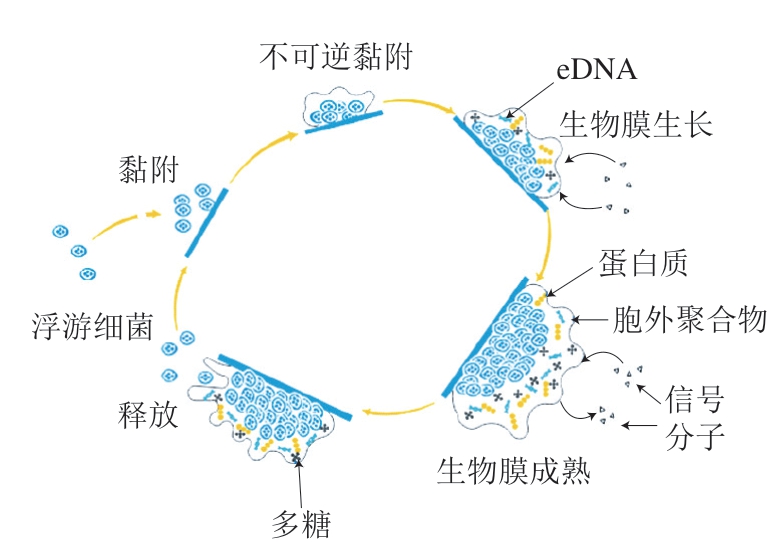
图 1 细菌生物膜形成动态过程[22-24]
Fig. 1 Schematic of the dynamic formation process of lactic acid bacteria biofilm[22-24]
1.3 影响乳酸菌生物膜形成的因素
1.3.1 培养基组分
影响乳酸菌生物膜形成的因素可用图2表示。培养基组分尤其是作为能量来源的碳源对乳酸菌生物膜的形成有重要作用,在乳酸菌培养基(MRS)中缺乏碳源的时候就会形成大量的生物膜,研究表明,在培养基中无葡萄糖时乳酸菌几乎不生长,也不形成生物膜,但是向培养基中添加葡萄糖等碳源后就会形成生物膜,且随着葡萄糖浓度的增加生物膜量逐渐减少,但当葡萄糖浓度超过一定值之后又会促进生物膜的产生。乳糖、果糖、蔗糖等其他碳源都有类似的效果,不过不同的碳源对不同乳酸菌生物膜形成能力的影响均有不同[25-26]。同时MRS中吐温-80的缺乏也会促进生物膜的形成[27]。
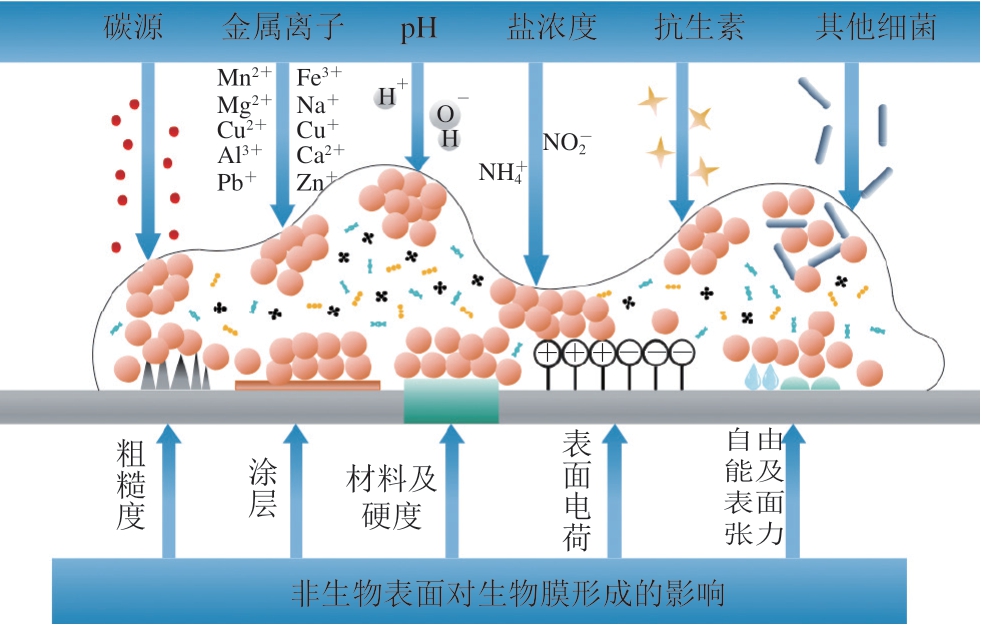
图 2 影响乳酸菌生物膜形成的因素
Fig. 2 Factors affecting the formation of lactic acid bacteria biofilm
1.3.2 金属离子和盐浓度
不同金属离子对生物膜的形成也有影响,如Mn2+、Fe3+、Mg2+和Na+在一定浓度下会对生物膜形成起到促进作用,其原因是这些离子能够促进或直接参与某些蛋白质和酶的合成,从而增强乳酸菌生物膜的黏附性和稳定性。而Cu2+、Cu+、Al3+、Ca2+、Pb+和Zn+等金属离子则会对生物膜的形成起到抑制作用。一般乳酸菌只有在盐添加量为4%~8%范围内能形成生物膜,超过这个范围其生物膜形成能力被抑制或完全不能形成[25,28]。
1.3.3 非生物表面
除此之外,非生物的表面因为是生物膜附着的载体,所以对生物膜的产生也起重要作用,这个影响主要是在细菌的黏附和定植阶段[29]。因此,材料的类型、粗糙度、涂层、电荷、自由能、硬度等因素都会影响生物膜的形成[30]。一般来说,表面不规则可以提供更大的表面积使细菌定植,其中不规则的凹面空间,使微生物能够找到有利的和具有保护性的微环境[31-32]。而且,不规则的表面阻碍了表面的清洁,因此有利于营养基质和微生物的积累[33]。表面涂层的不同,如不锈钢、陶瓷、聚苯乙烯、聚四氟乙烯等对生物膜生成的影响也不尽相同。表面电荷会影响细菌与材料的结合。一般来说,带正电的表面会促进与细菌的相互作用和生物膜的形成[34]。此外,表面能与表面反应性直接相关,疏水性或亲水性会影响细菌与表面的相互作用,这取决于细菌种别[35]。金属材料可提供高自由能、带负电荷的亲水表面,聚四氟乙烯可提供低自由能、带负电荷的疏水表面[36]。因此,相对于其他疏水性表面(聚四氟乙烯、尼龙、丁腈橡胶和氟化聚合物),提供高自由表面能的不锈钢和玻璃表面相对亲水,通常有助于形成大量细菌的生物膜。
1.3.4 其他因素
乳酸菌只有在适宜的pH值下才能以浮游状态生存,pH值过高和过低都会促进生物膜的产生[14]。一般来说最适合乳酸菌形成生物膜的pH值范围为5.5~6.8,而当pH值不在3.8~6.8范围内时,生物膜的形成能力会被极大地抑制[37]。当乳酸菌受到抗生素的胁迫时也可能形成生物膜来抵御,有研究表明在生物膜状态下的乳酸菌比浮游的乳酸菌对抗生素有更高的耐受性[38]。乳酸菌在遇到有害细菌时可以形成生物膜来共同应对,甚至可以抑制有害菌的生长[39]。
2 乳酸菌生物膜形成的调控机制
目前关于乳酸菌生物膜形成的调控机制研究相对较少。但可以确定的是,乳酸菌从浮游态到聚集形成生物膜的各个步骤中涉及到的调控机制是非常复杂的,不论是在乳酸菌的黏附还是生长或成熟期,都伴随着大量的基因表达和信号分子的传递以调控生物膜的形成[23,40]。Sun Linlin等[41]基于转录组测序的方法研究了植物乳杆菌J26(Lactobacillus plantarum J26)形成的生物膜特征,并试图阐明其潜在的代谢途径。结果表明,浮游状态和生物膜状态下的乳酸菌有1 051 个基因表达差异显著,其中513 个基因被上调,而538 个基因被下调,这些基因与代谢、氨基酸合成、应激反应、酶合成和群体感应密切相关。
2.1 群体感应
在一个细菌群体中,细菌之间可以通过某些小分子作为信号分子进行交流,这种小分子物质被称为“自诱导物质”(autoinducer,AI)。群体感应是细菌之间通过自诱导的信号分子进行相互交流,调控自身不同基因表达并调控群体行为的一种现象。群体感应涉及到细菌的多种功能,如孢子的形成、DNA转移、抗生素生成、生物发光性等,当然生物膜的形成也受到群体感应的调控[42-43]。根据信号分子的不同,群体感应通常分为3 种:第一种是以酰基高丝氨酸内酯类物质作为信号分子,存在于革兰氏阴性菌中[8];第二种是以经过修饰的寡肽类物质作为信号分子,存在于革兰氏阳性菌中[44];第三种是以AI-2作为信号分子,既存在于革兰氏阳性菌中也存在于革兰氏阴性菌中,乳酸菌的群体感应就受到AI-2信号分子的调节[45]。目前研究比较多的是乳酸菌生物膜的形成受到群体感应的调控[46]。
2.1.1 群体感应与抗逆性
外界环境变化会触发乳酸菌的群体感应从而调控生物膜的形成,并增强抗逆性。luxS/AI-2介导的群体感应可以调控生物膜的形成。luxS是控制AI-2产生的一个重要基因。在鼠李糖乳杆菌(Lactobacillus rhamnosus)和嗜酸乳杆菌中(Lactobacillus acidophilus),luxS的缺失会导致生物膜形成能力的下降,且外源添加AI-2或其前体分子可以促进生物膜的形成,在副植物乳杆菌中luxS的过表达会增加AI-2的产生并提高菌株的耐热性、胆汁盐抗性以及促进生物膜的形成,转录组测序结果表明,编码转运蛋白、膜蛋白和转录调节子的多个基因受luxS调控,这可能是乳酸菌抗逆性和生物膜形成能力提高的原因[47]。但在罗伊氏乳杆菌(Lactobacillus reuteri)中,这个结果似乎是相反的,有研究人员用1 株罗伊氏乳杆菌构建了不产自诱导分子AI-2的luxS突变体,与野生型相比,不论是在体外还是体内突变体的生物膜厚度都更厚,且外源添加的AI-2也不能使生物膜恢复到野生型的状态[48]。这些研究都表明,luxS/AI-2介导的群体感应系统在不同细菌生物膜的形成中发挥的作用是不同的,即使是在乳酸菌中发挥的作用也不尽相同,可能促进生物膜的形成,也可能抑制生物膜的形成,不过可以确定的是luxS/AI-2介导的群体感应系统确实参与了生物膜的形成(图3)。乳酸菌在遇到有害菌时也会刺激luxS的表达。在嗜酸乳杆菌与单核细胞增生性李斯特菌共培养时,嗜酸乳杆菌luxS基因的转录水平显著增加,而单核细胞增生性李斯特菌(Listeria monocytogenes)的生长明显被抑制,这与生物膜的形成可以增强乳酸菌的抗菌性可能有关[13,49]。
2.1.2 群体感应与黏附性
细菌的黏附性也是生物膜形成的一个重要因素,细菌的黏附能力增强其形成生物膜的能力也随之增强。群体感应能通过影响乳酸菌的黏附性来调控生物膜的形成。Jia Fangfang等[50]敲除植物乳杆菌(Lactobacillus plantarum KLDS1.0391)的luxS后,其对酸和胆汁盐的耐受性明显降低,且对Caco-2细胞的黏附能力明显降低,结合上文“luxS的缺失会影响生物膜的形成”,推测luxS/AI-2介导的群体感应可能影响乳酸菌的黏附性从而调控生物膜。肽介导的辅助基因调节器(accessory gene regulator,Agr)系统也是一个群体感应系统,由一个包含4 个基因的操纵子(agrBDCA)组成[51]。在植物乳杆菌WCFS1中,lamACD操纵子编码lamA基因,该操纵子是与金黄色葡萄球菌Agr系统同源的双组分调节系统,lamA与编码表面多糖、细胞膜蛋白和糖的利用有关,因此能控制植物乳杆菌的黏附性,影响生物膜的形成(图3)[52-53]。Perez-Ibarreche等[54]对清酒乳杆菌(Lactobacillus sakei CRL1862)的研究结果表明,CRL1862中对黏附起最重要调控作用的基因是srtA2,srtA1和srtA2能够通过识别LPXTG序列将大量功能不同的蛋白质锚定在细胞壁上,从而增加乳酸菌的黏附性(图3)。这与Call等[55]的报道类似,乳酸菌需要两种SrtA酶才能与结肠上皮细胞系产生结合,而某些酶的失活并不会影响黏附。但这些黏附基因是否受到群体感应的调控尚不明确。
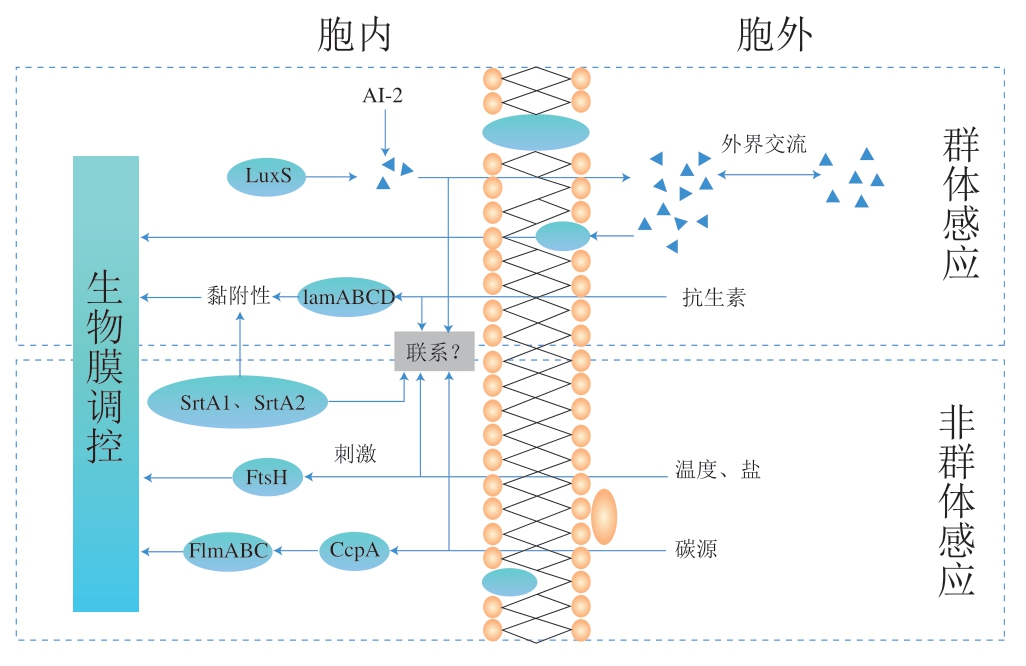
图 3 各种因素对乳酸菌生物膜的调控机制
Fig. 3 Regulatory effects of various factors on lactic acid bacteria biofilm
2.2 非群体感应因素
除luxS外,乳酸菌生物膜的形成还受到许多基因的调控。环境因素的改变会影响某些基因的表达,从而影响生物膜的形成,其机制可用图3概括表示。Bove等[56]的研究表明,在植物乳杆菌WCFS1(Lactobacillus plantarum WCFS1)中,ftsH发生突变使FtsH蛋白酶缺失,FtsH蛋白是一种ATP依赖性金属蛋白酶,其缺失会导致突变体耐热和耐盐性能变差,且形成生物膜能力降低。相反的,过量表达的FtsH可以使植物乳杆菌的耐热和耐盐性能增强,且生物膜形成能力也相应增强。因此,ftsH可以调控生物膜的形成以抵御外界不良环境,增强细菌的抗逆性。Muscariello等[57]在植物乳杆菌基因组中发现了flmA、flmB和flmC 3 个基因,并通过分离携带相应基因零突变的菌株,研究了flmA、flmB和flmC在生物膜形成中的作用。结果发现这3 个基因编码的Flm蛋白参与了生物膜的形成。flmA、flmB、flmC蛋白的氨基酸序列与变形链球菌生物膜调节蛋白(biofilm regulatory protein A,BrpA)的同源性较高,BrpA被认为是变形链球菌生物膜发育的调节因子[58]。此外,通过转录研究表明,flmA、flmB和flmC的表达受到分解代谢控制蛋白A(catabolite control protein A,CcpA)的调控,CcpA激活了flmA的表达,抑制了flmB和flmC的表达。CcpA是碳分解代谢抑制的中介调节因子,也被证明是革兰氏阳性菌中的一个重要调节因子[59]。碳源对生物膜的形成有着重要作用,因此CcpA介导的生物膜形成机制可能受到碳源的影响,当碳源缺乏的时候,乳酸菌可以通过CcpA促进生物膜的形成,而当碳源过量时则抑制生物膜的形成。许多研究表明,乳酸菌在遇到抗生素胁迫时同样会形成生物膜以抵御抗生素的胁迫。George等[60]研究发现亚抑制浓度的庆大霉素会促进lamBDCA操纵子的表达,调控乳酸菌的黏附性,从而促使植物乳杆菌MCC3011(Lactobacillus plantarum MCC3011)产生生物膜。生物膜的形成一方面可以使抗生素更加难以侵入细菌;另一方面也可以促进细菌间耐药基因的转移,这也是细菌产生耐药性的原因之一[61]。
3 乳酸菌生物膜在食品中的应用
目前关于生物膜的研究多集中在生物膜的负面影响方面,如在临床上,生物膜的形成给消毒带来了困难;在医疗器械上形成的生物膜也会污染器械;许多疾病的发生也与生物膜的形成有关,如牙周病、慢性中耳炎、尿路感染等[62]。在食品领域,生物膜的形成同样会污染食品生产管道或食品加工设备,因其难以杀灭甚至会污染食品原料,给食品安全带来了隐患[63-64]。乳酸菌作为一种益生菌存在于许多食品中,但某些条件下产生的生物膜依然会导致食品变质。据报道,许多乳酸菌菌种产生的生物膜会影响肉、奶酪、清酒、啤酒和沙拉的品质,如果糖乳杆菌(Lactobacillus fructivorans)会使蛋黄酱和味噌变质,醋酸乳杆菌(Lactobacillus acetotolerans)和短乳杆菌(Lactobacillus brevis)会导致食醋变质,植物乳杆菌亚种(Lactobacillus plantarum subsp. plantarum)可导致非常常见的食品生产厂污染和泡菜腐败[65-66]。但是从另一个角度看,乳酸菌作为一种益生菌,形成生物膜后抗逆性强,其抑菌特点也可以作为一种独特的优势。在某些情况下,乳酸菌生物膜可能会提高食品的品质,因为其产生的某些物质(如某些奶酪中的乳酸菌生物膜产生的醛类和酮类物质)会改变食品原始的香气和质地[67-68]。如果能利用好成膜的乳酸菌,其在食品工业中的潜力同样是巨大的[69]。
3.1 乳酸菌生物膜的抑菌作用
目前对乳酸菌生物膜应用研究较多的是其抑菌方面,乳酸菌的成膜能使乳酸菌对多种与其产生拮抗作用的病原菌产生抑制。有研究表明,乳酸菌生物膜能控制单核细胞增生李斯特菌、鼠伤寒沙门氏菌(Salmonella typhimurium)和大肠杆菌O157:H7(Escherichia coli O157:H7)的生长[70]。这使其可能应用于食品工业中以抑制有害菌的生长,如使用L. sakei CRL1862作为一种环保型卫生剂,可以减少或抑制用于肉类加工设施非生物表面上的单核细胞增生李斯特菌生物膜,避免即食食品在加工中受到污染,最终提高食品的安全性[54]。Speranza等[71]研究发现,植物乳杆菌(Lactobacillus plantarum)、干酪乳杆菌(Lactobacillus casei)、副干酪乳杆菌(Lactobacillus paracasei)和弯曲乳杆菌(Lactobacillus brevis)都能形成生物膜,用乳酸菌生物膜发酵的干酪中也含有优质生物膜,且这些干酪中的生物膜能有效抑制单核细胞增生李斯特菌的生长。Jalilsood等[72]的研究显示,植物乳杆菌AP21能够与几种病原性和食物腐败细菌(如肠炎沙门氏菌(Salmonella enteritidis)、蜡状芽孢杆菌(Bacillus cereus)、荧光假单胞菌(Pseudomonas fluorescens)和嗜水气单胞菌(Aeromonas hydrophila))结合,并抑制这几种细菌的生长。使用植物乳杆菌和发酵乳杆菌(Lactobacillus fermentum)混菌发酵也可以得到类似的抑菌效果,且该联用处理似乎还具有独特的抗炎特性[73]。这些都说明乳酸菌生物膜在食源性病原体的控制和预防食物腐败方面有着巨大的应用潜力。
3.2 乳酸菌生物膜在发酵方面的应用
3.2.1 发酵乳制品中的应用
虽然在食品和食品加工厂形成的生物膜通常会污染产品、损坏设备[74],但在某些发酵过程中,生物膜也有可能会有利于食品技术的发展。例如,在传统奶酪的生产中,意大利拉古萨诺(Ragusano)和法国萨勒(French Salers)奶酪都是用生牛奶制成的,而用于发酵和成熟的木桶中就有丰富的微生物生物膜,这些生物膜主要由嗜热链球菌(Streptococcus thermophilus)、乳酸菌、乳球菌、肠球菌和亮色单体菌组成。在该情况下,生物膜是人们希望产生的,而且对奶酪的独特风味起着重要的作用[75-77]。Hu Mengxin等[78]在静电纺丝纳米纤维膜上培养出了植物乳杆菌的生物膜,并且发现与浮游乳酸菌相比,纳米纤维膜上的乳酸菌生物膜有着优良的胃肠道抵抗能力,在体外消化3 h后存活细胞数量反而增加。使用含有植物乳杆菌生物膜的纳米纤维膜作为发酵剂发酵所生产酸奶显示出了优良的发酵性能,该生物膜发酵剂能够缩短发酵时间,并且使酸奶在货架期内益生菌的存活率更高。该生物膜发酵剂在发酵过程中可以源源不断地释放出乳酸菌进行发酵,有着很好的可重复利用性。
3.2.2 醋酸饮料中的应用
因为乳酸菌生物膜对酸和醇等不良环境的耐受性较强,所以生物膜发酵潜力更大,可以在更加广泛的环境下进行发酵[79],如可以在更低的pH值或更高的乙醇浓度下进行发酵。混菌发酵具有独特的优势,在醋酸发酵的过程中添加乳酸菌混菌发酵可能使醋的风味和品质更好[80]。但浮游状态的乳酸菌不一定能耐受醋酸发酵的环境,而成膜的乳酸菌则有可能耐受这个环境,并参与混菌发酵。同理,在酵母发酵过程中,浮游的乳酸菌对乙醇的耐受性很差,但是生物膜状态的乳酸菌则可以耐受更高浓度的乙醇,从而使乳酸菌参与酵母的混菌发酵[81]。如在米醋发酵过程中分离得到的一株植物乳杆菌和酵母菌以及醋酸菌都能形成良好的生物膜,并且能高效地产生乙醇和乙酸,对乙醇和pH值都有良好的耐受性,有望在发酵和酿造中应用[82]。
3.2.3 其他方面的应用
Rangaswamy等[83]利用德氏乳杆菌(Lactobacillus delbrueckii)在网状聚氨醋泡沫材料上形成的生物膜来发酵产乳酸,结果表明乳酸的生产速率有了明显的提高,在很长一段时间容积生产率可以达到5 g/(L·h)。上述发酵系统具有产率高、连续性好且稳定的特点,可长时间保持较高的产率。此外,乳酸菌生物膜还可以改善最终发酵产品的性能并延长其保质期,如在发酵橄榄中接种戊糖乳杆菌B281(Lactobacillus pentosus B281),乳酸菌在橄榄表面和发酵设备表面形成生物膜并大量繁殖,最终改善产品的理化特性和感官特性[84]。在发酵香肠中的清酒乳杆菌(Lactobacillus sake)也有助于改善产品质量[85]。
4 结 语
乳酸菌生物膜广泛存在于生物和非生物表面,目前对于乳酸菌生物膜的结构、成分和形成过程已经有了比较成熟的认识,但对于乳酸菌生物膜的调控机制并不是十分明确。由于乳酸菌生物膜在形成过程中涉及到许多基因的表达和多种机制的调控,不同的乳酸菌形成生物膜的方式不同,即使是同一种乳酸菌,在不同环境下形成生物膜的方式也可能不同,这些都给生物膜调控机制的研究带来了困难。由于涉及基因众多且调控复杂,因此可以考虑通过基因组、转录组、蛋白组等手段揭示其中的机制,最新的一些研究也已经开始从这些方面出发进行探索,这对乳酸菌生物膜的利用至关重要。除此以外,如何利用好乳酸菌生物膜对不良环境耐受性强等特点,开发出更加独特的发酵产品、缩短发酵时间、提高发酵产品的质量及延长发酵产品的货架期,以及利用乳酸菌生物膜对有害菌的抑制作用这一特性,控制病原菌和腐败微生物的生长,从而减少食物中毒、产品变质和化学试剂的使用,将是乳酸菌生物膜工业化与产业化的主要应用方向。
[1] BRUCK H L, DELVIGNE F, DHULSTER P, et al. Molecular strategies for adapting Bacillus subtilis 168 biosurfactant production to biofilm cultivation mode[J]. Bioresource Technology, 2019, 293:122090. DOI:10.1016/j.biortech.2019.122090.
[2] MERINO L, PROCURA F, TREJO F M, et al. Biofilm formation by Salmonella sp. in the poultry industry: Detection, control and eradication strategies[J]. Food Research International, 2017, 119: 530-540. DOI:10.1016/j.foodres.2017.11.024.
[3] FLEMMING H C, WUERTZ S. Bacteria and archaea on earth and their abundance in biofilms[J]. Nature Reviews Microbiology, 2019,17(4): 247-260. DOI:10.1038/s41579-019-0158-9.
[4] ZHANG Wenxiang, TANG Bing, BIN Liying. Research progress in biofilm-membrane bioreactor: a critical review[J]. Industrial& Engineering Chemistry Research, 2017, 56(24): 6900-6909.DOI:10.1021/acs.iecr.7b00794.
[5] HU Xuewei, CHEN Kai, LAI Xinke, et al. Effects of Fe(III) on biofilm and its extracellular polymeric substances (EPS) in fixed bed biofilm reactors[J]. Water Science & Technology, 2016, 73(9): 2060-2066.DOI:10.2166/wst.2016.042.
[6] LIRA M C, GIVISIEZ P E N, DE SOUSA F G C, et al. Biofilmforming and antimicrobial resistance traits of staphylococci isolated from goat dairy plants[J]. The Journal of Infection in Developing Countries, 2016, 10(9): 932-938. DOI:10.3855/jidc.6714.
[7] VILLA-ROJAS R, ZHU M J, PAUL N C, et al. Biofilm forming Salmonella strains exhibit enhanced thermal resistance in wheat flour[J]. Food Control, 2016, 73: 689-695. DOI:10.1016/j.foodcont.2016.09.021.
[8] TSENG B S, MAJERCZYK C D, PASSOS D S D, et al. Quorum sensing influences Burkholderia thailandensis biofilm development and matrix production[J]. Journal of Bacteriology, 2016, 198(19):2643-2650. DOI:10.1128/JB.00047-16.
[9] DANIEL P D S, MELISSA S, MATTHEW P, et al. An update on the sociomicrobiology of quorum sensing in Gram-negative biofilm development[J]. Pathogens, 2017, 6(4): 51-59. DOI:10.3390/pathogens6040051.
[10] KAEWIAD K, KAEWNOPPARAT S, KAEWNOPPARAT N. In vitro comparison of probiotic properties of Lactobacillus fermentum SK54 isolated from new born baby with Lactobacillus rhamnosus GG ATCC 53103[J]. Advanced Materials Research, 2015, 1060: 215-218.DOI:10.4028/www.scientific.net/AMR.1060.215.
[11] BAFNA H P, AJITHKRISHNAN C G, KALANTHARAKATH T, et al. Effect of short-term consumption of amul probiotic yogurt containing Lactobacillus acidophiluxs La5 and Bifidobacterium lactis Bb12 on salivary Streptococcus mutans count in high caries risk individuals[J]. International Journal of Applied & Basic Medical Research, 2018, 8(2): 111-115. DOI:10.4103/ijabmr.IJABMR_447_16.
[12] GALLO M, PASSANNANTI F, CANTE R C, et al. Effects of the glucose addition during lactic fermentation of rice, oat and wheat flours[J]. Applied Food Biotechnology, 2020, 7(1): 21-30.DOI:10.22037/afb.v7i1.26975.
[13] ABEE T, KOVÁCS A T, KUIPERS O P, et al. Biofilm formation and dispersal in Gram-positive bacteria[J]. Current Opinion in Biotechnology,2011, 22(2): 172-179. DOI:10.1016/j.copbio.2010.10.016.
[14] SALAS-JARAMJ, ILABACAA, VEGAM. Biofilm forming lactobacillus: new challenges for the development of probiotics[J]. Microorganisms, 2016, 4(3): 1-14. DOI:10.3390/microorganisms4030035.
[15] GEORGE J, HALAMI P M. Presence of extracellular DNA &protein in biofilm formation by gentamicin-resistant Lactobacillus plantarum[J]. Indian Journal of Medical Research, 2019, 149(2): 257-262. DOI:10.4103/ijmr.IJMR_2022_17.
[16] BERRÍOS P, FUENTES J A, SALAS D, et al. Inhibitory effect of biofilm-forming Lactobacillus kunkeei strains against virulent Pseudomonas aeruginosa in vitro and in honeycomb moth (Galleria mellonella) infection model[J]. Beneficial Microbes, 2018, 9(2):257-268. DOI:10.3920/BM2017.0048.
[17] DE ANGELIS M, SIRAGUSA S, CAMPANELLA D, et al.Comparative proteomic analysis of biofilm and planktonic cells of Lactobacillus plantarum DB200[J]. Proteomics, 2015, 15(13): 2244-2257. DOI:10.1002/pmic.201400363.
[18] 尹一婷. 乳杆菌生物膜成膜规律及其特性研究[D]. 无锡: 江南大学,2019: 1-2.
[19] NEU T R, KUHLICKE U. Fluorescence lectin bar-coding of glycoconjugates in the extracellular matrix of biofilm and bioaggregate forming microorganisms[J]. Microorganisms, 2017, 5(1): 1-13.DOI:10.3390/microorganisms5010005.
[20] VLAMAKIS H, CHAI Y R, BEAUREGARD P, et al. Sticking together: building a biofilm the Bacillus subtilis way[J]. Nature Reviews Microbiology, 2013, 11(3): 157-168. DOI:10.1038/nrmicro2960.
[21] VEERACHAMY S, YARLAGADDA T, MANIVASAGAM G, et al.Bacterial adherence and biofilm formation on medical implants: A review[J]. Proceedings of The Institution of Mechanical Engineers Part H-Journal of Engineering in Medicine, 2014, 228(10): 1083-1099.DOI:10.1177/0954411914556137.
[22] RODER H L, OLSEN N M C, WHITELEY M, et al. Unravelling interspecies interactions across heterogeneities in complex biofilm communities[J]. Environmental Microbiology, 2020, 22(1): 5-16.DOI:10.1111/1462-2920.14834.
[23] KOO H, ALLAN R N, HOWLIN R P, et al. Targeting microbial biofilms: current and prospective therapeutic strategies[J]. Nature Reviews Microbiology, 2017, 15(12): 740-755. DOI:10.1038/nrmicro.2017.99.
[24] 钟华晨. 高产生物膜乳酸菌的筛选、鉴定及胞外多糖分泌条件的研究[D]. 呼和浩特: 内蒙古农业大学, 2019: 1-4.
[25] MURUZOVIC M Z, MLADENOVIC K G, COMIC L R. In vitro evaluation of resistance to environmental stress by planktonic and biofilm form of lactic acid bacteria isolated from traditionally made cheese from Serbia[J]. Food Bioscience, 2018, 23: 54-59.DOI:10.1016/j.fbio.2018.03.005.
[26] YUNDA E, QUILES F. In situ spectroscopic analysis of Lactobacillus rhamnosus GG flow on an abiotic surface reveals a role for nutrients in biofilm development[J]. Biofouling, 2019, 35(5): 494-507.DOI:10.1080/08927014.2019.1617279.
[27] SLIZOVA M, NEMCOVA R, MAD’AR M, et al. Analysis of biofilm formation by intestinal lactobacilli[J]. Canadian Journal of Microbiology, 2015, 61(6): 437-446. DOI:10.1139/cjm-2015-0007.
[28] LEBEER S, VERHOEVEN T L, VELEZ M P, et al. Impact of environmental and genetic factors on biofilm formation by the probiotic strain Lactobacillus rhamnosus GG[J]. Applied and Environmental Microbiology, 2007, 73(21): 6768-6775. DOI:10.1128/AEM.01393-07.
[29] SHI Xianming, ZHU Xinna. Biofilm formation and food safety in food industries[J]. Trends in Food Science & Technology, 2009, 20(9): 407-413. DOI:10.1016/j.tifs.2009.01.054.
[30] HAHNEL S, WIESER A, LANG R, et al. Biofilm formation on the surface of modern implant abutment materials[J]. Clinical Oral Implants Research, 2014, 26(11): 1297-1301. DOI:10.1111/clr.12454.
[31] ANSELME K, DAVIDSON P, POPA A M, et al. The interaction of cells and bacteria with surfaces structured at the nanometer scale[J]. Acta Biomaterialia, 2010, 6(10): 3824-3846. DOI:10.1016/j.actbio.2010.04.001.
[32] IONESCU A, WUTSCHER E, BRAMBILLA E, et al. Influence of surface properties of resin-based composites on in vitro Streptococcus mutans biofilm development[J]. European Journal of Oral Sciences,2012, 120(5): 458-465. DOI:10.1111/j.1600-0722.2012.00983.x.
[33] ARENA M P, CAPOZZI V, SPANO G, et al. The potential of lactic acid bacteria to colonize biotic and abiotic surfaces and the investigation of their interactions and mechanisms[J]. Applied Microbiology and Biotechnology, 2017, 101(7): 2641-2657.DOI:10.1007/s00253-017-8182-z.
[34] CAMPOCCIA D, MONTANARO L, ARCIOLA C R. A review of the biomaterials technologies for infection-resistant surfaces[J]. Biomaterials, 2013, 34: 8533-8554. DOI:10.1016/j.biomaterials.2013.07.089.
[35] ZHANG Xiaoxue, WANG Ling, LEVANEN E. Superhydrophobic surfaces for the reduction of bacterial adhesion[J]. RSC Advances,2013, 3: 12003-12020. DOI:10.1039/c3ra40497h.
[36] ALZUBEIDI Y S, UDOMPIJITKUL P, TALUKDAR P K, et al.Inactivation of Clostridium perfringens spores adhered onto stainless steel surface by agents used in a clean-in-place procedure[J].International Journal of Food Microbiology, 2018, 277: 26-33.DOI:10.1016/j.ijfoodmicro.2018.04.016.
[37] 王星, 张华, 张淼, 等. 乳酸菌生物膜的形成及其影响因素[J].中国乳品工业, 2020, 48(3): 38-40; 46. DOI:10.19827/j.issn1001-2230.2020.03.008.
[38] SAUNDERS L P, BISCHOFF K M, BOWMAN M J, et al. Inhibition of Lactobacillus biofilm growth in fuel ethanol fermentations by Bacillus[J]. Bioresource Technology, 2019, 272: 156-161.DOI:10.1016/j.biortech.2018.10.016.
[39] WU Chienchen, LIN Chingting, WU Chingyi, et al. Inhibitory effect of Lactobacillus salivarius on Streptococcus mutans biofilm formation[J].Molecular Oral Microbiology, 2015, 30(1): 16-26. DOI:10.1111/omi.12063.
[40] LIU Lei, WU Ruiyun, ZHANG Jinlan, et al. D-Ribose interferes with quorum sensing to inhibit biofilm formation of Lactobacillus paraplantarum L-ZS9[J]. Frontiers in Microbiology, 2017, 8: 1860.DOI:10.3389/fmicb.2017.01860.
[41] SUN Linlin, ZHANG Yu, GUO Xiaojie, et al. Characterization and transcriptomic basis of biofilm formation by Lactobacillus plantarum J26 isolated from traditional fermented dairy products[J]. LWTFood Science and Technology, 2020, 125: 109333. DOI:10.1016/j.lwt.2020.109333.
[42] 邓曌曦, 音建华, 汪海峰. 乳酸菌群体感应与其肠道生物膜形成的研究进展 [J]. 微生物学报, 2018, 58(11): 1970-1978. 10.13343/j.cnki.wsxb.20180147.
[43] PARK H, SHIN H, LEE K, et al. Autoinducer-2 properties of kimchi are associated with lactic acid bacteria involved in its fermentation[J].International Journal of Food Microbiology, 2016, 225: 38-42.DOI:10.1016/j.ijfoodmicro.2016.03.007.
[44] PENG Pai, BALDRY M, GLESS B H, et al. Effect of co-inhabiting coagulase negative staphylococci on S. aureus agr quorum sensing, host factor binding, and biofilm formation[J]. Frontiers in Microbiology, 2019, 10: 2212. DOI:10.3389/fmicb.2019.02212.
[45] SONG Xiaodong, LIU Chenjian, HUANG Shihao, et al. Cloning,expression and characterization of two S-ribosylhomocysteine lyases from Lactobacillus plantarum YM-4-3: Implication of conserved and divergent roles in quorum sensing[J]. Protein Expression and Purification, 2018, 145: 32-38. DOI:10.1016/j.pep.2017.12.013.
[46] GU Yue, LI Bo, TIAN Jianjun, et al. The response of LuxS/AI-2 quorum sensing in Lactobacillus fermentum 2-1 to changes in environmental growth conditions[J]. Annals of Microbiology, 2018,68(5): 287-294. DOI:10.1007/s13213-018-1337-z.
[47] LIU Lei, WU Ruiyun, ZHANG Jinlan, et al. Overexpression of luxS promotes stress resistance and biofilm formation of Lactobacillus paraplantarum L-ZS9 by regulating the expression of multiple genes[J]. Frontiers in Microbiology, 2018, 9: 2628. DOI:10.3389/fmicb.2018.02628.
[48] TANNOCK G W, GHAZALLY S, WALTER J, et al. Ecological behavior of Lactobacillus reuteri 100-23 is affected by mutation of the luxS gene[J]. Applied and Environmental Microbiology, 2005, 71(12):8419-8425. DOI:10.1128/AEM.71.12.8419-8425.2005.
[49] MOSLEHI-JENABIAN S, VOGENSEN F K, JESPERSEN L. The quorum sensing luxS gene is induced in Lactobacillus acidophilus NCFM in response to Listeria monocytogenes[J]. International Journal of Food Microbiology, 2011, 149(3): 269-273. DOI:10.1016/j.ijfoodmicro.2011.08.018.
[50] JIA Fangfang, ZHENG Huiqi, SUN Sirui, et al. Role of luxS in stress tolerance and adhesion ability in Lactobacillus plantarum KLDS1.0391[J]. BioMed Research International, 2018, 2018:4506829. DOI:10.1155/2018/4506829.
[51] FUJII T, INGHAM C, NAKAYAMA J, et al. Two homologous agrlike quorum-sensing systems cooperatively control adherence, cell morphology, and cell viability properties in Lactobacillus plantarum WCFS1[J]. Journal of Bacteriology, 2008, 190(23): 7655-7665.DOI:10.1128/JB.01489-07.
[52] JAIME C, MARA B, BOJER M S, et al. Cross-talk between Staphylococcus aureus and other staphylococcal species via the agr quorum sensing system[J]. Frontiers in Microbiology, 2016, 7: 1733.DOI:10.3389/fmicb.2016.01733.
[53] STURME M H J, NAKAYAMA J, MOLENAAR D, et al. An agrlike two-component regulatory system in Lactobacillus plantarum is involved in production of a novel cyclic peptide and regulation of adherence[J]. Journal of Bacteriology, 2005, 187(15): 5224-5235.DOI:10.1128/JB.187.15.5224-5235.2005.
[54] PEREZ-IBARRECHE M, MENDOZA L M, VIGNOLO G,et al. Proteomic and genetics insights on the response of the bacteriocinogenic Lactobacillus sakei CRL1862 during biofilm formation on stainless steel surface at 10 ℃[J]. International Journal of Food Microbiology, 2017, 258: 18-27. DOI:10.1016/j.ijfoodmicro.2017.07.003.
[55] CALL E K, KLAENHAMMER T R. Relevance and application of sortase and sortase-dependent proteins in lactic acid bacteria[J]. Frontiers in Microbiology, 2013, 4: 73. DOI:10.3389/fmicb.2013.00073.
[56] BOVE P, CAPOZZI V, GAROFALO C, et al. Inactivation of the ftsH gene of Lactobacillus plantarum WCFS1: effects on growth,stress tolerance, cell surface properties and biofilm formation[J].Microbiological Research, 2012, 167(4): 187-193. DOI:10.1016/j.micres.2011.07.001.
[57] MUSCARIELLO L, MARINO C, CAPRI U, et al. CcpA and three newly identified proteins are involved in biofilm development in Lactobacillus plantarum[J]. Journal of Basic Microbiology, 2013,53(1): 62-71. DOI:10.1002/jobm.201100456.
[58] WEN Z T, BAKER H V, BURNE R A. Influence of BrpA on critical virulence attributes of Streptococcus mutans[J]. Journal of Bacteriology, 2006, 188(8): 2983-2992. DOI:10.1128/JB.188.8.2983-2992.2006.
[59] SEIDL K, GOERKE C, WOLZ C, et al. Staphylococcus aureus CcpA affects biofilm formation[J]. Infection and Immunity, 2008, 76(5):2044-2050. DOI:10.1128/IAI.00035-08.
[60] GEORGE J, HALAMI P M. Sub-inhibitory concentrations of gentamicin triggers the expression of aac(6’)Ie-aph(2”)Ia, chaperons and biofilm related genes in Lactobacillus plantarum MCC 3011[J].Research in Microbiology, 2017, 168(8): 722-731. DOI:10.1016/j.resmic.2017.06.002.
[61] JIANG Yu, GENG Mengxin, BAI Liping. Targeting biofilms therapy: current research strategies and development hurdles[J]. Microorganisms, 2020, 8(8): 1222. DOI:10.3390/microorganisms8081222.
[62] POZO D, LUIS J. Biofilm-related disease[J]. Expert Review of Anti-Infective Therapy, 2017, 16(1): 51-65. DOI:10.1080/14787210.2018.1417036.
[63] MIAO Jian, LIANG Yanrui, CHEN Lequn, et al. Formation and development of Staphylococcus biofilm: With focus on food safety[J].Journal of Food Safety, 2017, 37(4): 1-11. DOI:10.1111/jfs.12358.
[64] NAHAR S, MIZAN M F R, HA A J W, et al. Advances and future prospects of enzyme-based biofilm prevention approaches in the food industry[J]. Comprehensive Reviews in Food Science and Food Safety,2018, 17(6): 1484-1502. DOI:10.1111/1541-4337.12382.
[65] SOMERS E B, JOHNSON M E, WONG A C L. Biofilm formation and contamination of cheese by nonstarter lactic acid bacteria in the dairy environment[J]. Journal of Dairy Science, 2001, 84(9): 1926-1936. DOI:10.3168/jds.S0022-0302(01)74634-6.
[66] KUBOTA H, SENDA S, TOKUDA H, et al. Stress resistance of biofilm and planktonic Lactobacillus plantarum subsp. plantarum JCM 1149[J]. Food Microbiology, 2009, 26(6): 592-597. DOI:10.1016/j.fm.2009.04.001.
[67] SHOKRI D, KHORASGANI M R, MOHKAM M, et al. The inhibition effect of lactobacilli against growth and biofilm formation of Pseudomonas aeruginosa[J]. Probiotics and Antimicrobial Proteins,2018, 10(1): 34-42. DOI:10.1007/s12602-017-9267-9.
[68] RAMIREZ M D F, SMID E J, ABEE T, et al. Characterisation of biofilms formed by Lactobacillus plantarum WCFS1 and food spoilage isolates[J]. International Journal of Food Microbiology, 2015,207: 23-29. DOI:10.1016/j.ijfoodmicro.2015.04.030.
[69] ERCAN D, DEMIRCI A. Current and future trends for biofilm reactors for fermentation processes[J]. Critical Reviews in Biotechnology,2015, 35(1): 1-14. DOI:10.3109/07388551.2013.793170.
[70] GÓMEZ N C, RAMIRO J M P, QUECAN B X V, et al. Use of Potential probiotic lactic acid bacteria (LAB) biofilms for the control of Listeria monocytogenes, Salmonella Typhimurium, and Escherichia coli O157:H7 biofilms formation[J]. Frontiers in Microbiology, 2016,7: 863. DOI:10.3389/fmicb.2016.00863.
[71] SPERANZA B, SINIGAGLIA M, CORBO M R. Non starter lactic acid bacteria biofilms: A means to control the growth of Listeria monocytogenes in soft cheese[J]. Food Control, 2009, 20(11): 1063-1067. DOI:10.1016/j.foodcont.2009.01.006.
[72] JALILSOOD T, BARADARAN A, SONG A A, et al. Inhibition of pathogenic and spoilage bacteria by a novel biofilm-forming Lactobacillus isolate: a potential host for the expression of heterologous proteins[J]. Microbial Cell Factories, 2015, 14(1): 96.DOI:10.1186/s12934-015-0283-8.
[73] AOUDIA N, RIEU A, BRIANDET R, et al. Biofilms of Lactobacillus plantarum and Lactobacillus fermentum: Effect on stress responses,antagonistic effects on pathogen growth and immunomodulatory properties[J]. Food Microbiology, 2015, 53: 51-59. DOI:10.1016/j.fm.2015.04.009.
[74] 吴荣. 信号分子AI-2对乳酸菌生物膜形成的影响[D]. 呼和浩特:内蒙古农业大学, 2018: 4-5.
[75] SCATASSA M L, GAGLIO R, MACALUSO G, et al. Transfer,composition and technological characterization of the lactic acid bacterial populations of the wooden vats used to produce traditional stretched cheeses[J]. Food Microbiology, 2015, 52: 31-41.DOI:10.1016/j.fm.2015.06.008.
[76] DIDIENNE R, DEFARGUES C, CALLON C, et al. Characteristics of microbial biofilm on wooden vats (‘gerles’) in PDO Salers cheese[J].International Journal of Food Microbiology, 2012, 156(2): 91-101.DOI:10.1016/j.ijfoodmicro.2012.03.007.
[77] CARPINO S, RANDAZZO C L, PINO A, et al. Influence of PDO Ragusano cheese biofilm microbiota on flavour compounds formation[J]. Food Microbiology, 2017, 61: 126-135. DOI:10.1016/j.fm.2016.09.006.
[78] Hu Mengxin, Li Jinian, Guo Qian, et al. Probiotics biofilm-integrated electrospun nanofiber membranes: a new starter culture for fermented milk production[J]. Journal of Agricultural and Food Chemistry, 2019,67(11): 3198-3208. DOI:10.1021/acs.jafc.8b05024.
[79] LIU Lei, WU Ruiyun, LI Jun, et al. Stress resistance of biofilm and planktonic cells of lactobacillus paraplantarum L-ZS9 regulated by autoinducer 2[J]. Food Science, 2017, 38(22): 41-47. DOI:10.7506/spkx1002-6630-201722007.
[80] CHEN Yang, HUANG Yao, BAI Ye, et al. Effects of mixed cultures of Saccharomyces cerevisiae and Lactobacillus plantarum in alcoholic fermentation on the physicochemical and sensory properties of citrus vinegar[J]. LWT-Food Science & Technology, 2017, 84: 753-763.DOI:10.1016/j.lwt.2017.06.032.
[81] CHENG Kuanchen, DEMIRCI A, CATCHMARK J M. Advances in biofilm reactors for production of value-added products[J]. Applied Microbiology and Biotechnology, 2010, 87(2): 445-456. DOI:10.1007/s00253-010-2622-3.
[82] FURUKAWA S. Studies on formation, control and application of biofilm formed by food related microorganisms[J]. Bioscience Biotechnology & Biochemistry, 2015, 79(7): 1050-1056. DOI:10.1080/09168451.2015.1018126.
[83] RANGASWAMY V, RAMAKRISHNA S V. Lactic acid production by Lactobacillus delbrueckii in a dual reactor system using packed bed biofilm reactor[J]. Letters in Applied Microbiology, 2008, 46(6): 661-666. DOI:10.1111/j.1472-765X.2008.02362.x.
[84] GROUNTA A, DOULGERAKI A I, NYCHAS G J E, et al. Biofilm formation on Conservolea natural black olives during single and combined inoculation with a functional Lactobacillus pentosus starter culture[J]. Food Microbiology, 2016, 56: 35-44. DOI:10.1016/j.fm.2015.12.002.
[85] PERPETUINI G, PHAM-HOANG B N, SCORNEC H, et al. In Lactobacillus pentosus, the olive brine adaptation genes are required for biofilm formation[J]. International Journal of Food Microbiology,2016, 216: 104-109. DOI:10.1016/j.ijfoodmicro.2015.10.002.