枸杞(Lycium bararum L.)为茄科枸杞属的一种多分枝小灌木[1]。枸杞子即枸杞的果实,2002年3月国家卫生健康委员会公布的既是食品又是药品的物品名单中包括枸杞子。枸杞首载于《神农本草经》,最早将枸杞子记载为药用部位的本草文献是《名医别录》[2]。《中华人民共和国药典》(2015版)记载的宁夏枸杞成熟果实具有滋补肝肾、益精明目的功效,可用于治疗虚劳精亏、腰膝酸痛、眩晕耳鸣、阳萎遗精、内热消渴、血虚萎黄、目昏不明[3]等病症。枸杞子中具有多种活性成分,如枸杞多糖(Lycium barbarum polysaccharides,LBP)、黄酮类化合物、生物碱、枸杞色素、氨基酸类等。大量研究表明,枸杞子中最具有提取利用价值的是枸杞多糖[4]。本文将从枸杞多糖抗肿瘤、抗氧化、抗衰老、抗炎、降血糖、降血脂、神经保护、生殖保护、保肝和免疫调节等方面进行综述,以期对枸杞多糖的深入研究及开发利用提供参考。
1 枸杞多糖的生物活性
1.1 抗肿瘤活性
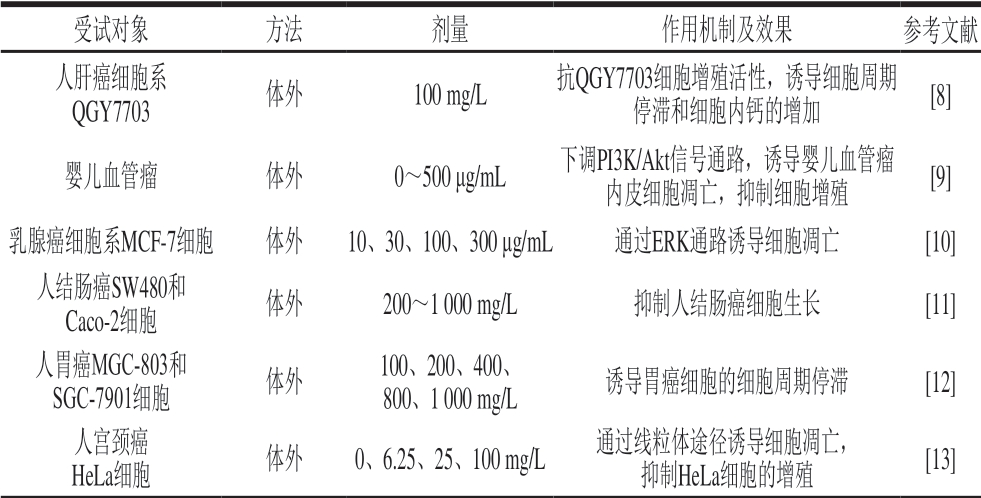
随着经济的发展,人民的健康水平和生活质量稳步提高,人群疾病构成发生了重大变化,恶性肿瘤的流行和分布出现了新趋势[5]。据2019年1月,国家癌症中心发布的最新全国癌症统计数据显示,2015年我国恶性肿瘤发病率为0.286%,中标发病率为0.191%,世标发病率为0.186%[6],其中死亡率居前10位的恶性肿瘤分别为胃癌、食管癌、肝癌、宫颈癌、肺癌、肠癌、白血病、鼻咽癌、乳腺癌和脑瘤[7],恶性肿瘤已成为危害和威胁我国居民健康的常见疾病之一。目前治疗癌症的方法大多数依赖于化学药物,但长期使用化学药物治疗会导致机体免疫力下降等副作用。因此,寻找高效、低毒、低副作用的天然抗肿瘤药物具有重要意义。大量的研究表明,枸杞多糖在抗肝癌、婴儿血管瘤、卵巢癌、宫颈癌、结肠癌、胃癌、肺腺癌、白血病、脑胶质瘤、膀胱癌、人舌鳞状癌等方面有较好的生物活性,枸杞多糖可能成为治疗或者辅助治疗这些肿瘤的良好天然化合物。枸杞多糖抗肿瘤活性的作用机制及效果见表1。
表 1 枸杞多糖抗肿瘤活性的作用机制及效果
Table 1 Recent studies on antitumor effect and mechanism of action of LBP
受试对象 方法 剂量 作用机制及效果 参考文献人肝癌细胞系QGY7703 体外 100 mg/L 抗QGY7703细胞增殖活性,诱导细胞周期停滞和细胞内钙的增加 [8]婴儿血管瘤 体外 0~500 μg/mL 下调PI3K/Akt信号通路,诱导婴儿血管瘤内皮细胞凋亡,抑制细胞增殖 [9]乳腺癌细胞系MCF-7细胞 体外 10、30、100、300 μg/mL 通过ERK通路诱导细胞凋亡 [10]人结肠癌SW480和Caco-2细胞 体外 200~1 000 mg/L 抑制人结肠癌细胞生长 [11]人胃癌MGC-803和SGC-7901细胞 体外 100、200、400、800、1 000 mg/L 诱导胃癌细胞的细胞周期停滞 [12]HeLa细胞 体外 0、6.25、25、100 mg/L 通过线粒体途径诱导细胞凋亡,抑制HeLa细胞的增殖 [13]人宫颈癌
续表1

注:DDP.顺铂(cisplatin);TRAIL.肿瘤坏死因子相关凋亡诱导配体(tumor necrosis factor-related apoptosis inducing ligand);PTX.紫杉醇(paclitaxel);PI3K/Akt.磷脂酰肌醇3激酶/蛋白激酶B(phosphoinositide-3 kinase/protein kinase B);ERK.细胞外调节蛋白激酶(extracellular signal-regulated protein kinase)。
受试对象 方法 剂量 作用机制及效果 参考文献小鼠结肠癌细胞系CT26-WT 体外 100 μg/mL通过Notch信号促进树突状细胞成熟,并增强树突状细胞介导的T淋巴细胞对结肠癌细胞CT26-WT的细胞毒性[14]大鼠 大鼠肝癌模型 20、40 mg/kg mb通过阻滞肝癌组织细胞周期分布,抑制肝癌组织细胞增殖,促进细胞凋亡 [15]人肺腺癌细胞A549 体外 DDP:6、12 mg/L;LBP:8、16 mg/L LBP与DDP联合作用可明显促进A549细胞凋亡,其机制主要与两者对细胞凋亡相关蛋白表达的调节有关[16]肝癌细胞SMMC-7721 体外 100、200、400 μg/mL 抑制肝癌细胞的迁移和侵袭,其机制可能与抑制血管内皮生长因子有关 [17]MLL急性淋巴细胞白血病细胞株KOCL44和KOCL45 体外LBP(100、500、1 000 mg/L)+TRAIL(25、50 ng/mL)LBP与TRAIL联合处理后,上调细胞表面TRAIL死亡受体DR5表达,激活Caspase与线粒体通路,增强MLL基因重排急性淋巴细胞白血病细胞株对TRAIL诱导凋亡的敏感性[18]HepG2肝癌细胞株 体外 0、200、400、800 mg/L抑制HepG2细胞的增殖,诱导细胞发生自噬和凋亡 [19]大鼠大鼠胶质瘤C6细胞的原位肿瘤模型25、50、100、200、400 mg/kg mb通过调节血脑屏障促使CD8阳性T淋巴细胞进入颅内,抑制肿瘤生长,延长胶质瘤大鼠的生存期[20]膀胱癌细胞株T-24 体外 100、200、400 μg/mL 抑制膀胱癌细胞株T-24增殖,促进细胞凋亡 [21]人舌鳞状癌CAL-27细胞 体外 10、50、100、200、400、800 μg/mL 诱导细胞凋亡和自噬 [22]恶性脑胶质瘤病人 口服 6 mg/kg mb提高病人机体免疫功能,增强抗肿瘤能力,降低肿瘤复发率,提高病人生存率[23]人上皮性卵巢癌HO-8910PM细胞株 体外LBP+PTX:(50+0.01)、(100+0.01)、(50+0.05)、(100+0.05) μg/mL抑制人上皮性卵巢癌细胞增殖、促进其凋亡,且LBP明显增强紫杉醇对HO-8910PM细胞株的增殖抑制及诱导凋亡作用[24]
1.2 抗氧化、抗衰老活性
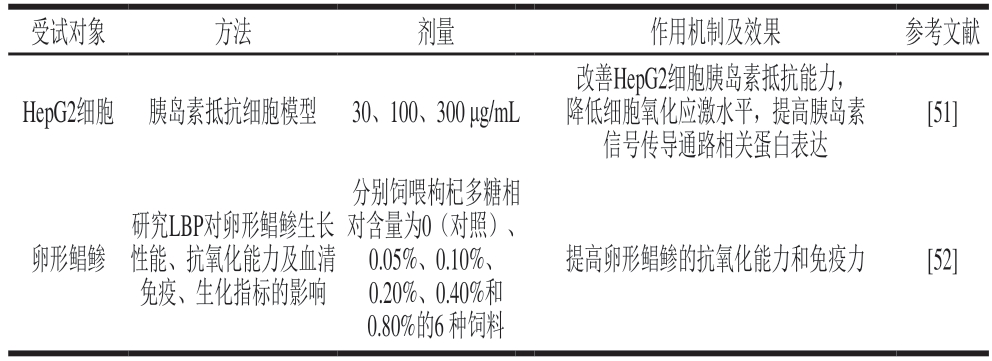
研究表明枸杞多糖具有抗氧化、抗衰老作用。通过枸杞多糖的抗氧化作用,可降低老年小鼠由年龄增长引起的自由基加速脂质过氧化的风险;保护由于激活氧化反应导致的急性肾损伤,缺血再灌注诱导的大鼠视网膜损伤,高氧诱导的急性肺损伤,H2O2诱导的细胞(人子宫内膜间质细胞、人小梁网(human trabecular meshwork,HTM)细胞、人滋养层细胞、血管内皮细胞、大鼠嗜铬细胞瘤PC-12细胞、人神经母细胞瘤SH-SY5Y细胞、人晶状体上皮细胞、人视网膜色素上皮细胞)氧化损伤和大鼠骨骼的氧化损伤;改善氧化应激诱导的大鼠胸主动脉内皮细胞功能障碍和HepG2细胞胰岛素抵抗的作用;抑制急性阿霉素(doxorubicin,DOX)诱导的心脏毒性;提高绿脓杆菌毒素(pyocyanin,PCN)作用后小鼠巨噬细胞的增殖能力和高脂饲料喂养的小鼠抗氧化酶活性等。枸杞多糖抗氧化作用可能会成功应用于低温保存濒危物种胚胎和辅助生殖医学技术。这是由于冷冻保存的胚胎,冷藏过程中会导致线粒体功能障碍并会促进活性氧物质的积累,进而导致早期胚胎发育的受损率增加[25-26]。而枸杞多糖作为抗氧化剂或通过调节线粒体分布、膜电位和功能,可能对先前冷冻保存的胚胎发育有特殊影响。此外,通过D-半乳糖诱导小鼠衰老模型实验[2 7]、对枸杞多糖不同浓度下胚胎的衰老分析[28]、果蝇饮食中补充3 种枸杞多糖制剂实验[29]等证明枸杞多糖具有抗衰老活性。通过分析不同浓度下枸杞多糖对线虫寿命的影响,发现枸杞多糖能够显著延长线虫的寿命[30]。枸杞多糖抗氧化、抗衰老活性的作用机制及效果见表2。
表 2 枸杞多糖抗氧化、抗衰老活性的作用机制及效果
Table 2 Recent studies on antioxidant and anti-aging effects and mechanism of action of LBP

受试对象 方法 剂量 作用机制及效果 参考文献小鼠双细胞胚胎 体外 50、100、200、400、800、1 600 μg/mL恢复线粒体功能,降低活性氧的生成,促进先前低温保存小鼠双细胞胚胎的发育 [31]小鼠 D-半乳糖诱导小鼠衰老模型 100 mg/kg mb抑制D-半乳糖诱导的小鼠体内衰老模型中的非酶糖基化 [32]成年家兔 四氧嘧啶致家兔高血糖水煎剂:0.25 g/kg mb;粗LBP:10 mg/kg mb LBP总抗氧化能力测定表明枸杞提取物/馏分具有抗氧化活性 [33]小鼠 老年小鼠 200、350、500 mg/kg mb降低由年龄引起的自由基加速脂质过氧化的风险 [34]小鼠 脂多糖诱导小鼠急性肾损伤模型200、400、800 mg/kg mb调节促炎细胞因子水平和Keap1-Nrf2/ARE信号通路,减轻炎症反应,激活抗氧化反应 [35]大鼠 缺血再灌注诱导大鼠视网膜损伤 1 mg/kg mb通过激活Nrf2/HO-1抗氧化通路,保护缺血再灌注后的视网膜 [36]小鼠 高氧诱导的急性肺损伤 100 mg/kg mb 通过Nrf2途径减轻小鼠高氧急性肺损伤 [37]大鼠动脉内皮细胞 H2O2诱导细胞损伤 110、220、440 g/mL 通过抗凋亡和抗氧化作用,在氧化损伤的血管内皮细胞中起保护作用 [38]人滋养层细胞 H2O2诱导细胞损伤 100、200、400 μg/mL 调节凋亡相关因子的表达,保护人滋养层细胞免受由H2O2诱导的氧化应激和细胞凋亡 [39]人子宫内膜间质细胞H2O2诱导的人子宫内膜间质细胞损伤 100 μg/mL抑制H2O2诱导的子宫内膜基质细胞凋亡,且对子宫内膜基质细胞提供显著的抗氧化应激保护[40]PC12细胞和SH-SY5Y细胞细胞氧化应激 100~500 μg/mL 通过miR-194激活PI3K/Akt途径降低氧化应激反应 [41]H2O2刺激诱导HTM细胞 HTM细胞暴露于H2O2构建氧化损伤模型 0~500 μg/mL 上调HTM细胞中的miR-4295,减轻H2O2诱导的损伤 [42]人晶状体上皮细胞 H2O2诱导细胞凋亡 0、50、100、200、400、800、1 600 mg/L抑制H2O2诱导的Bcl-2下调、Bax蛋白上调,提高超氧化物歧化酶和谷胱甘肽酶活性水平,减弱减缓细胞衰老[43]雄性大鼠 为大鼠设计锻炼计划 100、200、300 mg/kg mb大鼠 DOX诱导心脏毒性 200 mg/kg mb提高糖原水平和抗氧化酶活性,降低丙二醛水平和肌酸激酶活性,显著降低力竭运动引起的氧化应激防止DOX对心脏成肌细胞H9c2的细胞毒性,抑制氧化应激对DOX诱导的急性心脏毒性[44][45]小鼠 高脂饲料喂养 50、100、150 mg/kg mb 提高小鼠抗氧化酶活性,降低丙二醛水平 [46]小鼠 D-半乳糖诱导小鼠衰老模型 1、3 g/kg mb减轻糖代谢紊乱并减少抗脂质过氧化物等物质的产生 [27]斑马鱼胚胎 不同LBP质量浓度下胚胎的衰老分析 1、2、3、4 mg/mL LBP对细胞凋亡和衰老的影响可能是由p53途径介导的 [28]大鼠 氧化应激诱导的大鼠胸主动脉内皮细胞功能障碍400、800、1 600、3 200、 6 400 μg/mL通过调节EGFR、ErbB2、PI3K/Akt/e-NOS的活性来减少活性氧的产生,从而维持血管内皮的完整性[47]线虫 不同质量浓度下LBP对线虫寿命的影响 300 μg/mL 提高抵抗环境压力的能力,增强生殖潜能,保持肌肉完整性 [30]果蝇 在果蝇饮食中补充3 种枸杞多糖制剂 - 延长果蝇的平均寿命,提高其超氧化物歧化酶和过氧化氢酶活性,降低丙二醛水平 [29]人视网膜色素上皮细胞H2O2诱导人视网膜色素上皮细胞自噬 10、100、1 000 μg/mL 降低Beclin-1、LC3B I和LC3B II表达,上调H2O2诱导所致ARPE-19细胞的自噬水平 [48]小鼠巨噬细胞PCN诱导小鼠巨噬细胞氧化损伤 -抑制PCN造成的胞内活性氧产生,抑制IL-4释放,调控凋亡抑制蛋白Bcl-2、Bcl-xl和凋亡蛋白Caspase3的表达,提高PCN作用后小鼠巨噬细胞的增殖能力[49]PC12细胞 2,4-D诱导PC12细胞氧化损伤 250 mg/L LBP对2,4-D致PC12细胞的氧化损伤和凋亡具有一定的拮抗作用 [50]
续表2
注:IL-4.细胞白介素4(interleukin-4);EGFR.表皮因子生长受体(epidermal growth factor receptor);e-NOS.内皮型一氧化氮合酶(endothelial nitric oxide synthase);ErbB2.人类表皮生长因子受体2(human epidermalgrowth factor receptor-2);Nrf2.核因子E2相关因子2(nuclear factor-E2-related factor 2);ARE.抗氧化反应元件(antioxidant response element);HO-1.血红素加氧酶1(heme oxygenase 1);2,4-D. 2,4-二氯苯氧乙酸(2,4-dichlorophenoxyacetic acid);Keap1. Kelch样环氧氯丙烷相关蛋白1(Kelch-like epichlorohydrinassociated protein 1);-.原文献未指出,表4、9同。
受试对象 方法 剂量 作用机制及效果 参考文献HepG2细胞 胰岛素抵抗细胞模型 30、100、300 μg/mL改善HepG2细胞胰岛素抵抗能力,降低细胞氧化应激水平,提高胰岛素信号传导通路相关蛋白表达[51]卵形鲳鲹研究LBP对卵形鲳鲹生长性能、抗氧化能力及血清免疫、生化指标的影响分别饲喂枸杞多糖相对含量为0(对照)、0.05%、0.10%、0.20%、0.40%和0.80%的6 种饲料提高卵形鲳鲹的抗氧化能力和免疫力 [52]
1.3 降血糖、降血脂活性
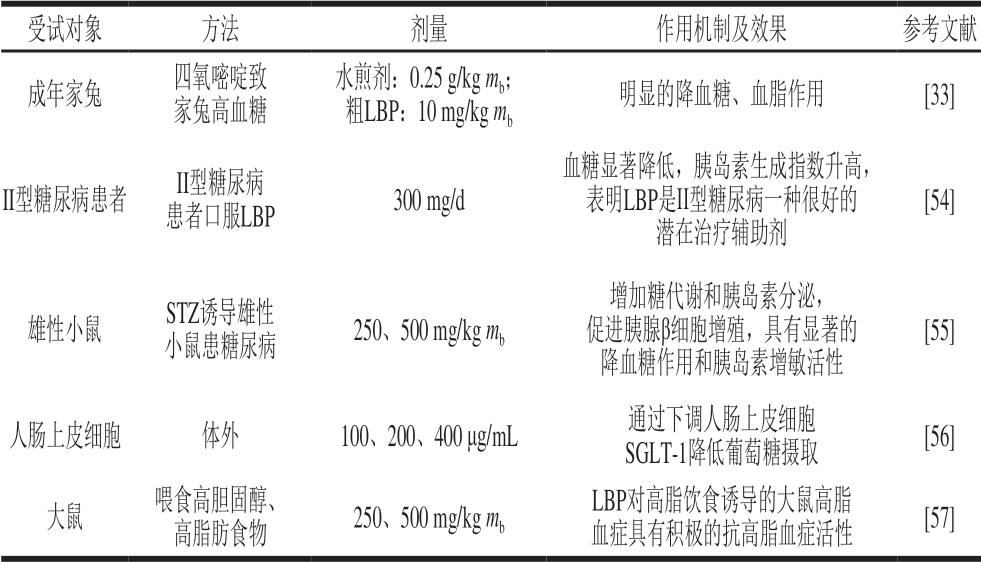
随着我国居民生活水平的提高及老龄化社会的步入,慢性非传染性疾病患病率迅速上升,高血压、糖尿病、肥胖、血脂异常等疾病患者表现出明显的上升趋势,“三高症”人群也呈现出较大幅度的增加[53]。近年来,此类疾病的中药治疗在国内外备受关注。研究表明,枸杞多糖对于降血糖、治疗糖尿病在药理实验、临床实验中均具有较好的生物活性。因此,枸杞多糖降血糖、降血脂、治疗糖尿病方面的作用机制及效果(表3)研究对于治疗人类糖尿病或辅助治疗糖尿病将具有巨大潜力。
表 3 枸杞多糖降血糖、降血脂、治疗糖尿病的作用机制及效果
Table 3 Recent studies on hypoglycemic and hypolipidemic effects and mechanism of action of LBP
注:STZ.链脲佐菌素(streptozotocin);SGLTs.钠依赖性葡萄糖协同转运蛋白(sodium-glucose cotransporters)。
受试对象 方法 剂量 作用机制及效果 参考文献成年家兔 四氧嘧啶致家兔高血糖水煎剂:0.25 g/kg mb;粗LBP:10 mg/kg mb明显的降血糖、血脂作用 [33]II型糖尿病患者 II型糖尿病患者口服LBP 300 mg/d雄性小鼠 STZ诱导雄性小鼠患糖尿病 250、500 mg/kg mb血糖显著降低,胰岛素生成指数升高,表明LBP是II型糖尿病一种很好的潜在治疗辅助剂增加糖代谢和胰岛素分泌,促进胰腺β细胞增殖,具有显著的降血糖作用和胰岛素增敏活性[54][55]人肠上皮细胞 体外 100、200、400 μg/mL 通过下调人肠上皮细胞SGLT-1降低葡萄糖摄取 [56]大鼠 喂食高胆固醇、高脂肪食物 250、500 mg/kg mb LBP对高脂饮食诱导的大鼠高脂血症具有积极的抗高脂血症活性 [57]
1.4 神经保护活性
枸杞多糖具有神经保护作用。研究表明,枸杞多糖可预防东莨菪碱(scopolamine,SCO)诱导的大鼠学习记忆障碍;保护谷氨酸诱导的PC12细胞凋亡、预防同型半胱氨酸(homocysteine,Hcy)诱导的神经元损伤、保护缺糖/缺氧再灌注(oxygen glucose deprivation/reperfusion,OGD/R)诱导的细胞凋亡和自噬性细胞死亡、保护谷氨酸培养的皮层神经元、预防慢性间歇性缺氧(chronic intermittent hypoxia,CIH)诱导大鼠的空间记忆缺陷、预防糖尿病性周围神经病变、抑制大鼠放射性脑损伤海马神经元的凋亡、保护PD小鼠黑质致密部多巴胺(dopamine,DA)能神经元及癫痫的大鼠神经元等;促进小鼠坐骨神经损伤的恢复;改善转基因小鼠的淀粉样蛋白病理和认知功能、高血糖加重的缺血性脑损伤等。枸杞多糖极有可能成为治疗或干预阿尔茨海默症(Alzheimer’s disease,AD)、脑缺血、癫痫等神经系统疾病方面的天然药物制剂。枸杞多糖对神经保护的作用机制及效果见表4。
表 4 枸杞多糖对神经保护的作用机制及效果
Table 4 Recent studies on neuroprotective effect and mechanism of action of LBP

注:mTOR.雷帕霉素靶蛋白(mammalian target of rapamycin)。
受试对象 方法 剂量 作用机制及效果 参考文献雄性大鼠 SCOs诱导大鼠学习记忆障碍 0.2、1 mg/kg mb可预防SCOs诱导的认知和记忆缺陷以及细胞增殖和神经母细胞分化的减少 [58]DPC12细胞谷氨酸诱导DPC12细胞凋亡 10、30 μg/mL 调节Akt和ERKs途径,抑制线粒体凋亡 [59]大鼠皮层神经元Hcy诱导神经元损伤 10、250 μg/mL LBP对暴露于Hcy的皮层神经元具有神经保护作用 [60]C57BL/6海马神经元OGD/R诱导细胞凋亡和自噬性细胞死亡15、30、60 μg/mL 激活PI3K/Akt/mTOR信号通路 [61]大鼠皮层神经元谷氨酸诱导细胞凋亡 10~500 μg/mL LBP对暴露于谷氨酸培养的皮层神经元有显著的神经保护作用 [62]大鼠 糖尿病和大脑中动脉闭塞模型 25 mg/kg mb LBP预处理通过维持线粒体动力学平衡改善高血糖加重的缺血性脑损伤 [63]大鼠 CIH诱导大鼠的空间记忆缺陷 1 mg/kg mb促进海马神经发生和负调控氧化应激、炎症激活的凋亡信号级联 [64]转基因小鼠 神经损伤模型 50 mg/kg mb LBP可能是针对AD的多个靶点(包括突触可塑性、Aβ病理学和神经病理学)治疗的潜在治疗剂 [65]大鼠 糖尿病性周围神经病变模型 500 mg/kg mb 抑制mTOR/p70S6K通路的激活 [66]小鼠 建立坐骨神经损伤模型 -LBP具有双向调节的作用,当坐骨神经损伤,小鼠机体免疫反应异常增强时,它可适当调节并降低机体的免疫反应,促进受损神经组织细胞的功能恢复[67]大鼠海马神经元大鼠放射性脑损伤海马神经元 50 mg/kg mb抑制放射性脑损伤海马神经元的凋亡,具备神经保护作用 [68]大鼠 大鼠癫痫模型 50 mg/kg mb LBP对癫痫模型大鼠进行干预后,大鼠海马齿状回颗粒层Brd U阳性细胞数、MAP-2和NeuN阳性神经元细胞表达均出现一定程度改善,具有较好的神经保护作用[69]小鼠采用1-甲基-4-苯基-1,2,3,6-四氢吡啶制备PD小鼠模型50、100 mg/kg mb减轻PD小鼠中脑氧化应激损伤,对黑质致密部DA能神经元起保护作用[70]
1.5 抗炎活性
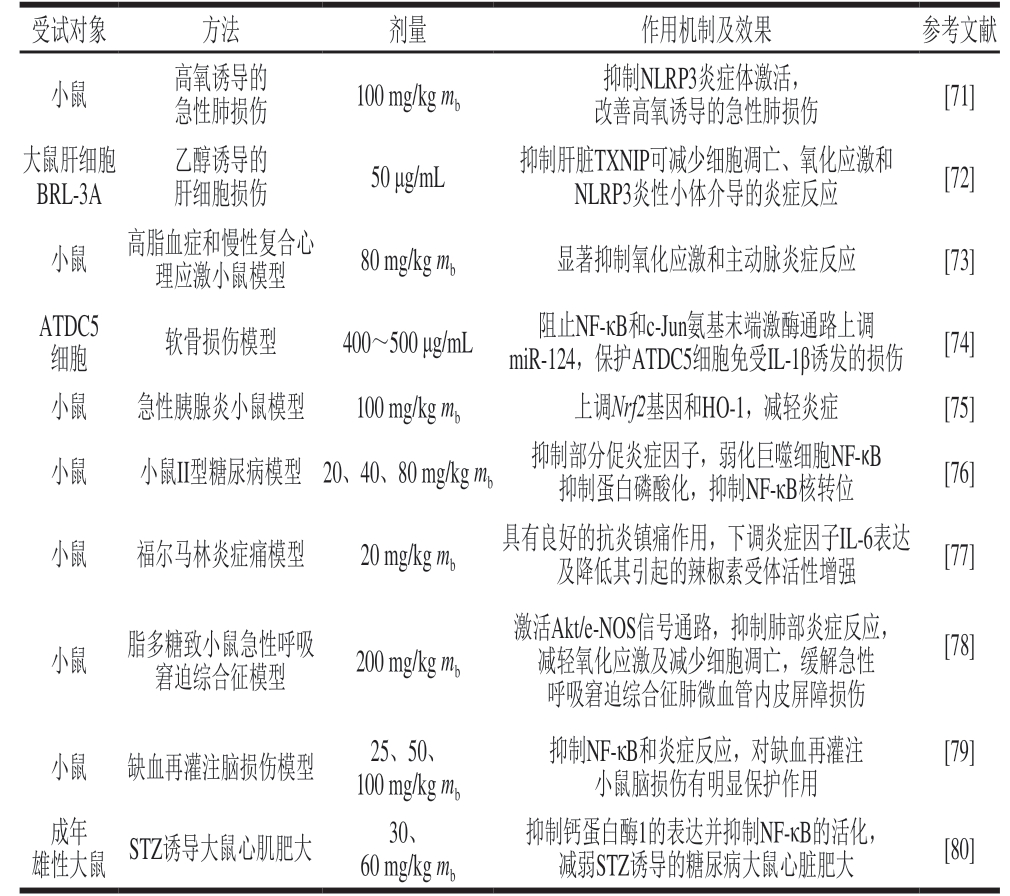
枸杞多糖具有良好的抗炎活性,其能减轻高氧诱导的急性肺损伤、乙醇诱导的肝细胞损伤、软骨损伤、小鼠急性胰腺炎等。枸杞多糖抗炎作用的主要机制有抑制炎症反应转录因子κB(nuclear factor-kappa B,NF-κB)活化、抑制NOD样受体热蛋白结构域相关蛋白3(NOD-like receptor thermal protein domain associated protein 3,NLRP3)炎症体等途径。虽已有研究表明枸杞多糖具有良好的抗炎活性,但其抗炎作用研究主要还集中在药理实验中,对于临床应用的研究较少且作用机制尚未明确,因此有待进一步对枸杞多糖抗炎作用进行研究,以充分发挥其良好的抗炎活性。枸杞多糖抗炎的作用机制及效果见表5。
表 5 枸杞多糖抗炎活性的作用机制及效果
Table 5 Recent studies on anti-inflammatory activity and mechanism of action of LBP
注:TXNIP.硫氧还蛋白互作蛋白(thioredoxin interacting protein)。
受试对象 方法 剂量 作用机制及效果 参考文献小鼠 高氧诱导的急性肺损伤 100 mg/kg mb抑制NLRP3炎症体激活,改善高氧诱导的急性肺损伤 [71]大鼠肝细胞BRL-3A 肝细胞损伤 50 μg/mL 抑制肝脏TXNIP可减少细胞凋亡、氧化应激和NLRP3炎性小体介导的炎症反应 [72]乙醇诱导的小鼠 高脂血症和慢性复合心理应激小鼠模型 80 mg/kg mb 显著抑制氧化应激和主动脉炎症反应 [73]ATDC5细胞 软骨损伤模型 400~500 μg/mL 阻止NF-κB和c-Jun氨基末端激酶通路上调miR-124,保护ATDC5细胞免受IL-1β诱发的损伤 [74]小鼠 急性胰腺炎小鼠模型 100 mg/kg mb 上调Nrf2基因和HO-1,减轻炎症 [75]小鼠 小鼠II型糖尿病模型 20、40、80 mg/kg mb抑制部分促炎症因子,弱化巨噬细胞NF-κB抑制蛋白磷酸化,抑制NF-κB核转位 [76]小鼠 福尔马林炎症痛模型 20 mg/kg mb具有良好的抗炎镇痛作用,下调炎症因子IL-6表达及降低其引起的辣椒素受体活性增强 [77]小鼠 脂多糖致小鼠急性呼吸窘迫综合征模型 200 mg/kg mb激活Akt/e-NOS信号通路,抑制肺部炎症反应,减轻氧化应激及减少细胞凋亡,缓解急性呼吸窘迫综合征肺微血管内皮屏障损伤[78]小鼠 缺血再灌注脑损伤模型 25、50、100 mg/kg mb抑制NF-κB和炎症反应,对缺血再灌注小鼠脑损伤有明显保护作用[79]雄性大鼠 STZ诱导大鼠心肌肥大 30、60 mg/kg mb成年抑制钙蛋白酶1的表达并抑制NF-κB的活化,减弱STZ诱导的糖尿病大鼠心脏肥大 [80]
1.6 生殖保护活性
表 6 枸杞多糖的生殖保护作用机制及效果
Table 6 Recent studies on reproductive system-protecting effect and mechanism of action of LBP

受试对象 方法 剂量 作用机制及效果 参考文献雄性小鼠 STZ诱导雄性小鼠患I型糖尿病10、20、40 mg/kg mb提高抗氧化酶活性和抑制细胞凋亡,调节糖尿病诱导的男性生精功能障碍 [81]雄性小鼠 STZ诱导雄性小鼠患I型糖尿病 40 mg/kg mb 抑制PI3K/Akt通路介导的睾丸过度自噬 [82]雄性大鼠及小鼠43 ℃热暴露诱导的大鼠睾丸损伤、H2O2诱导的小鼠睾丸细胞脱氧核糖核酸损伤50、100、200、400 μg/mL缩短阴茎勃起潜伏期,调节性激素分泌和提高激素水平,提高精子数量和质量 [83]小鼠MLTC-1细胞DDP诱导的MLTC-1细胞凋亡和自噬0、25、50、100 g/mL调节内质网应激途径,防止DDP诱导的MLTC-1细胞凋亡和自噬 [84]雄性小鼠 STZ对I型糖尿病雄性小鼠性行为和睾丸组织学变化10、20、40 mg/kg mb调节下丘脑-垂体-性腺轴内分泌活性,发挥雄性功能障碍的功能恢复 [85]雄性大鼠60Co γ射线辐照损伤雄性大鼠生殖系统和生精细胞 10 mg/kg mb上调Bcl-2的表达、下调Bax的表达,防止线粒体膜电位下降,显著降低生精细胞凋亡 [86]雄性大鼠 DOX诱导的睾丸毒性 200 mg/kg mb减弱DOX引起的曲细精管严重退行性改变、提高大鼠睾丸氧化应激和保护睾丸特异性毒性的能力[87]雄性大鼠 腺嘌呤诱导肾阳虚不育大鼠模型 10 mg/kg mb提高精子的数量、活动度及肾阳虚大鼠性激素水平 [88]雄性大鼠 大鼠海绵体神经损伤模型 10 mg/kg mb 促进损伤后的神经再生及勃起功能的恢复 [89]
糖尿病会引起一系列男性生殖功能障碍并发症,如睾丸功能障碍、生精功能障碍等。研究表明,枸杞多糖对STZ诱导雄性小鼠患I型糖尿病的生精功能障碍、睾丸功能障碍有显著的保护作用。此外,一定量的枸杞多糖对热暴露诱导的大鼠睾丸损伤、H2O2诱导的小鼠睾丸细胞脱氧核糖核酸损伤、辐射引起的雄性大鼠生殖系统和生精细胞损伤、化学物质诱导的生殖损伤等都具有一定的保护和功能恢复作用。枸杞多糖对生殖功能的保护作用机制可能与增强抗氧化酶活性、抑制细胞死亡、抑制PI3K/Akt信号通路、调节下丘脑-垂体-性腺轴内分泌活性、上调Bcl-2表达、下调Bax表达等途径有关。枸杞多糖的生殖保护作用机制及效果见表6。
1.7 保肝活性
早在明代《本草纲目》中就有记载,枸杞可滋养肝脏、改善视力。现代研究也证明枸杞子中的枸杞多糖具有保肝特性。枸杞多糖保肝的作用机制包括抑制NLRP3/6炎性体途径和NF-κB的活化、抑制细胞凋亡、抑制氧化应激反应、下调NF-κB活性、抑制Toll样受体(Toll-like receptor,TLRs)4/NF-κB信号通路、下调炎性因子TNF-α及IL-1β的水平。枸杞多糖是具有保肝特性的天然化合物,可充分利用其特性开发具有保肝特性的功能保健食品、临床中治疗肝损伤的治疗剂等。枸杞多糖保肝特性的作用机制及效果见表7。
表 7 枸杞多糖的保肝特性作用机制及效果
Table 7 Recent studies on hepatoprotective effect and mechanism of action of LBP

受试对象 方法 剂量 作用机制及效果 参考文献大鼠 高脂饮食诱导的非酒精性脂肪性肝炎大鼠模型 1 mg/kg mb具有多种保肝特性,可能在未来的临床实验中成为针对非酒精性脂肪性肝炎有效的补充治疗剂[90]小鼠 非酒精性脂肪性肝炎蛋氨酸-胆碱缺乏症诱导小鼠肝损伤 1 mg/kg mb LBP抑制NLRP3/6炎性体途径和NF-κB活化 [91]大鼠肝细胞系BRL-3A 乙醇诱导的肝细胞损伤 50 μg/mL 对肝TXNIP抑制,减少细胞凋亡、氧化应激和NLRP3炎性体介导的炎症 [92]小鼠 CCl4诱导的急性肝损伤 1、10 mg/kg mb有效减少化学毒素引起的坏死性炎症和氧化应激 [93]大鼠 CCl4诱导的肝纤维化 400、800、1 600 mg/kg mb抑制TLRs/NF-κB信号通路的表达,缓解大鼠肝纤维化 [94]大鼠 体积分数56%乙醇诱导慢性酒精性肝损伤ZnSO4+LBP低剂量组250 mg/kg mb;ZnSO4+LBP高剂量组500 mg/kg mb LBP和锌化合物联合可用于酒精性肝病的治疗 [95]小鼠 结扎小鼠胆总管后制备肝纤维化模型 30 μg/g mb抑制炎性因子TNF-α及IL-1β的水平,保护肝组织 [96]
1.8 护眼活性
糖尿病视网膜病变是糖尿病最常见的并发症之一,也是全世界视力丧失的主要原因之一。目前糖尿病性视网膜病的临床治疗仅限于激光光凝和玻璃体切除术[97],因此,针对糖尿病视网膜病变的创新治疗方法对于临床研究十分迫切。研究表明,枸杞多糖可用于治疗糖尿病视网膜病变,其机制可能是:1)通过调节糖尿病大鼠阻断Ras同源基因/Rock相关卷曲螺旋蛋白激酶(Rho/Rho associated coiled-coil forming protein kinase,Rho/ROCK)信号通路;2)改善糖尿病大鼠视网膜氧化应激,发挥有益的神经保护作用,激活Nrf2/HO-1抗氧化通路;3)上调视网膜Bcl-2 mRNA和蛋白表达水平,下调视网膜Caspase-3、Bax mRNA和蛋白表达水平,减少视网膜神经节细胞凋亡,从而保护视网膜。此外,枸杞多糖对缺血性视网膜病变、急性高眼压症、慢性高眼压症、局部视神经横断也具有显著的保护和恢复作用,因此,枸杞多糖可能成为治疗糖尿病引起视网膜病变的治疗剂、缺血性视网膜病变的神经保护剂、血管相关视网膜病变的潜在治疗手段。枸杞多糖护眼的研究作用机制及效果见表8。
表 8 枸杞多糖护眼的研究作用机制及效果
Table 8 Recent studies on eye-protecting effect and mechanism of action of LBP
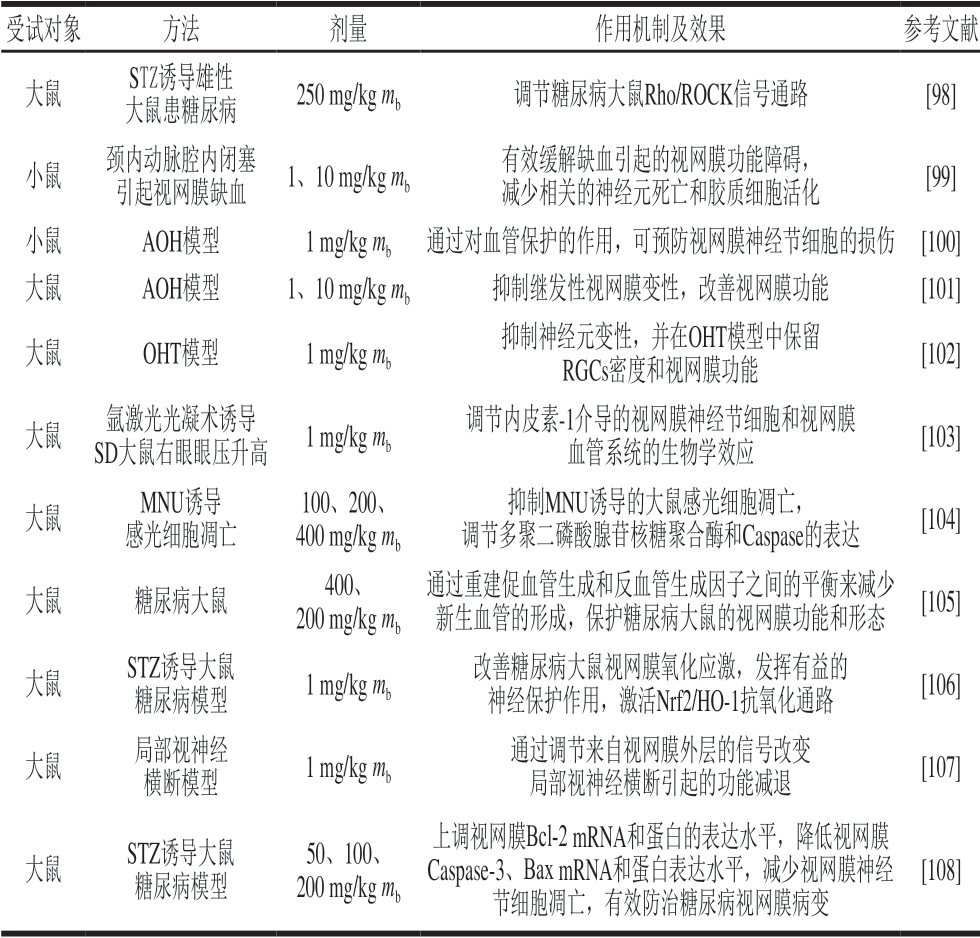
注:AOH.急性高眼压症(acute ocular hypertension);OHT.高眼压症(ocular hypertension);MNU. N-甲基-N-亚硝基脲(N-methyl-Nnitrosourea);RGCs.视网膜神经节细胞(retinal ganglion cells)。
受试对象 方法 剂量 作用机制及效果 参考文献大鼠 STZ诱导雄性大鼠患糖尿病 250 mg/kg mb 调节糖尿病大鼠Rho/ROCK信号通路 [98]小鼠 颈内动脉腔内闭塞引起视网膜缺血 1、10 mg/kg mb有效缓解缺血引起的视网膜功能障碍,减少相关的神经元死亡和胶质细胞活化 [99]小鼠 AOH模型 1 mg/kg mb 通过对血管保护的作用,可预防视网膜神经节细胞的损伤 [100]大鼠 AOH模型 1、10 mg/kg mb 抑制继发性视网膜变性,改善视网膜功能 [101]大鼠 OHT模型 1 mg/kg mb抑制神经元变性,并在OHT模型中保留RGCs密度和视网膜功能 [102]大鼠 氩激光光凝术诱导SD大鼠右眼眼压升高 1 mg/kg mb调节内皮素-1介导的视网膜神经节细胞和视网膜血管系统的生物学效应 [103]大鼠 MNU诱导感光细胞凋亡100、200、400 mg/kg mb抑制MNU诱导的大鼠感光细胞凋亡,调节多聚二磷酸腺苷核糖聚合酶和Caspase的表达 [104]大鼠 糖尿病大鼠 400、200 mg/kg mb通过重建促血管生成和反血管生成因子之间的平衡来减少新生血管的形成,保护糖尿病大鼠的视网膜功能和形态 [105]大鼠 STZ诱导大鼠糖尿病模型 1 mg/kg mb改善糖尿病大鼠视网膜氧化应激,发挥有益的神经保护作用,激活Nrf2/HO-1抗氧化通路 [106]大鼠 局部视神经横断模型 1 mg/kg mb通过调节来自视网膜外层的信号改变局部视神经横断引起的功能减退 [107]大鼠 STZ诱导大鼠糖尿病模型50、100、200 mg/kg mb上调视网膜Bcl-2 mRNA和蛋白的表达水平,降低视网膜Caspase-3、Bax mRNA和蛋白表达水平,减少视网膜神经节细胞凋亡,有效防治糖尿病视网膜病变[108]
1.9 其他活性
枸杞多糖除了具有抗肿瘤、抗氧化衰老、抗炎症、降低血糖血脂、神经保护、生殖保护、保肝护眼等功效外,还具有免疫调节、保护骨髓、改善肝/脑损伤和运动能力受损、保护肾脏、提高弱精症患者精子存活率及质量、改善过敏性哮喘、改善抑郁行为等作用(表9)。当枸杞多糖与美沙拉嗪联合使用时,其能够抑制葡聚糖硫酸酯钠盐(dextran sulfate sodium salt,DSS)诱导的慢性实验性结肠炎小鼠模型的肠道病变[109]。最新研究发现,枸杞多糖是良好的益生元来源,可以增加肠道菌群丰度、提高有益细菌水平、调节先天免疫应答,且有研究人员将枸杞多糖加入到小猪的饲料中,发现饲料中补充枸杞多糖可以提高断奶仔猪的生长性能,免疫状态和抗氧化能力,改善其肠道微生物种群[110]。
表 9 枸杞多糖其他的生物活性及其药理作用机制及效果
Table 9 Recent studies on other biological activities and mechanism of action of LBP
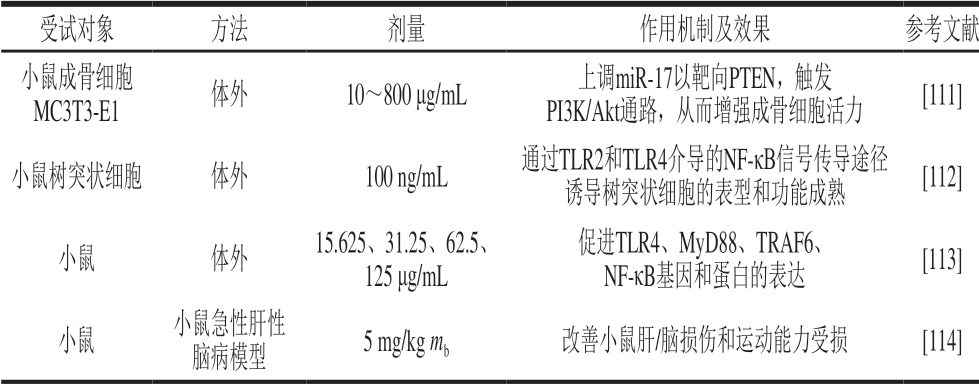
受试对象 方法 剂量 作用机制及效果 参考文献小鼠成骨细胞MC3T3-E1 体外 10~800 μg/mL 上调miR-17以靶向PTEN,触发PI3K/Akt通路,从而增强成骨细胞活力 [111]小鼠树突状细胞 体外 100 ng/mL 通过TLR2和TLR4介导的NF-κB信号传导途径诱导树突状细胞的表型和功能成熟 [112]小鼠 体外 15.625、31.25、62.5、125 μg/mL促进TLR4、MyD88、TRAF6、NF-κB基因和蛋白的表达 [113]小鼠 小鼠急性肝性脑病模型 5 mg/kg mb 改善小鼠肝/脑损伤和运动能力受损 [114]
续表9
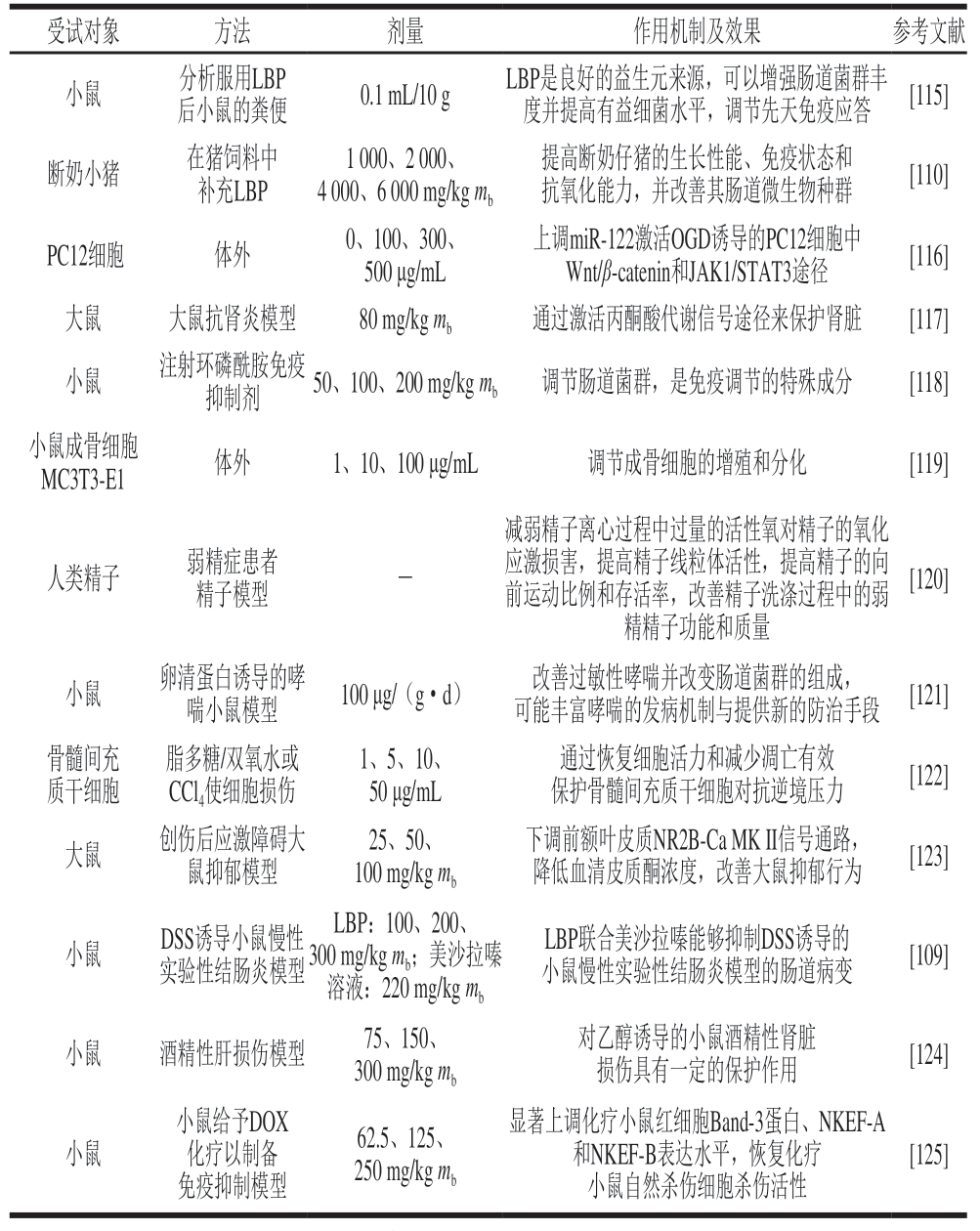
注:PTEN.磷酸酯酶与张力蛋白同源物(phosphatase and tensin homolog);JAK1/STAT3.蛋白酪氨酸激酶1/信号转导和转录活化因子3(Janus kinase 1/signal transducer and activator of transcription 3);NKEF.自然杀伤细胞增强因子(natural killer enhancing factor)。
受试对象 方法 剂量 作用机制及效果 参考文献小鼠 分析服用LBP后小鼠的粪便 0.1 mL/10 g LBP是良好的益生元来源,可以增强肠道菌群丰度并提高有益细菌水平,调节先天免疫应答 [115]断奶小猪 在猪饲料中补充LBP 1 000、2 000、4 000、6 000 mg/kg mb提高断奶仔猪的生长性能、免疫状态和抗氧化能力,并改善其肠道微生物种群 [110]PC12细胞 体外 0、100、300、500 μg/mL上调miR-122激活OGD诱导的PC12细胞中Wnt/β-catenin和JAK1/STAT3途径 [116]大鼠 大鼠抗肾炎模型 80 mg/kg mb 通过激活丙酮酸代谢信号途径来保护肾脏 [117]小鼠 注射环磷酰胺免疫抑制剂 50、100、200 mg/kg mb 调节肠道菌群,是免疫调节的特殊成分 [118]小鼠成骨细胞MC3T3-E1 体外 1、10、100 μg/mL 调节成骨细胞的增殖和分化 [119]人类精子 弱精症患者精子模型 -减弱精子离心过程中过量的活性氧对精子的氧化应激损害,提高精子线粒体活性,提高精子的向前运动比例和存活率,改善精子洗涤过程中的弱精精子功能和质量[120]小鼠 卵清蛋白诱导的哮喘小鼠模型 100 μg/(g·d) 改善过敏性哮喘并改变肠道菌群的组成,可能丰富哮喘的发病机制与提供新的防治手段 [121]骨髓间充质干细胞脂多糖/双氧水或CCl4使细胞损伤1、5、10、50 μg/mL通过恢复细胞活力和减少凋亡有效保护骨髓间充质干细胞对抗逆境压力 [122]大鼠 创伤后应激障碍大鼠抑郁模型25、50、100 mg/kg mb下调前额叶皮质NR2B-Ca MK II信号通路,降低血清皮质酮浓度,改善大鼠抑郁行为 [123]小鼠 DSS诱导小鼠慢性实验性结肠炎模型LBP:100、200、300 mg/kg mb;美沙拉嗪溶液:220 mg/kg mb LBP联合美沙拉嗪能够抑制DSS诱导的小鼠慢性实验性结肠炎模型的肠道病变 [109]小鼠 酒精性肝损伤模型 75、150、300 mg/kg mb对乙醇诱导的小鼠酒精性肾脏损伤具有一定的保护作用 [124]小鼠小鼠给予DOX化疗以制备免疫抑制模型62.5、125、250 mg/kg mb显著上调化疗小鼠红细胞Band-3蛋白、NKEF-A和NKEF-B表达水平,恢复化疗小鼠自然杀伤细胞杀伤活性[125]
2 枸杞多糖构效关系
枸杞多糖生物活性与其分子形状、相对分子质量及分子组成有关,且化学修饰改变枸杞多糖分子的结构可影响枸杞多糖生物活性,因此,探究其构效关系对枸杞多糖的深入研究与开发具有重要意义。
2.1 枸杞多糖分子形状、分子质量与其活性的关系
Zhang Min等[126]对5 个组分的枸杞多糖进行研究发现,具有紧密球形分子结构且分子质量较小的LBP-a4更有利于其发挥抗肝癌活性,而由松散絮状结构组成且分子质量较大的LBP-a8则不呈现此活性。Zhang Min等[127]的研究发现,通过将分子质量较大的枸杞多糖超微粉碎降解为小分子LBP-S后,枸杞多糖的抗氧化活性得到了显著提升。Gong Guiping等[128]对5 个组分的枸杞多糖研究发现,分子质量较小的多糖组分更能呈现较强的抗氧化活性,而对于免疫活性来说,分子质量在10~1 000 kDa范围内的多糖组分能呈现更强的免疫活性。
2.2 枸杞多糖分子组成与其活性的关系
Zhang Qian等[129]的研究发现,分子组成成分中含有更高蛋白质、醛酸和半乳糖含量的枸杞多糖诱导癌细胞凋亡的能力更强。Yao Ruyu等[130]研究发现,分子结构中含有较短阿拉伯半乳糖链的枸杞多糖组分抗氧化活性更强。钱怡霖等[131]研究发现,经初级纯化后的枸杞多糖分子内常含有Al、Ca、Mn等多种金属元素,金属元素的存在是枸杞多糖呈现良好抗氧化活性及抗人乳腺癌细胞活性的因素之一。
2.3 化学修饰改变枸杞多糖分子结构可影响其生物活性的发挥
孙玉姣[132]和王君敏[133-134]等的研究发现,硫酸化后的枸杞多糖具有更强的免疫调节活性、抗病毒活性、抗肿瘤活性,活性强弱与其硫酸基取代度在一定浓度范围内呈正比。彭天元等[135]的研究发现,乙酰化后的枸杞多糖具有更强的抗氧化活性及抗肿瘤活性,活性强弱与分子空间排布有关。Qiu Shulei等[136]的研究发现,硒化改性枸杞多糖能显著提高其抗氧化活性。
3 结 语
枸杞多糖因具有多种生物活性(如抗肿瘤、抗氧化、抗衰老及免疫调节等)及安全、高效、低毒等优势受到广大科研人员的关注。但目前枸杞多糖的临床应用还主要集中在抗衰老活性、保肝特性及辅助治疗糖尿病和肝癌方面,相对于枸杞多糖诸多的生物活性来说,其还具有广泛的应用前景和开发价值。尽管枸杞多糖在生物活性、机制及构效关系上的研究取得了一定的进展,但由于多糖结构的复杂性、不规律性及分子质量的分散性等特点,增大了枸杞多糖高级结构鉴定的难度,使得枸杞多糖分子结构与其生物活性之间的关系仍不明确,严重阻碍了对枸杞多糖的深入研究,这也是目前枸杞多糖研究大多数只停留在药理实验中而缺乏广泛临床应用的主要原因之一;此外,缺乏分子水平的深入研究,枸杞多糖发挥其生物活性的作用机制是多途径、多靶点、多效应的,目前虽已有大量文献报道其生物活性及作用机制,但针对枸杞多糖作用于某一具体生物活性机制的深入研究较少,且报道的作用机制单一。
综上,对于枸杞多糖的研究还可从以下几点出发:1)在传统技术的基础上创新、完善分析方法,明确枸杞多糖高级分子结构,深入探究其与生物活性间的关系,从分子水平上进行深入研究。2)从分子结构及作用机制上寻找枸杞多糖与其生物活性之间的规律性,探究枸杞多糖新型活性,这是科技发展的趋势。3)根据目前少量研究报道,枸杞多糖与其他药物联用会明显增强药物疗效如抗肿瘤疗效、保肝疗效等;因此,探究枸杞多糖与其他药物协同作用的机制,为最大限度发挥枸杞多糖生物活性指明了新的方向。4)随着大健康产业的发展,并在枸杞多糖药食同源的基础上开发功能食品、保健品等将是枸杞多糖日后发展的趋势。5)进一步完善和深入枸杞多糖添加于畜禽饲料中的研究,制定出各畜禽类饲料最优添加剂量、优化应用成本方案等,从而更好地提高畜禽生产水平以及促使畜禽业实现绿色可持续发展。总而言之,枸杞多糖的研究目前仍处于发展阶段,仍需广大研究人员的共同努力。
[1] 中国科学院中国植物志编辑委员会. 中国植物志: 第67卷[M]. 北京:科学出版社, 1978: 15.
[2] 李静, 余意, 张小波, 等. 药用枸杞本草考证[J]. 世界中医药, 2019,14(10): 2593-2597. DOI:10.3969/j.issn.1673-7202.2019.10.011.
[3] 国家药典委员会. 中华人民共和国药典: 2015年版一部[M]. 北京:中国医药科技出版社, 2015: 249.
[4] 朱彩平. 枸杞多糖的结构分析及生物活性评价[D]. 武汉: 华中农业大学, 2006: 21-27. DOI:10.7666/d.Y1005067.
[5] 曹毛毛, 陈万青. 中国恶性肿瘤流行情况及防控现状[J].中国肿瘤临床, 2019,46(3): 145-149. DOI:10.396 9/j.issn.1000-8179.2019.03.283.
[6] 佚名. 数据“说”癌[J]. 实用心脑肺血管病杂志, 2019, 27(2): 6.
[7] 邹小农, 赵平. 中国癌症态势七十年分析[J]. 中国肿瘤临床与康复,2019, 26(10): 1153-1161. DOI:10.13455/j.cnki.cjcor.2019.10.01.
[8] ZHANG M, CHEN H X, HUANG J, et al. Effect of Lycium barbarum polysaccharide on human hepatoma QGY7703 cells: inhibition of proliferation and induction of apoptosis[J]. Life Sciences, 2005,76(18): 2115-2124. DOI:10.1016/j.lfs.2004.11.009.
[9] LOU L, CHEN G, ZHONG B. Lycium barbarum polysaccharide induced apoptosis and inhibited proliferation in infantile hemangioma endothelial cells via down-regulation of PI3K/Akt signaling pathway[J]. Bioscience Reports, 2019, 39(8): 1-11. DOI:10.1042/BSR20191182.
[10] SHEN L L, DU G. Lycium barbarum polysaccharide stimulates proliferation of MCF-7 cells by the ERK pathway[J]. Life Sciences,2012, 91(9/10): 353-357. DOI:10.1016/j.lfs.2012.08.012.
[11] MAO F, XIAO B X, JIANG Z, et al. Anticancer effect of Lycium barbarum polysaccharides on colon cancer cells involves G0/G1 phase arrest[J]. Medical Oncology, 2011, 28(1): 121-126. DOI:10.1007/s12032-009-9415-5.
[12] MIAO Y, XIAO B X, JIANG Z, et al. Growth inhibition and cell-cycle arrest of human gastric cancer cells by Lycium barbarum polysaccharide[J]. Medical Oncology, 2010, 27(3): 785-790.DOI:10.1007/s12032-009-9286-9.
[13] ZHU C P, ZHANG S H. Lycium barbarum polysaccharide inhibits the proliferation of HeLa cells by inducing apoptosis[J]. Journal of the Science of Food and Agriculture, 2013, 93(1): 149-156. DOI:10.1002/jsfa.5743.
[14] WANG W, LIU M X, WANG Y, et al. Lycium barbarum polysaccharide promotes maturation of dendritic cell via notch signaling and strengthens dendritic cell mediated T lymphocyte cytotoxicity on colon cancer cell CT26-WT[J]. Evidence-based Complementary Alternative Medicine, 2018, 2018: 2305683.DOI:10.1155/2018/2305683.
[15] 韩永红, 刘兴祥. 枸杞多糖促进大鼠肝癌组织细胞的凋亡[J].现代食品科技, 2020, 36(2): 7-11.DOI:10.1398 2/j.mfst.1673-9078.2020.2.002.
[16] 韩何丹, 杜月梅, 刘云帆, 等. 枸杞多糖联合顺铂对人肺腺癌细胞A549氧化损伤及凋亡的影响[J]. 食品科学, 2020, 41(15): 194-200.DOI:10.7506/spkx1002-6630-20190714-185.
[17] 张多强, 辛国军. 枸杞多糖抑制SMMC-7721肝癌细胞的VEGF表达、迁移与侵袭[J]. 中国组织化学与细胞化学杂志, 2019, 28(1):26-31. DOI:10.16705/j.cnki.1004-1850.2019.01.005.
[18] 陈诚, 马钰, 李义德, 等. 枸杞多糖单独或联合TRAIL对MLL基因重排急性淋巴细胞白血病细胞凋亡的影响[J]. 中国实验血液学杂志, 2019, 27(4): 1104-1110. DOI:10.19746/j.cnki.issn1009-2137.2019.04.018.
[19] 张多强, 辛国军, 丁洋, 等. 枸杞多糖对HepG2肝癌细胞自噬与细胞凋亡的影响[J]. 中成药, 2017, 39(12): 2600-2602. DOI:10.3969/j.issn.1001-1528.2017.12.035.
[20] 王军成, 邹有瑞, 李怡, 等. 枸杞多糖通过调节血脑屏障抑制大鼠胶质瘤的生长[J]. 肿瘤, 2018, 38(2): 102-110; 151. DOI:10.3781/j.issn.1000-7431.2018.11.753.
[21] 黄汀, 卢军, 张显军, 等. 枸杞多糖对膀胱癌细胞的增殖及凋亡作用研究[J]. 中国临床药理学杂志, 2018, 34(12): 1447-1449.DOI:10.13699/j.cnki.1001-6821.2018.12.015.
[22] 姜鸣, 李卓能. 枸杞多糖诱导自噬抑制人舌鳞状癌细胞增殖[J].临床口腔医学杂志, 2017, 33(11): 656-659. DOI:10.3969/j.issn.1003-1634.2017.11.006.
[23] 单铁强, 单铁英, 董静, 等. 枸杞多糖对脑胶质瘤病人免疫调节作用及预后的影响[J]. 中西医结合心脑血管病杂志, 2017, 15(20): 2632-2634. DOI:10.3969/j.issn.1672-1349.2017.20.040.
[24] 郭华, 张旭, 董辉, 等. 枸杞多糖联合紫杉醇对人上皮性卵巢癌HO-8910PM细胞增殖及凋亡的影响[J]. 宁夏医科大学学报, 2017,39(6): 631-635; 737. DOI:10.16050/j.cnki.issn1674-6309.2017.06.005.
[25] GAO C, HAN H B, TIAN X Z, et al. Melatonin promotes embryonic development and reduces reactive oxygen species in vitrified mouse 2-cell embryos[J]. Journal of Pineal Research, 2012, 52(3): 305-311.DOI:10.1111/j.1600-079X.2011.00944.x.
[26] AHN H J, SOHN I P, KWON H C, et al. Characteristics of the cell membrane fluidity, actin fibers, and mitochondrial dysfunctions of frozen-thawed two-cell mouse embryos[J]. Molecular Reproduction and Development, 2002, 61(4): 466-476. DOI:10.1002/mrd.10040.
[27] TANG T, HE B X. Treatment of D-galactose induced mouse aging with Lycium barbarum polysaccharides and its mechanism study[J].African Journal of Traditional, Complementary and Alternative Medicines, 2013, 10(4): 12-17. DOI:10.4314/ajtcam.v10i4.3.
[28] XIA G Q, XIN N, LIU W, et al. Inhibitory effect of Lycium barbarum polysaccharides on cell apoptosis and senescence is potentially mediated by the p53 signaling pathway[J]. Molecular Medicine Reports, 2014, 9(4): 1237-1241. DOI:10.3892/mmr.2014.1964.
[29] TANG R, CHEN X Y, DANG T T, et al. Lycium barbarum polysaccharides extend the mean lifespan of Drosophila melanogaster[J]. Food & Function, 2019, 10(7): 4231-4241.DOI:10.1039/c8fo01751d.
[30] ZHANG Z Q, ZHOU Y N, FAN H T, et al. Effects of Lycium barbarum polysaccharides on health and aging of C. elegans depend on daf-12/daf-16[J]. Oxidative Medicine and Cellular Longevity, 2019,2019: 6379493. DOI:10.1155/2019/6379493.
[31] YANG L, GAO Z, LEI L, et al. Lycium barbarum polysaccharide enhances development of previously-cryopreserved murine two-cell embryos via restoration of mitochondrial function and down-regulated generation of reactive oxygen species[J]. Journal of Reproduction and Development, 2019, 65(2): 163-170. DOI:10.1262/jrd.2018-104.
[32] HONG B D, DA P C, JIAN M J, et al. Inhibiting effects of Achyranthes bidentata polysaccharide and Lycium barbarum polysaccharide on nonenzyme glycation in D-galactose induced mouse aging model[J]. Biomedical and Environmental Sciences, 2004, 16(3):267-275. DOI:10.3200/AEOH.58.9.592-596.
[33] LUO Q, CAI Y Z, YAN J, et al. Hypoglycemic and hypolipidemic effects and antioxidant activity of fruit extracts from Lycium barbarum[J]. Life Sciences, 2004, 76(2): 137-149. DOI:10.1016/j.lfs.2004.04.056.
[34] LI X M, MA Y L, LIU X J. Effect of the Lycium barbarum polysaccharides on age-related oxidative stress in aged mice[J].Journal of Ethnopharmacology, 2007, 111(3): 504-511. DOI:10.1016/j.jep.2006.12.024.
[35] HUANG Y Y, ZHOU F, SHEN C. LBP reduces the inflammatory injury of kidney in septic rat and regulates the Keap1-Nrf2/ARE signaling pathway 1[J]. Acta Cirurica Brasileira, 2019, 34(1):e20190010000003. DOI:10.1590/s0102-865020190010000003.
[36] HE M H, PAN H, CHANG R C C, et al. Activation of the Nrf2/HO-1 antioxidant pathway contributes to the protective effects of Lycium barbarum polysaccharides in the rodent retina after ischemia-reperfusion-induced damage[J]. PLoS ONE, 2014, 9(1):e84800. DOI:10.1371/journal.pone.0084800.
[37] ZHENG G Z, REN H J, LI H Q, et al. Lycium barbarum polysaccharide reduces hyperoxic acute lung injury in mice through Nrf2 pathway[J]. Biomedicine & Pharmacotherapy, 2019, 111:733-739. DOI:10.1016/j.biopha.2018.12.073.
[38] XUE S J, HU X H, ZHU L G, et al. Protective functions of Lycium barbarum polysaccharides in H2O2-injured vascular endothelial cells through anti-oxidation and anti-apoptosis effects[J]. Biomedical Reports, 2019, 11(5): 207-214. DOI:10.3892/br.2019.1240.
[39] LI J, DING Z J, YANG Y, et al. Lycium barbarum polysaccharides protect human trophoblast HTR8/SVneo cells from hydrogen peroxide-induced oxidative stress and apoptosis[J]. Molecular Medicine Reports, 2018, 18(3): 2581-2588. DOI:10.3892/mmr.2018.9274.
[40] SHAN T Y, SHAN T Q, LIU F L, et al. Effects of Lycium barbarum polysaccharides on the damage to human endometrial stromal cells induced by hydrogen peroxide[J]. Molecular Medicine Reports, 2017,15(2): 879-884. DOI:10.3892/mmr.2016.6080.
[41] NIU T, JIN L Z, NIU S Z, et al. Lycium barbarum polysaccharides alleviates oxidative damage induced by H2O2 through down-regulating microRNA-194 in PC-12 and SH-SY5Y cells[J]. Cellular Physiology and Biochemistry, 2018, 50(2): 460-472. DOI:10.1159/000494159.
[42] LIU Y X, ZHANG Y. Lycium barbarum polysaccharides alleviate hydrogen peroxide-induced injury by up-regulation of miR-4295 in human trabecular meshwork cells[J]. Experimental and Molecular Pathology, 2019, 106: 109-115. DOI:10.1016/j.yexmp.2018.12.007.
[43] QI B, JI Q S, WEN Y C, et al. Lycium barbarum polysaccharides protect human lens epithelial cells against oxidative stress-induced apoptosis and senescence[J]. PLoS ONE, 2014, 9(10): e110275.DOI:10.1371/journal.pone.0110275.
[44] NIU A J, WU J M, YU D H, et al. Protective effect of Lycium barbarum polysaccharides on oxidative damage in skeletal muscle of exhaustive exercise rats[J]. International Journal of Biological Macromolecules, 2008, 42(5): 447-449. DOI:10.1016/j.ijbiomac.2008.02.003.
[45] XIN Y F, WAN L L, PENG J L, et al. Alleviation of the acute doxorubicin-induced cardiotoxicity by Lycium barbarum polysaccharides through the suppression of oxidative stress[J]. Food and Chemical Toxicology, 2011, 49(1): 259-264. DOI:10.1016/j.fct.2010.10.028.
[46] WU H T, HE X J, HONG Y K, et al. Chemical characterization of Lycium barbarum polysaccharides and its inhibition against liver oxidative injury of high-fat mice[J]. International Journal of Biological Macromolecules, 2010, 46(5): 540-543. DOI:10.1016/j.ijbiomac.2010.02.010.
[47] ZHANG W J, YANG H F, ZHU L Q, et al. Role of EGFR/ErbB2 and PI3K/Akt/e-NOS in Lycium barbarum polysaccharides ameliorating endothelial dysfunction induced by oxidative stress[J]. The American Journal of Chinese Medicine, 2019, 47(7): 1523-1539. DOI:10.1142/S0192415X19500782.
[48] 曹茜, 杨玉倩, 左晶, 等. 枸杞多糖对H2O2诱导人视网膜色素上皮细胞自噬及Beclin-1、LC3B表达的影响[J]. 东南大学学报(医学版),2018, 37(6): 1010-1013. DOI:10.3969/j.issn.1671-6264.2018.06.016.
[49] 魏萌萌, 林雪, 薛頔, 等. 枸杞多糖抑制绿脓杆菌毒素引起的小鼠巨噬细胞RAW264.7氧化损伤作用研究[J]. 中国病原生物学杂志,2019, 14(6): 629-633. DOI:10.13350/j.cjpb.190603.
[50] 柴茹, 贾磊娜, 张亚娟, 等. 枸杞多糖对2,4-D诱导的PC12细胞氧化损伤及凋亡的影响[J]. 环境与健康杂志, 2019, 36(5): 396-399.DOI:10.16241/j.cnki.1001-5914.2019.05.005.
[51] 许拓, 凌宏艳, 龙佳, 等. 枸杞多糖对HepG2细胞胰岛素抵抗的改善作用及机制研究[J]. 中国应用生理学杂志, 2017, 33(6): 568-571.DOI:10.12047/j.cjap.5601.2017.134.
[52] 谭连杰, 林黑着, 黄忠, 等. 枸杞多糖对卵形鲳鲹生长性能、抗氧化能力及血清免疫、生化指标的影响[J]. 动物营养学报, 2019, 31(1):418-427. DOI:10.3969/j.issn.1006-267x.2019.01.049.
[53] 刘华, 王薇佳, 吕建峰. 口服中药三七对三高患者治疗作用的探讨与评价[J]. 中国卫生标准管理, 2017, 8(22): 104-107. DOI:10.3969/j.issn.1674-9316.2017.22.052.
[54] CAI H Z, LIU F F, ZUO P F, et al. Practical application of antidiabetic efficacy of Lycium barbarum polysaccharide in patients with type 2 diabetes[J]. Medicinal Chemistry, 2015, 11(4): 383-390. DOI:10.2174/1573406410666141110153858.
[55] ZHU J, LIU W, YU J P, et al. Characterization and hypoglycemic effect of a polysaccharide extracted from the fruit of Lycium barbarum L.[J].Carbohydrate Polymers, 2013, 98(1): 8-16. DOI:10.1016/j.carbpol.2013.04.057.
[56] CAI H Z, YANG X H, CAI Q, et al. Lycium barbarum L.polysaccharide (LBP) reduces glucose uptake via down-regulation of SGLT-1 in Caco-2 cell[J]. Molecules, 2017, 22(2): 341. DOI:10.3390/molecules22020341.
[57] PAI P G, UMMA H P, ULLAL S, et al. Evaluation of hypolipidemic effects of Lycium barbarum (Goji berry) in a murine model[J]. Journal of Natural Remedies, 2013, 13(1): 4-8.
[58] CHEN W W, CHENG X, CHEN J Z, et al. Lycium barbarum polysaccharides prevent memory and neurogenesis impairments in scopolamine-treated rats[J]. PLoS ONE, 2014, 9(2): e88076.DOI:10.1371/journal.pone.0088076.
[59] KOU L, DU M Z, ZHANG C P, et al. Polysaccharide purified from Lycium barbarum protects differentiated PC12 cells against L-Glu-induced toxicity via the mitochondria-associated pathway[J].Molecular Medicine Reports, 2017, 16(4): 5533-5540. DOI:10.3892/mmr.2017.7289.
[60] HO Y S, YU M S, YANG X F, et al. Neuroprotective effects of polysaccharides from wolfberry, the fruits of Lycium barbarum, against homocysteine-induced toxicity in rat cortical neurons[J]. Journal of Alzheimer’s Disease, 2010, 19(3): 813-827. DOI:10.3233/JAD-2010-1280.
[61] YU Y Y, WU X Q, PU J N, et al. Lycium barbarum polysaccharide protects against oxygen glucose deprivation/reoxygenation-induced apoptosis and autophagic cell death via the PI3K/Akt/mTOR signaling pathway in primary cultured hippocampal neurons[J]. Biochemical and Biophysical Research Communications, 2018, 495(1): 1187-1194.DOI:10.1016/j.bbrc.2017.11.165.
[62] HO Y S, YU M S, YIK S Y, et al. Polysaccharides from wolfberry antagonizes glutamate excitotoxicity in rat cortical neurons[J]. Cellular and Molecular Neurobiology, 2009, 29(8): 1233-1244. DOI:10.1007/s10571-009-9419-x.
[63] LIU W J, JIANG H F, REHMAN F U L, et al. Lycium barbarum polysaccharides decrease hyperglycemia-aggravated ischemic brain injury through maintaining mitochondrial fission and fusion balance[J].International Journal of Biological Sciences, 2017, 13(7): 901-910.DOI:10.7150/ijbs.18404.
[64] LAM C S, TIPOE G L, SO K F, et al. Neuroprotective mechanism of Lycium barbarum polysaccharides against hippocampal-dependent spatial memory deficits in a rat model of obstructive sleep apnea[J]. PLoS ONE,2015, 10(2): e0117990. DOI:10.1371/journal.pone.0117990.
[65] ZHOU Y, DUAN Y H, HUANG S C, et al. Polysaccharides from Lycium barbarum ameliorate amyloid pathology and cognitive functions in APP/PS1 transgenic mice[J]. International Journal of Biological Macromolecules, 2020, 144: 1004-1012. DOI:10.1016/j.ijbiomac.2019.09.177.
[66] LIU S Y, CHEN L, LI X C, et al. Lycium barbarum polysaccharide protects diabetic peripheral neuropathy by enhancing autophagy via mTOR/p70S6K inhibition in Streptozotocin-induced diabetic rats[J].Journal of Chemical Neuroanatomy, 2018, 89: 37-42. DOI:10.1016/j.jchemneu.2017.12.011.
[67] 程爱佳, 李光华, 韩梅. 枸杞多糖对坐骨神经损伤小鼠淋巴细胞增殖转化能力及血清IL-2与IL-12含量的影响[J]. 临床医学工程, 2019,26(10): 1337-1338. DOI:10.3969/j.issn.1674-4659.2019.10.1337.
[68] 王亿龙, 刘青峰. 枸杞多糖对大鼠放射性脑损伤海马神经元凋亡的保护作用及其对PI3K/Akt/mTOR信号通路影响[J]. 中国公共卫生,2019, 35(8): 1043-1045. DOI:10.11847/zgggws1124336.
[69] 冯云, 刘津, 唐海丹, 等. 枸杞多糖对癫痫大鼠神经的保护作用及机制[J]. 中国老年学杂志, 2017, 37(24): 6036-6038. DOI:10.3969/j.issn.1005-9202.2017.24.014.
[70] 陈浩, 张皓洁, 师亮, 等. 枸杞多糖对帕金森病小鼠的抗氧化作用和神经保护效应[J]. 中国神经精神疾病杂志, 2018, 44(10): 613-618.DOI:10.3969/j.issn.1002-0152.2018.10.008.
[71] HONG C Y, ZHANG H D, LIU X Y, et al. Attenuation of hyperoxic acute lung injury by Lycium barbarum polysaccharide via inhibiting NLRP3 inflammasome[J]. Archives of Pharmacal Research, 2019,42(10): 902-908. DOI:10.1007/s12272-019-01175-4.
[72] XIAO J, ZHU Y H, LIU Y H, et al. Lycium barbarum polysaccharide attenuates alcoholic cellular injury through TXNIP-NLRP3 inflammasome pathway[J]. International Journal of Biological Macromolecules, 2014, 69: 73-78. DOI:10.1016/j.ijbiomac.2014.05.034.
[73] ZHU X D, HU S T, ZHU L Q, et al. Effects of Lycium barbarum polysaccharides on oxidative stress in hyperlipidemic mice following chronic composite psychological stress intervention[J].Molecular Medicine Reports, 2015, 11(5): 3445-3450. DOI:10.3892/mmr.2014.3128.
[74] NI H W, WANG G X, XU Y, et al. Lycium barbarum polysaccharide alleviates IL-1β-evoked chondrogenic ATDC5 cell inflammatory injury through mediation of microRNA-124[J]. Artificial Cells,Nanomedicine, and Biotechnology, 2019, 47(1): 4046-4052.DOI:10.1080/21691401.2019.1673765.
[75] XIONG G F, LI D W, ZHENG M B, et al. The effects of Lycium Barbarum polysaccharide (LBP) in a mouse model of cerulein-induced acute pancreatitis[J]. Medical Science Monitor: International Medical Journal of Experimental and Clinical Research, 2019, 25: 3880-3886.DOI:10.12659/MSM.913820.
[76] 王凌霄, 刘婷婷, 杨晓辉, 等. 枸杞多糖对髓样分化因子88基因敲除小鼠2 型糖尿病模型炎症因子的影响[J]. 上海交通大学学报(医学版), 2019, 39(2): 136-141. DOI:10.3969/j.issn.1674-8115.2019.02.006.
[77] 杜军霞, 宫彬彬, 宋菲, 等. 枸杞多糖的抗炎镇痛作用研究[J].天然产物研究与开发, 2019, 31(2): 236-239. DOI:10.16333/j.1001-6880.2019.2.009.
[78] 李雯, 陈兰, 戚迪, 等. 枸杞多糖通过Akt/eNOS通路减轻LPS致ARDS小鼠肺损伤[J]. 中国药理学通报, 2018, 34(9): 1258-1263.DOI:10.3969/j.issn.1001-1978.2018.09.015.
[79] 葛建彬, 卢红建, 宋新建, 等. 枸杞多糖对小鼠脑缺血再灌注损伤的保护作用及其抑制NF-κB, TNF-α, IL-6和IL-1β表达的机制[J].中国中药杂志, 2017, 42(2): 326-331. DOI:10.19540/j.cnki.cjcmm.20161222.016.
[80] LIU Q Q, HAN Q Q, LU M L, et al. Lycium barbarum polysaccharide attenuates cardiac hypertrophy, inhibits calpain-1 expression and inhibits NF-κB activation in streptozotocin-induced diabetic rats[J].Experimental and Therapeutic Medicine, 2019, 18(1): 509-516.DOI:10.3892/etm.2019.7612.
[81] SHI G J, ZHENG J, WU J, et al. Beneficial effects of Lycium barbarum polysaccharide on spermatogenesis by improving antioxidant activity and inhibiting apoptosis in streptozotocin-induced diabetic male mice[J]. Food & Function, 2017, 8(3): 1215-1226.DOI:10.1039/c6fo01575a.
[82] SHI G J, ZHENG J, HAN X X, et al. Lycium barbarum polysaccharide attenuates diabetic testicular dysfunction via inhibition of the PI3K/Akt pathway-mediated abnormal autophagy in male mice[J]. Cell and Tissue Research, 2018, 374(3): 653-666. DOI:10.1007/s00441-018-2891-1.
[83] LUO Q, LI Z N, HUANG X L, et al. Lycium barbarum polysaccharides: protective effects against heat-induced damage of rat testes and H2O2-induced DNA damage in mouse testicular cells and beneficial effect on sexual behavior and reproductive function of hemicastrated rats[J]. Life Sciences, 2006, 79(7): 613-621.DOI:10.1016/j.lfs.2006.02.012.
[84] YANG F L, WEI Y X, LIAO B Y, et al. Lycium barbarum polysaccharide prevents cisplatin-induced MlTc-1 cell apoptosis and autophagy via regulating endoplasmic reticulum stress pathway[J].Drug Design, Development and Therapy, 2018, 12: 3211-3219.DOI:10.2147/DDDT.S176316.
[85] SHI G J, ZHENG J, WU J, et al. Protective effects of Lycium barbarum polysaccharide on male sexual dysfunction and fertility impairments by activating hypothalamic pituitary gonadal axis in streptozotocin-induced type-1 diabetic male mice[J]. Endocrine Journal, 2017, 64(9): 907-922. DOI:10.1507/endocrj.ej16-0430.0.
[86] LUO Q, LI J J, CUI X Y, et al. The effect of Lycium barbarum polysaccharides on the male rats’ reproductive system and spermatogenic cell apoptosis exposed to low-dose ionizing irradiation[J]. Journal of Ethnopharmacology, 2014, 154(1): 249-258. DOI:10.1016/j.jep.2014.04.013.
[87] XIN Y F, YOU Z Q, GAO H, et al. Protective effect of Lycium barbarum polysaccharides against doxorubicin-induced testicular toxicity in rats[J]. Phytotherapy Research, 2012, 26(5): 716-721.DOI:10.1002/ptr.3633.
[88] 南亚昀, 李卿慧, 赵飞, 等. 枸杞多糖对肾阳虚大鼠勃起功能及性激素的影响[J]. 山西中医, 2019, 35(8): 52-55.
[89] 刘波, 谭雅琴, 丁协刚, 等. 枸杞多糖促进大鼠海绵体神经损伤修复的实验研究[J]. 中华男科学杂志, 2017, 23(11): 1043-1046.DOI:10.13263/j.cnki.nja.2017.11.015.
[90] XIAO J, XING F Y, HUO J, et al. Lycium barbarum polysaccharides therapeutically improve hepatic functions in non-alcoholic steatohepatitis rats and cellular steatosis model[J]. Scientific Reports,2014, 4: 5587. DOI:10.1038/srep05587.
[91] XIAO J, WANG F, LIONG E C, et al. Lycium barbarum polysaccharides improve hepatic injury through NF-kappa-B and NLRP3/6 pathways in a methionine choline deficient diet steatohepatitis mouse model[J]. International Journal of Biological Macromolecules, 2018, 120: 1480-1489. DOI:10.1016/j.ijbiomac.2018.09.151.
[92] XIAO J, ZHU Y H, LIU Y X, et al. Lycium barbarum polysaccharide attenuates alcoholic cellular injury through TXNIP-NLRP3 inflammasome pathway[J]. International Journal of Biological Macromolecules, 2014, 69:73-78. DOI:10.1016/j.ijbiomac.2014.05.034.
[93] XIAO J, LIONG E C, CHING Y P, et al. Lycium barbarum polysaccharides protect mice liver from carbon tetrachloride-induced oxidative stress and necroinflammation[J]. Journal of Ethnopharmacology, 2012, 139(2): 462-470. DOI:10.1016/j.jep.2011.11.033.
[94] GAN F, LIU Q, LIU Y H, et al. Lycium barbarum polysaccharides improve CCl4-induced liver fibrosis, inflammatory response and TLRs/NF-κB signaling pathway expression in Wistar rats[J]. Life Sciences,2018, 192: 205-212. DOI:10.1016/j.lfs.2017.11.047.
[95] YAN Y M, WU W Q, LU L, et al. Study on the synergistic protective effect of Lycium barbarum L. polysaccharides and zinc sulfate on chronic alcoholic liver injury in rats[J]. Food Science & Nutrition,2019, 7(11): 3435-3442. DOI:10.1002/fsn3.1182.
[96] 庞志澜, 杜利军, 单铁英, 等. 口服枸杞多糖抑制实验性小鼠肝纤维化损伤的作用[J]. 职业与健康, 2019, 35(20): 2773-2776.DOI:10.13329/j.cnki.zyyjk.2019.0787.
[97] THOMPSON J T. Advantages and limitations of small gauge vitrectomy[J]. Survey of Ophthalmology, 2011, 56(2): 162-172.DOI:10.1016/j.survophthal.2010.08.003.
[98] WANG J H, YAO Y, LIU X Z, et al. Protective effects of Lycium barbarum polysaccharides on blood-retinal barrier via ROCK1 pathway in diabetic rats[J]. American Journal of Translational Research, 2019, 11(10): 6304-6315.
[99] YANG D, SO K F, LO A C Y. Lycium barbarum polysaccharide extracts preserve retinal function and attenuate inner retinal neuronal damage in a mouse model of transient retinal ischaemia[J]. Clinical &Experimental Ophthalmology, 2017, 45(7): 717-729. DOI:10.1111/ceo.12950.
[100] MI X S, FENG Q, LO A C Y, et al. Protection of retinal ganglion cells and retinal vasculature by Lycium barbarum polysaccharides in a mouse model of acute ocular hypertension[J]. PLoS ONE, 2012, 7(10):e45469. DOI:10.1371/journal.pone.0045469.
[101] LAKSHMANAN Y, WONG F S Y, YU W Y, et al. Lycium barbarum polysaccharides rescue neurodegeneration in an acute ocular hypertension rat model under pre-and post-treatment conditions[J].Investigative Ophthalmology & Visual Science, 2019, 60(6): 2023-2033. DOI:10.1167/iovs.19-26752.
[102] LAKSHMANAN Y, WONG F S Y, ZUO B, et al. Posttreatment intervention with Lycium barbarum polysaccharides is neuroprotective in a rat model of chronic ocular hypertension[J]. Investigative Ophthalmology & Visual Science, 2019, 60(14): 4606-4618.DOI:10.1167/iovs.19-27886.
[103] MI X S, CHIU K, VAN G, et al. Effect of Lycium barbarum polysaccharides on the expression of endothelin-1 and its receptors in an ocular hypertension model of rat glaucoma[J]. Neural Regeneration Research, 2012, 7(9): 645-651. DOI:10.3969/j.issn.1673-5374.2012.09.001.
[104] ZHU Y F, ZHAO Q P, GAO H, et al. Lycium barbarum polysaccharides attenuates N-methy-N-nitrosourea-induced photoreceptor cell apoptosis in rats through regulation of poly (ADP-ribose) polymerase and caspase expression[J]. Journal of Ethnopharmacology, 2016, 191:125-134. DOI:10.1016/j.jep.2016.05.037.
[105] YAO Q, YANG Y, LU X H, et al. Lycium barbarum polysaccharides improve retinopathy in diabetic sprague-dawley rats[J]. Evidence-Based Complementary and Alternative Medicine, 2018, 2018: 1-12.DOI:10.1155/2018/7943212.
[106] PAN H, SHI Z, YANG T G, et al. The protective effects of Lycium barbarum polysaccharides on retinal neurons in diabetic rats and its mechanism[J]. Chinese Journal of Applied Physiology, 2019, 35(1):55-59. DOI:10.12047/j.cjap.5706.2019.014.
[107] CHU P H W, LI H Y, CHIN M P, et al. Effect of Lycium barbarum(wolfberry) polysaccharides on preserving retinal function after partial optic nerve transection[J]. PLoS ONE, 2013, 8(12): e81339.DOI:10.1371/journal.pone.0081339.
[108] 王海彬, 董志军, 郭立涛, 等. 枸杞多糖对糖尿病大鼠视网膜Caspase-3、Bcl-2和Bax表达的影响[J]. 中国老年学杂志, 2019,39(20): 5070-5074. DOI:10.3969/j.issn.1005-9202.2019.20.058.
[109] 葛君, 刘爱琴, 黄文宇, 等. 枸杞多糖联合美沙拉嗪治疗慢性实验性结肠炎小鼠模型的实验研究[J]. 中国中西医结合杂志, 2019,39(11): 1366-1371. DOI:10.7661/j.cjim.20190419.135.
[110] CHEN J H, LONG L N, JIANG Q, et al. Effects of dietary supplementation of Lycium barbarum polysaccharides on growth performance, immune status, antioxidant capacity and selected microbial populations of weaned piglets[J]. Journal of Animal Physiology and Animal Nutrition, 2020, 104(4): 1106-1115.DOI:10.1111/jpn.13247.
[111] LIANG W Y, YUE Z. Lycium barbarum polysaccharides promote osteoblasts viability by regulating microRNA-17/PTEN[J]. Life Sciences, 2019, 225: 72-78. DOI:10.1016/j.lfs.2019.04.001.
[112] ZHU J, ZHANG Y Y, SHEN Y S, et al. Lycium barbarum polysaccharides induce Toll-like receptor 2 and 4 mediated phenotypic and functional maturation of murine dendritic cells via activation of NF-κB[J]. Molecular Medicine Reports, 2013, 8(4): 1216-1220.DOI:10.3892/mmr.2013.1608.
[113] BO R N, LIU Z G, ZHANG J, et al. Mechanism of Lycium barbarum polysaccharides liposomes on activating murine dendritic cells[J].Carbohydrate Polymers, 2019, 205: 540-549. DOI:10.1016/j.carbpol.2018.10.057.
[114] SUN X M, LV Y, HUANG L, et al. Pro-inflammatory cytokines serve as communicating molecules between the liver and brain for hepatic encephalopathy pathogenesis and Lycium barbarum polysaccharides protection[J]. Journal of Ethnopharmacology, 2020, 248: 112357.DOI:10.1016/j.jep.2019.112357.
[115] ZHU W, ZHOU S X, LIU J H, et al. Prebiotic, immuno-stimulating and gut microbiota-modulating effects of Lycium barbarum polysaccharide[J]. Biomedicine & Pharmacotherapy, 2020, 121:109591. DOI:10.1016/j.biopha.2019.109591.
[116] SONG S Q, LIN F L, ZHU P Y, et al. Lycium barbarum polysaccharide alleviates oxygen glucose deprivation-induced PC12 cells damage by up-regulating miR-24[J]. Artificial Cells,Nanomedicine, and Biotechnology, 2019, 47(1): 3994-4000.DOI:10.1080/21691401.2019.1673767.
[117] LU T, ZHAO W, ZHANG F, et al. Lycium barbarum polysaccharides attenuate rat anti-Thy-1 glomerulonephritis through mediating pyruvate dehydrogenase[J]. Biomedicine & Pharmacotherapy, 2019,116: 109020. DOI:10.1016/j.biopha.2019.109020.
[118] DING Y, YAN Y M, CHEN D, et al. Modulating effects of polysaccharides from the fruits of Lycium barbarum on the immune response and gut microbiota in cyclophosphamide-treated mice[J].Food & Function, 2019, 10(6): 3671-3683. DOI:10.1039/c9fo00638a.
[119] ZHANG H Y, ZHENG L, YUAN Z P. Lycium barbarum polysaccharides promoted proliferation and differentiation in osteoblasts[J]. Journal of Cellular Biochemistry, 2019, 120(4): 5018-5023. DOI:10.1002/jcb.27777.
[120] 颜贝, 王佳陪, 王娟, 等. 枸杞多糖对离心过程中弱精精子氧化应激的作用研究[J]. 重庆医学, 2019, 48(21): 3641-3645. DOI:10.3969/j.issn.1671-8348.2019.21.010.
[121] 崔芳, 史春丽, 尹梅, 等. 枸杞多糖对过敏性哮喘小鼠肠道菌群的影响[J]. 现代食品科技, 2019, 35(9): 67-73. DOI:10.13982/j.mfst.1673-9078.2019.9.007.
[122] 李静静, 杨丽丽, 张金宏, 等. 枸杞多糖增强骨髓间充质干细胞体外抗逆境能力[J]. 中药材, 2018, 41(5): 1197-1199. DOI:10.13863/j.issn1001-4454.2018.05.040.
[123] 楚胜. 枸杞多糖对创伤后应激障碍大鼠抑郁的保护作用研究[J]. 现代预防医学, 2019, 46(14): 2622-2625; 2637.
[124] 魏芬芬, 王文娟, 张波. 枸杞多糖对酒精性肝损伤小鼠肾脏的保护作用[J]. 癌变·畸变·突变, 2019, 31(2): 148-152. DOI:10.3969/j.issn.1004-616x.2019.02.010.
[125] 黄振华, 邓向亮, 张凯敏, 等. 枸杞多糖对免疫抑制小鼠红细胞免疫功能的影响[J]. 中国免疫学杂志, 2018, 34(2): 214-217.DOI:10.3969/j.issn.1000-484X.2018.02.011.
[126] ZHANG Min, TANG Xiuli, WANG Fang, et al. Characterization of Lycium barbarum polysaccharide and its effect on human hepatoma cells[J]. International Journal of Biological Macromolecules, 2013, 61:270-275. DOI:10.1016/j.ijbiomac.2013.06.031.
[127] ZHANG Min, WANG Fang, LIU Rui, et al. Effects of superfine grinding on physicochemical and antioxidant properties of Lycium barbarum polysaccharides[J]. LWT-Food Science and Technology,2014, 58(2): 594-601. DOI:10.1016/j.lwt.2014.04.020.
[128] GONG Guiping, DANG Tiantian, DENG Yangni, et al.Physicochemical properties and biological activities of polysaccharides from Lycium barbarum prepared by fractional precipitation[J].International Journal of Biological Macromolecules, 2018, 109: 611-618. DOI:10.1016/j.ijbiomac.2017.12.017.
[129] ZHANG Qian, LÜ Xiaoling, WU Tao, et al. Composition of Lycium barbarum polysaccharides and their apoptosis-inducing effect on human hepatoma SMMC-7721 cells[J]. Food & Nutrition Research,2015, 59(1): 28696. DOI:10.3402/fnr.v59.28696.
[130] YAO Ruyu, HUANG Chao, CHEN Xingfu, et al. Two complement fixing pectic polysaccharides from pedicel of Lycium barbarum L.promote cellular antioxidant defense[J]. International Journal of Biological Macromolecules, 2018, 112: 356-363. DOI:10.1016/j.ijbiomac.2018.01.207.
[131] 钱怡霖, 汪东风, 范明昊, 等. 多糖中金属离子对其抗氧化活性及抗肿瘤活性的影响[J]. 中国食品学报, 2020, 20(2): 52-60.DOI:10.16429/j.1009-7848.2020.02.007.
[132] 孙玉姣, 高润凝, 崔湘怡, 等. 枸杞多糖及其硫酸化产物的免疫调节活性[J]. 陕西科技大学学报, 2020, 38(1): 44-49; 70. DOI:10.19481/j.cnki.issn2096-398x.2020.01.008.
[133] 王君敏. 硫酸化枸杞多糖和硫酸化当归多糖抗病毒和增强免疫活性的研究[D]. 南京: 南京农业大学, 2011: 91-92.
[134] 王君敏, 薛敬礼, 葛蓓蕾, 等. 枸杞多糖及其硫酸酯体外免疫及抗肿瘤活性[J]. 郑州大学学报(医学版), 2015, 50(6): 809-813.DOI:10.13705/j.issn.1671-6825.2015.06.020.
[135] 彭天元, 刘家水, 颜红专. 乙酰化修饰枸杞多糖及其抗氧化、抗肿瘤活性研究[J]. 安徽中医药大学学报, 2015, 34(6): 61-66.DOI:10.3969/j.issn.2095-7246.2015.06.020.
[136] QIU Shulei, CHEN Jin, CHEN Xi, et al. Optimization of selenylation conditions for Lycium barbarum polysaccharide based on antioxidant activity[J]. Carbohydrate Polymers, 2014, 103: 148-153. DOI:10.1016/j.carbpol.2013.12.032.