在世界多地尤其是非洲和中东的干旱和半干旱地区,骆驼协助着人类的生产和生活,是一种具有重要社会经济价值的动物。据研究估计,世界上共有2 200万 峰骆驼,其中北非和西亚的骆驼占89%,其余的占11%,主要分布在包括中国和蒙古等亚洲国家[1]。骆驼乳产量较低,被称为沙漠黄金[2],通常是不透明的白色,有淡淡的甜味,比牛乳略咸[3]。骆驼乳是一种营养丰富的食物,与牛乳、羊乳等常见的反刍动物乳相比,骆驼乳具有低糖、低胆固醇、高矿物质(钾、钠、铜、铁、镁和锌)、高维生素和高浓度胰岛素的特性[2]。对于生存在干旱地区的人们来说,水分质量分数高达84%的骆驼乳可作为重要的水摄取来源[4]。骆驼乳除了可作为营养来源的食物以外,也可帮助缓解多种疾病、表现出特定的药用价值。几个世纪以来,人们一直在使用骆驼乳作为功能性食品帮助缓解疾病[2]。在中东和印度,骆驼乳被用来预防与缓解糖尿病、牛乳过敏、克罗恩病、自闭症、浮肿、黄疸、慢性肝炎、结核、哮喘、贫血和痔疮等疾病。近年来,在骆驼乳的生物学与医学应用方面已有不少研究报道。本文将从骆驼乳的营养价值、药用特性的生物作用基础以及在抗疾病中的应用与作用机制这几个方面进行综述。
1 骆驼乳的营养价值
骆驼乳在乳类中营养价值很高,富含多种维生素及矿物质,其蛋白质、脂类等物质的组成含量与其他乳类有着明显的差异。尤其是骆驼乳中乳铁蛋白含量为所有乳类中最高,其酪蛋白的组成与含量也与其他乳类不同。
1.1 骆驼乳的营养组成
骆驼乳的营养组成丰富,每100 mL的驼乳约含总蛋白质(3.35f0.62)g、脂肪(3.82f1.08)g、乳糖(4.46f1.03)g,总固体(12.47f1.53)g。驼乳内的蛋白质包括酪蛋白、乳清蛋白(camel whey protein,CWP)、乳铁蛋白、乳清酸蛋白(whey acid protein,WAP)、乳过氧化物酶和免疫球蛋白等[5]。关于骆驼乳所含蛋白质及其简要信息见表1。骆驼乳包含了所有的必需氨基酸,并且赖氨酸、甘氨酸、苏氨酸和缬氨酸等氨基酸含量也相对较高[5]。对于骆驼乳中所含的矿物质元素,利用火焰原子吸收光谱法(flame atomic absorption spectrometry,FAAS)测定可知其主要含有钾、钙、钠、镁、铁、锌、铜等矿物质[6],并且骆驼乳也富含锌、硒。骆驼乳中含有大量不同种类的维生素,如VA、VC、VE、VD和VB族[5],骆驼乳中维生素和矿物质的含量如表2所示。
表1 骆驼乳所含蛋白质的分子特性[7]
Table 1 Molecular properties of proteins in camel milk[7]
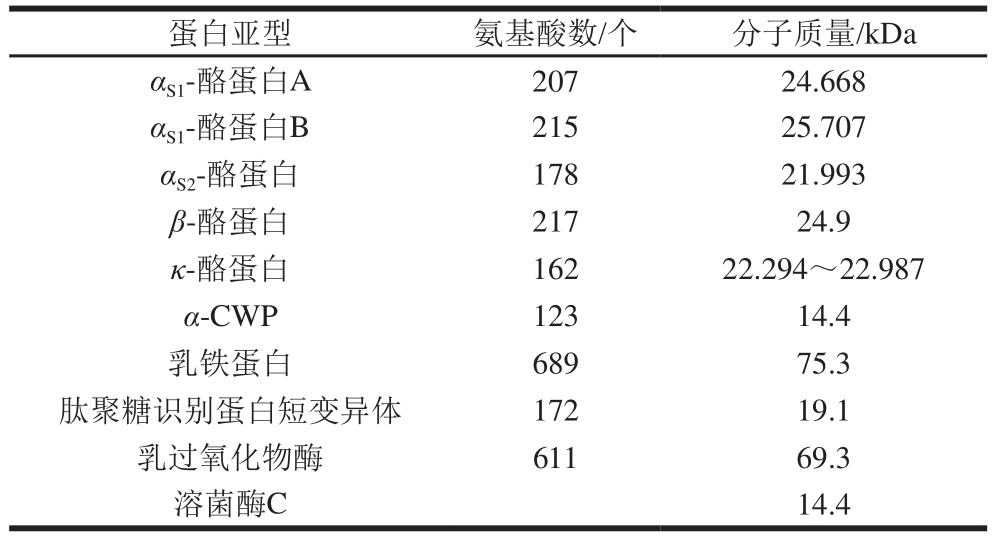
蛋白亚型 氨基酸数/个 分子质量/kDa αS1-酪蛋白A 207 24.668 αS1-酪蛋白B 215 25.707 αS2-酪蛋白 178 21.993 β-酪蛋白 217 24.9 κ-酪蛋白 162 22.294~22.987 α-CWP 123 14.4乳铁蛋白 689 75.3肽聚糖识别蛋白短变异体 172 19.1乳过氧化物酶 611 69.3溶菌酶C 14.4
表2 骆驼乳中主要维生素及矿物质的水平[1-2,8]
Table 2 Contents of major vitamins and minerals in camel milk[1-2,8]
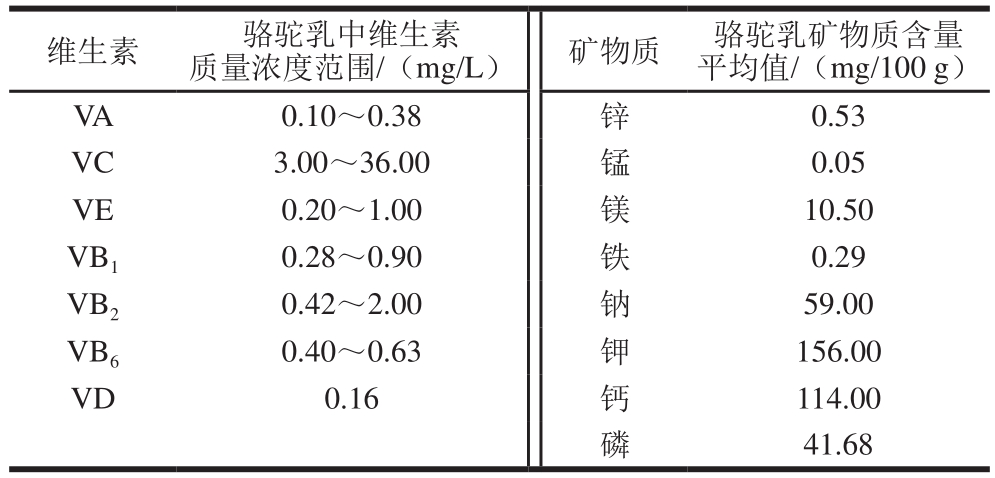
维生素 骆驼乳中维生素质量浓度范围/(mg/L)矿物质骆驼乳矿物质含量平均值/(mg/100 g)VA 0.10~0.38 锌 0.53 VC 3.00~36.00 锰 0.05 VE 0.20~1.00 镁 10.50 VB1 0.28~0.90 铁 0.29 VB2 0.42~2.00 钠 59.00 VB6 0.40~0.63 钾 156.00 VD0.16钙114.00磷41.68
1.2 品种和产地影响骆驼乳的营养成分
骆驼有两种,分别是有两个驼峰的双峰骆驼(Camelus bactrianus)和只有一个驼峰的单峰骆驼(Camelus dromedarius)。双峰驼主要分布于中亚国家和蒙古等区域;而单峰驼分布于西亚、中东和北非地区。单峰骆驼是一种存在于世界上几个沙漠地区的物种。单峰骆驼乳的益处可能与其含有高浓度的钾、镁、蛋白质和维生素有关[9]。我国是世界上双峰骆驼的主要分布区域之一,双峰骆驼在我国主要分布在新疆和内蒙古的沙漠和草原上。虽然双峰骆驼数量相对于单峰驼较少,但与单峰骆驼乳相比,双峰骆驼乳中的蛋白质、脂肪和乳糖含量均较高[10]。一般单峰骆驼乳的脂肪质量分数在1.2%~6.4%之间[3],哈萨克斯坦地区双峰骆驼乳脂肪质量分数(6.67%)高于该地区单峰骆驼乳(5.94%),但单峰骆驼乳不饱和脂肪酸更丰富[11]。在来自蒙古地区的双峰骆驼乳样品中,长链脂肪酸在总脂肪酸中所占比例较高,主要脂肪酸为棕榈酸(23.99%~30.72%)、油酸(17.21%~24.24%)和硬脂酸(11.13%~16.49%),优势氨基酸为亮氨酸、赖氨酸、缬氨酸和天冬氨酸;且蒙古不同地区双峰骆驼乳中脂肪酸和氨基酸组成存在较大差异,这说明地理位置对骆驼乳的成分有很大影响[12]。
1.3 骆驼乳与牛乳及其他乳类营养价值的比较
与牛乳相比,骆驼乳所含蛋白质更为丰富,并且酪蛋白的组成与含量和牛乳也有着明显的差异,更为重要的是,骆驼乳不饱和脂肪酸含量较高,维生素及矿物质的含量也优于牛乳,且乳糖和脂肪含量都相对较低,并含有更多的胰岛素。这些营养物质的组成与含量方面的差异,使得骆驼乳比牛乳有更好的降血糖作用和低致敏性。
牛乳中的蛋白质包括CWP、血清白蛋白和免疫球蛋白,而骆驼乳含有丰富的乳铁蛋白、免疫球蛋白、溶菌酶、α-乳白蛋白和血清白蛋白,但缺乏β-乳球蛋白[13]。骆驼乳中乳铁蛋白与免疫球蛋白的含量高于牛乳,并且骆驼乳清已被证明比牛乳乳清更耐热、更稳定。据报道,在80 ℃、30 min的条件下,骆驼乳清中的蛋白质变性率(32%~35%)低于牛乳清中的蛋白质(70%~75%)。而这其中的原因主要是两种不同来源的酪蛋白的结构差异[7]。骆驼乳中的酪蛋白含量较牛乳中低,其中65%为β-酪蛋白。在牛乳中,酪蛋白质量分数可达到80%以上,而其中仅有36%为β-酪蛋白[13]。在对牛乳和骆驼乳(4个品种)的蛋白质和脂质组分进行深入表征后发现,骆驼乳含有较低的饱和脂肪酸和较高的不饱和脂肪酸[14]。在氨基酸的含量方面,骆驼乳和牛乳中谷氨酸为主要氨基酸,分别占23.9%和21.8%。骆驼乳中的谷氨酸和丝氨酸含量高于牛乳,牛乳中丙氨酸、缬氨酸、赖氨酸、精氨酸和半胱氨酸的含量显著高于骆驼乳。然而,甘氨酸、亮氨酸、异亮氨酸和脯氨酸在骆驼乳蛋白中含量高于牛乳蛋白[13]。除此之外,骆驼乳中微量元素铁、锌、铜的含量也显著高于牛乳。与牛乳相比,骆驼乳中的VA、VE和VB1含量较低,而骆驼乳中的VC含量是牛乳的30 倍,是人奶的6 倍[1-2]。骆驼乳中所含降血糖物质包含胰岛素、类胰岛素蛋白等的含量也高于牛乳,尽管会受到泌乳期和贮存条件的影响,但已测得骆驼乳中存在较高浓度(52 IU/L)的胰岛素,并且骆驼乳中的类胰岛素蛋白的含量约为牛奶中的3 倍左右[15]。
骆驼乳和牛乳相比在诸多营养物质组成和含量上的显著差异使其具备了独特的应用价值,比如应用于牛奶过敏的婴幼儿群体。婴幼儿对牛奶过敏的发生率很高,当母乳喂养不可能或不足时,使用以骆驼乳为基础的低过敏性婴儿配方奶是有牛乳过敏或有可能发生牛乳过敏的婴儿的一种选择[3]。由于骆驼科与牛科有很大的进化距离,而且骆驼乳与牛乳蛋白组成不同,将骆驼乳作为低过敏性婴儿配方奶粉替代品具有一定的理论基础与必要性[16]。在2007年4月ü2010年2月在儿科进行的一项前瞻性队列研究中,对35 名6~12个月患有牛奶过敏(cow milk allergy,CMA)的儿童进行了调查,结果表明80%的CMA儿童能够安全饮用骆驼乳而不会发生任何不良过敏反应[17]。因此,在考虑配制婴儿配方奶时,可以建议将骆驼乳作为牛乳的合适替代品。
除了对比骆驼乳和牛乳的不同,也有研究对比了骆驼乳、牛乳、羊乳和人母乳在主要营养组成上的差异。如表3所示,与人母乳相比,骆驼乳含有相对更低的乳糖和更高比例的蛋白质。在酪蛋白的种类上牛乳以α-酪蛋白为主,骆驼乳和羊乳则以β-酪蛋白含量最多,人母乳不含αs2-酪蛋白,羊乳和骆驼乳含较少的αs2-酪蛋白和大量的β-酪蛋白,因此在酪蛋白组成方面骆驼乳比牛乳更接近人母乳[18]。
表3 骆驼乳、牛乳、羊乳和人母乳主要营养组成的区别[7,18]
Table 3 Differences in main nutritional composition of camel milk,cow milk, goat milk and human breast milk[7,18]
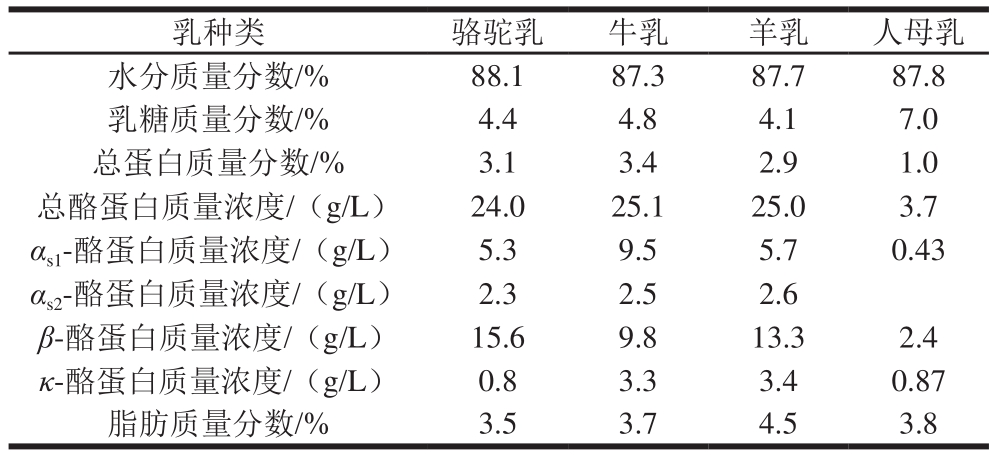
乳种类 骆驼乳 牛乳 羊乳 人母乳水分质量分数/% 88.1 87.3 87.7 87.8乳糖质量分数/% 4.4 4.8 4.1 7.0总蛋白质量分数/% 3.1 3.4 2.9 1.0总酪蛋白质量浓度/(g/L) 24.0 25.1 25.0 3.7 αs1-酪蛋白质量浓度/(g/L) 5.3 9.5 5.7 0.43 αs2-酪蛋白质量浓度/(g/L) 2.3 2.5 2.6 ü β-酪蛋白质量浓度/(g/L) 15.6 9.8 13.3 2.4 κ-酪蛋白质量浓度/(g/L) 0.8 3.3 3.4 0.87脂肪质量分数/% 3.5 3.7 4.5 3.8
另外,液体乳中乳脂的高分散状态对脂解酶接触小脂肪球有积极的影响,因此不同分散状态的乳脂在消化道内的消化难易程度不同。有人对比了几种乳中的乳脂球的粒径大小,平均直径最大的乳脂球是水牛乳(8.7 μm),最小的是骆驼乳(2.99 μm)和羊乳(3.19 μm),可见骆驼乳具有高分散状态的乳脂,因此也更容易被人类消化[1]。
2 骆驼乳具有药用价值的生物作用基础
2.1 骆驼乳具有药用特性及医学应用潜力的营养基础
骆驼乳作为一种乳品具有低胆固醇、低糖、高矿物质(钠、钾、铁、铜、锌和镁)、高维生素(VC、VB2、VA和VE)以及高浓度胰岛素等特性,并且骆驼乳中的乳铁蛋白及WAP等含量较高,这些特征是驼乳具有药用价值的营养基础。
由于骆驼乳中胰岛素含量更高,并已有动物实验证明骆驼乳可以显著降低血糖浓度,对肝脏和胰腺有保护作用[1,19]。与其他乳类相比,骆驼乳中乳铁蛋白的含量更高,从骆驼乳提取的乳铁蛋白具有多样化的药用特性,如抗菌、抗真菌、抗病毒、抗炎、抗肿瘤等[20]。更具体地说,它能抑制大肠杆菌、肺炎克雷伯菌、梭状杆菌、幽门螺杆菌、金黄色葡萄球菌、白色念珠菌等的生长。在抗病毒方面,骆驼乳铁蛋白对人免疫缺陷病毒、乙型和丙型肝炎、巨细胞病毒、单纯疱疹病毒1型感染也具有抗致病性活性[20]。骆驼乳中提取的乳铁蛋白还具有免疫调节作用,因为它可调节各种免疫细胞的激活和成熟,如中性粒细胞、巨噬细胞和淋巴细胞。乳铁蛋白还发挥抗肿瘤细胞增殖的作用[20]。并且,乳铁蛋白具有潜在的抗糖尿病的疗效,口服乳铁蛋白的2型糖尿病患者的血清白介素(interleukin,IL)-1β、IL-6、IL-18、肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)和脂质运载蛋白2的水平均有显著降低;在连续3个月每天服用乳铁蛋白的肥胖儿童中,其糖化血红蛋白、身体质量指数(body mass index,BMI)和血脂水平都有明显改善;这表明乳铁蛋白的摄入有助于更好地控制血糖[21]。除了乳铁蛋白,WAP也是骆驼乳中一种重要的蛋白质,其富含半胱氨酸的结构域被称为四二硫化物核心域(four-disulfide core,4-DSC)。与其他在乳汁中表达WAP的哺乳动物相反,骆驼WAP在第二个4-DSC结构域的开始处含有4个额外的氨基酸残基,并引入了一个磷酸化位点。有研究认为,WAP可能在调节乳腺上皮细胞的增殖中发挥重要作用,并且具有抑菌活性[22]。此外,骆驼乳中的免疫球蛋白具有独特特性,只含有两个重链,而轻链是缺失的;重链免疫球蛋白目前应用于多种疾病的免疫治疗,如癌症、多发性硬化症和阿尔茨海默病[20]。
上述这些骆驼乳的特殊营养价值以及特殊营养物质尤其是蛋白质类组成与含量的特性赋予了骆驼乳在医药应用方面不可忽视的潜力。
2.2 骆驼乳具有药用特性及医学应用潜力的生物学作用基础
大量研究表明,骆驼乳具有一定的调节机体功能的药用特性,对多种类型的涉及不同系统的疾病有潜在的益处。骆驼乳的营养组成特征赋予了其多样化的药用价值和在机体中发挥生物作用的能力,这些作用包括抗氧化、抗炎、免疫调节、肠道菌群微生态调节等方面,是骆驼乳在多种疾病体系中表现出有益功效的共有作用基础。
2.2.1 抵御氧化应激
氧化应激是多种疾病体系的共同病生理基础之一,抗氧化剂可防治或减轻多种疾病。骆驼乳含有多种抗氧化成分、具有抗氧化作用[23-24]。第一,骆驼乳CWP具有抗氧化活性,可以促进免疫细胞的增殖,减轻氧化应激反应和炎症,加速糖尿病期间的伤口愈合过程[25]。第二,骆驼乳蛋白中的乳铁蛋白已被证明可以通过发挥抗氧化和抗DNA损伤活性,抑制人结直肠癌(human colorectal tumors,HCT)-116细胞的增殖[26]。对于肾脏相关的氧化应激来说,驼乳可以通过降低脂质过氧化物水平和增强抗氧化防御来减轻肾脏凋亡细胞的死亡程度,从而保护肾脏[27]。第三,骆驼乳中含有抗氧化生物活性肽。有研究从骆驼乳蛋白质组分中提取抗氧化肽,用酵母细胞作为细胞模型,评价其抗氧化活性,结果发现酪蛋白和乳清组分中的肽显著增强了酵母细胞对过氧化物诱导的氧化应激的耐受性,说明骆驼乳中的酪蛋白和CWP均为具有显著自由基清除活性的生物活性肽,这预示着它们在预防和帮助缓解氧化应激相关疾病方面的潜力[23]。除此之外,骆驼乳中的酪蛋白经酶解后抗氧化性能有所提高[28-29]。有报道称,骆驼乳经碱性蛋白酶、菠萝蛋白酶和木瓜蛋白酶等酶解后可制得骆驼乳蛋白水解物(camel milk protein hydrolysates, CMPH),其比同样经过碱性蛋白酶、木瓜蛋白酶、胰凝乳蛋白酶和胰蛋白酶有限酶解的牛乳具有更高的抗氧化和抗菌活性[23,30]。未来可以考虑水解处理骆驼乳蛋白质以改善其技术功能和生物活性,从而将CMPH作为功能成分应用于特殊食品中[31]。此外,骆驼乳中的矿物质如铁、钠、铜、钾、镁、以及高含量的VC可以作为抗氧化剂直接中和自由基,或调节机体内抗氧化酶和非酶抗氧化分子的水平,从而发挥降低氧化应激的作用[32],进而抑制氧化应激相关病理过程的发生发展。
2.2.2 减轻炎症反应
氧化应激常常伴随着炎症反应的加剧,而炎症反应也是多种疾病的共同病生理基础。骆驼乳可改善氧化应激和脂多糖(lipopolysaccharide,LPS)诱导的大鼠急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)炎症反应[33]。ARDS是一种死亡率较高的复杂综合征,在LPS诱导的ARDS大鼠中,摄入骆驼乳降低了肺湿干质量比,显著减少了LPS诱导的中性粒细胞浸润增加、肺泡间质和肺泡内水肿、肺泡壁厚度和肺组织肺损伤。同时骆驼乳在LPS诱导的ARDS大鼠中表现出抗炎和抗氧化作用,在LPS刺激后,骆驼乳显著降低了肺组织中血清和氧化应激标记物中的促炎细胞因子(肿瘤坏死因子TNF、IL-10和IL-1)的水平。这些实验证据提示骆驼乳可以作为治疗ARDS的潜在补充食物[33]。炎症性肠病(inflammatory bowel diseases,IBD)包括溃疡性结肠炎和克罗恩病,是一种具有复发性和免疫介导特性的慢性胃肠道炎症,由于IBD治疗过程中常常伴发着不同的不良反应,因此对于患者来说找到副作用尽量小的药物十分重要。有研究已证明骆驼乳的抗炎特性对于大鼠的IBD有缓解作用;给大鼠灌胃骆驼乳可以有效抑制结肠的损伤,降低结肠TNF-α和IL-10细胞因子水平,并通过降低脂质过氧化物和一氧化氮来抑制氧化应激,从组织水平和分子水平改善炎症性肠病[34]。
2.2.3 调节免疫系统
免疫系统不仅抵御外界病毒、病菌的入侵,同时也监视并消除自身的病变细胞包括肿瘤细胞,免疫力决定着人体抵抗各种疾病的能力。骆驼乳中所含的保护蛋白(包括溶菌酶、乳铁蛋白、乳过氧化物酶和肽聚糖识别蛋白)具有抗腹泻/抗菌作用以及抗轮状病毒抗体的高滴度,并影响免疫系统[35]。在埃及,骆驼乳是丙型肝炎病毒(hepatitis C virus,HCV)感染者广泛使用的传统药物之一。有研究使患者服用当地农场产的全骆驼乳4个月(250 mL/d),并收集患者在喝骆驼乳之前和之后的血清,随后进行血清学评估,结果显示,饮骆驼乳4个月后,88%的患者谷丙转氨酶(alanine aminotransferase,ALT)活力降低,所有患者天门冬氨酸转氨酶(aspartate aminotransferase,AST)活力降低,70%~76%的患者在治疗后,体内免疫球蛋白中抗HCV的抗体谱显著降低,表明患者体内病毒感染滴度下降,大多数患者对骆驼乳的治疗反应积极[36]。对骆驼乳含有的蛋白质进行分析,从中纯化出多克隆免疫球蛋白(immunoglobulin,Ig)Gs和α-乳白蛋白,并用外周血单核细胞(peripheral blood mononuclear cell,PBMC)和人肝癌细胞7.5(human hepatoma cells,Huh7.5)细胞系检测其抗病毒活性;实验结果显示,在暴露于HCV感染时,只有骆驼乳IgGs显示出对HCV肽显著的识别能力,并且在一定浓度范围内能抑制细胞内HCV的复制[37]。
骆驼乳中含有的乳酸菌等益生菌可以改善小鼠体内的免疫应答反应,达到抗病菌抗感染的作用。益生菌是具有特殊特性的共生体,对免疫系统的发展至关重要,并可能保护黏膜表面免受病原体的侵害。有研究从沙特阿拉伯(麦加地区)和埃及(法尤姆)采集的不同原料和发酵骆驼奶样品中分离出几十株乳酸菌,并展现出良好的益生菌潜力,对多种食源性病原菌和皮肤真菌均表现出抑菌活性,体内研究表明,这些菌株通过增加小鼠肠道中Toll样受体(Toll-like receptor,TLR)2和干扰素(interferon,IFN)-γ mRNA的表达,并增加了小鼠血清中多克隆IgG、IgM和IgA的合成,显著改善了黏膜免疫应答[38]。
2.2.4 调节肠道菌群微生态
过去一二十年的研究让我们充分认识到肠道菌群的结构组成与肠道微生态平衡是宿主健康的基石,肠道菌群失调可引发多种疾病的发生或加重其进展。骆驼乳对肠道菌群微生态具有显著调节作用,据研究骆驼乳可以降低肠道微生物群中Romboutsia、乳杆菌、苏黎世杆菌和脱硫弧菌的相对丰度,但肠道菌群中的某些属,如别样棒菌、阿克曼氏菌和双歧杆菌相对丰度在骆驼乳的存在下大量增加,而这些属对生物体具有有益作用[10]。
3 骆驼乳在预防疾病中的应用及作用机制研究进展
骆驼乳传统上被认为具有药用特性,近年来的研究显示骆驼乳可缓解多种疾病(包括糖尿病、高血压、癌症、自闭症谱系障碍(autistic spectrum disorder,ASD)、肾脏及肝脏损伤等)(图1)。下文将分别汇总骆驼乳预防或帮助缓解这些疾病的研究进展(表4)。
图1 骆驼乳有潜在预防或治疗效果的疾病种类
Fig.1 Camel milk has potential therapeutic effects on several diseases
表4 骆驼乳在疾病预防中的作用及机制研究进展
Table 4 Recent progress in the therapeutic effects and mechanisms of action of camel milk on diseases

疾病 实验对象 实验结论 年份 参考文献糖尿病印度人群 经常饮用骆驼乳的骆驼饲养者和饲养部落患糖尿病的风险更低 2014 [39]四氧嘧啶诱导的糖尿病犬 骆驼乳对糖尿病犬的血糖、血脂水平等指标均有改善作用 2010 [40]糖尿病大鼠 骆驼乳提高了糖尿病大鼠伤口愈合的潜力 2015 [25]链脲霉素(streptozotocin,STZ)诱导的糖尿病鼠骆驼乳蛋白在伤口愈合中的有益作用和β-防御素2和3的表达相关 2013 [41]人胚胎肾(human embryonic kidney,HEK)293细胞 CWP可激活人胰岛素受体 2021 [42]HEK293细胞骆驼乳显著增强了胰岛素诱导的下游信号蛋白激酶B(protein kinase B,Akt)和细胞外调节蛋白激酶1/2(extracellular regulated protein kinase 1/2,ERK1/2)的激活2016 [43]肾脏损伤甲氨蝶呤(methotrexate,MTX)致肾损伤大鼠骆驼乳可以通过激活磷脂酰肌醇-3-激酶/Akt/内皮型一氧化氮合酶(phosphatidylinositol 3-kinase/Akt/endothelial nitric oxide synthase,PI3K/Akt/eNOS)信号和抗氧化作用来减轻MTX诱导的肾脏损伤2018 [27]5-氟尿嘧啶致肾损伤大鼠 骆驼乳对5-氟尿嘧啶诱导的肾损伤具有改善作用 2018 [44]硫代乙酰胺(thioacetamide,TAA)诱导致肝肾损伤大鼠 骆驼乳对TAA诱导的肝肾毒性有改善作用 2018 [45]肝脏损伤 酒精诱导肝损伤小鼠 骆驼乳可以提高小鼠肠道益生菌属的相对丰度,改善肠道微生态平衡,减轻酒精对小鼠肠道的损害 2020 [46]四氯化碳诱导肝硬化大鼠 骆驼乳可以改善四氯化碳诱导的肝硬化 2016 [47]癌症结直肠癌HCT-116和乳腺癌MCF-7细胞系骆驼乳通过诱导自噬,对人结直肠HCT-116和乳腺MCF-7癌细胞具有抗增殖作用 2018 [48]乳腺癌MCF-7细胞系 骆驼乳及其外泌体对MCF-7乳腺癌细胞具有抗癌潜力 2018 [49]ASD儿童 骆驼乳调节了抗氧化酶和非酶抗氧化物质的水平,进而降低氧化应激的影响,改善心理症状 2013 [50]自闭症患儿 骆驼乳治疗2 周可明显改善自闭症患儿的临床症状 2014 [51]丙戊酸钠诱导妊娠雌性大鼠的子代孤独症大鼠模型 骆驼乳可改善患有孤独症大鼠的各项指标 2018 [52]高血压 自发性高血压大鼠 发酵脱脂骆驼乳在短期内显著降低了自发性高血压大鼠的收缩压和舒张压 2017 [53]高盐诱导高血压大鼠 骆驼乳改善了高盐诱导的大鼠高血压 2016 [54]
3.1 抗糖尿病
糖尿病是一组以高血糖为特征的慢性代谢紊乱疾病,其核心病理基础是胰岛素抵抗,无法根治且患病率逐年增高[55]。已知骆驼乳低糖低脂,并含有较高浓度的胰岛素,有改善糖尿病的潜能[15,56]。1型糖尿病患者食用骆驼乳可以改善高血糖症状并减少胰岛素剂量[57]。事实上,其他使用1型或2型糖尿病动物模型(大鼠、兔子和狗)以及糖尿病患者的体内和体外研究也证实了骆驼乳对糖尿病治疗的有益作用,包括降低血糖、增加胰岛素分泌、降低胰岛素抵抗和改善血脂状况[19,40]。并且,根据印度进行的一项以人群为基础的研究,与其他不喝骆驼乳的社区相比,经常饮用骆驼乳的骆驼饲养者和饲养部落患糖尿病的风险更低[39]。此外,对牛乳中胰岛素样蛋白含量的比较研究表明,骆驼乳中胰岛素样蛋白含量是牛乳的3 倍[15]。2型糖尿病大鼠摄入骆驼乳后可改善高血糖、糖耐量异常、血脂紊乱等糖脂代谢异常的症状[15]。
骆驼乳的抗糖尿病特性的具体作用机理涉及许多分子和细胞机制,包括糖代谢和转运方面,以及胰岛素的合成和分泌[58]。从细胞和分子的层面来看,骆驼乳可能同时在不同的水平起作用,第一,影响胰岛细胞的存活、生长和整体活性;第二,直接或间接影响胰腺细胞的胰岛素分泌;第三,影响胰岛素受体功能和胰岛素敏感组织中的葡萄糖转运。例如,有研究显示,与对照组患者和动物相比,给患者和动物(大鼠和兔子)喂食骆驼乳可以恢复胰岛素合成和释放。这可能意味着骆驼乳对胰腺细胞功能具有不同水平和方式的作用,包括刺激胰岛素的合成和释放以及防止胰腺细胞的损伤和凋亡[15]。此外,骆驼乳抗糖尿病作用的一种可能机制可以归因于抑制与糖尿病进展相关的代谢酶活性,例如骆驼乳蛋白可以水解产生独特的二肽基肽酶(dipeptidyl peptidase IV,DPP-IV)抑制肽段,在人体中产生抗糖尿病特性[42,59]。除此之外,骆驼乳对胰岛素受体具有变构作用从而调节其激活状态,进而对其细胞内信号传导产生不同的影响[15]。有研究使用生物发光能量转移(bioluminescence resonance energy transfer,BRET)技术发现,在人胚胎肾(human embryonic kidney,HEK)293细胞中,胰岛素和CWP均会促进人胰岛素受体(human insulin receptor,hIR)和胰岛素受体底物1(insulin receptor substrate 1,IRS1)之间的BRET信号强度呈剂量依赖性增加,说明胰岛素和CWP均可激活hIR,并且CWP可诱导HEK293和人肝癌(human hepatoellular carcinomas,HepG2)细胞中Akt和ERK1/2磷酸化,通过对hIR的正向变构调节,激活下游代谢通路,同时hIR选择性拮抗剂S961显著抑制了胰岛素诱导的BRET升高,而非CWP诱导的BRET升高,提示了CWP抗糖尿病的分子基础可能并不依赖于hIR[42]。同样是利用BRET技术,对阿拉伯骆驼(Camelus dromedarius)的研究显示,在没有胰岛素刺激的情况下,骆驼乳不会促进hIR和IRS1之间的BRET信号强度的增加,但会显著增强hIR和生长因子受体结合蛋白2之间由胰岛素刺激的BRET信号,这提示了另一种骆驼乳抗糖尿病的可能机理[43]。
骆驼乳中含有丰富的不饱和脂肪酸,尤其是亚麻酸(C18:3)质量分数(5.09%)明显高于牛乳(0.36%)、羊乳(0.34%)、人乳(2.96%)[60]。亚麻酸属n-3多不饱和脂肪酸,和胰岛素激活剂有相似作用机理,能促进胰岛素分泌,有效调节血糖。因此,骆驼乳与牛乳、羊乳、人乳等动物奶相比,具有更好的辅助治疗糖尿病和缓解糖尿病引起的并发症的效果[60]。
此外,对于糖尿病患者来说,高血糖容易引起细菌感染、周围神经病变和炎症反应的增加,这些都使糖尿病患者容易发生溃疡且难以愈合,严重者甚至导致脓毒症和截肢[61]。研究显示,骆驼乳在糖尿病动物(小鼠和大鼠)中提高了伤口愈合的潜力。这可能是由于CWP的抗氧化活性促进了免疫细胞的增殖,加速了糖尿病期间发生的伤口愈合过程,同时也意味着氧化和炎症过程的减弱[25]。有报道显示,骆驼乳对消炎霉素诱导的胃损伤及导致的溃疡有较强的促愈合作用[62]。另一项研究发现骆驼乳蛋白在伤口愈合中的有益作用与β-防御素2和3的表达相关[41],同时这些蛋白具有一定的抗菌特性且对伤口修复和免疫细胞有刺激作用。以上研究表明,骆驼乳蛋白在糖尿病伤口的免疫调节中的应用可能很有前景[15]。
3.2 保护肾脏
肾脏是分泌尿液、排泄代谢废物和毒物的重要器官,肾脏受损则会导致肾功能下降甚至衰竭。研究表明骆驼乳对肾脏损伤有一定的保护作用。
骆驼乳可以减轻MTX诱导的肾脏损伤。MTX作为一种经典的叶酸拮抗剂,通常用作治疗多种恶性肿瘤(包括乳腺癌、骨肉瘤、淋巴瘤、头颈癌),具有严重的肾毒性副作用,可造成从亚临床肾小管病变到急性肾损伤的肾脏损害。有研究显示,驼乳可以通过激活PI3K/Akt/eNOS信号,对抗氧化应激,降低脂质过氧化物、恢复烟酰胺腺嘌呤二核苷酸磷酸氧化酶-1(nicotinamide adenine dinucleotide phosphate oxidase-1,NOX-1)水平,增强大鼠肾脏抗氧化的能力,从而减轻肾凋亡细胞死亡来起到肾脏保护作用[27]。
骆驼乳对5-氟尿嘧啶诱导的肾损伤具有肾保护作用。在5-氟尿嘧啶引起的肾脏损伤中,骆驼乳可以抑制肌酐、肾损伤分子(kidney injury molecule,KIM)-1和嗜中性粒细胞明胶酶相关的脂钙蛋白等肾损伤相关生物标志物水平的升高;并能抑制氧化应激,增强肾脏抗氧化能力,恢复NOX-1、核因子E2相关因子2(nuclear factor erythrocyte 2 related factor 2,Nrf-2)和血红素氧化酶1(heme oxidase 1,HO-1)水平;骆驼乳还能抑制肾炎症反应,抑制髓过氧化物酶、TNF、IL-1、IL-18和单核细胞趋化蛋白1(monocyte chemoattractant protein 1,MCP-1)等促炎因子水平,上调IL-10水平,下调基质金属蛋白酶-2(matrix metalloprotein-2,MMP-2)和MMP-9的表达[44]。
此外,还有研究证明骆驼乳对硫代乙酰胺(thioacetamide,TAA)诱导的肝肾毒性有改善作用,在皮下注射TAA后,TAA中毒大鼠血清中丙氨酸转氨酶、天门冬氨酸转氨酶、γ-谷酰胺转肽酶、碱性磷酸酶、尿素、肌酐、尿酸、钠、钾等指标水平显著增高,而骆驼乳组的大鼠的血清生化指标和脂质指标均下降并趋于正常水平,相关组织病理学的证据也表明了骆驼乳对于TAA中毒大鼠的肝肾保护作用[45]。
3.3 保护肝脏
酒精性肝病(alcoholic liver disease,ALD)在世界范围内的发病率逐年攀升。急性酒精摄入会导致小鼠结肠内肠道微生态失衡,包括乳杆菌的相对丰度显著降低和拟杆菌的丰度增高,而肠道菌群在酒精性肝损伤中发挥关键介导作用。骆驼乳的干预可以显著提高乳杆菌的相对丰度并降低拟杆菌相对丰度;从菌群整体的角度来看,骆驼乳可以通过提高小鼠肠道益生菌属的相对丰度,改善肠道微生态平衡,减轻酒精对小鼠肠道的损害,预防肠道菌群的失衡;对于ALD小鼠,骆驼乳的摄入可下调IL-17和TNF-α通路中炎症相关基因的表达,缓解ALD小鼠的肝脏炎症症状,达到肝脏保护的作用[46]。
骆驼乳对四氯化碳诱导的肝脏损伤也有一定的保护作用。用四氯化碳诱导大鼠肝硬化会显著降低肝脏组织磷酸化酶活性,显著增加碳水化合物不耐受和胰岛素抵抗指数。此外,四氯化碳诱导也会导致氧化应激的显著增加以及促纤维化细胞因子基因TNF-α和TGF-β表达的增加。骆驼乳可以改善与肝脏损伤相关的生化指标,作用的机制可能涉及到促纤维化细胞因子的转录调控以及氧化还原状态的改善,而促纤维化细胞因子参与肝硬化的诱导,氧化状态的改善参与肝纤维化的发病机制[47]。
3.4 抗癌症
化疗是癌症的主要治疗方式,虽然能够杀死肿瘤细胞,但对正常细胞也有严重的副作用。天然食品中也含有一些具有抗肿瘤作用的活性功能因子,其安全性很高,毒副作用极低甚至没有,这方面的研究一直是领域内的热点。一些体外研究报道了骆驼乳的抑癌作用,骆驼乳及其衍生的外泌体可在人结直肠癌细胞系HCT-116和乳腺癌细胞系MCF-7中发挥诱导自噬、促进凋亡、抗肿瘤细胞增殖的作用[48]。
也有研究评估了骆驼乳及其外泌体对MCF-7乳腺癌细胞的抗癌潜力,发现使用骆驼乳衍生的外泌体比使用骆驼乳有更好的抗癌效果,并且局部注射外泌体比口服治疗效果更好;骆驼乳及其外泌体在肿瘤微环境中可能通过诱导细胞凋亡以及抑制氧化应激、炎症、血管生成和转移等作用发挥抗癌作用;这些研究结果提示骆驼乳及其外泌体可应用于癌症治疗[49]。
3.5 抗ASD
ASD是一种严重的神经发育障碍,其特征是患者存在社交取向、沟通和重复行为方面的障碍。在一些地区,骆驼乳用于自闭症治疗[3]。在沙特阿拉伯对60 名自闭症患者(2~12岁)进行的一项研究中,研究人员对儿童进行了为期两周、每天两次、每次500 mL的乳汁喂养,以评估骆驼乳和牛乳的效果。在分析初始阶段,所有儿童的抗氧化分子水平都很低。两周后,骆驼乳显著改善了认知和行为测试。研究人员发现,骆驼乳调节了抗氧化酶和非酶抗氧化物质的水平,进而降低氧化应激的影响,改善心理症状[50]。这项研究提示骆驼乳可能通过改善氧化应激来改善自闭症症状。除了蛋白质,骆驼乳所含的高水平的维生素和矿物质,如铁、钠、铜、钾、镁及大量的VC可以作为抗氧化剂抑制自由基。在2014年进行的一项调查中,对自闭症儿童服用骆驼乳2 周后的氧化应激生物标志物(谷胱甘肽、超氧化物歧化酶和髓过氧化物酶)水平进行了评估,数据分析表明,所有参数均显著提高,提示骆驼乳可以通过提升抗氧化酶和非酶抗氧化分子水平,降低氧化应激作用[32]。此外,另一项研究也显示骆驼乳治疗2 周可明显改善自闭症患儿的临床症状,同时降低了血清胸腺和激活调节趋化因子(thymus and activation-regulated chemokine,TRAC)水平[51]。
有研究人员采用丙戊酸钠诱导妊娠雌性大鼠的子代孤独症大鼠模型,研究骆驼乳对于自闭症的改善作用,结果发现,与对照组相比,经骆驼乳治疗的自闭症动物组的所有检测指标和基因表达量均有显著改善,包括自闭症大鼠的氧化应激标志物、神经递质和炎症细胞因子等;这表明驼乳作为一种潜在的治疗自闭症的药物可能是通过调节子代自闭症大鼠的氧化应激、炎症和凋亡通路来改善自闭症行为[52]。
3.6 抗高血压
高血压是世界范围内最常见的疾病之一,防治高血压对降低心血管疾病风险具有重要意义。研究显示,发酵脱脂骆驼乳在短期内(24 h)对自发性高血压大鼠的收缩压和舒张压均有显著降低,且骆驼乳中含有在发酵过程中释放的抑制血管紧张素转化酶(angiotensin converting enzyme,ACE)的活性肽[53]。还有一项研究在高盐诱导大鼠高血压模型中详细研究了骆驼乳对血压的改善作用,该研究将实验动物随机分为4 组,I组正常喂养,II组8%盐饮食喂养10 周,III组8%盐饮食喂养10 周,并加喂驼乳(5 mL/(kggd)),IV组8%盐饮食喂养10 周,并使其口服100 mg/kg的二甲双胍和10 mg/kg的硝苯地平;对比II组和III组,饮用骆驼乳的实验组大鼠收缩压明显下降,血压值由140 mm汞柱降至121 mm汞柱,心率由486 次/min降至384 次/min;这可能是因为骆驼乳中存在ACE抑制肽前体,可以减轻ACE对血压的影响,从而降低血压;同时在该研究中,盐负荷大鼠血浆总胆固醇、甘油三酯、低密度脂蛋白胆固醇和极低密度脂蛋白胆固醇水平均有升高,且高密度脂蛋白胆固醇水平明显降低;这些血脂异常的表现可能归因于循环中钠浓度的增加激活了交感神经系统,以及通过盐皮质激素受体发出的信号强度增加,导致活性氧的产生量增加,从而导致氧化应激,最终导致血脂异常,经骆驼乳处理后,上述变化得以恢复正常[54]。
4 骆驼乳衍生品与功能食品开发
骆驼乳也可衍生出多种驼乳制品,如驼乳奶粉、驼乳酸奶、驼乳奶酪、驼乳奶油、驼乳奶片、驼乳乳饮料、驼乳奶糖、驼乳冰淇淋、驼乳奶茶等。这些功能食品因驼乳的特性也具备了特殊的功能和价值。比如,最近有研究发现骆驼益生菌发酵乳具有抗糖尿病作用,通过诱导胰高血糖素样肽-1(glucagon-like peptide-1,GLP-1)分泌改善肠道屏障功能,该团队从发酵骆驼乳中分离出14种益生菌,这些益生菌都具有有益特性[63]。
值得特别一提的是CMPH,研究发现,与未水解骆驼乳蛋白相比,CMPH的乳化活性指数、表面疏水性和蛋白质溶解度等功能性指标均有改善;与未水解骆驼乳蛋白相比,CMPH对水分和脂肪的吸收能力较低[31]。在真实的食品模型系统中测试CMPH抑制鱼糜和葡萄籽油水乳状液中脂质过氧化的能力,结果显示CMPH对脂质过氧化具有抑制作用[31]。除此之外,还有研究显示CWP水解物对人肝癌HepG2细胞具有潜在的抗肿瘤活性,且具有剂量依赖性;CWP水解后其抗肝癌细胞增殖、抗糖尿病和抗炎活性均增强[64]。这些研究提示,CMPH作为一种食品原料,具有改良食品性状、增强食品体系抗氧化能力以及增强的生物活性等特性,在食品工业和功能保健食品或特殊医学膳食中具有独特的应用价值。
5 结 语
本文综述了骆驼乳各类营养素的基本组成、与牛乳及其他乳类的差别,及其在疾病体系中发挥有益功效的相关研究进展,并分析了骆驼乳医药应用价值的生物作用基础。作为高营养价值的乳类,骆驼乳目前已被发现在帮助缓解多种疾病包括糖尿病、高血压、肝肾损伤、肿瘤及自闭症方面均有效果,骆驼乳及其衍生品在功能食品开发方面具有广泛的应用前景。但现有研究更多集中于细胞模型或动物模型,且对于骆驼乳及其所含营养物质帮助缓解疾病的具体作用机制缺乏深入解析。以骆驼乳研究较多的抗糖尿病功效为例,尽管在人和动物模型中已有不少证据表明骆驼乳可改善葡萄糖稳态,但这些研究在解释骆驼乳具体而确切的抗糖尿病机理和鉴别骆驼乳中所含有效抗糖尿病成分方面仍不深入。同样的,骆驼乳在保护肾脏、保护肝脏、抗癌、抗ASD和抗高血压等方面的有益效果的作用机制仍需进一步阐明。因此,领域内学者对骆驼乳应用范围及作用机制的进一步研究将有助于骆驼乳功能食品开发以及药物潜能的发掘。
骆驼乳因其在营养组成上与其他种类乳的明显区别及其在医学应用潜能上的优势,得到越来越广泛的关注、认可与青睐。当前,骆驼乳产业正在成为乳业中冉冉升起的一颗新星。据国家统计局数据显示,2000年我国骆驼期末数量为32.62万 峰,2009年降至最低点22.59万 峰,2010~2019年数量开始逐年增加,2019年达到40.53万 峰。由于骆驼乳收集有一定难度,受骆驼养殖范围、养殖规范性要求等因素的限制,骆驼乳产量较低。目前我国具有骆驼乳加工能力的企业数量较少,行业尚未形成大规模生产,骆驼乳的乳源可能成为骆驼乳相关行业发展的关键限制因素。
[1] GIZACHEW A, TEHA J, BIRHANU T.Review on medicinal and nutritional values of camel milk[J].Nature and Science, 2014, 12(12):35-40.
[2] MABOOD F, JABEEN F, AHMED M, et al.Development of new NIR-spectroscopy method combined with multivariate analysis for detection of adulteration in camel milk with goat milk[J].Food Chemistry, 2017, 221: 746-750.DOI:10.1016/j.foodchem.2016.11.109.
[3] ZIBAEE S, HOSSEINI S M A R, YOUSEFI M, et al.Nutritional and therapeutic characteristics of camel milk in children: a systematic review[J].Electronic Physician, 2015, 7(7): 1523-1528.DOI:10.19082/1523.
[4] ABDOUN K A, AMIN A S A, ABDELATIF A M.Milk composition of dromedary camels (Camelus dromedarius): nutritional effects and correlation to corresponding blood parameters[J].Pakistan Journal of Biological Sciences,2007, 10(16): 2724-2727.DOI:10.3923/pjbs.2007.2724.2727.
[5] KONUSPAYEVA G, FAYE B, LOISEAU G.The composition of camel milk: a meta-analysis of the literature data[J].Journal of Food Composition & Analysis, 2009, 22(2): 95-101.DOI:10.1016/j.jfca.2008.09.008.
[6] 邵伍军, 梁剑平, 余四九, 等.FAAS法测定骆驼奶中矿物元素的含量[J].中兽医医药杂志, 2007, 26(3): 42-43.DOI:10.3969/j.issn.1000-6354.2007.03.018.
[7] HAILU Y, HANSEN E B, SEIFU E, et al.Functional and technological properties of camel milk proteins: a review[J].The Journal of Dairy Research, 2016, 83(4): 422-429.DOI:10.1017/S0022029916000686.
[8] ZHANG H, YAO J, ZHAO D, et al.Changes in chemical composition of Alxa bactrian camel milk during lactation[J].Journal of Dairy Science, 2005, 88(10): 3402-3410.DOI:10.3168/jds.S0022-0302(05)73024-1.
[9] BOUHADDAOUI S, CHABIR R, ERRACHIDI F, et al.Study of the biochemical biodiversity of camel milk[J].The Scientific World Journal, 2019, 2019: 1-7.DOI:10.1155/2019/2517293.
[10] WANG Z X, ZHANG W Y, WANG B N, et al.Influence of bactrian camel milk on the gut microbiota[J].Journal of Dairy Science, 2018,101(7): 5758-5769.DOI:10.3168/jds.2017-13860.
[11] 李超颖, 张娟, 卿德刚, 等.骆驼乳营养成分及生物活性研究进展[J].食品工业科技, 2014, 35(23): 387-391; 396.
[12] HE J, XIAO Y, ORGOLDOL K, et al.Effects of geographic region on the composition of bactrian camel milk in mongolia[J].Animals, 2019,9(11): 890.DOI:10.3390/ani9110890.
[13] MAQSOOD S, AL-DOWAILA A, MUDGIL P, et al.Comparative characterization of protein and lipid fractions from camel and cow milk, their functionality, antioxidant and antihypertensive properties upon simulated gastro-intestinal digestion[J].Food Chemistry, 2019,279: 328-338.DOI:10.1016/j.foodchem.2018.12.011.
[14] KONUSPAYEVA G, LEMARIE É, FAYE B, et al.Fatty acid and cholesterol composition of camel’s (Camelus bactrianus, Camelus dromedarius and hybrids) milk in Kazakhstan[J].Dairy Science and Technology, 2008, 88(3): 327-340.DOI:10.1051/dst:2008005.
[15] AYOUB M A, PALAKKOTT A R, ASHRAF A, et al.The molecular basis of the anti-diabetic properties of camel milk[J].DiabetesResearch and Clinical Practice, 2018, 146: 305-312.DOI:10.1016/j.diabres.2018.11.006.
[16] MARYNIAK N Z, HANSEN E B, BALLEGAARD A S R, et al.Comparison of the allergenicity and immunogenicity of camel and cow’s milk: a study in brown norway rats[J].Nutrients, 2018, 10(12):1903.DOI:10.3390/nu10121903
[17] EHLAYEL M S, HAZEIMA K A, AL-MESAIFRI F, et al.Camel milk:an alternative for cow’s milk allergy in children[J].Allergy and Asthma Proceedings, 2011, 32(3): 255-258.DOI:10.2500/aap.2011.32.3429.
[18] 宋宏新, 张小苗, 薛海燕.牛羊乳蛋白组分比较研究[J].中国酿造,2012, 31(2): 21-23.
[19] SHORI A B.Camel milk as a potential therapy for controlling diabetes and its complications: a review of in vivo studies[J].Journal of Food and Drug Analysis, 2015, 23(4): 609-618.DOI:10.1016/j.jfda.2015.02.007.
[20] RASHEED Z.Medicinal values of bioactive constituents of camel milk: a concise report[J].International Journal of Health Sciences,2017, 11(5): 1-2.
[21] MOHAMED W A, SCHAALAN M F.Antidiabetic efficacy of lactoferrin in type 2 diabetic pediatrics; controlling impact on PPAR-γ,SIRT-1, and TLR4 downstream signaling pathway[J].Diabetology &Metabolic Syndrome, 2018, 10: 89.DOI:10.1186/s13098-018-0390-x.
[22] RYSKALIYEVA A, HENRY C, MIRANDA G, et al.The main WAP isoform usually found in camel milk arises from the usage of an improbable intron cryptic splice site in the precursor to mRNA in which a GC-AG intron occurs[J].BMC Genetics, 2019, 20(1): 14.DOI:10.1186/s12863-018-0704-x.
[23] IBRAHIM H R, ISONO H, MIYATA T.Potential antioxidant bioactive peptides from camel milk proteins[J].Animal Nutrition, 2018, 4(3):273-280.DOI:10.1016/j.aninu.2018.05.004.
[24] IBRAHIM H M, MOHAMMED-GEBA K, TAWFIC A A, et al.Camel milk exosomes modulate cyclophosphamide-induced oxidative stress and immuno-toxicity in rats[J].Food & Function, 2019, 10(11): 7523-7532.DOI:10.1039/c9fo01914f.
[25] EBAID H, ABDEL-SALAM B, HASSAN I, et al.Camel milk peptide improves wound healing in diabetic rats by orchestrating the redox status and immune response[J].Lipids in Health and Disease, 2015,14: 132.DOI:10.1186/s12944-015-0136-9.
[26] HABIB H M, IBRAHIM W H, SCHNEIDER-STOCK R, et al.Camel milk lactoferrin reduces the proliferation of colorectal cancer cells and exerts antioxidant and DNA damage inhibitory activities[J].Food Chemistry, 2013, 141(1): 148-152.DOI:10.1016/j.foodchem.2013.03.039.
[27] ARAB H H, SALAMA S A, MAGHRABI I A.Camel milk attenuates methotrexate-induced kidney injury via activation of PI3K/Akt/eNOS signaling and intervention with oxidative aberrations[J].Food &Function, 2018, 9(5): 2661-2672.DOI:10.1039/c8fo00131f.
[28] SALAMI M, MOOSAVI-MOVAHEDI A A, MOOSAVI-MOVAHEDI F, et al.Biological activity of camel milk casein following enzymatic digestion[J].The Journal of Dairy Research, 2011, 78(4): 471-478.DOI:10.1017/S0022029911000628.
[29] KUMAR D, CHATLI M K, SINGH R, et al.Enzymatic hydrolysis of camel milk casein and its antioxidant properties[J].Dairy Science &Technology, 2016, 96(3): 391-404.DOI:10.1007/s13594-015-0275-9.
[30] SALAMI M, MOOSAVI-MOVAHEDI A A, EHSANI M R, et al.Improvement of the antimicrobial and antioxidant activities of camel and bovine whey proteins by limited proteolysis[J].Journal of Agricultural and Food Chemistry, 2010, 58(6): 3297-3302.DOI:10.1021/jf9033283.
[31] AL-SHAMSI K A, MUDGIL P, HASSAN H M, et al.Camel milk protein hydrolysates with improved technofunctional properties and enhanced antioxidant potential in in vitro and in food model systems[J].Journal of Dairy Science, 2018, 101(1): 47-60.DOI:10.3168/jds.2017-13194.
[32] HOMAYOUNI-TABRIZI M, ASOODEH A, SOLTANI M.Cytotoxic and antioxidant capacity of camel milk peptides: effects of isolated peptide on superoxide dismutase and catalase gene expression[J].Journal of Food and Drug Analysis, 2017, 25(3): 567-575.DOI:10.1016/j.jfda.2016.10.014.
[33] ZHU W W, KONG G Q, MA M M, et al.Short communication: camel milk ameliorates inflammatory responses and oxidative stress and downregulates mitogen-activated protein kinase signaling pathways in lipopolysaccharide-induced acute respiratory distress syndrome in rats[J].Journal of Dairy Science, 2016, 99(1): 53-56.DOI:10.3168/jds.2015-10005.
[34] ARAB H H, SALAMA S A, EID A H, et al.Camel’s milk ameliorates TNBS-induced colitis in rats via downregulation of inflammatory cytokines and oxidative stress[J].Food and Chemical Toxicology,2014, 69: 294-302.DOI:10.1016/j.fct.2014.04.032.
[35] YAGIL R.Camel milk and its unique anti-diarrheal properties[J].The Israel Medical Association Journal, 2013, 15(1): 35-36.
[36] EL-FAKHARANY E M, EL-BAKY N A, LINJAWI M H, et al.Influence of camel milk on the hepatitis C virus burden of infected patients[J].Experimental and Therapeutic Medicine, 2017, 13(4):1313-1320.DOI:10.3892/etm.2017.4159.
[37] EL-FAKHARANY E M, ABEDELBAKY N, HAROUN B M, et al.Anti-infectivity of camel polyclonal antibodies against hepatitis C virus in Huh7.5 hepatoma[J].Virology Journal, 2012, 9: 201.DOI:10.1186/1743-422X-9-201.
[38] ELBANNA K, EL HADAD S, ASSAEEDI A, et al.In vitro and in vivo evidences for innate immune stimulators lactic acid bacterial starters isolated from fermented camel dairy products[J].Scientific Reports, 2018, 8(1): 12553.DOI:10.1038/s41598-018-31006-3.
[39] BHAT D K, KANGA U, KUMAR N, et al.The Raikas: a unique combination of high prevalence of type 1 diabetes susceptibility genes and near zero incidence of the disease[J].Human Immunology, 2014,75(12): 1252-1258.DOI:10.1016/j.humimm.2014.09.009.
[40] SBOUI A, KHORCHANI T, DJEGHAM M, et al.Anti-diabetic effect of camel milk in alloxan-induced diabetic dogs: a dose-response experiment[J].Journal of Animal Physiology and Animal Nutrition,2010, 94(4): 540-546.DOI:10.1111/j.1439-0396.2009.00941.x.
[41] BADR G.Camel whey protein enhances diabetic wound healing in a streptozotocin-induced diabetic mouse model: the critical role of β-defensin-1, -2 and -3[J].Lipids in Health and Disease, 2013, 12: 46.DOI:10.1186/1476-511X-12-46.
[42] ASHRAF A, MUDGIL P, PALAKKOTT A, et al.Molecular basis of the anti-diabetic properties of camel milk through profiling of its bioactive peptides on dipeptidyl peptidase IV (DPP-IV) and insulin receptor activity[J].Journal of Dairy Science, 2021, 104(1): 61-77.DOI:10.3168/jds.2020-18627.
[43] ABDULRAHMAN A O, ISMAEL M A, AL-HOSAINI K, et al.Differential effects of camel milk on insulin receptor signaling: toward understanding the insulin-like properties of camel milk[J].Frontiers in Endocrinology, 2016, 7: 4.DOI:10.3389/fendo.2016.00004.
[44] ARAB H H, SALAMA S A, MAGHRABI I A.Camel milk ameliorates 5-fluorouracil-induced renal injury in rats: targeting MAPKs, NF-κB and PI3K/Akt/eNOS pathways[J].Cellular Physiology and Biochemistry, 2018, 46(4): 1628-1642.DOI:10.1159/000489210.
[45] AHMAD A, AL-ABBASI F A, SADATH S, et al.Ameliorative effect of camel’s milk and oil against thioacetamide-induced hepatorenal damage in rats[J].Pharmacognosy Magazine, 2018, 14(53): 27-35.DOI:10.4103/pm.pm_132_17.
[46] MING L, QIAO X Y, YI L, et al.Camel milk modulates ethanolinduced changes in the gut microbiome and transcriptome in a mouse model of acute alcoholic liver disease[J].Journal of Dairy Science,2020, 103(5): 3937-3949.DOI:10.3168/jds.2019-17247.
[47] SADEK K, BELTAGY D, SALEH E, et al.Camel milk and bee honey regulate profibrotic cytokine gene transcripts in liver cirrhosis induced by carbon tetrachloride[J].Canadian Journal of Physiology and Pharmacology, 2016, 94(11): 1141-1150.DOI:10.1139/cjpp-2015-0596.
[48] KRISHNANKUTTY R, ISKANDARANI A, THERACHIYIL L, et al.Anticancer activity of camel milk via induction of autophagic death in human colorectal and breast cancer cells[J].Asian Pacific Journal of Cancer Prevention, 2018, 19(12): 3501-3509.DOI:10.31557/APJCP.2020.21.5.1495.
[49] BADAWY A A, EL-MAGD M A, ALSADRAH S A.Therapeutic effect of camel milk and its exosomes on MCF7 cells in vitro and in vivo[J].Integrative Cancer Therapies, 2018, 17(4): 1235-1246.DOI:10.1177/1534735418786000.
[50] AL-AYADHI L Y, ELAMIN N E.Camel milk as a potential therapy as an antioxidant in autism spectrum disorder (ASD)[J].Evidence-Based Complementary and Alternative Medicine, 2013, 2013: 602834.DOI:10.1155/2013/602834.
[51] BASHIR S, AL-AYADHI L Y.Effect of camel milk on thymus and activation-regulated chemokine in autistic children: double-blind study[J].Pediatric Research, 2014, 75(4): 559-563.DOI:10.1038/pr.2013.248.
[52] HAMZAWY M A, EL-GHANDOUR Y B, ABDEL-AZIEM S H, et al.Leptin and camel milk abate oxidative stress status, genotoxicity induced in valproic acid rat model of autism[J].International Journal of Immunopathology and Pharmacology, 2018, 32: 1-11.DOI:10.1177/2058738418785514.
[53] YAHYA M A, ALHAJ O A, AL-KHALIFAH A S.Antihypertensive effect of fermented skim camel (Camelus dromedarius) milk on spontaneously hypertensive rats[J].Nutricion Hospitalaria, 2017,34(2): 416-421.DOI:10.20960/nh.116S3.
[54] MAINASARA A S, ISA S A, DANDARE A, et al.Blood pressure profile and insulin resistance in salt-induced hypertensive rats treated with camel milk[J].Mediterranean Journal of Nutrition and Metabolism, 2016, 9: 75-83.DOI:10.3233/MNM-160060.
[55] American Diabetes Association.Diagnosis and classification of diabetes mellitus[J].Diabetes Care, 2013, 36(Suppl 1): S67-S74.DOI:10.2337/dc13-S067.
[56] KORISH A A, ABDEL GADER A G M, ALHAIDER A A.Comparison of the hypoglycemic and antithrombotic (anticoagulant)actions of whole bovine and camel milk in streptozotocin-induced diabetes mellitus in rats[J].Journal of Dairy Science, 2020, 103(1): 30-41.DOI:10.3168/jds.2019-16606.
[57] AGRAWAL R P, JAIN S, SHAH S, et al.Effect of camel milk on glycemic control and insulin requirement in patients with type 1 diabetes: 2-years randomized controlled trial[J].European Journal of Clinical Nutrition, 2011, 65(9): 1048-1052.DOI:10.1038/ejcn.2011.98.
[58] MIHIC T, RAINKIE D, WILBY K J, et al.The therapeutic effects of camel milk: a systematic review of animal and human trials[J].Journal of Evidence-Based Complementary & Alternative Medicine, 2016,21(4): NP110-NP126.DOI:10.1177/2156587216658846.
[59] NONGONIERMA A B, PAOLELLA S, MUDGIL P, et al.Identification of novel dipeptidyl peptidase IV (DPP-IV) inhibitory peptides in camel milk protein hydrolysates[J].Food Chemistry, 2018,244: 340-348.DOI:10.1016/j.foodchem.2017.10.033.
[60] 王曙阳.骆驼奶活性成分评价及对Ⅱ型糖尿病辅助治疗作用的研究[D].兰州: 甘肃农业大学, 2011: 20-32.
[61] AUGUSTINE R, HASAN A, DALVI Y B, et al.Growth factor loaded in situ photocrosslinkable poly(3-hydroxybutyrate-co-3-hydroxyvalerate)/gelatin methacryloyl hybrid patch for diabetic wound healing[J].Materials Science & Engineering C, Materials for Biological Applications, 2021, 118: 111519.DOI:10.1016/j.msec.2020.111519.
[62] HU Z J, CHANG X M, PAN Q, et al.Gastroprotective and ulcer healing effects of camel milk and urine in hcl/etoh, non-steroidal antiinflammatory drugs (indomethacin), and water-restraint stress-induced ulcer in rats[J].Pharmacognosy Magazine, 2017, 13(52): 559-565.DOI:10.4103/pm.pm_135_17.
[63] WANG Y M, DILIDAXI D, WU Y, et al.Composite probiotics alleviate type 2 diabetes by regulating intestinal microbiota and inducing GLP-1 secretion in db/db mice[J].Biomedecine & Pharmacotherapie, 2020,125: 109914.DOI:10.1016/j.biopha.2020.109914.
[64] KAMAL H, JAFAR S, MUDGIL P, et al.Inhibitory properties of camel whey protein hydrolysates toward liver cancer cells, dipeptidyl peptidase-IV, and inflammation[J].Journal of Dairy Science, 2018,101(10): 8711-8720.DOI:10.3168/jds.2018-14586.