作为一种传统的食品烹饪或加工方法,油炸因具有耗时短、操作方便和产品口感独特而对大多数消费者具有强烈的吸引力[1]。然而,一般情况下,随着油炸时间的延长,煎炸油会发生一系列的化学反应,包括甘油三酯的热氧化反应、水解反应和美拉德反应;如果这些反应过度进行,则可能产生一些危害物质,严重威胁消费者健康[2-3]。
丙烯酰胺(acrylamide,AA)是一种无色无味的低分子质量晶体化合物,已被IARC归类为2A组“可能的人类致癌物”[4]。AA是一种神经毒素和基因毒素,主要是富含碳水化合物的食品(如面包、咖啡、薯条或薯片等产品)经美拉德反应途径和丙烯醛途径而生成[5-7]。一般而言,AA的生产量受温度、加热时间以及天冬酰胺、还原糖等因素的影响[8-9],所以在实际生产中,可以通过调节这些因素控制AA的产生。主要的减少策略反映在油炸条件的控制[10]和外源化合物的添加上,如醋酸[11]、氨基酸[12]、酶[13]、植物提取物[14]和离子化合物[15]。其中,植物提取物因其天然无害、对食品影响小而受到研究者的青睐。Urbancic等[16]发现在煎炸油中添加迷迭香提取物可显著降低AA含量38%。Demirok等[17]评估了绿茶提取物可以降低炸鸡鸡腿和鸡翅中的AA含量,但不会影响其感官特性。
石榴是常见的水果之一,深受消费的青睐。但是,石榴果实中只有约25%的可食部分,剩下石榴籽、果皮和中果皮常常作为废弃物而未被利用。然而,这些废弃物中却含有丰富的单宁、单宁酸、花青素和其他多酚、萜类和生物碱等植物活性成分,是功能性食品中活性成分的潜在来源,极具商业价值[18-19]。Guo Changjiang等[20]通过铁离子还原力(ferric ion reducing antioxidant power,FRAP)分析测定了我国28 种常见水果的果皮、果肉和种子,发现石榴皮的抗氧化活性最高,且因其单宁含量高常被用作纺织品的着色剂。Elfalleh等[21]的研究结果也表明石榴皮水提物和醇提物的抗氧化活性顺序为果皮>花>叶>种子;且与水提物相比,醇提物表现出更高的活性。基于石榴皮显著的抗氧化活性,本研究通过石榴皮醇提物(ethanol extract of pomegranate peel,EEPP),并分析其抗氧化性质;再将其按一定浓度添加至大豆油中,用于深度油炸薯条,评估不同浓度EEPP对大豆油煎炸薯条过程中的热氧化稳定性及薯条中AA生成情况的影响,旨在为合理利用水果加工副产物,以及拓展植物醇提物在煎炸油及煎炸食品品质控制中的应用提供理论基础。
1 材料与方法
1.1 材料与试剂
精制大豆油(金龙鱼一级)、新鲜土豆、石榴 市购。
AA(纯度≥99%) 上海阿拉丁生化科技股份有限公司;C18固相萃取柱(500 mg,6 mL) 美国Aglient公司;没食子酸、Folin-Ciocalteu试剂、1,1-二苯基-2-三硝基苯肼(1,1-dipheny1-2-picryl-hydrazyl,DPPH)、2,4,6-三吡啶-S-三嗪、2,2’-联氮基-双-(3-乙基苯并噻唑啉-6-磺酸)二铵盐(2,2’-amino-di(3-ethylbenzothiazoline sulphonic acid-6)ammonium salt,ABTS)美国Sigma-Aldrich公司;硅胶(100~200 目)、乙醚、石油醚(沸点30~60 ℃)、硫代硫酸钠、氢氧化钾、无水硫酸钠国产均为分析纯;甲醇、乙醇、正己烷(均为色谱纯) 成都化学试剂有限公司。
1.2 仪器与设备
HL-2B恒流泵、层析柱(2.6 cm×50 cm) 上海沪西分析仪器厂有限公司;RE52CS真空旋转蒸发仪上海亚荣生化仪器厂;FD-1A-50真空冷冻干燥机 北京博医康实验仪器有限公司;ITO-80电炸锅 广州艾拓机电制造有限公司;Varioskan flash酶标仪 美国Thermo Electron公司;U3000液相色谱仪(配有可变波长紫外检测器和CM7.1.7.2色谱工作站) 赛默飞世尔科技有限公司;MTN-2800D氮吹浓缩装置 天津奥特赛恩斯仪器有限公司;TGL16MB冷冻离心机 湘智离心机仪器有限公司;KQ5200DB液晶超声波清洗器 昆山结力美超声仪器有限公司。
1.3 方法
1.3.1 EEPP的制备
以乙醇作为溶剂并采用超声波辅助实现EEPP的提取[22-23]。首先,新鲜石榴皮经真空冷冻干燥后粉碎,25 g石榴皮粉以60%乙醇溶液为提取溶剂,在60 ℃超声提取30 min,抽滤后通过真空旋转蒸发得到粗石榴皮提取物。然后用大孔树脂(XDA-7)纯化粗提物,以60%乙醇溶液作为洗脱溶剂,将洗脱液在45 ℃下真空旋转蒸发,浓缩后的洗脱液再真空冷冻干燥,得到精制EEPP粉末保存在-20 ℃。
1.3.2 EEPP抗氧化活性的测定
1.3.2.1 DPPH自由基清除活性
分别制备0.02~1 mg/mL石榴皮醇提液和VC溶液。DPPH自由基清除率参照Cai Yizhong等[24]的方法并稍作修改。取25 μL加入1 mL 0.06 mmol/L DPPH乙醇溶液,充分混匀后静置避光30 min,在波长517 nm处测定吸光度。用蒸馏水代替样品溶液作为空白组,乙醇代替DPPH溶液作为对照组。DPPH自由基清除率按式(1)计算:
式中:A为样品的吸光度;A1为对照组的吸光度;A0为空白组的吸光度。
1.3.2.2 ABTS阳离子自由基清除活性
参考Ozgen等[25]的方法并稍作修改。0.7 mmol/L的ABTS阳离子自由基溶液与2.45 mmol/L过硫酸钾溶液等体积混合,避光反应12~16 h制得ABTS储备液。用磷酸盐缓冲液(0.2 mol/L,pH 7.4)稀释储备液至在波长734 nm处吸光度为0.7±0.02,得到ABTS稀释液。取0.1 mL不同浓度EEPP和VC溶液与3 mL ABTS稀释液混合,30 ℃反应20 min,在波长734 nm处测定吸光度,以无水乙醇代替ABTS稀释液作空白对照。ABTS阳离子自由基清除率按式(2)计算:
式中:A为样品的吸光度;A0为空白组的吸光度。
1.3.2.3 FRAP值测定
参考Song Fenglin等[26]的方法并稍作修改。FRAP溶液制备:将300 mmol/L醋酸盐缓冲液(pH 3.6)、10 mmol/L 2,4,6-三吡啶基-S-三嗪溶液和20 mmol/L FeCl3溶液以10∶1∶1的比例混匀,37 ℃预热。称取0.055 6 g七水合硫酸亚铁用蒸馏水定容至50 mL,分别移取0.25、0.5、1、2、4、5 mL定容至10 mL,制得浓度分别为0.1、0.2、0.4、0.8、1.6、2 mmol/L的FeSO4溶液。将0.1 mL不同浓度的FeSO4与3 mL FRAP溶液混合1 min,并在37 ℃反应4 min,波长593 nm处测定吸光度,每个样品平行测定3 次,以浓度为X轴,吸光度为Y轴绘制标准曲线。将不同浓度的EEPP和VC溶液按上述步骤测定吸光度。以每克干质量还原Fe2+物质的量表示(mmol/g)。
1.3.3 EEPP总酚含量的测定
采用Ainsworth等[27]的方法并稍作修改。将100 μL提取物与200 μL 10%(V/V)福林-酚试剂混合,5 min后,添加400 μL 7.5 g/100 mL Na2CO3溶液。将混合物在室温下避光反应1 h,并在波长760 nm处测定吸光度。根据没食子酸(0.02~0.1 mg/mL)校准曲线计算总酚含量,结果表示为每克干质量的没食子酸当量(mg/g)。
1.3.4 薯条和煎炸油的制备
在5 L电炸锅内倒入2.5 L大豆油,180 ℃预热25 min。将新鲜土豆去皮并切成5 cm×0.8 cm×0.8 cm的长条,称取60 g浸没入电炸锅内油炸5 min,间隔25 min,之后再放入下一批新鲜薯条进行油炸,每天油炸10 h,连续油炸3 d,每隔2 h取一次油样30 mL和薯条60 g,将薯条粉碎并4 ℃贮存备用。
EEPP按0.01%、0.02%、0.03%、0.07%和0.14%的添加量(相对于煎炸油的体积)溶于乙醇(1∶8)并加入到大豆油中,待均匀溶解后,按上述油炸步骤进行油炸实验,以不添加EEPP作为阴性对照,添加0.02%特丁基对苯二酚(tert-butyl hydroquinone,TBHQ)作为阳性对照。
1.3.5 煎炸油热氧化稳定性的测定
酸价(acid value,AV)的测定参照GB 5009.229—2016《食品中酸价的测定》[28];过氧化值(peroxide value,POV)的测定参照GB 5009.227—2016《食品中过氧化值的测定》[29];总极性组分(total polar compounds,TPC)含量的测定参照GB 5009.202—2016《食用油中极性组分(PC)的测定》[30]。
1.3.6 AA的测定
1.3.6.1 AA标准溶液的配制
称取0.1 g AA标准品(电泳级),用超纯水配制成1 mg/mL的母液,再把母液稀释至0.8、1、2、4、6、8、10 μg/mL等不同质量浓度的标准品溶液,采用高效液相色谱(high performance liquid chromatography,HPLC)法进行分析。采用外标法,绘制峰面积与质量浓度的校准曲线,根据样品的峰面积计算样品中AA的质量浓度。
1.3.6.2 样品前处理
根据Wang Haiyan等[31]的方法测定薯条和煎炸油中的AA。称取2 g薯条粉末于50 mL离心管,加入20 mL超纯水,于恒温振荡箱25 ℃振荡30 min,然后以3 000 r/min离心10 min。取上清液加10 mL正己烷萃取,重复2 次。向脱脂后的样品中加入Carrez I和Carrez II试剂各2 mL,净化除去样品中的蛋白质等杂质。将净化后的样品以8 000 r/min离心10 min,取上清液5 mL过C18固相萃取小柱(预先用6 mL甲醇和6 mL水活化),并用10 mL乙酸乙酯洗脱,收集洗脱液氮吹浓缩至干,加入1 mL超纯水混合,使AA充分溶解,过0.22 μm滤膜,待HPLC检测。
称取油样1 g于50 mL离心管,加入10 mL正己烷溶解,再加入10 mL水振摇30 min,静置分层后,吸取下层于另一个50 mL的离心管中,再加入10 mL水重复提取2 次,合并提取液,之后按上述步骤制备样品。
1.3.6.3 色谱条件
ZORBAX Eclipse XDB-C18色谱柱(4.6 mm×250 mm,5 μm);流动相A为超纯水,流动相B为甲醇,采用梯度洗脱,洗脱程序如下:95% A、5% B持续15 min,从15~17 min降至20% A、80% B,并保持5 min,从22~24 min增加至95% A、5% B,并保持16 min。流速0.5 mL/min,检测波长210 nm,柱温30 ℃,进样量20 μL。
1.4 数据处理
采用Office Microsoft Excel 2010进行数据处理,采用Origin 8.0和Heml等软件进行图形绘制。
2 结果与分析
2.1 提取物抗氧化活性分析
根据没食子酸校准曲线(y=6.566 2x+0.084 7,R2=0.997 1)计算,EEPP的总酚含量为20.14 mg/g。如图1所示,在0.4 mg/mL质量浓度范围内,EEPP对DPPH自由基和ABTS阳离子自由基清除率高于VC,当质量浓度超过0.4 mg/mL时,EEPP和VC对DPPH自由基清除率均在90%以上,分别可达96.96%和95.78%;对ABTS阳离子自由基清除率最高分别为90.03%和89.19%。黄琦等[32]研究了石榴皮总多酚对DPPH自由基的清除作用,结果表明提取物对DPPH自由基半清除质量浓度(IC50)为0.28 mg/mL,与VC清除能力相近,具有较强的抗氧化作用。Pagliarulo等[33]发现石榴果皮对DPPH自由基清除率(94.7%)显著高于果汁(75.8%),并鉴定出石榴果皮中含有丰富的单宁、儿茶素和没食子酸等酚类活性物质。由此看出,EEPP中大量的酚类化合物使其具有较强的自由基清除能力,可作为新型的天然抗氧化剂。
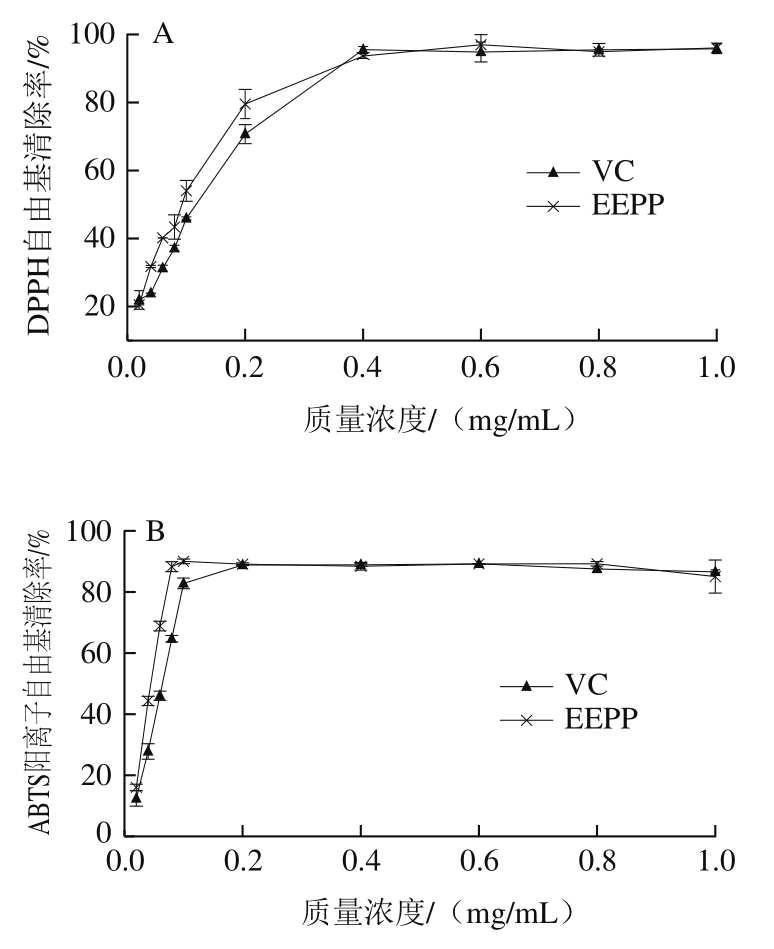
图1 EEPP对DPPH自由基(A)和ABTS阳离子自由基(B)的清除率
Fig. 1 Scavenging effect of EEPP against DPPH radical (A) and ABTS radical cation (B)
FRAP标准曲线方程为y=0.410 8x+0.063 8,R2=0.999 6。如图2所示,在低质量浓度(0.02~0.1 mg/mL)下,EEPP的FRAP值高于VC,当质量浓度超过0.1 mg/mL时,VC始终高于EEPP,但相差不大。随着质量浓度的增加,FRAP相应增加,在质量浓度为1.0 mg/mL时,EEPP和VC的FRAP值分别为8.24 mmol/g和10.37 mmol/g。Elfalleh等[34]研究表明突尼斯石榴的果皮和果汁的FRAP分别为21.24~29.80 mmol/100 g和6.44~8.65 mmol/100 g,说明石榴皮的抗氧化作用较强。有研究表明石榴皮提取物的主要抗氧化成分是单宁和黄酮,其含量与抗氧化能力具有密切的联系,具有剂量效应关系[35],由EEPP的总酚含量(20.14 mg/g)和抗氧化作用可以看出,EEPP具有较高的总酚含量和较强的抗氧化活性。
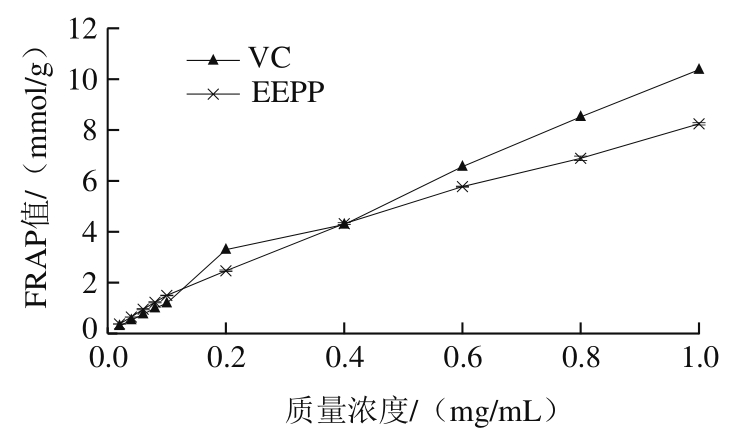
图2 EEPP的FRAP值
Fig. 2 FRAP value of EEPP
2.2 煎炸油的热氧化稳定性
AV能反映油炸过程中水解反应产生的游离脂肪酸含量。在深度油炸过程中,伴随着三酰甘油的水解和不饱和脂肪酸的氧化分解,游离脂肪酸产生,其含量逐渐增大,导致煎炸油中AV数值的持续增加[36]。如图3A所示,随着煎炸时间的延长,AV总体呈逐渐上升的趋势,但所有处理组煎炸3 d后,其AV均不超过食用植物油的法定最大允许值(5 mg/g)[37],因此未能判断EEPP对延长煎炸油使用时间的情况。另外,煎炸期间添加0.02% EEPP煎炸油AV含量(0.088~3.882 mg/g)高于其他处理组(0.088~2.085 mg/g);与其他浓度的EEPP实验组相比,添加0.14% EEPP的煎炸油具有最低的AV水平,且与TBHQ实验组相当,其增长趋势比未添加抗氧化剂的缓慢。这表明0.14% EEPP对游离脂肪酸分解具有一定的抑制效果,具有明显的抑制油脂水解和不饱和脂肪深度氧化酸败的作用,其抑制作用可能与TBHQ相当甚至更好。
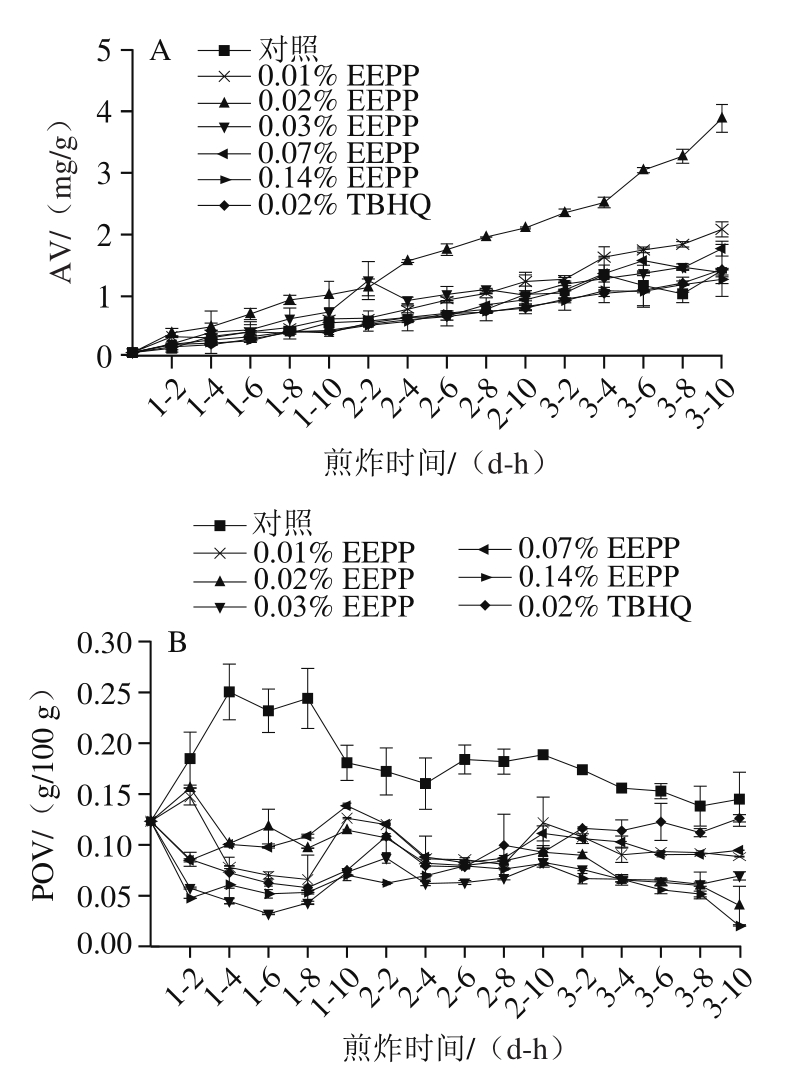
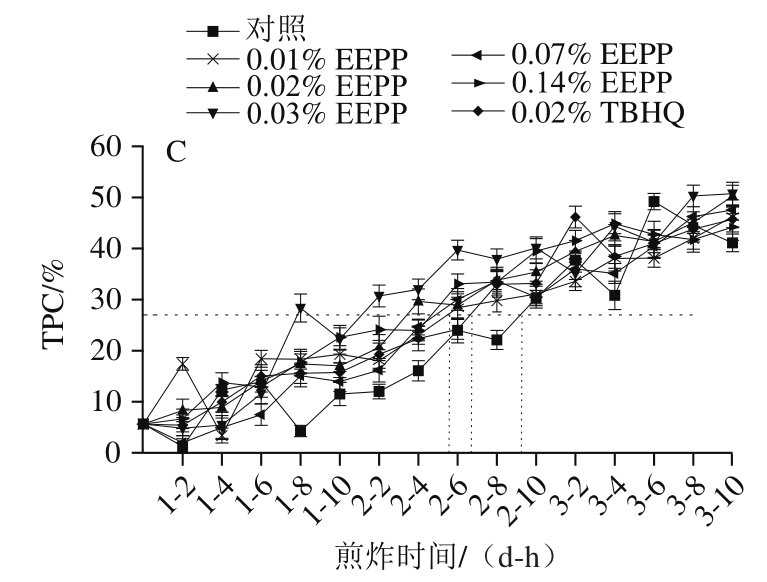
图3 不同添加量EEPP的煎炸油深炸薯条过程中的AV(A)、POV(B)及TPC(C)含量变化
Fig. 3 Changes in AV (A), POV (B), and TPC (C) contents of frying oil added with different EEPP concentrations during processing of French fries
从图3B可以看出,在薯条油炸过程中,不同添加量EEPP实验组的煎炸油POV变化趋势总体上呈波动性。与阴性对照组相比(0.123~0.250 g/100 g),添加EEPP和TBHQ的煎炸油具有更小的POV变化范围(0.020~0.139 g/100 g)。与添加TBHQ的煎炸油相比(0.058~0.126 g/100 g),添加0.14% EEPP的煎炸油表现出较小的变化幅度(0.020~0.123 g/100 g),这表明EEPP的添加能抑制油脂的氧化,表现出较强的抗氧化作用,且0.14% EEPP可能表现出比TBHQ更好的抑制POV的能力,可能是由于高添加量的EEPP中生物活性成分较多,清除自由基能力更强。所有实验组的POV在每天都呈先升高后降低的趋势,这与油炸期间过氧化物的分解以及次生化合物(醇、羧酸等)的形成有关[37]。POV在1~10 h到2~2 h开始降低,说明过氧化物的分解速度大于生成速度,此时煎炸油不能使用。Martinez等[38]研究也发现在180 ℃下煎炸10 次薯条后煎炸油的POV增加,但第15次煎炸后煎炸油的POV逐渐减小。
作为检测煎炸油质量的常用特征指标之一,TPC是食用油煎炸过程中某些极性成分的总称,由于煎炸过程中的氧化和水解反应,使产物具有额外氧原子基团,这些成分产生比甘油三酯更大的极性[39]。如图3C所示,TPC含量随着煎炸时间的延长而增加,这与Osawa等[40]的研究结果一致,可能是由于煎炸时间的延长导致油脂氧化产生过氧化物,其分解物和聚合物都将使极性化合物增加。根据GB 2716—2018《植物油》,煎炸油的TPC最高含量不能超过27%。连续煎炸近2 d后,所有处理组的TPC含量均超过27%,表明此时煎炸油已超过使用极限。此外,可以注意到,EEPP和TBHQ在油炸的早期阶段可以延缓TPC的生成速率,但在后期反而会促进TPC形成,这可能是由于EEPP受温度的影响较大,即长时间高温处理导致了酚类物质含量降低,表现出较弱的抗氧化性;而油脂中产生的羰基化合物、酯类等也能加速油的劣变[41]。
2.3 EEPP对AA形成的影响
如图4所示,在第7分钟时检测到了AA标准物质。根据峰面积与AA质量浓度(0.05~10 μg/mL)之间的关系绘制校准曲线,表示为y=3.114 1x+0.026 8(R2=0.999 5)。式中,x轴为AA质量浓度(μg/L),y轴为峰面积。
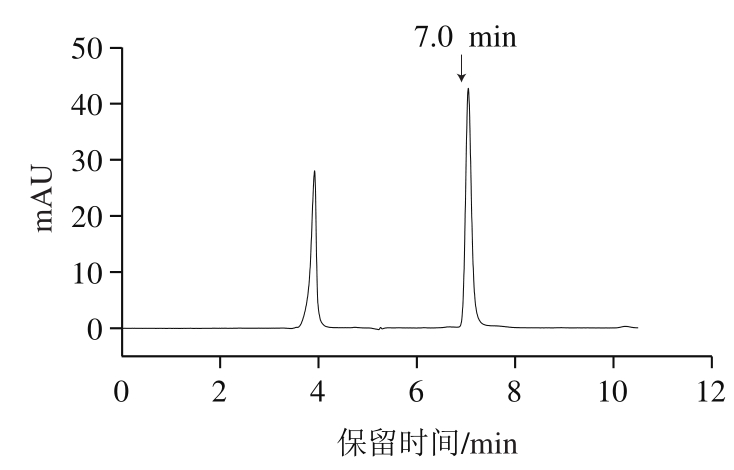
图4 AA标准品的HPLC图
Fig. 4 HPLC chromatogram of acrylamide standard
在煎炸油不饱和甘油三酯氧化分解反应产物中,醛类可以替代食物中的羰基化合物与氨基化合物发生美拉德反应,生成的Schiff碱进一步脱羧后的产物如3-氨基丙烯酰胺能水解为AA[42]。例如,甘油三酯完全水解产生的甘油经脱水后生成丙烯醛,进一步氧化成丙烯酸,与天冬酰胺反应形成AA。也有研究表明丙烯醛也可直接由亚麻酸经氧化分解反应产生[43]。因此,可以通过影响AA的前体物质抑制AA的产生[44]。
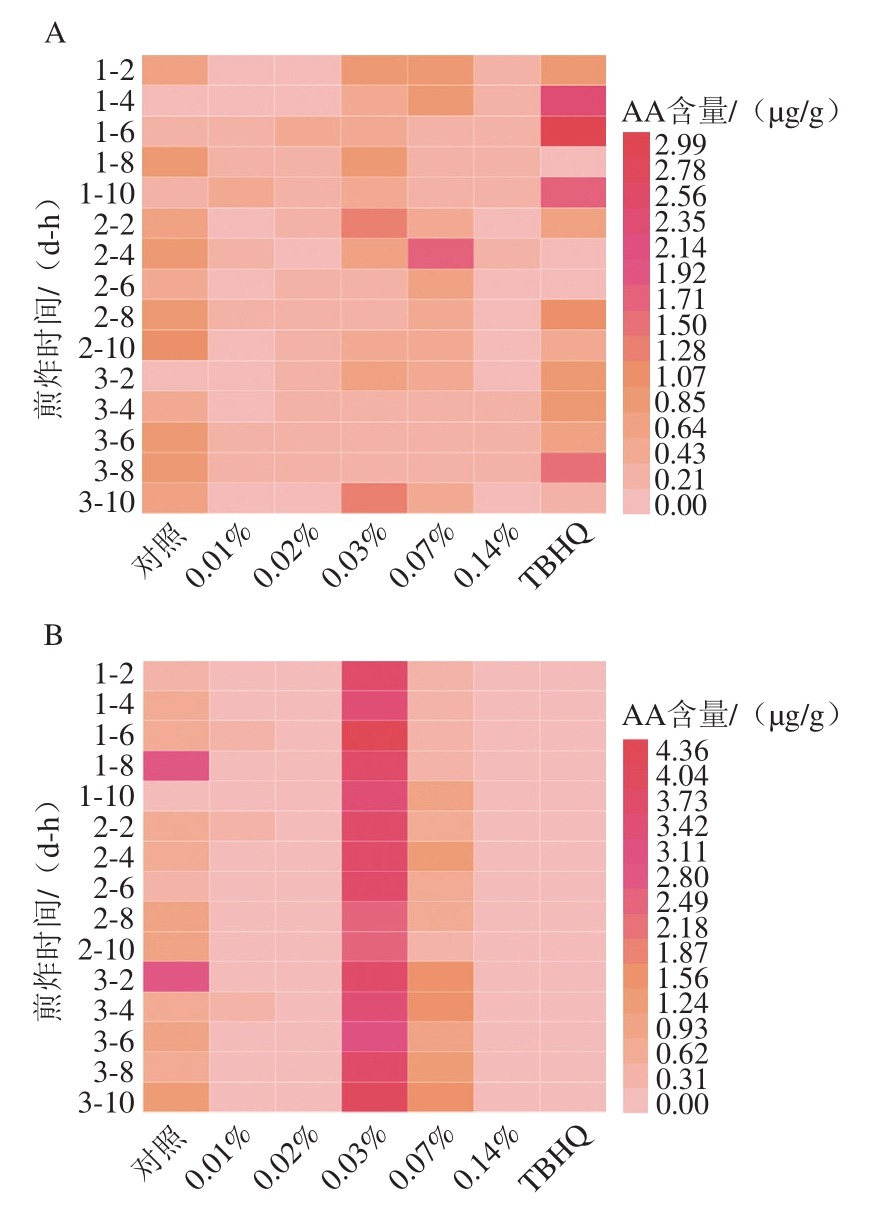
图5 不同添加量EEPP的薯条(A)和煎炸油(B)中AA的热图分析
Fig. 5 Heatmap of acrylamide contents of French fries (A) and frying oil (B) added with different EEPP concentrations
图5显示了经历3 d油炸期间(10 h/d)薯条和煎炸油中AA的含量变化。在油炸过程结束时,阴性对照组、EEPP处理组(0.01%、0.02%、0.03%、0.07%和0.14%)和阳性处理组的薯条样品中AA含量分别为0.83、0.11、0.16、1.32、0.43、0.15、0.33 μg/g。阴性对照组、EEPP处理组(0.01%、0.03%、0.07%)的煎炸油中AA含量分别为1.29、0.20、4.30、1.87 μg/g,其余各处理组均未检测到AA。煎炸油中检测到AA的样品相对较少,可能的原因有:AA具有亲水性,较难溶于煎炸油中,而易被薯条所吸收而存在于薯条基质中且在高温下易分解;EEPP通过抑制多不饱和脂肪的氧化分解而间接降低了AA的生成量,进一步减少了AA存在于煎炸油中的可能性。
与阴性对照组相比,EEPP实验组的薯条中AA含量分别降低了87%、81%、58%、48%和83%,TBHQ实验组的薯条中AA含量降低了60%;添加0.01% EEPP实验组的煎炸油中AA含量降低了85%。Morales等[45]评估了绿茶、肉桂、牛至提取物对薯片中AA形成的影响,结果表明3 种提取物不会对薯片的理化、感官和质地特性产生任何显著变化,并且使AA含量分别降低了62%、39%和17%,低于本研究中的EEPP对AA的抑制率。Mekawi等[46]将制备的冻干石榴皮纳米颗粒提取物(1 g/kg)添加到葵花籽油中油炸薯片,结果表明与对照组相比,冻干石榴皮纳米颗粒提取物使薯片中AA的含量显著降低了54%,证明了该冻干石榴皮纳米颗粒提取物具有作为一种抑制AA生成的抗氧化剂的潜力。这可能是由于EEPP具有较强的清除自由基能力,其酚类物质含有带羟基的芳香环,可以与脂质自由基反应形成苯氧基,苯氧基通过芳香环周围未配对电子的离域而达到稳定,防止脂质氧化产生丙烯醛(AA的前体物质之一),从而达到减少AA生成的效果[47]。EEPP添加量为0.03%和0.07%反而促进了煎炸油中AA的生成。随着煎炸时间的延长,薯条和煎炸油中AA的含量呈现波动的趋势,这可能与添加新的薯条样品有关,新的薯条会使油温急剧下降,需要几分钟才能恢复到初始温度;另一个可能的原因是AA在高温下容易分解,导致其含量不稳定。总的来说,EEPP通过影响AA前体物质而影响AA的产生,其添加量为0.01%和0.14%都能有效抑制薯条和煎炸油中AA的形成。
3 结 论
EEPP具有较强的DPPH自由基、ABTS阳离子自由基清除能力和FRAP,能延缓油脂的水解氧化反应。在油炸前添加0.14%的EEPP可以使煎炸油的氧化变质的速率变慢,热氧化稳定性得到一定程度的提高,并有效抑制薯条和煎炸油中AA的形成,抑制率达到83%,高于TBHQ实验组的抑制率(60%)。由此看出,EEPP在油炸过程中能有效地发挥较强的抗氧化活性,作为潜在的天然抗氧化剂,具有广阔的应用前景和开发价值。本研究有利于石榴皮的深度开发利用、为水果加工副产物的合理应用提供了新的途径;但EEPP中具体的抗氧化活性成分以及作用机理还有待进一步研究。
[1]GADIRAJU T V, PATEL Y, GAZIANO J M, et al. Fried food consumption and cardiovascular health: a review of current evidence[J]. Nutrients, 2015, 7(10): 8424-8430. DOI:10.3390/nu7105404.
[2]CHOE E, MIN D B. Chemistry of deep-fat frying oils[J]. Journal of Food Science, 2007, 72(5): R77-R86. DOI:10.1111/j.1750-3841.2007.00352.x.
[3]ZHANG Q, SALEH A S M, CHEN J, et al. Chemical alterations taken place during deep-fat frying based on certain reaction products:a review[J]. Chemistry and Physics of Lipids, 2012, 165(6): 662-681.DOI:10.1016/j.chemphyslip.2012.07.002.
[4]IARC. Acrylamide. In IARC monographs on the evaluation of carcinogenic risks to humans[C]. Lyon, France: International Agency for Research on Cancer, 1994: 389-433.
[5]KNOL J J, LINSSEN J P H, VAN BOEKEL M A J S. Unravelling the kinetics of the formation of acrylamide in the Maillard reaction of fructose and asparagine by multiresponse modelling[J].Food Chemistry, 2010, 120(4): 1047-1057. DOI:10.1016/j.foodchem.2009.11.049.
[6]MAAN A A, ANJUM M A, KHANM K I, et al. Acrylamide formation and different mitigation strategies during food processing: a review[J].Food Reviews International, 2020, 38(1): 70. DOI:10.1080/87559129.2020.1719505.
[7]KITAHARA Y, OKUYAMA K, OZAWA K, et al. Thermal decomposition of acrylamide from polyacrylamide time-resolved pyrolysis with ion-attachment mass spectrometry[J]. Journal of Thermal Analysis and Calorimetry, 2012, 110(1): 423-429.DOI:10.1007/s10973-012-2544-7.
[8]TEPE T K, KADAKAL C. Temperature and slice size dependences of acrylamide in potato fries[J]. Journal of Food Processing and Preservation, 2019, 43(12): e14270. DOI:10.1111/jfpp.14270.
[9]VINCI R M, MESTDAGH F, DE MEULENAER B. Acrylamide formation in fried potato products-present and future, a critical review on mitigation strategies[J]. Food Chemistry, 2012, 133(4): 1138-1154.DOI:10.1016/j.foodchem.2011.08.001.
[10]PEDRESCHI F, KAACK K, GRANBY K, et al. Acrylamide reduction under different pre-treatments in french fries[J]. Journal of Food Engineering, 2007, 79(4): 1287-1294. DOI:10.1016/j.jfoodeng.2006.04.014.
[11]KITA A, BRATHEN E, KNUTSEN S H, et al. Effective ways of decreasing acrylamide content in potato crisps during processing[J].Journal of Agricultural and Food Chemistry, 2004, 52(23): 7011-7016.DOI:10.1021/jf049269i.
[12]ZOU Y Y, HUANG C H, PEI K H, et al. Cysteine alone or in combination with glycine simultaneously reduced the contents of acrylamide and hydroxymethylfurfural[J]. LWT-Food Science and Technology, 2015, 63(1): 275-280. DOI:10.1016/j.lwt.2015.03.104.
[13]MEGHAVARNAM A K, JANAKIRAMAN S. Evaluation of acrylamide reduction potential of L-asparaginase from fusarium culmorum (Asp-87) in starchy products[J]. LWT-Food Science and Technology, 2018, 89: 32-37. DOI:10.1016/j.lwt.2017.09.048.
[14]BECALSKI A, LAU B P, LEWIS D, et al. Acrylamide in foods:occurrence, sources, and modeling[J]. Journal of Agricultural and Food Chemistry, 2002, 51(3): 802-808. DOI:10.1021/jf020889y.
[15]KALITA D, JAYANTY S S. Reduction of acrylamide formation by vanadium salt in potato french fries and chips[J]. Food Chemistry,2013, 138(1): 644-649. DOI:10.1016/j.foodchem.2012.09.123.
[16]URBANCIC S, KOLAR M H, DIMITRIJEVIC D, et al. Stabilisation of sunflower oil and reduction of acrylamide formation of potato with rosemary extract during deep-fat frying[J]. LWT-Food Science and Technology, 2014, 57(2): 671-678. DOI:10.1016/j.lwt.2013.11.002.
[17]DEMIROK E, KOLSARICI N. Effect of green tea extract and microwave pre-cooking on the formation of acrylamide in fried chicken drumsticks and chicken wings[J]. Food Research International,2014, 63: 290-298. DOI:10.1016/j.foodres.2014.04.003.
[18]MEKNI M, FLAMINI G, GARRAB M, et al. Aroma volatile components, fatty acids and antibacterial activity of four Tunisian Punica granatum L. flower cultivars[J]. Industrial Crops and Products,2013, 48: 111-117. DOI:10.1016/j.indcrop.2013.04.005.
[19]TEHRANIFAR A, ZAREI M, NEMATI Z, et al. Investigation of physico-chemical properties and antioxidant activity of twenty Iranian pomegranate (Punica granatum L.) cultivars[J]. Scientia Horticulturae,2010, 126(2): 180-185. DOI:10.1016/j.scienta.2010.07.001.
[20]GUO C J, YANG J J, WEI J Y, et al. Antioxidant activities of peel,pulp and seed fractions of common fruits as determined by FRAP assay[J]. Nutrition Research, 2003, 23(12): 1719-1726. DOI:10.1016/j.nutres.2003.08.005.
[21]ELFALLEH W, TLILI N, NASRI N, et al. Antioxidant capacities of phenolic compounds and tocopherols from tunisian pomegranate(Punica granatum) fruits[J]. Journal of Food Science, 2011, 76(5):C707-C713. DOI:10.1111/j.1750-3841.2011.02179.x.
[22]熊何健, 郭倩倩, 乔小瑞. 荔枝多酚柱层析纯化工艺条件研究[J].江西农业大学学报, 2010, 32(6): 1274-1278. DOI:10.3969/j.issn.1000-2286.2010.06.034.
[23]赵艳红, 李建科. 响应曲面法建立超声波辅助提取石榴皮多酚数学模型[J]. 农产品加工(学刊), 2009(3): 126-131. DOI:10.3969/j.issn.1671-9646-B.2009.03.033.
[24]CAI Y Z, SUN M, CORKE H. Antioxidant activity of betalains from plants of the amaranthaceae[J]. Journal of Agricultural and Food Chemistry, 2003, 51(8): 2288-2294. DOI:10.1021/jf030045u.
[25]OZGEN M, REESE R N, TULIO A Z J, et al. Modified 2,2-azinobis-3-ethylbenzothiazoline-6-sulfonic acid (ABTS) method to measure antioxidant capacity of selected small fruits and comparison to ferric reducing antioxidant power (FRAP) and 2,2'-diphenyl-1-picrylhydrazyl (DPPH) methods[J]. Journal of Agricultural and Food Chemistry, 2006, 54(4): 1151-1157. DOI:10.1021/jf051960d.
[26]SONG F L, GAN R Y, ZHANG Y A, et al. Total phenolic contents and antioxidant capacities of selected Chinese medicinal plants[J].International Journal of Molecular Sciences, 2010, 11(6): 2362-2372.DOI:10.3390/ijms11062362.
[27]AINSWORTH E A, GILLESPIE K M. Estimation of total phenolic content and other oxidation substrates in plant tissues using Folin-Ciocalteu reagent[J]. Nature Protocols, 2007, 2(4): 875-877.DOI:10.1038/nprot.2007.102.
[28]卫生部. 食品中酸价的测定: GB 5009.229—2016[S]. 北京: 中国标准出版社, 2016.
[29]卫生部. 食品中过氧化值的测定: GB 5009.227—2016[S]. 北京:中国标准出版社, 2016.
[30]卫生部. 食用油中极性组分(PC)的测定: GB 5009.202—2016[S].北京: 中国标准出版社, 2016.
[31]WANG H Y, FENG F, GUO Y, et al. HPLC-UV quantitative analysis of acrylamide in baked and deep-fried Chinese foods[J]. Journal of Food Composition and Analysis, 2013, 31: 7-11. DOI:10.1016/j.jfca.2013.02.006.
[32]黄琦, 王启越, 李颖, 等. 石榴皮总多酚的微波辅助提取工艺及抗氧化活性研究[J]. 食品研究与开发, 2016, 37(12): 46-51; 61.DOI:10.3969/j.issn.1005-6521.2016.12.011.
[33]PAGLIARULO C, DE VITO V, PICARIELLO G, et al. Inhibitory effect of pomegranate (Punica granatum L.) polyphenol extracts on the bacterial growth and survival of clinical isolates of pathogenic Staphylococcus aureus and Escherichia coli[J]. Food Chemistry, 2016,190: 824-831. DOI:10.1016/j.foodchem.2015.06.028.
[34]ELFALLEH W, TLILI N, NASRI N, et al. Antioxidant capacities of phenolic compounds and tocopherols from Tunisian pomegranate(Punica granatum) fruits[J]. Journal of Food Science, 2011, 76(5):C707-C713. DOI:10.1111/j.1750-3841.2011.02179.x.
[35]张茜, 贾冬英, 姚开, 等. 石榴皮提取物的抗氧化作用研究[J]. 中国油脂, 2006, 31(8): 51-54. DOI:10.3321/j.issn:1003-7969.2006.08.016.
[36]TIAN J R, QI D S, WAN C. et al. Quality assessment of frying oil using short-chain fatty acid profile and infrared spectrum coupled with partial least squares[J]. Journal of Food Measurement and Characterization,2020, 14(4): 2289-2299. DOI:10.1007/s11694-020-00476-3.
[37]PARK J M, KOH J H, KIM J M. Determining the reuse of frying oil for fried sweet and sour pork according to type of oil and frying time[J]. Food Science of Animal Resources, 2020, 40(5): 785-794.DOI:10.5851/kosfa.2020.e54.
[38]MARTINEZ P M, FERRER M A, VERCET A, et al. Physicochemical characterization of changes in different vegetable oils (olive and sunflower) under several frying conditions[J]. CyTA-Journal of Food,2011, 9(4): 301-306. DOI:10.1080/19476337.2011.601817.
[39]LI X, WU G, YANG F, et al. Influence of fried food and oil type on the distribution of polar compounds in discarded oil during restaurant deep frying[J]. Food Chemistry, 2018, 272: 12-17. DOI:10.1016/j.foodchem.2018.08.023.
[40]OSAWA C C, GONÇALVES L A G, GUMERATO H F, et al. Study of the effectiveness of quick tests based on physical properties for the evaluation of used frying oil[J]. Food Control, 2012, 26: 525-530.DOI:10.1016/j.foodcont.2012.01.008.
[41]SZYDŁOWSKA-CZERNIAK A, RABIEJ D. Effect of new antioxidants: phenolipids on quality of fried French fries and rapeseed oil[J]. Journal of Food Science and Technology-Mysore, 2020, 58(7):2589-2598. DOI:10.1007/s13197-020-04765-z.
[42]LIU Y B, WANG P P, CHEN F, et al. Role of plant polyphenols in acrylamide formation and elimination[J]. Food Chemistry, 2015, 186:46-53. DOI:10.1016/j.foodchem.2015.03.122.
[43]ENDO Y, HAYASHI C, YAMANAKA T, et al. Linolenic acid as the main source of acrolein formed during heating of vegetable oils[J].Journal of the American Oil Chemists Society, 2013, 90(7): 959-964.DOI:10.1007/s11746-013-2242-z.
[44]戚岱莎, 张清. 食物油炸过程中丙烯酰胺和杂环胺的形成及控制方法研究进展[J]. 食品科学, 2021, 42(21): 338-346. DOI:10.7506/spkx1002-6630-20200410-141.
[45]MORALES G, JIMENEZ M, GARCIA O, et al. Effect of natural extracts on the formation of acrylamide in fried potatoes[J]. LWTFood Science and Technology, 2014, 58(2): 587-593. DOI:10.1016/j.lwt.2014.03.034.
[46]MEKAWI E M, SHAROBA A M, RAMADAN M F. Reduction of acrylamide formation in potato chips during deep-frying in sunflower oil using pomegranate peel nanoparticles extract[J]. Journal of Food Measurement and Characterization, 2019, 13(4): 3298-3306.DOI:10.1007/s11694-019-00252-y.
[47]ROMANI S, BACCHIOCCA M, ROCCULI P, et al. Effect of frying time on acrylamide content and quality aspects of French fries[J].European Food Research and Technology, 2006, 226(3): 555-560.DOI:10.1007/s00217-007-0570-7.