利用膳食纤维替代脂肪开发健康低脂香肠是当前加工肉制品行业的研究热点[1-6]。从营养角度,膳食纤维被誉为“第七大营养素”,能够改善肠道益生菌群和降低心血管疾病的发生几率[7]。世界卫生组织建议膳食纤维每日摄入量应该达到25 g[8]。然而相关实验结果显示:不同类型的膳食纤维作为脂肪替代物对低脂香肠的感官质构影响差异显著,例如:抗性淀粉和卡拉胶等既能够降低低脂香肠蒸煮损失,而且改善质构特性(硬度和咀嚼性)[9-10];微晶纤维素等能够显著降低低脂香肠蒸煮损失,但是对质构影响差异不显著[11];羧甲基纤维素和黄原胶等对低脂香肠质构甚至有负面作用[11]。此外,研究者还发现膳食纤维在香肠中的运用存在添加量极限。例如:卡拉胶改善火鸡香肠感官质构的添加量极限为0.8%;甘蔗不溶膳食纤维改善猪肉低脂香肠感官质构的添加量极限为2.0%[12-16]。目前,膳食纤维影响蛋白凝胶类产品的质构特性的作用机制还鲜有文章报道。
魔芋胶提取于魔芋草本植物的根部,其主要成分是魔芋葡甘聚糖。魔芋葡甘聚糖是一种非离子型水溶性高分子多糖,由D-葡萄糖和D-甘露糖聚合而成。魔芋胶作为一种膳食纤维,具有零卡路里、螯合胆固醇和促进肠道蠕动功能作用[17-18]。因此,本实验以肌原纤维蛋白-魔芋胶(myofibrillar protein-konjac glucomannan,MP-KG)为模拟体系,通过微观结构(石蜡切片和扫描电镜)、图像分析软件技术(分维分析和缺项分析)和质构特性,进而阐释微观结构对蛋白凝胶质构的调控机制,为KG在低脂肉制品中的应用提供一定的理论基础。
1 材料与方法
1.1 材料与试剂
猪后腿肉购于苏果超市;KG 上海北联生物科技有限公司;过氧化氢、氢氧化钠、盐酸、氯化钠、乙二醇-双-2-氨基乙醚四乙酸(ethylene glycol bis (2-aminoethyl ether) tetraacetic acid,EGTA)、碳酸一氢钠、碳酸二氢钠、氯化镁、戊二醛 西格玛试剂有限公司;所有试剂均为分析纯。
1.2 仪器与设备
MM-12绞肉机 中国丰伟机械有限公司;切片机德国徕卡公司;T25DS25I KA均质机、磁力搅拌器德国IKA公司;Avanti JXN-30离心机 美国Beckman公司;TW20水浴锅 德国Julabo公司;TA-XT Plus质构仪英国Stable Micro Systems公司;PQ001低场核磁共振仪苏州纽迈公司;S-3000N扫描电镜 日本Hitachi公司。
1.3 方法
1.3.1 MP的提取和复合体系的制备
剔除猪后腿肉中结缔组织和脂肪并绞肉机绞碎(0.6 mm孔板),用双层真空包装袋(聚乙烯)进行分装,每袋500 g,贮存于-20 ℃。提取前取出猪后腿肉并放置于0~4 ℃冷库中解冻至中心温度为0 ℃。
MP提取方法参照Han Minyi等[19],并稍作改动。具体操作步骤如下:将50 g斩拌后的肉糜和4 倍体积的磷酸缓冲溶液(10 mmol/L NaH2PO4/Na2HPO4、0.1 mmol/L NaCl、2 mmol/L MgCl2、1 mmol/L EGTA、pH 7.0,4 ℃)混合均质(6 000×g,30 s)。将均质后混合溶液用双层纱布进行过滤后离心(3 000×g,15 min)取沉淀,重复上述过程两遍,最终沉淀物即为纯MP。双缩脲方法测定纯MP浓度。将甘蔗膳食纤维进行超微粉碎,过100 目筛的标记为100 目,剩余通过50 目的标记为50 目。将甘蔗不溶性膳食纤维添加到MP中,并将蛋白质量浓度稀释至50 mg/mL(0.6 mol/L NaCl,pH 7.0)。不同粒径(50、100 目)甘蔗膳食纤维添加量为3 个梯度:1.0%、2.0%和3.0%。用搅拌器搅拌混合体系3 min,以确保甘蔗膳食纤维均匀分布。将部分样品进行蒸煮(80 ℃、20 min)并冷却至室温4 ℃,另一部分样品用于流变测定。
1.3.2 水分分布
参照Bertram等[20]方法,并稍作改动。将样品加入直径为1 cm的石英玻璃管中并避免气泡的产生,进而水浴(80 ℃)加热凝胶并冷却至室温。使用PQ001低场核磁共振仪对样品进行测定,质子共振频率为22.3 MHz,样品测试温度为32 ℃,采用的测试算法为CPMG序列(carrpurcell-meiboom-gill sequence)。测试具体参数如下:90°脉冲和180°脉冲时间间隔为250 μs;回波次数12 000。利用3 组分算法分析并生成弛豫时间图;3 个不同水分组分的弛豫初始时间、峰值时间和结束时间以及3 个不同水分组分对应的峰面积和占比比例。为方便描述,弛豫图每个组分的峰值时间作为弛豫时间,以T2i表示,而每个组分峰面积所占总积分面积的百分比,以PT2i表示。
1.3.3 复合凝胶的形变特性
参照Czerner等[21]方法并稍作改动。使用质构仪测定样品(直径2 cm、高度2 cm)的复合凝胶断裂时的形变特性,具体参数如下:下降速率2.0 mm/s、测试速率1.0 mm/s,质构探头为P50型号,压缩比90%。其中的复合凝胶断裂形变时的应变计算公式如下[22]:
式中:H0为样品初始高度;H为样品发生断裂形变时的压缩高度。
复合凝胶断裂形变时的应力计算按照下式计算[23]:
式中:F为压缩过程中所测得的力;A为样品接触探头的表面积。
1.3.4 石蜡切片
将凝胶样品切割成1 cm×1 cm×2 cm的长方体,并用4%的多聚甲醛进行结构固定。将样品从固定液取出后,进行切片和染色后,用正置明场显微镜放大1 000 倍观察切片的微观结构。每个样品取5 个不同的观察视野。
1.3.5 扫描电镜和图像处理
扫描电镜及其图像处理的方法参照Han Minyi等[19],并稍作改动。将凝胶样品切割成侧面1 cm2的长方体,并用2.5%的戊二醛磷酸缓冲溶液进行结构固定。固定后用磷酸缓冲溶液对样品进行多次漂洗后,用不同体积分数乙醇溶液对样品脱水。脱水干燥后的样品粘于金属台上进行喷金镀膜。最后将样品置于S-3000N扫描电镜中进行放大2 000 倍观察。每个样品分别观察5 个视野。将扫描电镜图像导入ImageJ v1.47后,利用其Fraclac 2.5 v插件对其进行处理分析。首先,在图像的像素调整到640×432后,对其进行二维化处理。分维分析反映不规则复杂结构占有空间的有效性。盒计数法为在图像上定义几个尺寸缩小的网格,并计算每个网格中包含蛋白三维网络结构的像素数量。分维维度按下式计算[24]:
式中:D为凝胶蛋白三维网络结构的分维维度;Nε为不同尺寸网格中所包含的像素数量;ε为网格的尺寸。
缺项分析是反映凝胶三维网络结构中水孔隙的均匀程度。缺项分析定义为在图像中定义N 个数量相同大小的网格,计算这些网格中代表水相形成水孔隙的目标像素的变异系数。缺项分析基于下式计算[11]:
式中:Ʌ为目标像素的缺项;σ为所有大小网格内目标像素数量的标准差;μ为所有大小网格内目标像素数量的平均值。
1.4 数据分析
本实验设计采用完全随机区组的方法,所有处理重复3 次。所有的数据用SAS 9.0统计软件进行分析,添加KG处理组采用方差分析,比较方法采用Duncan多重比较分析,P<0.05,差异显著。
2 结果与分析
2.1 MP-KG凝胶的形变特性
通过质构仪测定MP-KG凝胶破碎瞬间的参数,并利用公式计算得到复合凝胶断裂形变时应力应变[10,25-26]。如图1所示,KG添加量对复合凝胶断裂形变时应力应变影响显著。随着KG添加量提高,复合凝胶的断裂形变时应力变化呈现抛物线形,这说明KG对复合凝胶的应力改善具有添加量极限。复合凝胶断裂形变时应变的变化趋势和应力相似,但是两者的添加量极限不同。图1显示添加1%的KG组断裂形变时的应力最大为13.73 kPa,添加0.5%的KG组断裂形变时的应变最大为1.02。当KG添加量达到2%时,复合凝胶的断裂形变时的应力应变最低,分别为16.31 kPa和0.68。这说明当KG超过添加量极限后会显著降低复合凝胶的质构特性,甚至要低于对照组。
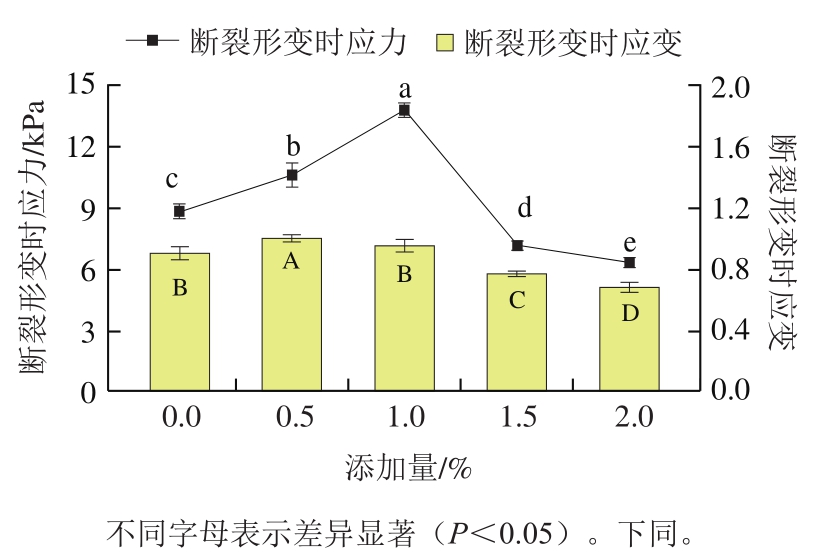
图1 KG添加量对复合凝胶断裂形变时应力应变的影响
Fig. 1 Effect of KG concentration on fracture stress and fracture strain of composite gels
2.2 低场核磁共振
在MP凝胶体系中水分子存在3 种分布状态:1)结合水,能和MP分子紧密结合在一起,弛豫时间(T2b)分布在1~10 ms;2)不易流动水,被束缚于MP凝胶网络结构的间隙中,弛豫时间(T21)分布在200~400 ms;3)自由水,其不被凝胶网络结构所束缚并自由流动,弛豫时间(T22)分布在1 000~2 000 ms[20,27]。在肌原纤维凝胶体系中,水分子的分布状态能够直接反映MP凝胶结构体系,尤其是不易流动水,其弛豫时间越短说明肌原纤维凝胶网络结构越致密,是因为凝胶结构对水分子的束缚能力越强[19,27-28]。因此,测定不易流动水的弛豫时间能够直接反映KG对MP交联程度的影响。如表1所示,添加不同比例KG对复合凝胶中3 种分布状态的水分子弛豫时间和相对百分比。结果显示:随着KG添加量的增加,不易流动水的弛豫时间呈现勾状变化趋势,在添加1.0%时不易流动水的弛豫时间最低且其相对百分比最高,分别为274 ms和92.79%。这说明KG能够有效的促进形成致密的蛋白凝胶网络结构提高对水分子的束缚。当添加量增加到2%时,处理组的弛豫时间最高且相对百分比最低,分别为343.51 ms和77.51%。这说明当KG超过添加量极限后会抑制MP凝胶网络结构的聚集。此外,KG添加量的变化对结合水的影响不显著,说明结合水的变化只与MP比例相关。KG添加量显著影响自由水的百分比,在添加1.0% KG时自由水的百分比最低,这说明凝胶网络结构能够束缚足够多的不易流动水,进而降低了自由水的比例。
表1 KG对MP凝胶中水分弛豫时间和百分比的影响
Table 1 Effect of KG concentration on relaxation times and percentage peak areas of water in composite gels
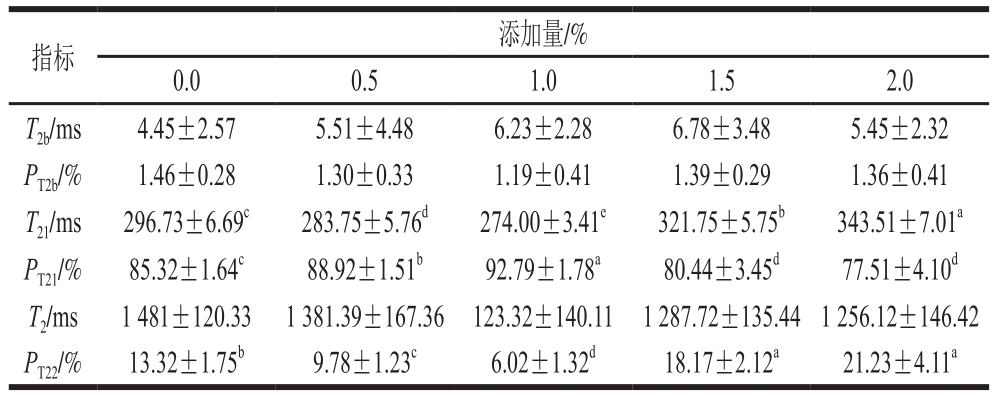
注:不同字母表示差异显著(P<0.05)。
指标 添加量/%0.0 0.5 1.0 1.5 2.0 T2b/ms 4.45±2.57 5.51±4.48 6.23±2.28 6.78±3.48 5.45±2.32 PT2b/% 1.46±0.28 1.30±0.33 1.19±0.41 1.39±0.29 1.36±0.41 T21/ms 296.73±6.69c 283.75±5.76d 274.00±3.41e 321.75±5.75b 343.51±7.01a PT21/% 85.32±1.64c 88.92±1.51b 92.79±1.78a 80.44±3.45d 77.51±4.10d T2/ms 1 481±120.33 1 381.39±167.36 123.32±140.11 1 287.72±135.441 256.12±146.42 PT22/% 13.32±1.75b 9.78±1.23c 6.02±1.32d 18.17±2.12a 21.23±4.11a
2.3 相限行为
如图2所示,石蜡切片能够清晰显示不同添加量的KG在肌原纤维凝胶网络结构中的相限行为,其中红色部分是MP,白色部分是水相,灰色阴影部分是KG。对照组显示MP凝胶微观结构,其为多孔的不规则的三维网络结构。未添加KG时,对照组的MP三维网络结构均匀,三维网络结构间隙中均匀的分布着形状大小各异的白色水空穴。当添加少量KG时,KG以分散相的形式被包裹在MP凝胶网络体系中。KG的形状大小显著大于对照组中的水空穴,因此复合凝胶的微观结构不再均匀。当KG添加量超过1%时,KG不再镶嵌在MP网络结构中。KG自身可以通过氢键作用发生水合形成弱凝胶结构,进而与MP凝胶结构相互渗透交叉,形成双连续相。本实验显示KG在MP凝胶网络体系中的相限行为随着添加量而变化:KG添加量低于1%时,碳水化合物以分散相的形式被包裹在MP凝胶网络体系中;KG添加量高于1%时,碳水化合物和MP均形成连续相,且两者相互渗透交叉。
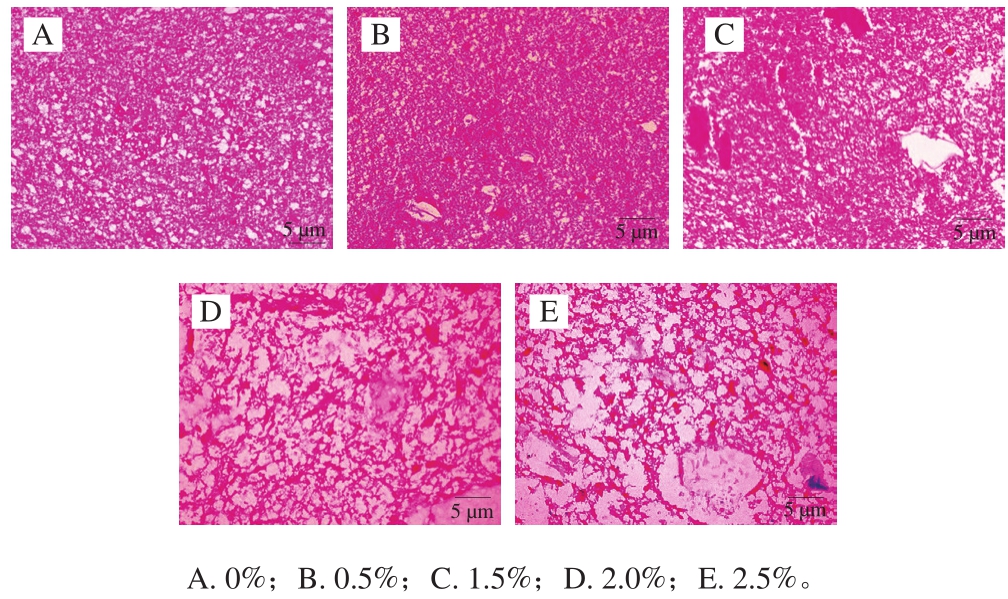
图2 不同添加量的KG在蛋白凝胶中的空间分布
Fig. 2 Spatial distribution of konjac glucomannan at various concentrations in composite gels
2.4 扫描电镜结果
如图3所示,扫描电镜能够清晰显示不同添加量的KG对肌原纤维蛋热诱导交联程度的影响,其中白色部分为MP骨架结构。观察结果显示添加不同比例KG对MP三维凝胶网络结构影响显著。观察对照组发现MP凝胶网络结构呈粗丝状甚至部分区域呈现团状结构,说明在加热过程中MP折叠结构并没有充分展开,大量疏水基团依然包埋在分子内部,进而在后续加热过程中没有大量疏水基团进行彼此交联形成致密的三维网络结构[14,29-30]。此外,在MP三维网络结构间隙中存在大量黑色空穴,这些黑色空穴相互交联进而形成水沟壑,将MP三维网络凝胶结构分割成片状化[12]。
当KG添加量小于1.0%时,观察处理组扫描电镜发现MP凝胶网络结构呈细丝状且交联致密,没有粗丝和团状蛋白存在。和对照组相比MP三维网络结构间隙中黑色空穴数量和大小显著降低。这说明在常温下KG通过氢键与水合作用将水分子束缚在KG分子结构中,降低了水沟壑的形成以及其对MP三维网络凝胶结构的分割。但是当KG添加量超过1.0%时,观察处理组扫描电镜发现MP的三维网络凝胶结构没有细丝的出现,整个结构呈现粗丝状且相当疏松。此外,和对照组相比MP三维网络结构间隙中黑色沟壑数量和大小显著增加,并与MP网络结构相互交叉贯穿。这说明添加高浓度的KG时,KG会和MP溶液中的水分形成连续的水凝胶,KG水凝胶和MP两者互不相溶并形成相互穿插,这使得MP被分割成碎片化。
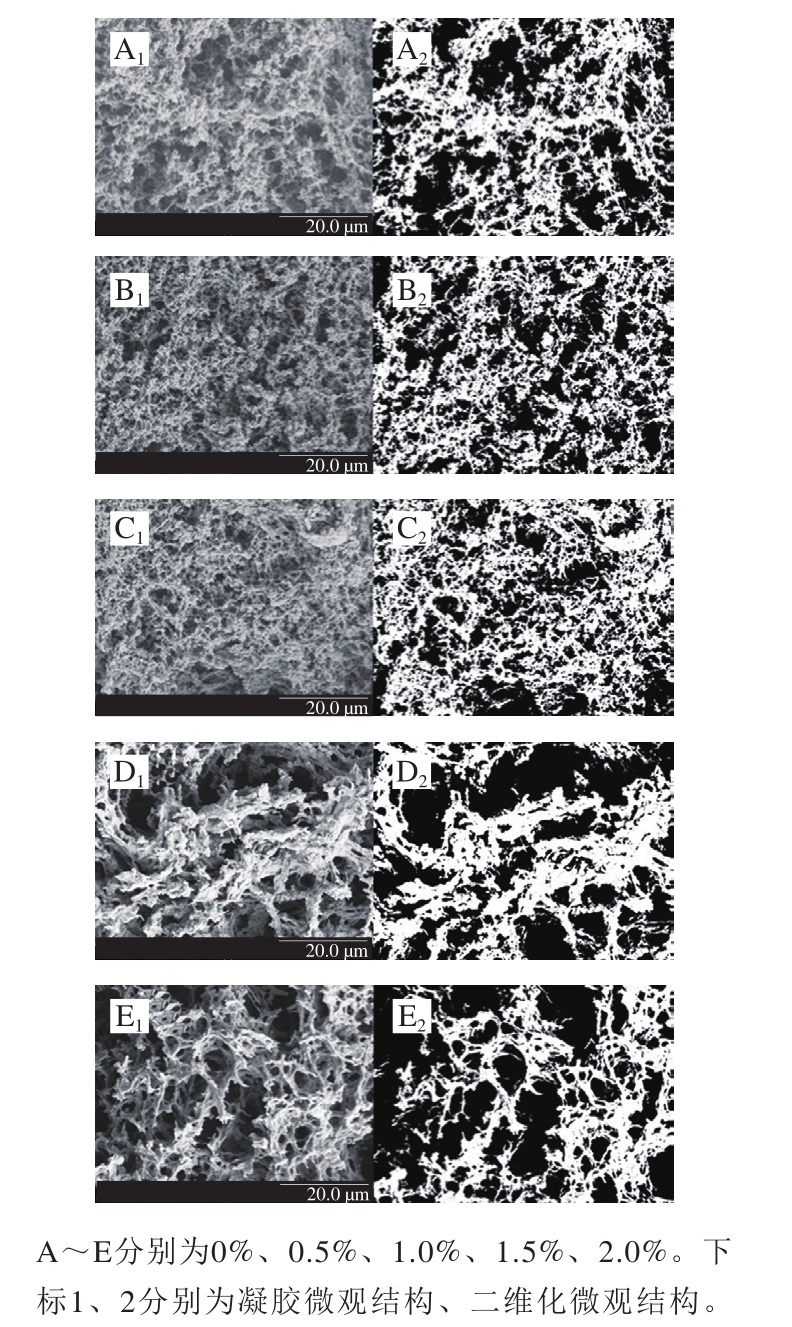
图3 不同添加量的KG对MP微观结构的影响
Fig. 3 Effect of KG concentration on scanning electron micrographs of composite gels
为进一步客观比较KG添加量对MP网络结构的影响,本实验使用图像处理软件对MP网络结构(白色部分)进行分维分析和沟壑(黑色部分)进行缺项分析(图4)。分维分析结构的数值大小和MP网络结构致密度呈正比;缺项分析与沟壑大小和形状的差异性呈正比[12,21,23,31]。分析结果显示处理组(添加1% KG)MP凝胶网络结构的分维维度1.872显著高于其他KG组(P<0.05),而缺项值0.279显著小于其他添加KG组(P<0.05)。处理组(添加2% KG)MP凝胶网络结构的分维维度1.789显著低于其他KG组(P<0.05),而缺项值0.345显著高于其他添加KG组(P<0.05)。
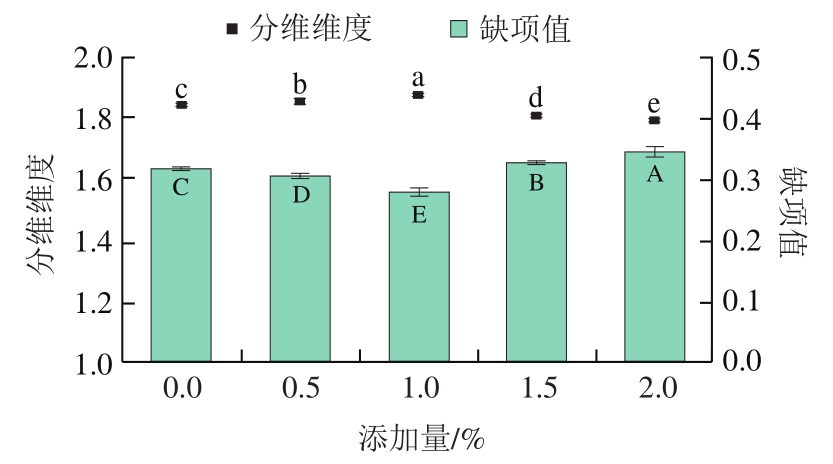
图4 KG添加量对MP凝胶网络结构分维维度和缺项值的影响
Fig. 4 Effect of KG concentration on fractal dimension and lacunary of composite gels
2.5 MP-KG凝胶体系微观结构对感官质构特性的调控
实验证明KG作为优质的脂肪替代物的可行性,并进一步研究MP-KG微观结构对复合凝胶质构特性的调控机制。从微观角度分析,石蜡切片显示KG和MP属于热力不相溶体系,随着KG添加量提高,两者的相行为结构呈现填充结构到互穿结构的转变。当复合凝胶呈现为互穿结构时,KG通过氢键和水合作用形成的水凝胶为弱凝胶,其凝胶强度显著小于MP凝胶强度;KG形成的水凝胶会严重阻碍MP疏水基团的暴露以及后续加热过程中的交联。因此,在互穿体系中MP不能进行充分交联,以及KG水凝胶本身是弱凝胶,进而导致最终复合凝胶质构劣变。当复合凝胶呈现为填充结构时,MP为连续相KG为填充相,通过扫描电镜显示填充结构中的MP凝胶网络结构更加致密且水空穴显著降低。由于溶液状态的MP过热过程中变性展开后渗出大量水分,形成相互交错的水沟壑并导致MP三维网络结构分割成片状化。添加KG后,KG的水合能力降低水沟壑的形成,进而形成致密整体化的三维网络凝胶结构。
从复合凝胶质构角度,当添加KG(<1%)能够显著提高复合凝胶断裂形变时的应力和应变,降低不易流动水的弛豫时间,这显示添加少量KG能够显著改善复合凝胶质构。当添加KG(>1%)时,复合凝胶断裂形变时的应力和应变显著降低,不易流动水的弛豫时间显著提高降低,这显示KG添加量超过1%会导致复合凝胶质构的劣变。
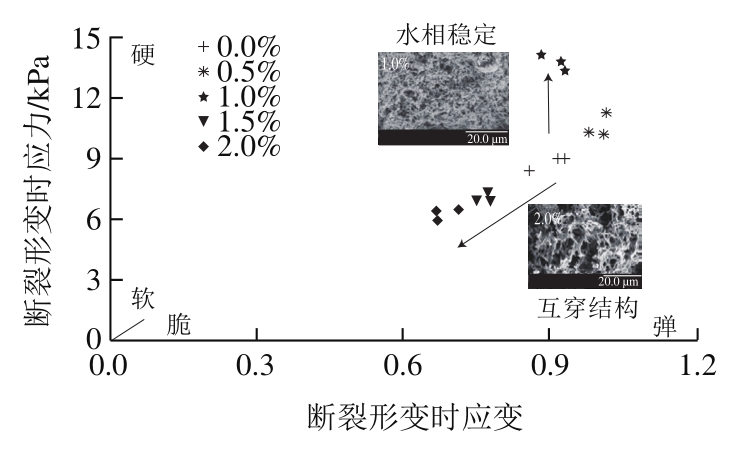
图5 MP-KG凝胶体系中微观结构对感官质构的调控机制
Fig. 5 Regulatory mechanism of the microstructure of MP-KG composite gels on their textural properties
如图5所示,KG的水相稳定能力能够减少MP中水沟壑的形成,促进致密的整体化MP凝胶网络结构的形成,进而提高复合凝胶断裂形变时应力和应变。MP-KG的相行为为互穿结构时,KG通过氢键和水合作用形成的水凝胶为弱凝胶,其凝胶强度显著小于MP凝胶强度;KG形成的水凝胶会严重阻碍MP疏水基团的暴露以及后续加热过程中的交联,进而使得复合凝胶质构劣变(即断裂形变时的应力和应变显著降低)。
3 结 论
KG显著影响MP凝胶的质构品质,当添加量小于0.5%时复合凝胶的断裂形变时的应力应变显著提高;当添加量大于1%时复合凝胶的断裂形变时的应力应变显著降低。从石蜡切片和扫描电镜显示,当KG添加量小于1%时,KG均匀分散在蛋白基质中呈填充结构,其稳定水相减少热诱导凝胶过程中蛋白网络结构内部水沟壑的形成,间接促进MP之间的交联,形成致密均一的网络结构并改善复合凝胶的质构特性;当KG添加量大于1%,KG通过水合作用形成的连续弱凝胶,与MP形成互穿结构,进而严重阻碍MP在后续加热过程中的交联,进而使得复合凝胶质构劣变。
[1]庞广昌, 陈庆森, 胡志和, 等. 食品营养与免疫代谢关系研究进展[J]. 食品科学, 2018, 39(1): 1-15. DOI:10.7506/spkx1002-6630-201801001.
[2]刘阳, 唐莉娟, 王凌云, 等. 即食肉制品产业发展现状与市场前景[J]. 食品工业, 2017, 38(2): 275-279. DOI:CNKI:SUN:SP GY.0.2017-02-074.
[3]SIRI-TARINO P W, SUN Q, HU F B, et al. Saturated fat, carbohydrate,and cardiovascular disease[J]. The American Journal of Clinical Nutrition, 2010, 91(3): 502. DOI:10.3945/ajcn.2008.26285.
[4]PANERAS E D, BLOUKAS J G. Vegetable oils replace pork backfat for low-fat frankfurters[J]. Journal of Food Science, 2010, 59(4): 725-728. DOI:10.1111/j.1365-2621.1994.tb08113.x.
[5]SCHMIELE M, POLLONIO M A R. Dietary fiber as fat substitute in emulsified and cooked meat model system[J]. LWT-Food Science and Technology, 2015, 61(1): 105-111. DOI:10.1016/j.lwt.2014.11.037.
[6]ALEJANDRE M, POYATO C, ANSORENA D, et al. Linseed oil gelled emulsion: a successful fat replacer in dry fermented sausages[J]. Meat Science, 2016, 121: 107-113. DOI:10.1016/j.meatsci.2016.05.010.
[7]TALUKDER S. Effect of dietary fiber on properties and acceptance of meat products: a review[J]. Critical Reviews in Food Science and Nutrition, 2015, 55(7): 1005-1011. DOI:10.1080/10408398.2012.682230.
[8]MEHTA N, AHLAWAT S. Novel trends in development of dietary fiber rich meat products: a critical review[J]. Journal of Food Science and Technology, 2015, 52(2): 633-647. DOI:10.1007/s13197-013-1010-2.
[9]SUN F Y, XIONG S L, ZHAO S. Effects and mechanism of modified starches on the gel properties of myofibrillar protein from grass carp[J]. International Journal of Biological Macromolecules, 2014, 64:17-24. DOI:10.1016/j.ijbiomac.2013.11.019.
[10]WU C H, YE X H, HU Y J. The effect of curdlan on the rheological properties of restructured ribbonfish (Trichiurus spp.) meat gel[J]. Food Chemistry, 2015, 179: 222-231. DOI:10.1016/j.foodchem.2015.01.125.
[11]GIBIS M, SCHUH V, WEISS J. Effects of carboxymethyl cellulose(CMC) and microcrystalline cellulose (MCC) as fat replacers on the microstructure and sensory characteristics of fried beef patties[J]. Food Hydrocolloids, 2015, 45: 236-246. DOI:10.1016/j.foodhyd.2014.11.021.
[12]MONTERO P, HURTADO J L, PEREZMATEOS M. Microstructural behavior and gelling characteristics of myosystem protein gels interacting with hydrocolloids[J]. Food Hydrocolloids, 2000, 14(5):455-461. DOI:10.1016/S0268-005X(00)00025-4.
[13]ZHAO Y Y, HOU Q, ZHUANG X M, et al. Effect of regenerated cellulose fiber on the physicochemical properties and sensory characteristics of fat-reduced emulsified sausage[J]. LWT-Food Science and Technology, 2018, 97: 157-163. DOI:10.1016/j.lwt.2018.06.053.
[14]ZHUANG X B, JIANG X P, ZHOU H Y, et al. Insight into the mechanism of myofibrillar protein gel influenced by konjac glucomannan: moisture stability and phase separation behavior[J]. Food Chemistry, 2020, 229: 127941. DOI:10.1016/j.foodchem.2020.127941.
[15]ZHUANG X B, JIANG X P, ZHOU H Y, et al. Insight into the mechanism of physicochemical influence by three polysaccharides on myofibrillar protein gelation[J]. Carbohydrate Polymers, 2020, 229:115449. DOI:10.1016/j.carbpol.2019.115449.
[16]AYADI M, KECHAOU A, MAKNI I, et al. Influence of carrageenan addition on turkey meat sausages properties[J].Journal of Food Engineering, 2009, 93(3): 278-283. DOI:10.1016/j.jfoodeng.2009.01.033.
[17]ZHANG T, XU X Q, JI L, et al. Phase behaviors involved in surimi gel system: effects of phase separation on gelation of myofibrillar protein and kappa-carrageenan[J]. Food Research International, 2017, 100:361-368. DOI:10.1016/j.foodres.2017.07.025.
[18]PERRECHIL F A, CUNHA R L. Stabilization of multilayered emulsions by sodium caseinate and kappa-carrageenan[J].Food Hydrocolloids, 2013, 30(2): 606-613. DOI:10.1016/j.foodhyd.2012.08.006.
[19]HAN M Y, XU X, ZHOU G L. Low-field NMR study of heatinduced gelation of pork myofibrillar proteins and its relationship with microstructural characteristics[J]. Food Research International, 2014,62: 1175-1182. DOI:10.1016/j.foodres.2014.05.062.
[20]BERTRAM H C, KRISTENSEN M, ANDERSEN H J. Functionality of myofibrillar proteins as affected by pH, ionic strength and heat treatment: a low-field NMR study[J]. Meat Science, 2004, 68(2): 249-256. DOI:10.1016/j.meatsci.2004.03.004.
[21]CZERNER M, FASCE L A, MARTUCCI J F, et al. Deformation and fracture behavior of physical gelatin gel systems[J].Food Hydrocolloids, 2016, 60: 299-307. DOI:10.1016/j.foodhyd.2016.04.007.
[22]GRAVELLE A J, BARBUT S, MARANGONI A G. Food-grade filler particles as an alternative method to modify the texture and stability of myofibrillar gels[J]. Science Report, 2017, 7(1): 11544. DOI:10.1038/s41598-017-11711-1.
[23]PUGNALONI L A, MATIA-MERINO L, DICKINSON E.Microstructure of acid-induced caseinate gels containing sucrose:quantification from confocal microscopy and image analysis[J].Colloids and Surfaces B-Biointerfaces, 2005, 42(3/4): 211-217.DOI:10.1016/j.colsurfb.2005.03.002.
[24]SALVADOR P, TOLDRA M, PARES D. Microstructure-function relationships of heat-induced gels of porcine haemoglobin[J].Food Hydrocolloids, 2009, 23(7): 1654-1659. DOI:10.1016/j.foodhyd.2008.12.003.
[25]XIONG G Q, CHENG W, YE L X, et al. Effects of konjac glucomannan on physicochemical properties of myofibrillar protein and surimi gels from grass carp (Ctenopharyngodon idella)[J]. Food Chemistry, 2009, 116(2):413-418. DOI:10.1016/j.foodchem.2009.02.056.
[26]WU M, XIONG Y L, JIE C, et al. Rheological and microstructural properties of porcine myofibrillar protein-lipid emulsion composite gels[J]. Journal of Food Science, 2010, 74(4): 207-217. DOI:10.1111/j.1750-3841.2009.01140.x.
[27]SHAO X L, LI Y F. Application of low-field NMR to analyze water characteristics and predict unfrozen water in blanched sweet corn[J]. Food and Bioprocess Technology, 2013, 6(6): 1593-1599.DOI:10.1007/s11947-011-0727-z.
[28]GOETZ J, KOEHLER P. Study of the thermal denaturation of selected proteins of whey and egg by low resolution NMR[J]. LWTFood Science and Technology, 2005, 38(5): 501-512. DOI:10.1016/j.lwt.2004.07.009.
[29]ZHUANG X B, HAN M Y, JIANG X P, et al. The effects of insoluble dietary fiber on myofibrillar protein gelation: microstructure and molecular conformations[J]. Food Chemistry, 2019, 275: 770-777.DOI:10.1016/j.foodchem.2018.09.141.
[30]ZHUANG X B, ZHANG W G, LIU R, et al. Improved gel functionality of myofibrillar proteins incorporation with sugarcane dietary fiber[J]. Food Research International, 2017, 100: 586-594.DOI:10.1016/j.foodres.2017.07.063.
[31]DAVILA E, TOLDRA M, PARES D. Characterization of plasma protein gels by means of image analysis[J]. LWT-Food Science and Technology, 2007, 40(8): 1321-1329. DOI:10.1016/j.lwt.2006.10.004.