枸杞(Lycium bararum)是茄科、枸杞属植物,主要种植于中国、韩国、日本、欧洲、北美和地中海的干旱和半干旱地区[1]。目前,枸杞的主要产地是中国,其年均产量已达10万 t[2]。枸杞的品种包括宁夏枸杞(Lycium bararum L.)、枸杞(Lycium chinense Mill.)、黑果枸杞(Lycium ruthenicum Murr.)、截萼枸杞(Lycium truncatum Y. C. Wang)、新疆枸杞(Lycium dasystemum Pojark)、柱筒枸杞(Lycium cylindricum)和云南枸杞(Lycium yunnanense Kuang)7种[3],其中宁夏枸杞是唯一被2015年版《中华人民共和国药典》收录的品种[4]。
枸杞子是枸杞的果实,具有免疫调节、抗氧化、抗衰老、抗糖尿病、抗肿瘤、细胞保护和神经保护等功能活性[1,5],在2002年被国家卫生健康委员会确认为药食同源食物[6]。枸杞子中成分复杂,包括多糖、类胡萝卜素、莨菪亭(7-羟基-6-甲氧基香豆素)、黄酮、甜菜碱、多酚、脑苷脂、β-谷甾醇、蛋白质、不饱和脂肪酸及微量元素等200多种物质[1-2]。其中,枸杞子多糖(Lycium bararum polysaccharides,LBP)是一组分子质量为10~2 300 kDa的水溶性糖缀合物,占枸杞子干质量的5%~8%,是枸杞子中主要的功能活性物质[1]。截至目前,LBP已被证实在免疫调节、抗氧化和抗衰老等方面均能发挥显著的功能活性[7-8]。
免疫系统与人体各项生命活动息息相关。现有研究表明,LBP对外周免疫器官(脾脏、肠系膜淋巴结和扁桃体等)、中枢免疫器官(骨髓和胸腺)的生长均有促进作用,因而能够提高机体免疫力[9]。另一方面,当机体自身免疫水平过高时,LBP还能调节T淋巴细胞、B淋巴细胞、自然杀伤(natural killer,NK)细胞、抗原呈递细胞的生长分化和细胞因子分泌[10],下调机体免疫应答水平,拮抗过度免疫应答[11]。因此,LBP可通过多靶点、多途径发挥双向免疫调节作用,帮助机体恢复免疫稳态。但现有研究多从LBP对某一免疫器官或某一免疫细胞的作用效果出发,探讨其促进机体免疫功能的分子机制,缺乏对其双向免疫调节机制的全面阐释。本文将综合考虑LBP对免疫系统的促进和抑制作用,对LBP在肠黏膜屏障、肠道菌群、免疫细胞、神经内分泌免疫系统的作用机制进行综述(图1)。
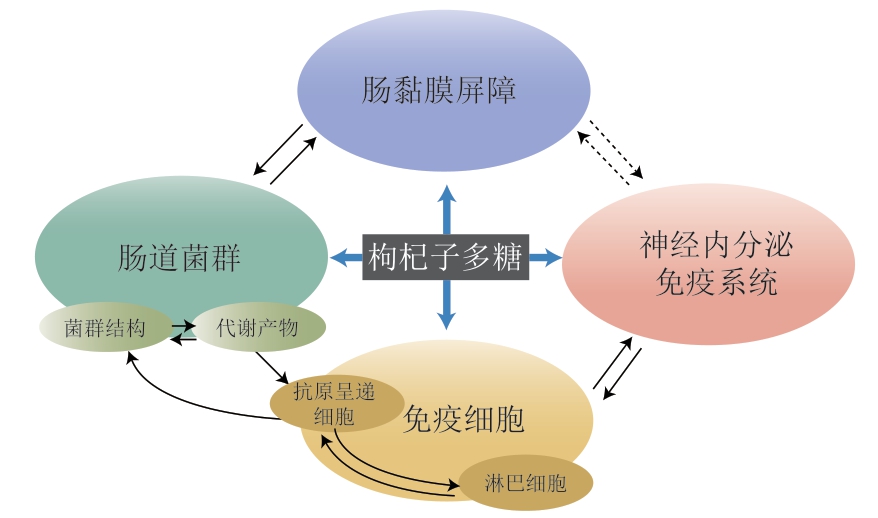
图1 LBP对机体免疫系统的影响
Fig. 1 Effect of Lycium barbarum polysaccharides on the immune system
近年来,病毒、癌症和过敏等均已成为人类生存的重大威胁。多数病毒和癌细胞能够严重破坏机体的免疫抵抗功能。因此,具有加速诱导免疫应答功能的免疫增强剂已被广泛地应用于抗病毒治疗、抗肿瘤治疗、多种疫苗开发和动物饲料新配方中[12-13]。过敏一般指机体对自身或无害的食物/药品/环境中的某些成分所产生的过度免疫反应[14-15],可引发各类症状:如皮肤方面的瘙痒、红肿、荨麻疹;呼吸道方面的哮喘、咳嗽;胃肠道方面的恶心、呕吐、腹泻等,严重时可引发过敏性休克甚至死亡[15]。免疫抑制剂可降低免疫应答水平,阻碍免疫反应的发生,因此对于过敏性疾病的预防和治疗具有重要作用。本文对LBP发挥双向免疫调节功能的作用途径和分子机制进行综述,以期为其进一步在抗病毒治疗、抗肿瘤治疗、多种疫苗开发、动物饲料免疫增强配方和抗过敏药物/食品中的应用提供参考。
1 枸杞子多糖对肠黏膜屏障的保护作用
人类小肠黏膜面积约300 m2,含有大量淋巴组织,并覆盖有人体80%以上免疫球蛋白分泌细胞[16]。这些组织与细胞共同构成了肠道黏膜屏障,保护机体免受细菌、病毒等致病性微生物的侵袭。石玉祥等[17]使用C57BL/J小鼠模型研究了LBP摄入对小肠上皮淋巴细胞(intestinal epithelial lymphocytes,IEL)和小肠绒毛上杯状细胞(goblet cell,GC)的影响,结果发现LBP作用后,上述两种细胞的数量增加且具有向肠内层移动的趋势,同时,肠黏膜白细胞介素(interleukin,IL)-2的含量也显著增加。IEL是肠道相关淋巴组织的重要组成部分,其数量与肠道吞噬抗原能力和杀灭病原微生物效果密切相关[18-19]。IEL的数量增加,证明小肠局部黏膜免疫屏障的完整性有所提升,小肠的免疫防御功能更加完善。GC作为一种分泌细胞,可大量分泌黏蛋白(mucin,MUC)2[20-21],从而形成黏液层,保护肠上皮表面免受细菌、病毒及水解酶的侵害[22]。石玉祥等[17]的研究证明,LBP可通过增加GC数量、改变GC在不同肠段的数量分布,保护小肠上皮黏液层结构,进而增强机体的特异性免疫。但该研究中所使用的LBP纯度仅有50%左右,结构特征尚未得到表征。Kang Yifei等[23]的研究也证实,日常摄入枸杞可增加肠道内MUC1的分泌,对结肠炎具有一定治疗和缓解作用。Zhao Qihan等[24]研究发现,灌胃枸杞和黄芪的粗多糖混合物后,兔血液中的D-乳酸和细菌内毒素含量显著降低。D-乳酸是肠道菌群的主要代谢产物。细菌内毒素主要存在于肠杆菌的细胞壁中[25]。当肠黏膜屏障破坏时,肠道通透性随之改变,D-乳酸和细菌内毒素会被大量释放到血液中[26]。
理论上,LBP可作为一种非消化性多糖被肠道微生物代谢,从而避免了微生物因营养物质匮乏而去分解肠道内的黏蛋白(图2)。非消化性多糖如卡拉胶、硫酸软骨素、海藻酸钠、菊粉等均能通过该途径维持黏液层厚度,避免有害微生物跨越肠黏膜屏障[27-28]。值得注意的是,不同肠道微生物对不同多糖的分解效率并不一致,而这与多糖的结构特征具有密不可分的关系。具体来说,革兰氏阳性双歧杆菌更倾向于利用聚合度较低的多糖;变形菌门只能降解单糖和双糖,半乳糖胺含量太高则会降低炎症性变形菌的丰度;拟杆菌属最善于利用糖胺聚糖[29]。Ding Yu等[30]的研究证实,摄入LBP后的小鼠肠隐窝更深,绒毛更长,结肠GC数量更多且排列更加整齐。此外,有些多糖还能通过提升肠道内MUC2、紧密连接蛋白(闭锁小带蛋白1(zonula occludens 1,ZO-1)、Claudin-1、Claudin-4等)的表达水平,从而提高肠黏膜免疫屏障的完整性[31]。除保护肠道屏障外,肠道黏蛋白还能促进抗原呈递细胞的表型和功能成熟[32],从而提高机体对外源危害性微生物的免疫应答水平。
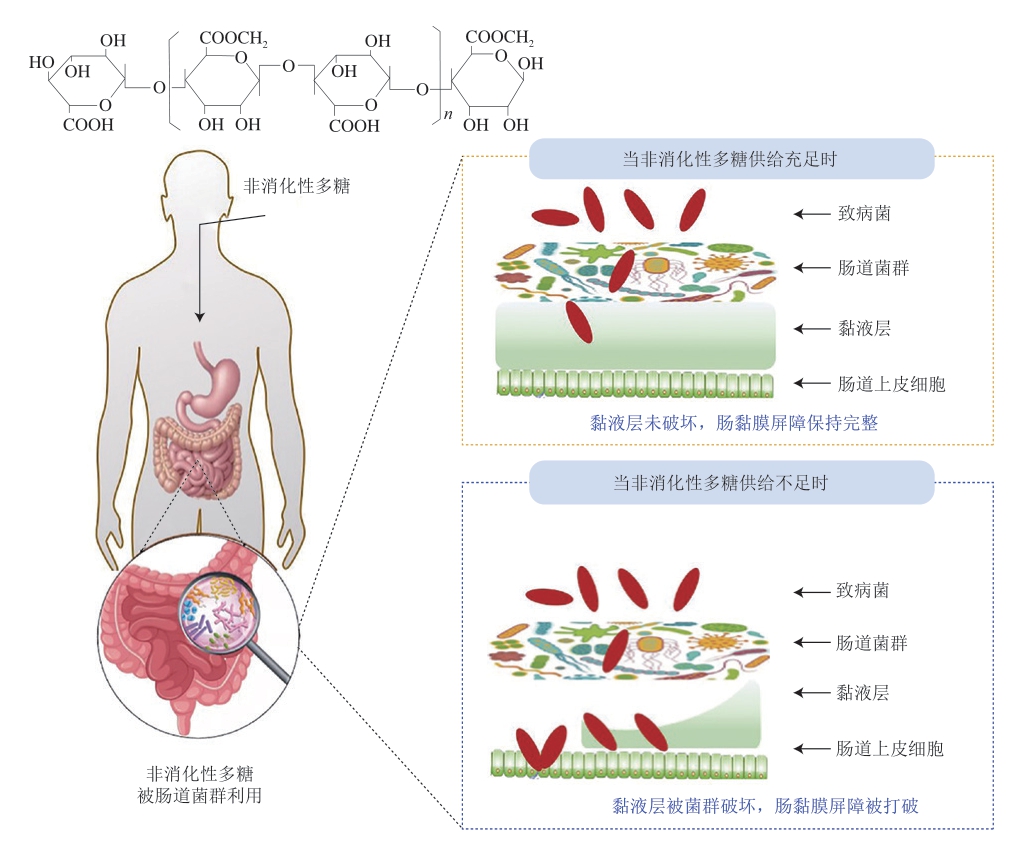
图2 非消化性多糖对胃肠黏膜的保护作用
Fig. 2 Protective effect of non-digestible polysaccharides on gastrointestinal mucosa
本课题组前期用柱层析法分离得到均一性的LBP组分,其结构为以β-(1→6)-半乳糖为主链,C3位被少量半乳糖和大量阿拉伯糖取代的多分支阿拉伯半乳聚糖结构[33]。为了提升LBP提取的效率和得率,本课题组进一步优化了其分离纯化工艺,通过分步沉淀法可以快速大量制备均一性的枸杞子阿拉伯半乳聚糖组分LBGP-I-3(mw 91.2 kDa)[33],为充分解析LBP结构与其功能之间的构效关系奠定了基础。后期实验结果表明,LBGP-I-3是LBP主要的功能性成分,能发挥免疫调节、抗衰老、抑制癌细胞生长等多种生物功能[34-37]。摄入LBGP-I-3后,结肠炎小鼠的肠黏膜屏障损伤明显得到修复,肠道黏蛋白MUC2和ZO-1的表达水平显著升高,说明LBGP-I-3能保障肠道黏膜屏障的完整性,维持机体正常的免疫功能[36]。然而,目前有关LBP对不同肠道上皮细胞(如GC和微褶皱细胞)的具体影响及LBP调控肠道黏蛋白分泌的分子机制尚未阐明,后期研究可针对以上问题继续深入探究,为进一步理解LBP保护肠黏膜屏障的具体机理奠定基础。
2 枸杞子多糖对肠道菌群结构及其代谢产物的调节作用
2.1 肠道菌群结构
肠道菌群及其代谢产物可与机体免疫系统相互作用,因此能够对机体产生免疫调节作用[38]。某些高分子质量的LBP可作为能量物质被肠道菌群利用,由此改变菌群的结构、丰度和代谢产物,从而调控机体免疫状态。此外,由于不同菌群所表达的糖苷酶体系不同,LBP可对不同菌种产生促生长或抑制生长的不同影响[39]。王莹[9]利用水提醇沉提取、DEAE-52纤维素柱和HW-65色谱柱层析法纯化到了两个均一性的LBP组分(LBP1和LBP2),其分子质量分别为1 207.4 kDa和125 kDa。经体外模拟消化和Caco-2细胞模型转运实验发现,LBP1和LBP2均能耐受消化,且不易被小肠吸收。上述LBP1显著提高了双歧杆菌、乳杆菌、拟杆菌、普雷沃氏菌科和理研菌科的相对丰度,降低了大肠杆菌、副拟杆菌和瘤胃球菌的相对丰度[9]。有研究表明,当小鼠结肠中的双歧杆菌和乳杆菌丰度增加时,机体针对β-乳球蛋白的过度免疫反应得到了明显抑制[40]。
Zhou Fang等[41]使用水溶醇沉和大孔树脂S-8纯化得到LBP(阿拉伯糖、鼠李糖、木糖、甘露糖、半乳糖和葡萄糖的物质的量比为0.18∶0.81∶0.07∶2.17∶0.23∶6.52),并重点研究了LBP对肠道内乳酸菌的调控作用,发现LBP促进了乳酸菌中的长双歧杆菌、婴儿双歧杆菌Bi-26和嗜酸乳杆菌NCFM的增殖,其作用机制可能是LBP促进了菌体内丙酮酸代谢、碳代谢和糖酵解/糖异生等生物代谢过程。此外,LBP还提高了婴儿双歧杆菌 Bi-26中β-半乳糖苷酶(β-galactosidase,β-GAL)和乳酸脱氢酶(lactate dehydrogenase,LDH)的活性[41]。嗜酸乳杆菌NCFM与LBP共培养时,β-GAL、LDH、己糖激酶、6-磷酸果糖激酶和丙酮酸激酶的活性也显著升高[41]。与该结果类似的是,Zhu Wei等[42]使用LBP(阿拉伯糖、鼠李糖、木糖、甘露糖、半乳糖、葡萄糖物质的量比为0.18∶0.81∶0.07∶2.17∶0.23∶6.52)刺激昆明小鼠后发现,嗜酸乳杆菌和长双歧杆菌的相对丰度明显增加。嗜酸乳杆菌可刺激人外周血单核细胞分泌抗炎细胞因子(如肿瘤坏死因子(tumor necrosis factor,TNF)-β和IL-10),双歧杆菌可诱导机体分泌免疫球蛋白(如免疫球蛋白(immunoglobulin,Ig)G和IgA)[43]。这些益生菌都能提高人体的自身免疫功能,同时避免过度免疫的发生。
程翔[44]使用LBP刺激肠道菌群失调的昆明小鼠,发现小鼠肠道内的肠杆菌、双歧杆菌和乳杆菌丰度明显增加。Ding Yu等[45]使用水提醇沉法得到枸杞粗多糖LBPS,并以此刺激BALB/c小鼠,发现LBPS可以有效改善环磷酰胺诱导的免疫抑制,提升肠道中乳杆菌和拟杆菌的相对丰度。本课题组的研究也同样表明,小鼠经口摄入枸杞子阿拉伯半乳聚糖后,肠道中Muribaculaceae、Lachnospiraceae、Ruminococcaceae、Prevotellaceae和Rikenellaceae等有益菌丰度上升[36]。已有研究使用Pearson法对上述部分菌种的相对丰度与免疫功能指数之间的相关性进行分析,结果发现Prevotellaceae和Rikenellaceae丰度越高,免疫器官指数(脾脏指数和胸腺指数)、淋巴细胞(T细胞和B细胞)数量、免疫球蛋白(IgG和IgM)水平以及CD4+T细胞数量越高[3]。
2.2 肠道菌群的代谢产物
LBP可作为能量物质促进部分肠道菌群生长,同时产生乙酸、丙酸等短链脂肪酸(short-chain fatty acids,SCFAs)。SCFAs可通过多种途径调控机体免疫状态:1)抑制组蛋白脱乙酰酶的活性,从而下调促炎因子和肿瘤坏死因子的表达[46];2)负向调控核因子κB(nuclear factor κB,NF-κB)通路,降低氧化应激水平,减轻机体炎症反应[39];3)通过肠道上皮细胞或免疫细胞表面的G蛋白偶联受体(G protein-coupled receptors,GPR)(包括GPR43和GPR41)传递信号[47],抑制腺苷酸环化酶的活性,减少环磷酸腺苷的产生,同时提升细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK)和促分裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)通路的应答水平[48]。MAPK、ERK通路的激活往往伴随着细胞因子(如IL-4、IL-10、TNF-β)分泌量的增加,从而改变机体的免疫/炎症水平。
从SCFAs对机体免疫系统的调节效果来看,双向调控作用较为多见。一方面,SCFAs可通过GPR43受体刺激抗炎型巨噬细胞M2的增殖与极化[49],促进中性粒细胞的迁移[50],提高机体的免疫应答水平;另一方面,SCFAs可诱导形成促炎因子TNF-α,激活NOD样受体热蛋白结构域相关蛋白3(NOD-like receptor thermal protein domain associated protein 3,NLRP3)炎症小体[51],最后诱导炎症小体释放IL-18[52]。IL-18可与抗原呈递细胞和初始T细胞反应,诱导形成调节型T细胞,防止机体产生Th2型过度免疫应答[53]。
近年来,精准解析LBP对肠道菌群和其代谢产物的调节机制已成为研究热点。Ding Yu等[54]利用水提醇沉法提取得到LBP,其单糖组成的物质的量分数为葡萄糖酸5.12%、半乳糖醛酸12.40%、葡萄糖2.15%、半乳糖39.67%和阿拉伯糖40.66%。研究证实,LBP在肠道菌群的作用下代谢生成了乙酸、丙酸、丁酸、异丁酸、戊酸、异戊酸、己酸和异己酸,其中乙酸含量最高,约占SCFAs总产量的55%,戊酸含量最低,约占SCFAs总产量的6%[54]。Cao Cui等[36]的研究表明,枸杞子阿拉伯半乳聚糖LBP-3显著促进了结肠炎模型小鼠肠道中乙酸、丙酸、丁酸的生成,恢复了肠道稳态,提升了机体免疫抵抗水平。
3 枸杞子多糖对免疫细胞的作用
3.1 枸杞子多糖进入机体内循环的机制
免疫细胞大多存在于机体的血液、淋巴组织、黏膜等部位,多糖需首先跨越肠道屏障吸收入血,才能与各免疫细胞作用。现有研究对于多糖能否跨越上皮细胞屏障进入机体内循环系统尚存在争议。王莹[9]借助Caco-2细胞模型研究小肠上皮细胞对LBP中两个组分(LBP1和LBP2,mw 1 207.4 kDa和125 kDa)的转运效率,结果发现其累积转运率极低,分别为0.99%和1.15%。说明上述两组分在小肠中不易吸收。相较于大分子物质,低分子质量、体积较小的分子更易跨过肠道上皮细胞屏障而进入机体内循环。如唐华丽[55]的研究表明,LBP3(mw 4.92 kDa)能够以原型形式参与吸收和代谢。口服异硫氰酸酯荧光素(fluorescein isothiocyanate,FITC)标记的LBP3(LBP3-FITC)1 h后,大鼠的小肠和胃部检测到了大量的LBP3-FITC;口服6 h后,小肠和胃部的LBP3-FITC含量降低,但肝脏、肾脏和大肠中的LBP3-FITC含量显著上升[55]。针对上述研究结果不一致的情况,分析其原因主要在于各研究中使用的多糖提取及纯化手段不一样,导致提取得到组分的分子质量差异较大。其次,各研究中借助的细胞或动物模型并不一致,也对研究结果影响较大。
一些支持多糖可以进入内循环的研究者认为,人体消化系统内缺乏针对多糖类物质的水解酶,因此口服多糖可通过与胃肠道上皮细胞或肠相关淋巴组织结合,从而进入机体内循环[56]。根据相关文献,可总结出3 条多糖跨越肠道上皮细胞的途径(图3)。途径一:肠道相关的淋巴组织(gut associated lymphoid tissue,GALT)中某些组织,如派氏淋巴结和孤立淋巴滤泡中的微褶皱细胞,可通过跨细胞途径从肠腔中摄取大分子物质(包括多糖)。随后,这些物质被呈递给位于上皮细胞下方或者M细胞基底表面“口袋”中的树突状细胞(dendritic cell,DC),推动下一步生化反应[57-58]。途径二:DC通过延伸“触角”摄取肠腔中的多糖,并将免疫信号传递给血液中的淋巴细胞[59]。途径三:多糖被肠道微生物分解为寡糖片段,菌群将多糖代谢后也可产生SFAC,这些小分子物质可经肠上皮细胞的跨细胞途径进入血液,从而与诸多免疫细胞反应,调节机体免疫状态。
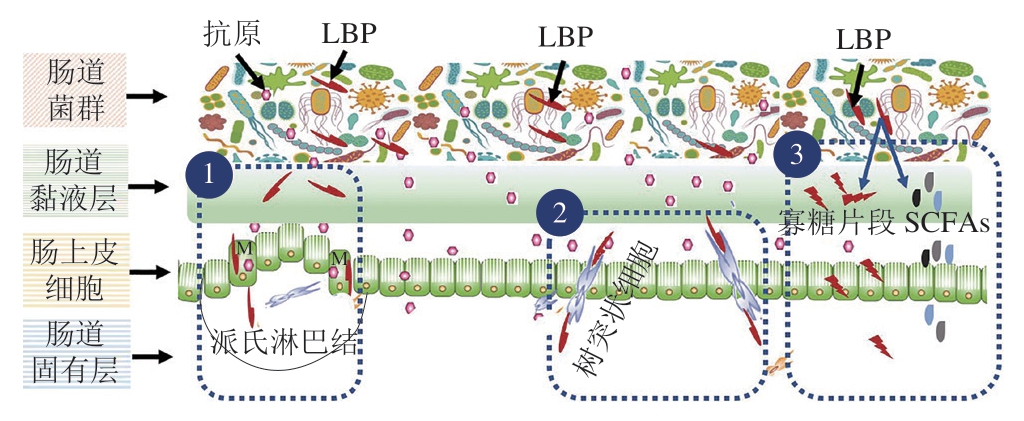
图3 多糖跨越肠道上皮细胞的可能途径
Fig. 3 Possible pathways for polysaccharides to cross intestinal epithelial cells
3.2 枸杞子多糖对抗原呈递细胞的影响
机体内存在多种免疫细胞,不同细胞的功能各不相同。抗原呈递细胞(主要包括巨噬细胞和DC)可与入侵机体的病原微生物或抗原直接反应,随后合成和分泌趋化因子和细胞因子[60],激活T/B淋巴细胞或调整T淋巴细胞的分化方向[38],从而调节整个免疫反应的进程。
3.2.1 巨噬细胞
LBP对巨噬细胞的影响效果呈现双向特征,一方面,LBP可增强巨噬细胞的吞噬能力[61],促进其分泌TNF-α[34]、IL-1β、IL-6以及NO等炎症介质,提升机体对外源有毒有害物质的免疫应答水平[62];另一方面,在细胞脂多糖与LBP共同刺激巨噬细胞时,LBP抑制了TNF-α、IL-6和NO的过度产生,降低了脂多糖的毒害作用[63],而且这种抑制作用可能与对c-Jun氨基末端激酶(c-Jun N-terminal kinase,JNK)通路和ERK1/2/MAPK通路的抑制效果有关[11]。此外,LBP还能调节促炎型巨噬细胞M1与抗炎型巨噬细胞M2之间的相互转化[64-65],从而发挥“提升机体对病原微生物的免疫应答”和“抑制过度免疫应答”的双向调节作用。
LBP调控巨噬细胞的分子机制已被众多学者反复探究,目前多项证据显示,LBP可与巨噬细胞表面的Toll样受体(toll-like receptor,TLR)2/4结合,刺激细胞内的髓样分化因子(myeloid differentiation factor,MyD)88、TIR结构域衔接蛋白(TIR domain-containing adaptor,TRIF)等信号蛋白,进而激活MAPK、NF-κB等信号通路,诱使巨噬细胞分泌TNF-α、IL-1、IL-6等炎症因子[39,66]。张小锐[67]使用水溶醇沉和DEAE纤维素柱纯化法得到了LBP与蛋白的复合物LBPF4,又通过Pronase E降解释放得到均一性的多糖组分LBPF4-OL(mw 81 kDa)。通过使用抗体封闭、3H-胸腺嘧啶核苷掺入法、TLR基因突变小鼠实验等手段,证明了LBPF4在巨噬细胞表面的作用受体为TLR4和TLR2[67]。王莹[9]借助小鼠单核巨噬细胞白血病细胞(RAW264.7)模型研究均一性枸杞子多糖组分LBP1(1 207.5 kDa)和LBP2(125 kDa)的免疫调节活性,发现LBP1和LBP2均能显著促进RAW264.7细胞增殖,提高细胞中IL-6、TNF-α、IL-1β和诱导型一氧化氮合酶(inducible nitric oxide synthase,iNOS) mRNA表达量,同时诱导p-JNK MAPKs信号通路的激活。
另外,LBP对巨噬细胞的增殖、细胞活力和吞噬功能均有促进作用[68]。如Zhang Xiaorui等[69]发现LBPF4-OL(mw 181 kDa)可显著刺激BALB/c小鼠体内的巨噬细胞增殖;杨青[65]发现LBP可刺激RAW264.7细胞的增殖;Gong Guiping等[34]的研究显示,枸杞子阿拉伯半乳聚糖(mw 91.2 kDa)不仅能将RAW264.7细胞活力提升到126.39%(空白组的细胞活力设置为100%),同时还能提升RAW264.7细胞的吞噬能力和酸性磷酸酶(acid phosphatase,AP)活力。AP是巨噬细胞的标志性酶,可协助细胞完成吞噬行为[70]。AP活力越高,代表巨噬细胞的免疫活性越强[2]。
从主链-支链的结构特征来看,LBP对巨噬细胞的刺激可能与其多支链结构有着密切联系:Peng Qiang等[71]在前期通过凝胶渗透色谱法对黑果枸杞中的多糖进行分离纯化,得到了多糖组分LRGP3,并表征其为以β-(1→3)-Gal为主链,O6位被大量半乳糖和阿拉伯糖取代的多分支结构。随后,该团队继续对LRGP3进行化学改性,通过乙酰化、部分酸水解和酶消化将LRGP3的主链与测链分离,发现与主链结构相比,侧链结构(阿拉伯糖、半乳糖、鼠李糖的物质的量比为16.8∶1.4∶1.0)更能刺激巨噬细胞的增殖[72]。
许多研究中提取得到的LBP都是阿拉伯半乳聚糖,而阿拉伯半乳聚糖具有许多功能性基团,可影响其免疫调节活性。Xie Gang等[73]的研究表明,阿拉伯半乳聚糖中硫酸基的含量与其激活巨噬细胞的能力有关。Li Ningyang等[74]推测,这是由于硫酸基含量越高,多糖在水中的溶解性越强,也越容易通过与其他功能性基团接枝来发挥免疫调节活性。Wang Xuesong等[75]的研究表明,半乳糖醛酸骨架中的乙酰基含量越高,其免疫调节活性越差。Ferreira等[76]报道称,具有脱酯化同型半乳糖醛酸骨架的阿拉伯半乳聚糖往往具有免疫抑制活性,而该现象的产生与半乳糖醛酸残基中带负电荷的羧基有关。
3.2.2 树突状细胞
DC广泛分布于机体的皮肤、气道、口腔黏膜、胃肠道上皮和淋巴器官等部位,可通过摄取、加工处理和递呈抗原介导细胞免疫应答,对机体的免疫状态起到至关重要的作用[77]。根据DC的发育状态可将其分为4 类,分别是DC前体细胞、未成熟DC、迁移期DC和成熟DC[78]。在病原体感染、炎症因子或病原微生物的刺激下,DC前体细胞会分化为未成熟DC。未成熟DC主要发挥吞噬功能,具有极强的抗原摄取能力,但往往不能呈递抗原或活化初始T细胞[78]。而成熟DC能够加工、处理抗原,并将抗原以抗原肽——主要组织相容性复合体2类分子复合物(major histocompatibility complex class II,MHCII)形式呈递给初始T细胞,诱导下一步免疫反应[78]。迁移期DC是处于未成熟DC和成熟DC中间阶段的一类DC[77]。与其他3种类别相比,未成熟DC在机体内的含量最高[79]。
LBP对DC的影响可概括为4个方面:1)促进DC增殖;2)诱导DC表型和功能的成熟;3)刺激DC产生不同细胞因子,推动后续免疫反应;4)改变DC的吞噬效率。如郝习等[80]研究表明,LBP可促进DC的增殖;Zhu Jie等[81]研究表明,LBP(mw 31 kDa)可与DC表面的TLR2/4受体结合,继而激活NF-κB通路,诱导细胞产生炎性介质IL-12 p40(图4)。Duan Xiangguo等[82]发现LBP可通过TLR4-MAPK-Erk1/2-Blimp1通路刺激DC表型成熟,表现为细胞表面MHC-II、CD80和CD86表达量上升,炎性介质IL-6分泌量上升(图4)。此外,还有研究表明LBP可通过TLR2/4受体刺激p38 MAPK等通路,从而释放IL-6、IL-10、单核细胞趋化蛋白-1(monocyte chemotactic protein-1,MCP-1)、干扰素(interferon,IFN)-γ、TNF等细胞因子[83-84]。但也有研究表明,LBP既可以促进未成熟的DC吞噬抗原,也能适度抑制DC的成熟[85]。
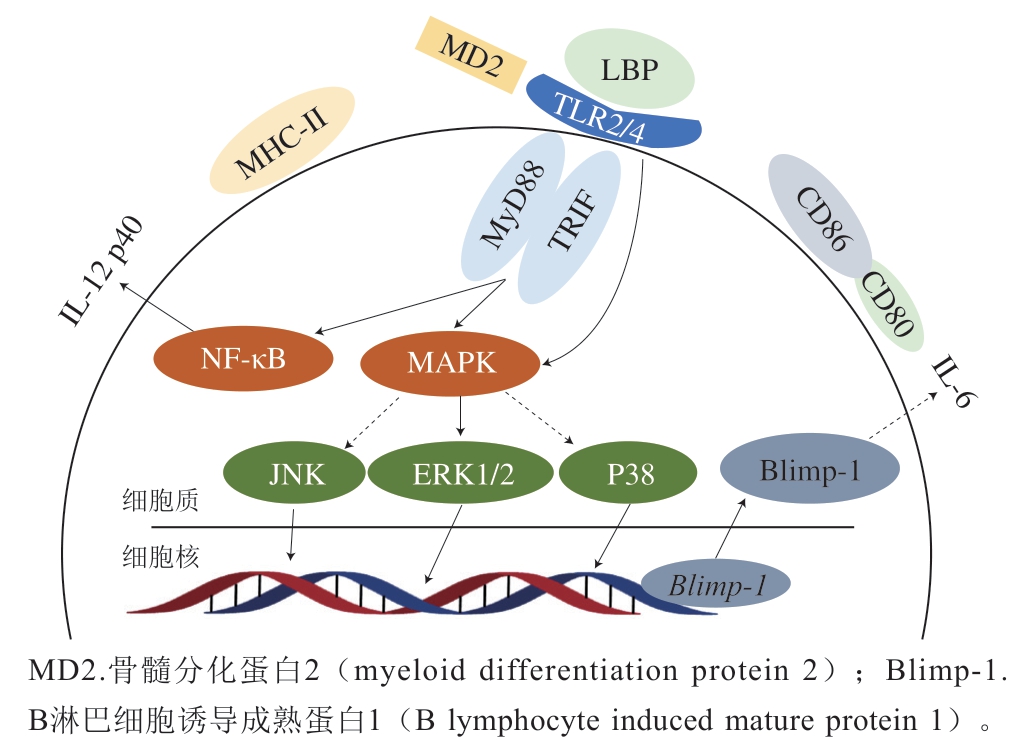
图4 LBP对树突状细胞中部分信号通路的影响[81-82]
Fig. 4 Effect of LBP on some signaling pathways in dendritic cells[81-82]
廖海峰[83]研究表明,不同分子质量的LBP刺激DC成熟的效果各不相同。与其他分子质量范围的LBP相比,LBP3(mw 40~350 kDa)可显著诱导DC表面共刺激因子CD80、CD86、MHC-II的表达,促进细胞的成熟。此外,LBP3还能刺激DC分泌NO[83]。在抗感染免疫机制中,NO与含铁酶活性部位中的Fe-S基团结合,形成铁-亚硝酞基复合物,促使感染病原体的细胞中铁含量迅速降低,从而破坏许多含铁细胞酶的活性,阻断细胞的ATP合成及DNA复制,提升机体对病原体的免疫应答水平[86]。相似地,Zhang Minghui等[87]的研究显示,DC可通过分泌NO抑制T淋巴细胞的增殖,从而起到抑制过度免疫的作用。由此可见,DC可双向调节机体的免疫应答,LBP借助DC发挥免疫调节功能的具体机制还需要全面而系统的研究。
3.3 枸杞子多糖对淋巴细胞的影响
淋巴细胞主要存在于淋巴管中循环的淋巴液中,是机体免疫应答功能的重要细胞成分。淋巴细胞是一类具有免疫识别功能的细胞系,按其发生迁移、表面分子和功能的不同,可分为T淋巴细胞(又名T细胞)、B淋巴细胞(又名B细胞)和NK细胞。与LBP对DC的影响类似,LBP也可对淋巴细胞增殖、T细胞分化方向、细胞因子分泌等进行调控。
3.3.1 T细胞
除了可以刺激活化的T细胞增殖[88],LBP还能影响T细胞内凋亡因子的表达量,从而调控T细胞的凋亡[89]。Bo Ruonan等[90]研究发现,卵清蛋白和LBP的合成脂质体有效刺激了体内CD4+T和CD8+T细胞增殖。CD4+和CD8+T细胞是T淋巴细胞的两个亚群,它们的数量及比例与机体的免疫功能息息相关。王莹[9]的研究表明,LBP1(1 207.4 kDa)和LBP2(125 kDa)能有效上调CD4+T和CD8+T细胞的数量,同时提高CD4+T/CD8+T的比值。除了直接刺激T淋巴细胞外,LBP也能通过促进DC细胞功能和表型的成熟,促使DC呈递抗原,从而推动CD4+T大量分化为Th1、Th2细胞或滤泡辅助T(follicular helper T,Tfh)细胞[91]。Th1细胞能够激活巨噬细胞、CD8+T细胞和CD4+T细胞。活化的巨噬细胞吞噬并消化细胞内细菌,IFN-γ激活iNOS合成NO从而直接杀死细胞内细菌和其他病原微生物。Th2细胞可通过分泌IL-4、IL-5、IL-9、IL-10、IL-13和IL-25等细胞因子,刺激浆细胞产生抗体或激活嗜酸性粒细胞攻击微生物,从而提升机体免疫应答水平[38]或诱发超敏反应[38]。作为辅助T细胞的一个亚群,Tfh细胞能调节B细胞成熟,促使其发挥抗体分泌功能。Su Chunxia等[92]研究发现,LBP激活了CXCR5+PD-1+Tfh细胞并诱导其分泌炎性因子IL-21。IL-21可推动初始B细胞的分化,同时介导IgG1和IgG3之间的转换。因此,LBP可作为促进Tfh细胞生成的免疫佐剂来增强T细胞依赖性免疫反应。
3.3.2 B细胞
B细胞主要位于淋巴结皮质浅层的淋巴小结和脾脏的淋巴小结内,在抗原刺激下可分化为浆细胞,浆细胞可合成和分泌抗体,从而参与调节机体的免疫应答。口服LBP可以刺激浆细胞分泌抗体IgG、IgM、IgA,维护机体对氟化钠的抵抗力[93]。Zhang Xiaorui等[94]的研究表明,LBPF4-OL(mw 181 kDa)可通过刺激巨噬细胞分泌TNF-α和IL-1β,而后引发B细胞增殖。该学者又继续对LBPF4-OL的化学结构进行研究,发现LBPF4-OL的单糖组成为鼠李糖、阿拉伯糖和半乳糖(物质的量比为0.05∶1.33∶1.0),其主链的重复单元由β-(1,4)-键连接的半乳糖组成,主链上的分支糖包括少量β-(1,3)-半乳糖和大量的阿拉伯糖[94]。经过酸水解去除支链后,LBPF4-OL的生物活性明显降低,提示LBPF4的分支结构和高聚合度是其发挥免疫调节活性的重要条件[94]。此外,LBP也可通过刺激Th2细胞分泌IL-4,从而诱导B细胞产生IgE[92]。IgE是介导I型变态反应最重要的媒介,它可刺激肥大细胞和嗜碱性粒细胞释放组胺、5-羟色胺和白三烯,从而诱发支气管痉挛、腹泻、过敏性休克等过敏症状[38,95]。但也有报道称,肥大细胞和嗜碱性粒细胞脱颗粒所释放的β-氨基己糖苷酶等物质可以刺激胃肠蠕动和支气管收缩、降低胃液的pH值,从而有效去除影响机体健康的微生物[96]。
3.3.3 NK细胞
NK细胞能够识别靶细胞、杀伤介质,参与机体的抗肿瘤、抗感染和超敏反应。与T、B淋巴细胞不同的是,NK细胞无需预先致敏就能非特异性杀伤肿瘤细胞和病毒感染后的细胞[97]。Yan Tinghu等[98]验证了灰树花多糖、香菇多糖、灵芝多糖、酵母葡聚糖和LBP对NK细胞的影响。结果发现这些多糖均可促进NK细胞分泌IFN-γ和穿孔素,显著增加NK细胞的细胞毒性。刘彦平等[99]的研究表明,LBP能提高被环磷酰胺抑制的NK细胞活性,恢复机体免疫功能。Li Qi等[100]使用不同植物多糖刺激NK细胞,结果发现枸杞多糖能提高NK细胞的细胞毒活性。黄振华等[101]借助免疫抑制小鼠模型,发现LBP提高了NK细胞的杀伤活性,并进一步推测LBP的免疫促进功能与Band-3蛋白(能维持正常红细胞形态和功能)表达水平的恢复有关。肖芳等[102]的研究表明,LBP能够通过上调人前髓细胞HL-60表面靶细胞相应配体的表达水平,刺激NK细胞增强杀伤活性,提升机体对白血病等肿瘤疾病的抵抗作用。
4 枸杞子多糖对神经内分泌免疫系统的作用
免疫系统、神经系统和内分泌系统三者相互影响,形成神经内分泌免疫系统(图5)。脊髓、脑干、下丘脑、海马体和大脑皮层中都存在调节免疫活动的神经中枢。这些神经中枢可以支配免疫器官的神经末梢释放神经递质如乙酰胆碱(acetylcholine,Ach)、去甲肾上腺素(noradrenaline,NA)和5-羟色胺(5-hydroxytryptamine,5-HT),也能刺激下丘脑-垂体-巴腺体轴释放促甲状腺激素和生长素[103]。LBP对神经内分泌免疫系统具有明显影响[39]。聂伟等[104]报道称LBP能降低脾脏和下丘脑中NA、5-HT的水平。而NA和5-HT均能够激活B细胞从而提升机体免疫功能[105]。
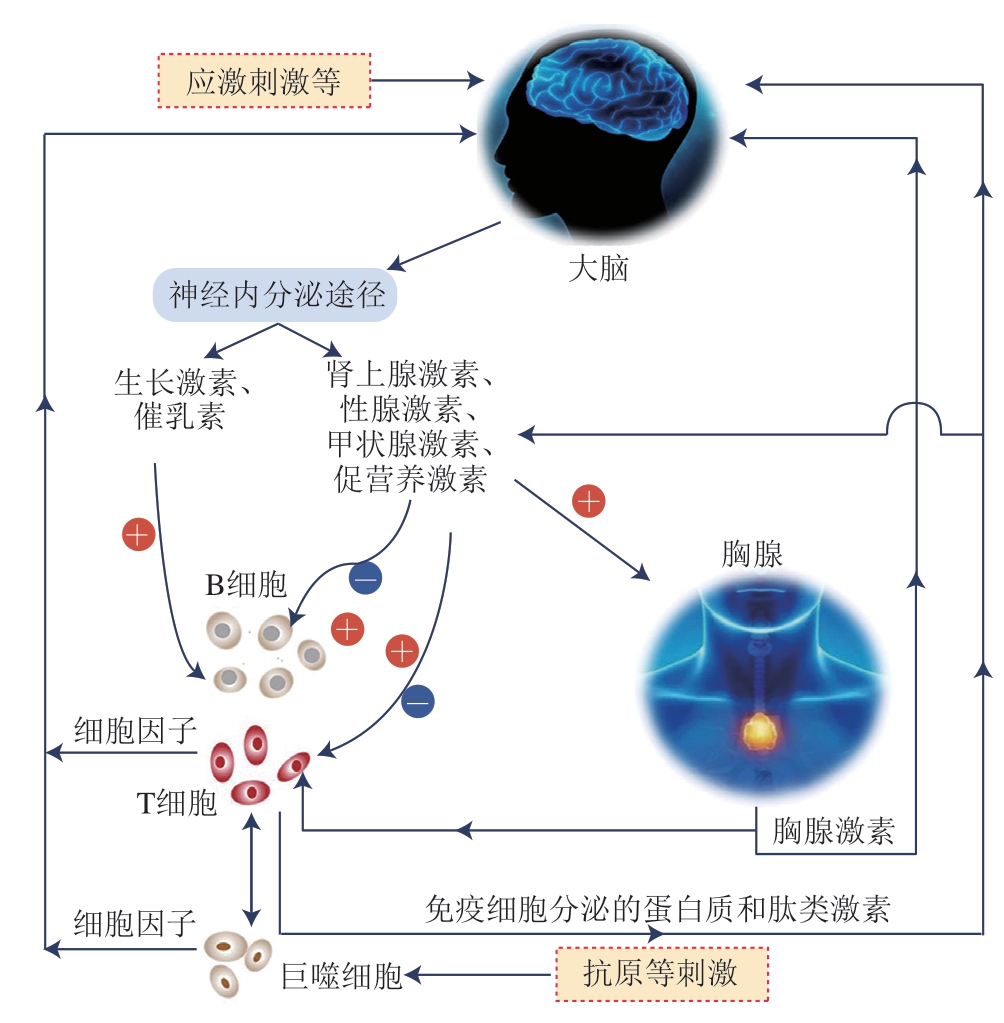
图5 神经内分泌免疫系统[103]
Fig. 5 Neuroendocrine immune system[103]
Xiao Zhiyong等[39]推测LBP还能通过下丘脑-垂体肾上腺/性腺轴或下丘脑-自主神经系统-外周免疫器官(如脾脏)等通路发挥免疫调节作用。王莹[9]、蒋艳[106]等均发现LBP显著提高了小鼠体内免疫器官(脾脏和胸腺)的脏器指数,证明LBP可以促进机体免疫器官的生长发育,也有研究发现LBP可以增加肠道内PP的数目[107],增强机体免疫功能。
5 结 语
由于各研究中所使用的提纯方法并不一致,导致LBP的免疫调节效果和作用机制也并不相同。但这些不同的LBP组分可通过多种途径作用于机体的不同靶点,由此发挥免疫调节作用。在LBP作用的众多靶点中,肠道菌群及其产生的SCFAs、巨噬细胞、DC、T细胞、B细胞和神经内分泌免疫系统均能双向调节机体的免疫应答状态,使LBP发挥免疫增强/抑制的双重作用。虽然众多研究已从不同角度揭示了LBP的部分免疫调节机制,但还有以下问题尚待解决:1)从结构-功能关系的解析情况来看,部分研究使用从生物公司购买的LBP开展实验,研究内容侧重于探究LBP对肠道菌群生长的调控机制及其在不同细胞中的作用靶点和作用通路[11,82,93]等功能活性方面。这些研究对明确LBP发挥生物活性的具体机制具有重要意义,但因研究重点有所侧重,该类报道中LBP的化学结构特征并不十分明确。此外,LBP不同组分中存在不同的支链结构[34,108],这些支链各自发挥什么样的免疫调节功能,又分别能与免疫细胞表面哪一种受体结合,多糖组分中的主链与支链在免疫调节过程中扮演了什么样的角色?这些问题尚需阐明。因此,LBP发挥免疫功能的效用成分和其作用机制有待进一步明确,LBP结构及其免疫调节活性之间的紧密联系也有待进一步解析[109]。2)从受体结合方面来看,虽然目前的研究已经表明,LBP能够与树突细胞、巨噬细胞表面的TLR2/4受体结合[69],但究竟是多糖中的哪一段糖链与TLR2/4受体中的哪一段氨基酸结合,多糖的受体结合位点有着什么样的结构特征?这些问题都缺乏深入的研究。Xiao Zhiyong等[39]推测,通过对特定糖苷键和残基进行化学修饰,同时利用蛋白酶对TLR受体蛋白进行可控性水解,再结合表面等离子共振、等温滴定量热法、亲和电泳等技术手段,将能有效解决上述难题。3)从代谢产物方面来看,LBP是一种非消化性多糖,被胃肠微生物分解后可以形成多糖/寡糖片段和不同的短链脂肪酸等代谢产物[110-111],后续研究可深入解析代谢产物的结构,探究多糖代谢过程及其代谢产物对机体免疫系统的影响。4)从免疫调节方面来看,现有文献对LBP的免疫增强功能挖掘较多,而对其免疫抑制活性的关注较少。目前仅有少量研究报道了LBP在抗肿瘤方面所起到的“降低抗肿瘤药物的免疫毒性/增加机体对肿瘤的免疫抵抗”的双向功能[11,112-113]。后续研究可着重关注多糖在下调机体免疫应答方面的效果与机制。此外,LBP的免疫调节功能涉及机体多种器官、细胞和通路,后续研究需综合考虑多糖对不同组织、细胞的影响,全面而深入地探索其免疫调节机制。
综上,LBP的提取纯化方式、结构特征、对不同免疫细胞的作用效果、与细胞表面受体结合的分子机制、刺激细胞内部信号通路的情况等均需进行更深入的研究。未来研究也可从多糖组分的化学修饰和代谢产物入手,开发新型免疫调节活性物质,为LBP的精深利用提供理论基础。
[1]TIAN X J, LIANG T S, LIU Y L, et al. Extraction, structural characterization, and biological functions of Lycium barbarum polysaccharides: a review[J]. Biomolecules, 2019, 9(9): 389.DOI:10.3390/biom9090389.
[2]龚桂萍. 枸杞多糖的分步沉淀法纯化及各组分理化性质和生物活性研究[D]. 西安: 西北大学, 2018: 8-9.
[3]缪凤. 枸杞多糖酶提、分离纯化及抗氧化和免疫活性研究[D]. 扬州: 扬州大学, 2021: 1-2.
[4]王莹, 高丽, 金红宇, 等. 枸杞多糖调节肠道菌群及免疫功能研究进展[J]. 现代医药卫生, 2021, 37(4): 584-587.
[5]WANG H, LI J, TAO W, et al. Lycium ruthenicum studies: molecular biology, phytochemistry and pharmacology[J]. Food Chemistry, 2018,240(1): 759-766. DOI:10.1016/j.foodchem.2017.08.026.
[6]谢文, 陈华国, 赵超, 等. 枸杞多糖的生物活性及作用机制研究进展[J].食品科学, 2021, 42(5): 349-359. DOI:10.7506/spkx1002-6630-20200212-118.
[7]TIAN X M, WANG R, ZHANG B K, et al. Impact of Lycium barbarum polysaccharide and Danshensu on vascular endothelial growth factor in the process of retinal neovascularization of rabbit[J]. International Journal of Ophthalmology, 2013, 6(1): 59-61.DOI:10.3980/j.issn.2222-3959.2013.01.12.
[8]CHANG C C, SO K F. Use of anti-aging herbal medicine, Lycium barbarum, against aging-associated diseases. What do we know so far?[J]. Cellular and Molecular Neurobiology, 2008, 28(5): 643-652.DOI:10.1007/s10571-007-9181-x.
[9]王莹. 枸杞多糖的分离纯化及基于对肠道菌群调节的免疫作用机制研究[D]. 北京: 北京中医药大学, 2020: 124-125.
[10]杨青, 白光, 王巍, 等. 枸杞多糖通过诱导巨噬细胞极化抗胰腺癌的研究[J]. 天津医药, 2015, 43(11): 5-9.
[11]BO R, LIU Z, ZHANG J, et al. Mechanism of Lycium barbarum polysaccharides liposomes on activating murine dendritic cells[J].Carbohydrate Polymers, 2018, 205: 540-549. DOI:10.1016/j.carbpol.2018.10.057.
[12]樊燕燕. 黄芪多糖在动物饲料添加剂与免疫增强剂中的应用: 评《特种经济动物饲料学》[J]. 中国饲料, 2021(21): 153.
[13]张学武, 宋仕花. 蜂胶佐剂在兽用疫苗中的应用[J]. 中国动物保健,2021, 23(12): 103-104. DOI:10.3969/j.issn.1008-4754.2021.12.066.
[14]杨洋, 尹彦超, 杨光洁, 等. 磺胺类药物交叉过敏管理的临床调查和现状分析[J]. 药物流行病学杂志, 2021, 30(12): 822-826.DOI:10.19960/j.cnki.issn1005-0698.2021.12.007.
[15]傅玲琳, 王彦波. 食物过敏: 从致敏机理到控制策略[J]. 食品科学,2021, 42(19): 1-19. DOI:10.7506/spkx1002-6630-20210726-302.
[16]LUCAS-GONZALEZ R, VIUDA-MARTOS M, PEREZ-ALVAREZ J A, et al. In vitro digestion models suitable for foods: opportunities for new fields of application and challenges[J]. Food Research International, 2018, 107: 423-436. DOI:10.1016/j.foodres.2018.02.055.
[17]石玉祥, 闫金坤, 王雪敏. 枸杞多糖对小鼠肠道上皮内淋巴细胞和杯状细胞数量、分布及对IL-2水平影响[J]. 食品科学, 2011, 32(13):318-320.
[18]VITALE S, PICASCIA S, GIANFRANI C. The cross-talk between enterocytes and intraepithelial lymphocytes[J]. Molecular and Cellular Pediatrics, 2016, 3(1): 20-24. DOI:10.1186/s40348-016-0048-4.
[19]VANGARDEREN E, VANDIJK J E, VANDENINGH T. The biology and pathobiogy of the intestinal intraepithelial lymphocyte: a review of the literature[J]. Veterinary Quarterly, 1991, 13(4): 225-232.DOI:10.1080/01652176.1991.9694312.
[20]TIWARI S, BEGUM S, MOREAU F, et al. Autophagy is required during high MUC2 mucin biosynthesis in colonic goblet cells to contend metabolic stress[J]. American Journal of Physiology.Gastrointestinal and Liver Physiology, 2021, 321(5): G489-G499.DOI:10.1152/ajpgi.00221.2021.
[21]TANG X, MA W, ZHAN W, et al. Internal biliary drainage superior to external biliary drainage in improving gut mucosa barrier because of goblet cells and mucin-2 upregulation[J]. Bioscience Reports, 2018,38(3): BSR20171241. DOI:10.1042/BSR20171241.
[22]胡艳艳, 刘小伟. 肠道杯状细胞结构和功能的研究进展[J]. 国际病理科学与临床杂志, 2013, 33(5): 424-430.
[23]KANG Yifei, YANG Guan, ZHANG Shuming, et al. Goji berry modulates gut microbiota and alleviates colitis in IL-10-deficient mice[J]. Molecular Nutrition & Food Research, 2018, 62(22):e1800535. DOI:10.1002/mnfr.201800535.
[24]ZHAO Qihan, LI Jingjing, YAN Jun, et al. Lycium barbarum polysaccharides ameliorates renal injury and inflammatory reaction in alloxan-induced diabetic nephropathy rabbits[J]. Life Sciences, 2016,157: 82-90. DOI:10.1016/j.lfs.2016.05.045.
[25]丁春龙, 王玉海, 杨理坤, 等. 血清D-乳酸、细菌内毒素及二胺氧化酶在创伤性颅脑损伤后肠道黏膜屏障功能评估中的作用[J]. 中华神经外科杂志, 2019, 35(12): 1258-1261.
[26]何志捷, 植耀炜, 黄超泰, 等. 血清二胺氧化酶、D-乳酸和细菌内毒素在重症患者肠道功能评估中的作用[J]. 岭南现代临床外科, 2017,17(4): 400-403.
[27]SHIMOTOYODOME A, MEGURO S, HASE T, et al. Sulfated polysaccharides, but not cellulose, increase colonic mucus in rats with loperamide-induced constipation[J]. Digestive Diseases & Sciences,2001, 46(7): 1482-1489. DOI:10.1023/A:1010644021888.
[28]XIE S Z, LIU B, YE H Y, et al. Dendrobium huoshanense polysaccharide regionally regulates intestinal mucosal barrier function and intestinal microbiota in mice[J]. Carbohydrate Polymers, 2019,206: 149-162. DOI:10.1016/j.carbpol.2018.11.002.
[29]DIDIER N, GILBERT H J. Biochemistry of complex glycan depolymerisation by the human gut microbiota[J]. FEMS Microbiology Reviews, 2018, 42(2): 146-164. DOI:10.1093/femsre/fuy002.
[30]DING Yu, CHEN Dan, YAN Yamei, et al. Effects of long-term consumption of polysaccharides from the fruit of Lycium barbarum on host’s health[J]. Food Research International, 2021, 139: 109913.DOI:10.1016/j.foodres.2020.109913.
[31]BAI Y J, HUANG F, ZHANG R F, et al. Longan pulp polysaccharides relieve intestinal injury in vivo and in vitro by promoting tight junction expression[J]. Carbohydrate Polymers, 2020, 229: 115475.DOI:10.1016/j.carbpol.2019.115475.
[32]MELO-GONZALEZ F, FENTON M, FORSS C, et al. Intestinal mucin activates human dendritic cells and IL-8 production in a glycanspecific manner[J]. Journal of Biological Chemistry, 2018, 293(22):8543-8553. DOI:10.1074/jbc.M117.789305.
[33]WANG Z, YANG L, SUN Y, et al. Structural characterization of LbGp1 from the fruits of Lycium barbarum L[J]. Food Chemistry,2014, 159(9): 137-142. DOI:10.1016/j.foodchem.2014.02.171.
[34]GONG Guiping, DANG Tiantian, DENG Yangni, et al.Physicochemical properties and biological activities of polysaccharides from Lycium barbarum prepared by fractional precipitation[J].International Journal of Biological Macromolecules, 2018, 109: 611-618. DOI:10.1016/j.ijbiomac.2017.12.017.
[35]GONG G P, LIU Q, DENG Y N, et al. Arabinogalactan derived from Lycium barbarum fruit inhibits cancer cell growth via cell cycle arrest and apoptosis[J]. International Journal of Biological Macromolecules,2020, 149: 639-650. DOI:10.1016/j.ijbiomac.2020.01.251.
[36]CAO Cui, ZHU Beiwei, LIU Zhengqi, et al. An arabinogalactan from Lycium barbarum attenuates DSS-induced chronic colitis in C57BL/6J mice associated with the modulation of intestinal barrier function and gut microbiota[J]. Food & Function, 2021, 12(20): 9829-9843.DOI:10.1039/d1fo01200b.
[37]TANG R, CHEN X Y, DANG T T, et al. Lycium barbarum polysaccharides extend the mean lifespan of Drosophila melanogaster[J]. Food & Function, 2019, 10(7): 4231-4241.DOI:10.1039/c8fo01751d.
[38]YANG T, LI C, XUE W, et al. Natural immunomodulating substances used for alleviating food allergy[J]. Critical Reviews in Food Science and Nutrition, 2021, 2021: 1-19. DOI:10.1080/10408398.2021.1975257.
[39]XIAO Zhiyong, DENG Qi, ZHOU Wenxia, et al. Immune activities of polysaccharides isolated from Lycium barbarum L. What do we know so far?[J]. Pharmacology & Therapeutics, 2021, 229: 107921.DOI:10.1016/j.pharmthera.2021.107921.
[40]JI X M, LI A L, YAO L, et al. Studies on Lactobacillus acidophilus inhibits cow milk allergy[J]. Journal of Chinese Institute of Food Science & Technology, 2016, 16(7): 33-38. DOI:10.16429/j.1009-7848.2016.07.005.
[41]ZHOU Fang, JIANG Xiaoying, WANG Tao, et al. Lycium barbarum polysaccharide (LBP): a novel prebiotics candidate for Bifidobacterium and Lactobacillus[J]. Frontiers in Microbiology, 2018, 9: 1034.DOI:10.3389/fmicb.2018.01034.
[42]ZHU Wei, ZHOU Shuxin, LIU Jihua, et al. Prebiotic, immunostimulating and gut microbiota-modulating effects of Lycium barbarum polysaccharide[J]. Biomedicine & Pharmacotherapy, 2020,121: 109591. DOI:10.1016/j.biopha.2019.109591.
[43]史佳鹭, 李慧臻, 闫芬芬, 等. 益生菌对免疫细胞的影响及其在自身免疫性疾病中的应用[J]. 食品工业科技, 2020, 41(5): 354-360.DOI:10.13386/j.issn1002-0306.2020.05.057.
[44]程翔. 采用PCR-DGGE方法测定枸杞多糖对小鼠肠道菌群失调的调整作用[D]. 佳木斯: 佳木斯大学, 2013: 27-33.
[45]DING Yu, YAN Yamei, CHEN Dan, et al. Modulating effects of polysaccharides from the fruits of Lycium barbarum on the immune response and gut microbiota in cyclophosphamide-treated mice[J].Food & Function, 2019, 10(6): 3671-3683. DOI:10.1039/c9fo00638a.
[46]VERNIA F, LONGO S, STEFANELLI G, et al. Dietary factors modulating colorectal carcinogenesis[J]. Nutrients, 2021, 13(1): 143.DOI:10.3390/nu13010143.
[47]FEEHLEY T, NAGLER C R. Cellular and molecular pathways through which commensal bacteria modulate sensitization to dietary antigens[J]. Current Opinion in Immunology, 2014, 31: 79-86.DOI:10.1016/j.coi.2014.10.001.
[48]BOLOGNINI D, TOBIN A B, MILLIGAN G, et al. The pharmacology and function of receptors for short-chain fatty acids[J]. Molecular Pharmacology, 2016, 89(3): 388-398. DOI:10.1124/mol.115.102301.
[49]JI J, SHU D M, ZHENG M Z, et al. Microbial metabolite butyrate facilitates M2 macrophage polarization and function[J]. Scientific Reports, 2016, 6: 24838. DOI:10.1038/srep24838.
[50]KAMP M E, SHIM R, NICHOLLS A J, et al. G protein-coupled receptor 43 modulates neutrophil recruitment during acute inflammation[J]. PLoS ONE, 2016, 11(9): e0163750. DOI:10.1371/journal.pone.0163750.
[51]MACIA L, TAN J, VIEIRA A T, et al. Metabolite-sensing receptors GPR43 and GPR109A facilitate dietary fibre-induced gut homeostasis through regulation of the inflammasome[J]. Nature Communications,2015, 6: 6734. DOI:10.1038/ncomms7734.
[52]ZAKI H, BOYD K L, VOGEL P, et al. The NLRP3 inflammasome protects against loss of epithelial integrity and mortality during experimental colitis[J]. Immunity, 2010, 32(3): 379-391. DOI:10.1016/j.immuni.2010.03.003.
[53]CHISTIAKOV D A, OREKHOV A N, BOBRYSHEV Y V. Immuneinflammatory responses in atherosclerosis: role of an adaptive immunity mainly driven by T and B cells[J]. Immunobiology, 2016,221(9): 1014-1033. DOI:10.1016/j.imbio.2016.05.010.
[54]DING Yu, YAN Yamei, PENG Yujia, et al. In vitro digestion under simulated saliva, gastric and small intestinal conditions and fermentation by human gut microbiota of polysaccharides from the fruits of Lycium barbarum[J]. International Journal of Biological Macromolecules, 2019, 125: 751-760. DOI:10.1016/j.ijbiomac.2018.12.081.
[55]唐华丽. 枸杞多糖的结构分析及代谢组学研究[D]. 南京: 东南大学,2016: 84-85.
[56]RICE P J. Oral delivery and gastrointestinal absorption of soluble glucans stimulate increased resistance to infectious challenge[J].Journal of Pharmacology & Experimental Therapeutics, 2005, 314(3):1079-1086. DOI:10.1124/jpet.105.085415.
[57]BATBAYAR S, DONG H L, KIM H W. Immunomodulation of fungal β-glucan in host defense signaling by dectin-1[J].Biomolecules and Therapeutics, 2012, 20(5): 433-445. DOI:10.4062/biomolther.2012.20.5.433.
[58]傅玲琳, 谢梦华, 王翀, 等. 肠道菌群调控下的食物过敏机制研究进展[J]. 食品科学, 2018, 39(17): 305-313. DOI:10.7506/spkx1002-6630-201817048.
[59]JIE Z. Lycium barbarum polysaccharides induce Toll-like receptor 2- and 4-mediated phenotypic and functional maturation of murine dendritic cells via activation of NF-κB[J]. Molecular Medicine Reports, 2013, 8: 1216-1220. DOI:10.3892/mmr.2013.1608.
[60]王莹, 金红宇, 李耀磊, 等. 不同分子量枸杞多糖对RAW264.7巨噬细胞的免疫调节作用[J]. 中国新药杂志, 2021, 30(12): 1079-1086.
[61]高翔. 枸杞多糖对小鼠巨噬细胞免疫功能的影响研究[J].中国现代药物应用, 2013, 7(12): 237-238. DOI:10.3969/j.issn.1673-9523.2013.12.198.
[62]ZHANG L, WANG C C. Inflammatory response of macrophages in infection[J]. Hepatobiliary & Pancreatic Diseases International, 2014,13(2): 138-152. DOI:10.1016/S1499-3872(14)60024-2.
[63]FENG L, XIAO X, LIU J, et al. Immunomodulatory effects of Lycium barbarum polysaccharide extract and its uptake behaviors at the cellular level[J]. Molecules, 2020, 25(6): 1351. DOI:10.3390/molecules25061351.
[64]ZHANG X R, ZHOU W X, ZHANG Y X. Immunoregulation and Lycium barbarum[M]. Berlin: Springer, 2015: 22-24.
[65]杨青. 枸杞多糖通过诱导巨噬细胞极化抗胰腺癌的实验研究[D]. 锦州: 锦州医科大学, 2016: 52-67.
[66]许金霞. 枸杞多糖的制备及其活化巨噬细胞机理的研究[D]. 杭州:浙江大学, 2007: 37-40.
[67]张小锐. 枸杞多糖LBPF4-OL免疫调节靶细胞及其作用位点研究[D].北京: 中国人民解放军军事医学科学院, 2011: 21-26.
[68]CHENG J, ZHOU Z W, SHENG H P, et al. An evidence-based update on the pharmacological activities and possible molecular targets of Lycium barbarum polysaccharides[J]. Drug Design Development and Therapy, 2015, 9: 33-78. DOI:10.2147/dddt.572892.
[69]ZHANG Xiaorui, QI Chunhui, CHENG Junping, et al. Lycium barbarum polysaccharide LBPF4-OL may be a new Toll-like receptor 4/MD2-MAPK signaling pathway activator and inducer[J].International Immunopharmacology, 2014, 19(1): 132-141.DOI:10.1016/j.intimp.2014.01.010.
[70]KE C, QIAO D, LUO J, et al. Immunostimulatory activity and structure of polysaccharide from Streptococcus equi subsp.zooepidemicus[J]. International Journal of Biological Macromolecules,2013, 57: 218-225. DOI:10.1016/j.ijbiomac.2013.03.033.
[71]PENG Qiang, SONG Jingjing, LÜ Xiaopeng, et al. Structural characterization of an arabinogalactan-protein from the fruits of Lycium ruthenicum[J]. Journal of Agricultural and Food Chemistry,2012, 60(37): 9424-9429. DOI:10.1021/jf302619c.
[72]PENG Qiang, XU Qingsong, YIN Heng, et al. Characterization of an immunologically active pectin from the fruits of Lycium ruthenicum[J].International Journal of Biological Macromolecules, 2014, 64: 69-75.DOI:10.1016/j.ijbiomac.2013.11.030.
[73]XIE Gang, SCHEPETKIN I A, SIEMSEN D W, et al. Fractionation and characterization of biologically-active polysaccharides from Artemisia tripartita[J]. Phytochemistry, 2008, 69(6): 1359-1371.DOI:10.1016/j.phytochem.2008.01.009.
[74]LI Ningyang, WANG Chaofan, GEORGIEV M I, et al. Advances in dietary polysaccharides as anticancer agents: structure-activity relationship[J]. Trends in Food Science & Technology, 2021, 111: 360-377. DOI:10.1016/j.tifs.2021.03.008.
[75]WANG Xuesong, LIU Liu, FANG Jinian. Immunological activities and structure of pectin from Centella asiatica[J]. Carbohydrate Polymers,2005, 60(1): 95-101. DOI:10.1016/j.carbpol.2004.11.031.
[76]FERREIRA S S, PASSOS C P, MADUREIRA P, et al. Structurefunction relationships of immunostimulatory polysaccharides: a review[J]. Carbohydrate Polymers, 2015, 132: 378-396. DOI:10.1016/j.carbpol.2015.05.079.
[77]孙彬, 魏玉香, 石炳毅. 树突状细胞分类及调节性树突状细胞获取方式的研究进展[J]. 器官移植, 2019, 10(2): 198-201.
[78]COLLIN M, MCGOVERN N, HANIFFA M. Human dendritic cell subsets[J]. Immunology, 2013, 140(1): 22-30. DOI:10.1111/imm.12117.
[79]COLLIN M, BIGLEY V. Human dendritic cell subsets: an update[J].Immunology, 2018, 154(1): 3-20. DOI:10.1111/imm.12888.
[80]郝习, 赵明耀. 枸杞多糖对树突状细胞的成熟及免疫学功能的影响[J].中医研究, 2010, 23(11): 4-8.
[81]ZHU Jie, ZHANG Yuanyuan, SHEN Yueshuang, et al. Lycium barbarum polysaccharides induce Toll-like receptor 2- and 4-mediated phenotypic and functional maturation of murine dendritic cells via activation of NF-kappa B[J]. Molecular Medicine Reports, 2013, 8(4):1216-1220. DOI:10.3892/mmr.2013.1608.
[82]DUAN Xiangguo, LAN Yaru, ZHANG Xiaoyu, et al. Lycium barbarum polysaccharides promote maturity of murine dendritic cells through Toll-like receptor 4-Erk1/2-Blimp1 signaling pathway[J]. Journal of Immunology Research, 2020, 2020: 1751793.DOI:10.1155/2020/1751793.
[83]廖海锋. 不同分子量枸杞多糖对树突状细胞成熟的影响[D]. 广州:广州中医药大学, 2016: 36-46.
[84]兰亚如. 枸杞多糖通过TLR4-NFκB/MAPK-Blimp1通路促进小鼠树突状细胞成熟的研究[D]. 银川: 宁夏医科大学, 2020: 28-34.
[85]张炜, 万巧凤, 马锐, 等. 枸杞多糖对DC2.4细胞增殖、抗原吞噬及成熟的影响[J]. 宁夏医科大学学报, 2020, 42(10): 979-982.
[86]卢秀红, 邓祝新, 黄维义, 等. 一氧化氮在免疫效应机制中的作用及其细胞因子的调控[J]. 河南畜牧兽医(综合版), 2009(12): 3-9.
[87]ZHANG Minghui, TANG Hong, GUO Zhenhong, et al. Splenic stroma drives mature dendritic cells to differentiate into regulatory dendritic cells[J]. Nature Immunology, 2014, 15(11): 1090-1090. DOI:10.1038/ni1114-1090a.
[88]胡国俊, 白惠卿, 杜守英, 等. 枸杞对T、B淋巴细胞增殖和T细胞亚群变化的调节作用[J]. 中国免疫学杂志, 1995(3): 163-166.
[89]YUAN L G, DENG H B, CHEN L H, et al. Reversal of apoptotic resistance by Lycium barbarum glycopeptide 3 in aged T cells[J].Biomedical and Environmental Sciences, 2008, 21(3): 212-217.DOI:10.1016/s0895-3988(08)60031-8.
[90]BO Ruonan, SUN Yaqin, ZHOU Shuzhen, et al. Simple nanoliposomes encapsulating Lycium barbarum polysaccharides as adjuvants improve humoral and cellular immunity in mice[J]. International Journal of Nanomedicine, 2017, 12: 6289-6301. DOI:10.2147/ijn.s136820.
[91]AMAGASE H, FARNSWORTH N R. A review of botanical characteristics, phytochemistry, clinical relevance in efficacy and safety of Lycium barbarum fruit (Goji)[J]. Food Research International, 2011,44(7): 1702-1717. DOI:10.1016/j.foodres.2011.03.027.
[92]SU Chunxia, DUAN Xiangguo, LIANG Lijun, et al. Lycium barbarum polysaccharides as an adjuvant for recombinant vaccine through enhancement of humoral immunity by activating Tfh cells[J].Veterinary Immunology and Immunopathology, 2014, 158(1/2): 98-104. DOI:10.1016/j.vetimm.2013.05.006.
[93]符古雅, 李伯灵, 邹志方, 等. 复合枸杞多糖对接触氟化物者免疫调节和抗脂质过氧化作用[J]. 职业与健康, 2007(5): 324-325.
[94]ZHANG Xiaorui, ZHOU Wenxia, ZHANG Yongxiang, et al.Macrophages, rather than T and B cells are principal immunostimulatory target cells of Lycium barbarum L. polysaccharide LBPF4-OL[J]. Journal of Ethnopharmacology, 2011, 136(3): 465-472.DOI:10.1016/j.jep.2011.04.054.
[95]田阳, 饶欢, 薛文通. 花生过敏原检测、降敏加工及脱敏治疗研究进展[J]. 食品工业科技, 2017, 38(18): 306-311. DOI:10.13386/j.issn1002-0306.2017.18.058.
[96]柳文锋. 燕麦生物碱B与β-乳球蛋白复合物对IgE介导的嗜碱性粒细胞脱颗粒的影响[D]. 南昌: 南昌大学, 2019: 40-52.
[97]秦旭军. 病原生物与免疫学基础[M]. 北京: 人民军医出版社, 2008:120-129.
[98]YAN Tinghu, LI Qi, YANG Hui, et al. Protective effect of polysaccharides on simulated microgravity-induced functional inhibition of human NK cells[J]. Carbohydrate Polymers, 2014, 101:819-827. DOI:10.1016/j.carbpol.2013.10.021.
[99]刘彦平, 李积东. 枸杞多糖对小鼠NK细胞和白细胞活性的免疫调节作用[J]. 青海医学院学报, 2001(1): 1-5.
[100]LI Qi, MEI Qibing, ZHANG Mingjie, et al. Effects of bioactive polysaccharides on immunocompetence of human NK cells[J]. Food Science, 2013, 34(1): 315-318.
[101]黄振华, 邓向亮, 张凯敏, 等. 枸杞多糖对免疫抑制小鼠红细胞免疫功能的影响[J]. 中国免疫学杂志, 2018, 34(2): 214-217.DOI:10.3969/j.issn.1000-484X.2018.02.011.
[102]肖芳, 吴琦. 枸杞多糖在白血病患者中的应用及对HL-60和NK细胞杀伤活性的影响[J]. 中国老年学杂志, 2017, 37(13): 3140-3142.
[103]ZHOU W, CHENG X, ZHANG Y. Effect of Liuwei Dihuang decoction,a traditional Chinese medicinal prescription, on the neuroendocrine immunomodulation network[J]. Pharmacology Therapeutics, 2016,162(4): 170-178. DOI:10.1016/j.pharmthera.2016.02.004.
[104]聂伟, 张永祥. 多糖的免疫调节作用及其作用机制研究进展[J]. 中国药理学通报, 1999, 15(6): 484-487.
[105]SHAJIB M S, KHAN W I. The role of serotonin and its receptors in activation of immune responses and inflammation[J]. Acta Physiologica, 2015, 213(3): 561-574. DOI:10.1111/apha.12430.
[106]蒋艳, 姜孝新. 枸杞多糖对肝癌荷瘤小鼠的抗肿瘤作用及其机制[J].肿瘤药学, 2011, 1(4): 391-394.
[107]李相玲. 不同分子量的枸杞多糖提取分析及对细胞迁移的影响[D].广州: 广州中医药大学, 2014: 78-90.
[108]ZHOU L S, HUANG L L, YUE H, et al. Structure analysis of a heteropolysaccharide from fruits of Lycium barbarum L. and antiangiogenic activity of its sulfated derivative[J]. International Journal of Biological Macromolecules, 2018, 108: 47-55. DOI:10.1016/j.ijbiomac.2017.11.111.
[109]叶兴乾, 周声怡, 姚舒婷, 等. 枸杞多糖的提取方式,结构及生物活性研究进展[J]. 食品与发酵工业, 2020, 46(6): 292-300. DOI:10.13995/j.cnki.11-1802/ts.022778.
[110]YANG Y, CHANG YF, WU Y, et al. A homogeneous polysaccharide from Lycium barbarum: structural characterizations, anti-obesity effects and impacts on gut microbiota[J]. International Journal of Biological Macromolecules, 2021, 183: 2074-2087. DOI:10.1016/j.ijbiomac.2021.05.209.
[111]YANG M, YIN Y X, WANG F, et al. Supplementation with Lycium barbarum polysaccharides reduce obesity in high-fat diet-fed mice by modulation of gut microbiota[J]. Frontiers in Microbiology, 2021, 183:2074-2087. DOI:10.3389/fmicb.2021.719967.
[112]DENG X L, LUO S, LUO X, et al. Fraction from Lycium barbarum polysaccharides reduces immunotoxicity and enhances antitumor activity of doxorubicin in mice[J]. Integrative Cancer Therapies, 2018,17(3): 860-866. DOI:10.1177/1534735417753544.
[113]BIE M, LV Y, REN C R, et al. Lycium barbarum polysaccharide improves bipolar pulse current-induced microglia cell injury through modulating autophagy[J]. Cell Transplantation, 2015, 24(3): 419-428.DOI:10.3727/096368915x687453.