咖啡是世界三大饮料之一,其原材料咖啡豆原产于非洲的埃塞俄比亚,相继被引入欧洲、美洲、亚洲已有数百年的历史[1]。近年来,由于冷萃咖啡制备方式简单,口感独特,格外受到全球咖啡爱好者的喜爱。在中国,冷萃咖啡年均复合增长超150%,成为咖啡中增长率最高的品类[2]。相对于热萃咖啡的制备方式,冷萃咖啡选用室温或温度更低的水,低温萃取12~24 h,从而获得更加温和而又平衡的口感。但是,对于冷萃咖啡的研究远不如热萃咖啡,对影响冷萃咖啡品质的因素影响作用知之甚少。近几年,个别冷萃咖啡的研究表明,咖啡豆品种(产地)、研磨度、萃取时间和萃取方式都会影响冷萃咖啡的萃取品质[3-4],冷萃咖啡的可滴定酸值低于热萃咖啡样品,冷萃咖啡相较于热萃咖啡具有更浓郁的甜味、果香和花香,而苦味和酸度更低。然而,咖啡豆烘焙度被认为是影响萃取品质的重要因素之一,而其对冷萃咖啡影响的相关研究鲜有报道。
现有热萃咖啡研究表明,不同烘焙度的咖啡豆热萃饮品的风味成分上往往有显著差异[5-7]。咖啡豆烘焙过程发生了美拉德反应和焦糖化反应,可产生令人愉快或不愉快的香气物质,直接决定咖啡萃取的品质,同时,烘焙过程中咖啡豆的糖、酸、咖啡因和绿原酸等风味及功能性物质也在发生变化。此外,热萃咖啡饮料的品质还受到咖啡种类、种植条件、处理方式等多种因素的影响[8-10],在过去的几十年,研究都集中在美洲、非洲咖啡豆。现有关于冷萃咖啡研究往往也选用非洲埃塞俄比亚和南美洲巴西等产区咖啡豆[11-13],而关于亚洲(咖啡产区三大洲之一)种植咖啡豆的研究鲜有涉及。
因此,本研究以2种亚洲的中国云南与印度尼西亚苏门答腊产地的咖啡豆为研究对象,选择浅、中、深3种烘焙度,选用顶空固相微萃取-气相色谱-质谱(head space-solid phase microextraction-gas chromatographymass spectrometry,HS-SPME-GC-MS)联用法测定挥发性成分,高效液相色谱(high performance liquid chromatography,HPLC)法测定咖啡因、葫芦巴碱、绿原酸等主要苦涩味成分,同时,这些物质对人体具有特殊的生理活性作用,咖啡因是一种中枢神经兴奋剂,具有抗疲劳功效;葫芦巴碱常见于豆科植物中,具有降血糖、抗肿瘤等功效;绿原酸常见于咖啡中的是3-咖啡酰奎尼酸,具有抗肿瘤、清除自由基等功效[14]。因此,探究烘焙度对冷萃咖啡咖啡因、葫芦巴碱、绿原酸含量的影响十分有意义。本研究拟从咖啡基本理化特性、非挥发性成分和挥发性成分等方面比较冷萃咖啡与热萃咖啡的差异,探究烘焙度对冷萃咖啡品质的影响。
1 材料与方法
1.1 材料与试剂
咖啡豆均购买于上海焱焙咖啡有限公司:中国云南生产的卡蒂姆种咖啡豆的浅烘豆、中烘豆和深烘豆,印度尼西亚苏门答腊生产的卡蒂姆种咖啡豆的浅烘豆、中烘豆和深烘豆,使用高精度色度仪测定L值(代表白度或明暗度),浅烘豆颜色L值范围为30~32;中烘豆颜色L值范围为26~29;深烘豆颜色L值范围为23~25。
咖啡因、葫芦巴碱、绿原酸标准品(纯度均为99%),1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)(纯度98%) 上海源叶生物科技有限公司;2,2’-联氮双(3-乙基苯并噻唑啉-6-磺酸)(2,2’-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS)、2-辛醇标准品(纯度均为99%) 上海泰坦科技股份有限公司。
1.2 仪器与设备
UV-1800分光光度计、GCMS-TQ80 GC-MS联用仪、LC-20A HPLC仪、SPD-M20A二极阵列检测器 日本岛津公司;EK43s咖啡磨豆机 意大利Mahlkonig公司;Pal-Coffee TDS测定仪 日本ATAGO公司;HACA-3000高精度分光测色仪 杭州远方光电信息股份有限公司。
1.3 方法
1.3.1 咖啡样品制备
冷萃咖啡的制备条件:将咖啡豆磨粉(研磨度11,粒径范围200~600 μm),按照咖啡粉与水质量比1∶16的比例添加5 ℃冷水,置于容器中密封5 ℃浸泡16 h,浸泡完毕后过滤除去咖啡渣即可。
热萃咖啡的制备条件:将咖啡豆磨粉(研磨度11),按照咖啡粉与水质量比1∶16添加92 ℃热水,控制注水和浸泡总时间为3 min,浸泡完毕后过滤除去咖啡渣即可。本研究冷萃和热萃条件下制备得到的咖啡萃取量均基本趋于饱和。
1.3.2 咖啡液萃取浓度、萃取率的测定
咖啡液萃取浓度使用Pal-Coffee TDS折光率测定仪测定。取0.5 mL咖啡液,滴在测定仪上测定,读取并记录萃取浓度参数,此仪器用常温咖啡冲泡水清零。
咖啡液萃取率计算方法参照Liang Jiexin等[15],咖啡液萃取率按式(1)计算:
1.3.3 咖啡液可滴定酸、总糖及总酚的测定
咖啡液可滴定酸的测定参照Cordoba等[16]的方法。取稀释10 倍的咖啡液10 mL,加入1~2 滴酚酞溶液,以0.1 mol/L NaOH溶液滴定至溶液黄褐色,加入5 mL 70 ℃蒸馏水,再滴定至溶液呈现微红色即停止,记录此时NaOH溶液滴定量。
咖啡液总糖的测定参照高文军等[17]的方法。配制3,5-二硝基水杨酸溶液,静置1 周;取稀释3 倍的咖啡液3 mL,加入1 mL 6 mol/L HCl溶液,沸水浴加热水解30 min。冷却后,用6 mol/L NaOH溶液中和,定容至10 mL;取1 mL水解咖啡液2 倍稀释,加入1.5 mL 3,5-二硝基水杨酸溶液沸水浴5 min,定容至25 mL,使用紫外分光光度计在波长540 nm处测吸光度,带入葡萄糖标准曲线后×0.9得到总糖含量。
咖啡液总酚的测定参照Bilge[18]的方法。取稀释50 倍咖啡液0.5 mL,加入等量0.25 mol/L福林-酚试剂,混匀静置3 min后再加入1 mL 15% Na2CO3溶液,混匀后于25 ℃,以120 r/min避光离心1 h,使用紫外分光光度计在波长765 nm处测定吸光度,根据焦性没食子酸标准曲线,计算总酚含量。
1.3.4 咖啡液咖啡因、葫芦巴碱及绿原酸的测定
咖啡因含量的测定:参照GB 5009.139—2014《饮料中咖啡因的测定》[19],采用HPLC法。色谱条件:WondaSilTM C18色谱柱(150 mm×3.9 mm,5 μm);流动相:甲醇-水(24∶76,V/V),等度洗脱,流速1.0 mL/min;柱温30 ℃;进样量10 μL。检测器条件:二级阵列检测器,波长为272 nm。样品处理:取稀释10 倍咖啡液5 mL,加入0.5 g MgO,振摇,静置,取上清液经22 μm微孔滤膜过滤。定量方式:使用咖啡因标准品外标定量。
葫芦巴碱含量的测定:参照NY/T 3012—2016《咖啡及制品中葫芦巴碱的测定》[20],采用HPLC法。色谱条件:SHIMADAZU-GL WondaCract ODS-2色谱柱(150 mm×3.9 mm,5 μm);流动相:甲醇-水(12∶88,V/V),等度洗脱,流速1.0 mL/min;柱温30 ℃;进样量10 μL。检测器条件:二级阵列检测器,波长260 nm。样品处理:取稀释2 倍咖啡液5 mL,经22 μm微孔滤膜过滤。定量方式:使用葫芦巴碱标准品外标定量。
绿原酸含量的测定:参照GB/T 22250—2008《保健食品中绿原酸的测定》[21],采用HPLC法。流动相:乙腈-0.5%乙酸(15∶85,V/V),等度洗脱。检测器条件:二级阵列检测器,波长为327 nm。其他条件同葫芦巴碱。定量方式:使用绿原酸标准品外标定量。
1.3.5 咖啡液抗氧化能力的测定
咖啡液DPPH自由基当量测定参照Bilge[18]的方法。样品组:取稀释50 倍咖啡液0.25 mL,再取0.75 mL蒸馏水,再加入DPPH试剂(0.2 mmol/L,1 mL),于室温下避光30 min,使用紫外分光光度计在波长517 nm处测吸光度为Ai;样品对照组:实验方法同上,无水乙醇代替DPPH试剂,测得吸光度为Aj;空白对照组:方法同样品组,蒸馏水代替稀释后的咖啡液,测得吸光度为Ac。
咖啡液DPPH自由基清除率(R1)按式(2)计算:
咖啡液ABTS阳离子自由基当量测定参照Gorecki等[22]的方法。取稀释50 倍咖啡液0.1 mL,再加入1.9 mL ABTS试剂,于室温下避光6 min,使用紫外分光光度计在波长734 nm处测吸光度为Ax,并以蒸馏水代替咖啡液测得A0。
咖啡液ABTS阳离子自由基清除率(R2)按式(3)计算:
将R1、R2分别带入水溶性VE配制的标准曲线,分别得到DPPH自由基当量和ABTS阳离子自由基当量。
1.3.6 咖啡液挥发性化合物的测定
参照Cheong等[23]的方法,采用HS-SPME-GCMS法。
SPME条件:采用1 cm 50/30 μm DVB/CAR/PDMS StableFlex固相微萃取头,咖啡液5 mL,加入内标10 μL,水浴60 ℃,预热15 min,吸附30 min。
GC条件:RTX-WAX聚乙二醇强极性毛细管柱(30 m×0.25 mm,0.25 μm);升温程序:起始40 ℃保持2 min,以2 ℃/min至130 ℃,以4 ℃/min至220 ℃,保持4 min,以10 ℃/min至250 ℃,保持5 min;载气(He)(纯度99.999%)流速1.6 mL/min,压力2.4 kPa;进样方式:进样口温度200 ℃,SPME顶空进样2 min;分流比为不分流。
MS条件:电子电离源;电子能量70 eV;传输线温度275 ℃;离子源温度230 ℃;母离子m/z 285;激活电压1.5 V;质量扫描范围m/z 35~350。
定量方式:参考Bonino等[24]使用2-辛醇作为内标物质,内标量44 μg/kg,结果根据每个化合物峰面积相对于内标物峰面积之比,按照内标物质浓度换算,按式(4)计算:
1.4 数据统计
实验重复3 次,结果以 ±s表示,采用GraphPad Prism 9.0统计软件进行主成分分析(principal component analysis,PCA)、单因素方差分析,P<0.05,差异显著。
2 结果与分析
2.1 烘焙度对冷萃咖啡萃取质量分数、萃取率的影响
如图1所示,本研究发现2种亚洲产区(云南、苏门答腊)咖啡豆通过冷萃与热萃方式获得的咖啡萃取液,均呈现随着烘焙度的增加,其萃取质量分数与萃取率均有显著上升(P<0.05)的趋势。这与Somporn等[25]研究发现的热萃咖啡规律相似,该研究指出,将生咖啡豆在100~240 ℃下加热10 min左右,生咖啡豆的物质在高温下不断分解,并形成新的物质,随着烘焙温度上升,烘焙时间延长,美拉德反应、Strecker反应和焦糖化反应也在不断地进行,挥发性前体化合物(如糖、胺和绿原酸)的降解,从而产生大量水溶性化合物,因此萃取浓度和萃取率会不断上升。另一方面Cantaragiu等[26]的研究指出随着烘焙度增加,咖啡豆组织结构变得蓬松,空腔变大,更有利于物质溶出和萃取率上升。本研究还发现相同烘焙度下,热萃咖啡的萃取率显著低于冷萃咖啡(P<0.05),这可能是因为在相同烘焙度下,咖啡粉在高温浸泡时的吸水率也有所提高,同样质量的咖啡粉,加入同等水后,冷萃咖啡往往能得到更多的咖啡液[25],因此冷萃咖啡拥有更高的萃取率。
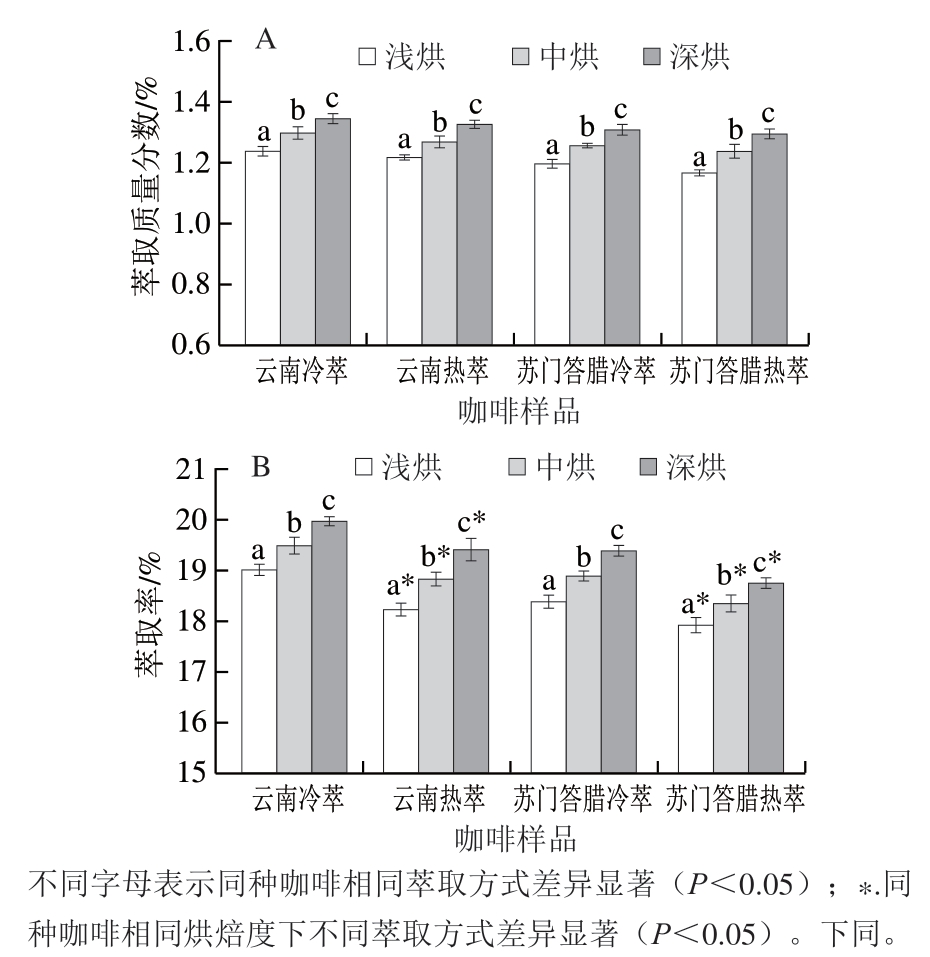
图1 不同烘焙度冷萃和热萃亚洲咖啡萃取质量分数(A)和萃取率(B)
Fig. 1 Extract concentration (A) and extraction efficiency (B) of hot and cold brew coffee with different roasting degrees
2.2 烘焙度对冷萃咖啡非挥发性成分的影响
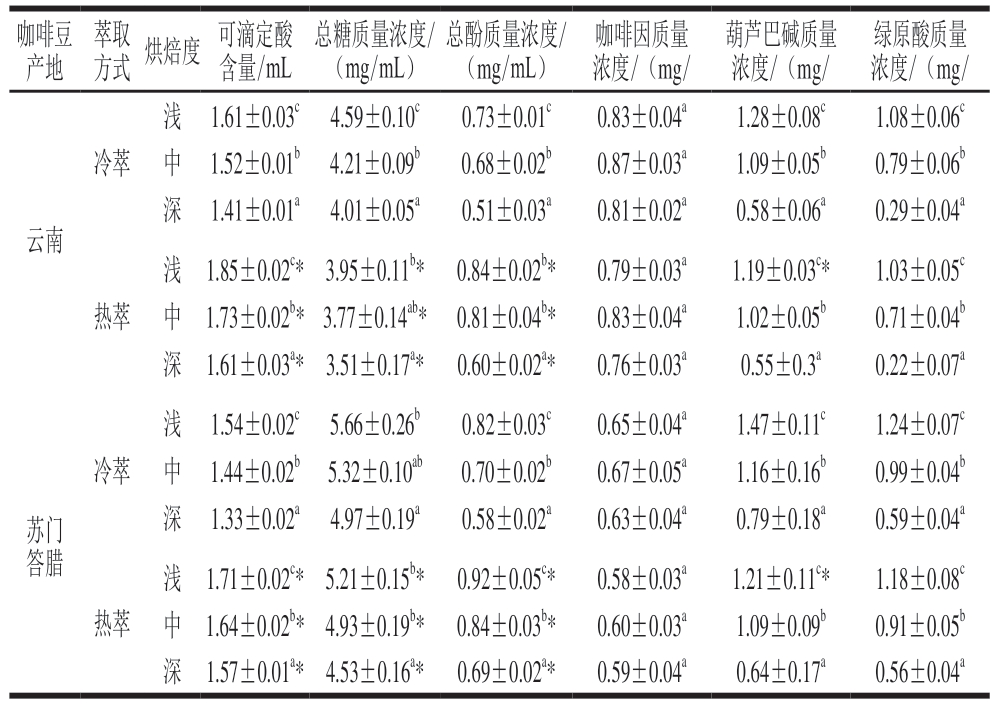
由表1可见,随云南与苏门答腊咖啡豆咖啡烘焙度增加,冷萃咖啡的可滴定酸含量、总糖含量以及总酚含量变化与热萃咖啡中的变化趋势相类似,呈下降趋势,其中可滴定酸均显著降低(P<0.05),深烘冷萃咖啡较浅烘冷萃咖啡可滴定酸含量下降约10%,总糖含量下降约10%,总酚含量下降约25%。本研究中亚洲豆热萃咖啡的非挥发性物质变化规律与非洲及美洲豆的研究结果是相似的,同时这些研究表明可滴定酸、总糖和总酚含量的减少,与高温烘焙过程中一系列的反应密不可分[16-18]。另一方面,相同烘焙度下,冷萃咖啡的可滴定酸含量和总酚含量均显著低于的热萃咖啡(P<0.05),分别减少约13%、10%,这可能是由于高温水能更好地使酸类物质和酚类物质溶出[27]。而总糖在冷萃咖啡中的含量均显著高于相同烘焙度的热萃咖啡(P<0.05),约增高10%。
咖啡因、葫芦巴碱、绿原酸是咖啡中主要的能带来苦的味觉感受的组分,研究指出咖啡中10%~30%的苦味由咖啡因贡献,而葫芦巴碱、绿原酸及其衍生产物也是咖啡苦味的重要来源[28-29]。本研究发现2种亚洲豆随着烘焙度的上升,冷萃和热萃咖啡液中的葫芦巴碱、绿原酸含量均显著下降(P<0.05),这是由于葫芦巴碱和绿原酸在200 ℃以上烘焙时会快速分解[30-31],以致含量降低,深烘咖啡较浅烘咖啡萃取液种的葫芦巴碱含量下降约50%,绿原酸含量下降约60%,而由于咖啡因热稳定性较强,其含量相对稳定。在咖啡感官认识中,烘焙度越高的咖啡豆,其萃取液越苦,但在本研究中3种苦味物质总含量却呈下降趋势,这可能是因为随着咖啡豆烘焙度增加,由美拉德反应新产生的吡嗪、呋喃、吡咯类等苦味物质增强了咖啡的苦味[32]。另一方面,在相同烘焙度下,冷萃咖啡的咖啡因、葫芦巴碱、绿原酸含量略高于热萃咖啡,这与热萃咖啡比冷萃咖啡感官上更苦的通识相背,可能是与咖啡感官受入口温度影响有关[33]。
表1 不同烘焙度冷萃和热萃亚洲咖啡非挥发性成分
Table 1 Non-volatile components of cold and hot brew coffee with different roasting degrees
咖啡豆产地萃取方式 烘焙度 可滴定酸含量/mL总糖质量浓度/(mg/mL)总酚质量浓度/(mg/mL)咖啡因质量浓度/(mg/葫芦巴碱质量浓度/(mg/绿原酸质量浓度/(mg/冷萃浅 1.61±0.03c 4.59±0.10c 0.73±0.01c 0.83±0.04a 1.28±0.08c 1.08±0.06c中 1.52±0.01b 4.21±0.09b 0.68±0.02b 0.87±0.03a 1.09±0.05b 0.79±0.06b深 1.41±0.01a 4.01±0.05a 0.51±0.03a 0.81±0.02a 0.58±0.06a 0.29±0.04a云南热萃浅 1.85±0.02c* 3.95±0.11b* 0.84±0.02b* 0.79±0.03a 1.19±0.03c* 1.03±0.05c中 1.73±0.02b*3.77±0.14ab* 0.81±0.04b* 0.83±0.04a 1.02±0.05b 0.71±0.04b深 1.61±0.03a* 3.51±0.17a* 0.60±0.02a* 0.76±0.03a 0.55±0.3a 0.22±0.07a冷萃苏门答腊浅 1.54±0.02c 5.66±0.26b 0.82±0.03c 0.65±0.04a 1.47±0.11c 1.24±0.07c中 1.44±0.02b 5.32±0.10ab 0.70±0.02b 0.67±0.05a 1.16±0.16b 0.99±0.04b深 1.33±0.02a 4.97±0.19a 0.58±0.02a 0.63±0.04a 0.79±0.18a 0.59±0.04a热萃浅 1.71±0.02c* 5.21±0.15b* 0.92±0.05c* 0.58±0.03a 1.21±0.11c* 1.18±0.08c中 1.64±0.02b* 4.93±0.19b* 0.84±0.03b* 0.60±0.03a 1.09±0.09b 0.91±0.05b深 1.57±0.01a* 4.53±0.16a* 0.69±0.02a* 0.59±0.04a 0.64±0.17a 0.56±0.04a
2.3 烘焙度对冷萃咖啡抗氧化能力的影响
咖啡中的酚类、绿原酸与葫芦巴碱类等都具有抗氧化活性[34],并且咖啡豆在烘焙过程中由美拉德反应产生的类黑精也具有抗氧化活性[35],因此咖啡中的抗氧化体系是相对复杂的。本研究通过DPPH自由基和ABTS阳离子自由基清除能力,探究烘焙度对冷萃咖啡抗氧化能力的影响。如图2所示,随着云南与苏门答腊咖啡豆烘焙度增加,冷萃咖啡液中的DPPH自由基和ABTS阳离子自由基清除当量与热萃咖啡的变化趋势一致,均呈现显著降低(P<0.05)的趋势,这与Samsonowicz等[34]关于美洲咖啡豆热萃咖啡抗氧化能力的研究结果相似。另一方面,本研究发现冷萃咖啡的DPPH自由基和ABTS阳离子自由基清除当量均显著低于同烘焙度下热萃咖啡(P<0.05),这可能与热萃咖啡中含有更多的具有抗氧化活性的非去质子酸有关[35]。此外,深烘冷萃咖啡DPPH自由基清除当量较热萃方式下降幅度更为明显,这有可能与深烘咖啡豆中存在某些低温水溶性较差的抗氧化物质有关。
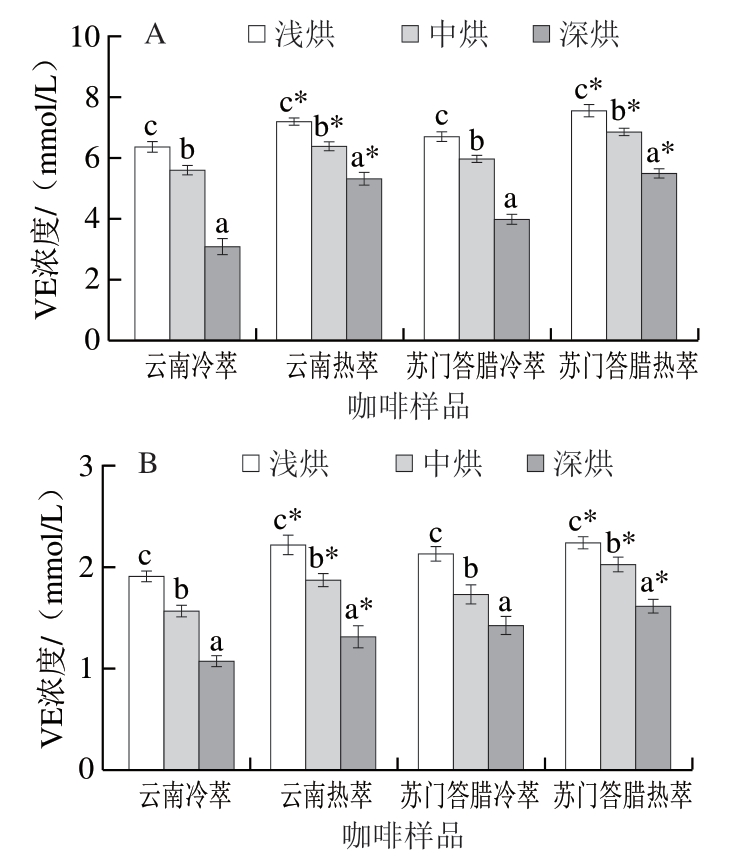
图2 不同烘焙度冷萃和热萃亚洲咖啡DPPH自由基(A)和ABTS阳离子自由基(B)清除当量
Fig. 2 DPPH radical (A) and ABTS radical cation (B) scavenging effects of hot and cold brew coffee with different roasting degrees
2.4 烘焙度对冷萃咖啡中挥发性化合物的影响
本研究从12 组咖啡样品中筛选出76种主要的挥发性风味成分,这些物质中包括多种酮、醛、酚、醇、酯、酸、吡嗪、吡咯和呋喃等。参考精品咖啡协会的咖啡风味分类,将筛选出的76种香气成分分为酶促反应香气(花果香类)、美拉德反应香气(烘焙坚果类)、干蒸馏类、瑕疵类四大类。由表2可知,无论冷萃还是热萃方式,云南豆咖啡萃取液中花果类挥发性成分相对占比约2%~4%,而苏门答腊豆咖啡萃取液中花果类香气占比更高,约5%~11%;2种亚洲豆咖啡液中的烘焙坚果类香气占比约75%~90%,剩余部分为约4%~19%的瑕疵类香气和约2%~5%的干蒸馏类香气。在相同烘焙度下,冷萃咖啡的挥发性成分总量多于热萃咖啡,各大类香气含量也分别高于热萃咖啡,同时,冷萃咖啡的花果香类挥发性成分相对占比更高,而烘焙坚果类挥发性成分相对占比较低。这与陈仲娜等[36]关于云南小粒咖啡冷萃和热萃咖啡香气成分的研究结果相近,该研究发现云南冷萃在柑橘类香、甜香、水果香、坚果香均比热萃浓郁且丰富,而热萃在酸香、爆谷物香、烟熏香、焦香均比冷萃的浓郁且丰富。此外,本研究发现对于云南咖啡豆,冷萃相对于热萃的萃取液中瑕疵类挥发性成分更少,对于苏门答腊咖啡豆,冷萃的瑕疵类挥发性成分则多于热萃。
值得注意的是,随着烘焙度的增加,冷萃与热萃咖啡中的挥发性成分总量均呈现增加趋势,尤其是2-甲基丁醛、2-乙基吡嗪、榛子吡嗪、糠基甲基硫醚和乙酸糠醇酯等呈现烘焙坚果类、瑕疵类和干蒸馏类香气成分含量呈现增加的趋势(P<0.05),而花果香类挥发性成分含量较为稳定。而从相对占比上看,随着烘焙度的增加,花果香类和烘焙坚果类挥发性成分相对占比均呈现下降趋势,而瑕疵类和干蒸馏类相对占比均上升趋势,这种趋势在云南豆冷萃的咖啡中更为明显。特别是深烘咖啡相较于浅烘咖啡,冷萃液中醚类、酚类、酮类和杂环类物质含量有50%以上的增加,这些成分主要呈烘焙坚果类、瑕疵类和干蒸馏类香气,尤其是呈现烘焙坚果类香气的糠基甲醚、2-(呋喃-2-基甲基)呋喃,瑕疵类香气的1-甲基吡咯、苯酚和邻甲酚,干蒸馏类香气的糠基甲基硫醚、2-乙酰-1-甲基吡咯等物质增加显著,这可能是消费者品尝使用深度烘焙豆冷萃的咖啡时感受到香气更加浓郁的主要原因。
表2 不同烘焙度冷萃和热萃亚洲咖啡挥发性化合物含量
Table 2 Volatile compound contents of hot and cold brew coffee with different roasting degrees

含量/(μg/kg)云南豆 苏门答腊豆冷萃 热萃 冷萃 热萃浅烘 中烘 深烘 浅烘 中烘 深烘 浅烘 中烘 深烘 浅烘 中烘 深烘香气种类 序号 挥发性成分 气味描述2-丁酮 果味 4.78 2.67 1.81 0.52 — — 6.66 4.01 2.77 1.90 1.65 1.32 2 2-甲基丁酸甲酯 果味、苹果 — — — — — — 3.23 3.47 3.41 0.87 0.62 0.73 3 2-丁烯醛 花香 1.37 0.84 — 1.02 — — — — — — — —4 2,3-戊二酮 甜味、奶油 8.06 7.27 4.06 5.41 5.27 2.81 25.18 19.56 17.83 14.86 13.09 8.89 5己醛 草味、果味 1.06 0.93 0.77 0.87 0.62 0.44 12.04 8.63 4.02 4.80 4.77 3.86 6 2-庚醇 柠檬、草、花香 1.31 1.08 2.17 — — — 2.18 2.46 3.86 1.93 — —7 3-辛醇 柑橘 — — — — — — 3.14 3.15 4.27 — — —8 (Z)-芳樟醇氧化物 花香、甜味 — — — — — — 30.84 21.29 17.47 31.10 21.09 19.01 9 (E)-芳樟醇氧化物 花香 — — — — — — 17.04 13.90 11.23 13.46 10.46 8.66 10 (E)-2-壬醛 柑橘 — — — — — — 4.46 5.87 9.22 2.45 3.15 3.55 11 芳樟醇 柑橘、花香、甜味 11.93 13.19 10.29 5.03 5.17 5.08 48.90 44.88 44.91 14.57 15.77 15.73 12 苯乙酮 甜味、山楂、杏仁 — — 4.62 — — 2.44 — 10.26 7.15 3.68 4.73 4.54 13 α-松油醇 丁香花、花香 2.92 3.87 4.63 1.16 1.03 3.04 11.67 13.83 15.23 3.99 4.12 4.73 14 异戊酸糠醇酯 浆果、果味、葡萄 0.56 4.22 11.50 — 4.44 6.22 2.66 3.67 13.49 — — 4.40 15 水杨酸甲酯 绿薄荷 — — — — — — 5.24 8.63 17.65 7.07 11.50 12.38 16 香叶醇 甜味、花香、果味 4.91 — — 1.05 — — 14.22 7.28 5.77 6.65 — —17 3,4-二甲氧基苯乙烯 花香、草味、果味 3.82 5.63 7.99 2.91 6.63 7.79 5.36 7.23 15.47 4.24 9.28 10.44 18 2-异丁基-3-甲氧基吡嗪 豌豆 3.07 3.15 3.01 0.86 0.89 0.93 3.60 4.08 3.81 1.27 1.32 1.29小计 43.79 42.85 50.85 18.83 24.05 28.75 196.42 182.20 197.56 112.84 101.55 99.53占比/% 4.38 3.47 3.20 2.24 2.22 2.20 11.30 8.88 7.77 7.32 5.63 5.10 19 2-乙基吡嗪 花生、黄油、坚果 13.88 17.24 21.42 13.42 13.75 16.34 17.41 20.45 22.26 20.71 20.84 22.62 20 3,4-己烷二酮 黄油、杏仁、坚果 1.52 2.13 3.03 1.07 1.24 2.88 1.49 2.70 4.82 2.66 2.68 3.17 21 川芎嗪 坚果 1.27 1.35 2.14 0.81 0.96 1.80 — — — — — —22 2,5-二乙基吡嗪 坚果 4.93 5.54 8.65 2.86 3.08 3.39 5.08 5.54 5.62 2.84 3.45 4.55 23 2,6-二乙基吡嗪 坚果 51.66 54.94 62.70 36.01 41.13 58.76 11.66 43.49 18.35 37.44 8.91 8.44 24 2-乙酰呋喃 甜味、杏仁、可可 24.24 31.98 39.45 20.68 30.89 34.51 32.99 49.40 84.83 45.76 58.99 65.89 25 异戊酸肉桂酯 甜味、香料、果味 — — 3.27 — 1.86 2.73 — — — — — —26 2,3-丁二酮 黄油、甜味、奶油 2.67 3.09 4.47 2.05 2.24 3.09 7.27 9.39 11.33 4.94 5.62 7.95 27 2-甲基丁醛 可可、咖啡、坚果 20.26 24.83 24.47 12.54 15.35 18.23 21.23 24.22 27.37 18.71 22.57 24.87 28 异戊醛 巧克力 12.72 14.23 15.89 7.13 7.18 7.12 42.16 49.33 48.13 14.53 21.41 9.91 29 2,5-二甲基呋喃 肉味、焙烤、牛肉 0.75 1.32 2.89 0.33 0.57 0.68 1.39 1.98 4.03 0.32 0.52 0.62 30 2-甲基-2-丁烯醛 刺鼻的、坚果 — 0.40 0.77 — — 0.57 — 0.94 1.42 — — 0.38 31 2,4,5-三甲基恶唑 坚果、焙烤 0.77 1.29 3.01 0.63 0.75 1.02 1.18 1.17 2.71 1.50 1.09 1.08 32 糠基甲醚 焙烤 1.26 3.54 7.31 0.97 1.46 3.58 3.33 5.74 9.72 2.50 2.20 3.98 33 2-甲基吡嗪 坚果、可可、焙烤 26.78 31.94 37.27 25.11 31.44 37.37 40.25 45.23 50.81 36.96 41.50 45.33 34 2,5-二甲基吡嗪 可可、烤坚果、烤肉 — — — — — — 27.41 18.10 30.08 27.56 29.17 23.70 35 甲基糠硫醇 焙烤 1.41 10.33 18.67 0.68 7.95 14.64 — — — — 16.43 17.63 36 2-乙基-6-甲基吡嗪 焙烤、马铃薯 31.93 35.38 41.45 27.89 30.63 31.88 45.79 54.19 56.76 36.89 46.29 47.88 1酶促反应香气(花果香)焦糖化反应香气(烘焙坚果)37 咖啡吡嗪 坚果、草、焙烤 21.72 23.43 26.35 18.97 20.54 23.63 28.09 30.11 33.46 22.95 28.03 30.56 38 榛子吡嗪 坚果、玉米、面包 20.88 23.30 28.27 19.13 21.64 25.47 12.32 14.44 15.29 23.34 26.73 28.32 39 糠醇 焦糖 288.54 239.65 128.74 293.15 250.63 110.58 624.43 523.23 424.88 589.45 461.08 321.89 40 2-甲基-5-乙烯基吡嗪 焙烤、坚果 1.89 4.67 6.03 1.57 2.29 5.07 1.79 3.40 8.69 3.08 4.63 5.10 41 3,5-二乙基-2-甲基吡嗪 坚果、肉味 16.81 20.49 21.78 8.25 9.66 10.34 22.23 25.11 28.55 5.77 7.22 7.69 42 5-甲基糠醛 香料、焦糖 186.47 215.09 140.35 150.18 231.83 138.46 199.31 231.23 192.12 188.87 271.33 258.10 43 1-甲基-2-吡咯甲醛 焙烤、坚果 24.33 44.07 50.22 21.34 37.85 40.33 33.42 42.14 51.24 42.41 76.60 86.32 44 2-(呋喃-2-基甲基)呋喃 焙烤 3.46 6.89 26.66 3.46 7.89 23.37 7.42 8.93 26.01 3.49 9.04 17.79 45 2-乙酰吡咯 坚果、核桃、面包 3.93 6.62 9.24 2.91 9.22 16.02 15.85 7.43 20.42 5.06 11.33 12.83 46 二糠基醚 坚果、泥土 5.81 16.38 59.21 4.23 14.19 52.54 18.02 15.84 67.86 12.41 23.15 45.06 47 3-己酮 甜味、果味、葡萄 0.83 1.34 2.64 0.33 0.59 0.89 1.30 1.59 3.40 0.46 0.68 0.88 48 乙酸糠醇酯 甜味、果味、香蕉 90.83 165.49 317.30 67.02 110.60 265.46 156.35 404.19 563.72 126.16 239.00 424.22 49 2,3-己二酮 甜味、焦糖、黄油 1.59 2.36 3.07 0.98 1.25 1.44 5.07 6.86 7.36 2.62 3.03 2.96 50 丙酮醇 甜味、焦糖 1.22 1.11 — 1.18 1.13 — 2.46 2.21 — 1.44 - -51 乙基环戊烯酮 甜味、焦糖、枫树 — — 27.83 — 2.22 29.63 — 1.65 40.73 16.80 32.30 25.55
续表2
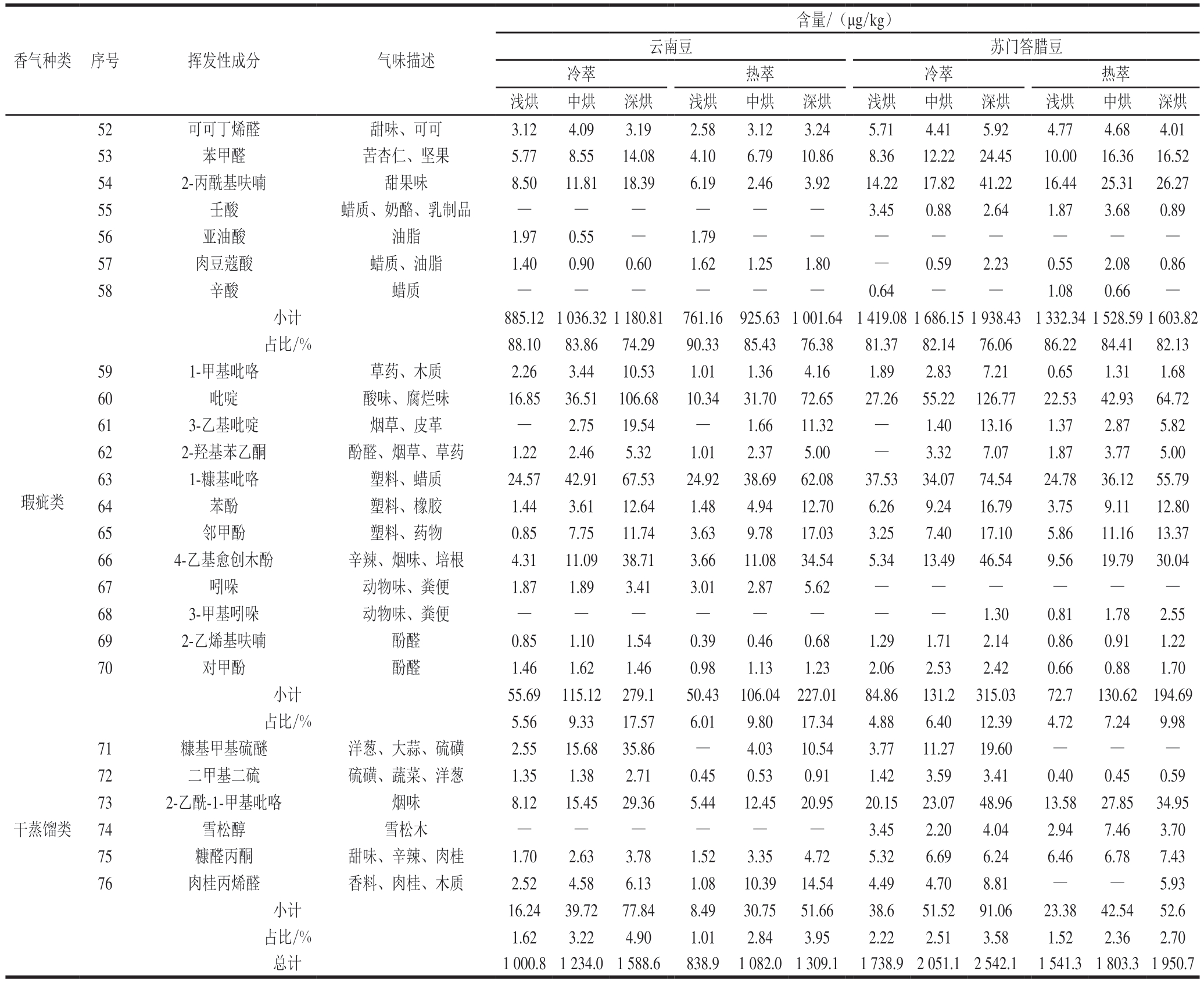
注:化合物匹配度大于90%,气味描述参考文献[36-37];每种挥发性成分含量为3 组平行均值;—.未检出。
含量/(μg/kg)云南豆 苏门答腊豆冷萃 热萃 冷萃 热萃浅烘 中烘 深烘 浅烘 中烘 深烘 浅烘 中烘 深烘 浅烘 中烘 深烘52 可可丁烯醛 甜味、可可 3.12 4.09 3.19 2.58 3.12 3.24 5.71 4.41 5.92 4.77 4.68 4.01 53 苯甲醛 苦杏仁、坚果 5.77 8.55 14.08 4.10 6.79 10.86 8.36 12.22 24.45 10.00 16.36 16.52 54 2-丙酰基呋喃 甜果味 8.50 11.81 18.39 6.19 2.46 3.92 14.22 17.82 41.22 16.44 25.31 26.27 55 壬酸 蜡质、奶酪、乳制品 — — — — — — 3.45 0.88 2.64 1.87 3.68 0.89 56 亚油酸 油脂 1.970.55— 1.79— — — — — — — —57 肉豆蔻酸 蜡质、油脂 1.40 0.90 0.60 1.62 1.25 1.80 — 0.59 2.23 0.55 2.08 0.86 58 辛酸 蜡质 — — — — — — 0.64— — 1.080.66—小计 885.121 036.321 180.81 761.16 925.631 001.64 1 419.081 686.151 938.43 1 332.341 528.591 603.82占比/% 88.10 83.86 74.29 90.33 85.43 76.38 81.37 82.14 76.06 86.22 84.41 82.13香气种类 序号 挥发性成分 气味描述59 1-甲基吡咯 草药、木质 2.26 3.44 10.53 1.01 1.36 4.16 1.89 2.83 7.21 0.65 1.31 1.68 60 吡啶 酸味、腐烂味 16.85 36.51 106.68 10.34 31.70 72.65 27.26 55.22 126.77 22.53 42.93 64.72 61 3-乙基吡啶 烟草、皮革 — 2.75 19.54 — 1.66 11.32 — 1.40 13.16 1.37 2.87 5.82 62 2-羟基苯乙酮 酚醛、烟草、草药 1.22 2.46 5.32 1.01 2.37 5.00 — 3.32 7.07 1.87 3.77 5.00 63 1-糠基吡咯 塑料、蜡质 24.57 42.91 67.53 24.92 38.69 62.08 37.53 34.07 74.54 24.78 36.12 55.79 64 苯酚 塑料、橡胶 1.44 3.61 12.64 1.48 4.94 12.70 6.26 9.24 16.79 3.75 9.11 12.80 65 邻甲酚 塑料、药物 0.85 7.75 11.74 3.63 9.78 17.03 3.25 7.40 17.10 5.86 11.16 13.37 66 4-乙基愈创木酚 辛辣、烟味、培根 4.31 11.09 38.71 3.66 11.08 34.54 5.34 13.49 46.54 9.56 19.79 30.04 67 吲哚 动物味、粪便 1.87 1.89 3.41 3.01 2.87 5.62 — — — — — —68 3-甲基吲哚 动物味、粪便 — — — — — — — — 1.30 0.81 1.78 2.55 69 2-乙烯基呋喃 酚醛 0.85 1.10 1.54 0.39 0.46 0.68 1.29 1.71 2.14 0.86 0.91 1.22 70 对甲酚 酚醛 1.46 1.62 1.46 0.98 1.13 1.23 2.06 2.53 2.42 0.66 0.88 1.70小计 55.69 115.12 279.1 50.43 106.04 227.01 84.86 131.2 315.03 72.7 130.62 194.69占比/% 5.56 9.33 17.57 6.01 9.80 17.34 4.88 6.40 12.39 4.72 7.24 9.98 71 糠基甲基硫醚 洋葱、大蒜、硫磺 2.55 15.68 35.86 — 4.03 10.54 3.77 11.27 19.60 — — —72 二甲基二硫 硫磺、蔬菜、洋葱 1.35 1.38 2.71 0.45 0.53 0.91 1.42 3.59 3.41 0.40 0.45 0.59 73 2-乙酰-1-甲基吡咯 烟味 8.12 15.45 29.36 5.44 12.45 20.95 20.15 23.07 48.96 13.58 27.85 34.95干蒸馏类 74 雪松醇 雪松木 — — — — — — 3.45 2.20 4.04 2.94 7.46 3.70 75 糠醛丙酮 甜味、辛辣、肉桂 1.70 2.63 3.78 1.52 3.35 4.72 5.32 6.69 6.24 6.46 6.78 7.43 76 肉桂丙烯醛 香料、肉桂、木质 2.52 4.58 6.13 1.08 10.39 14.54 4.49 4.70 8.81 — — 5.93小计 16.24 39.72 77.84 8.49 30.75 51.66 38.6 51.52 91.06 23.38 42.54 52.6占比/% 1.62 3.22 4.90 1.01 2.84 3.95 2.22 2.51 3.58 1.52 2.36 2.70总计 1 000.8 1 234.0 1 588.6 838.9 1 082.0 1 309.1 1 738.9 2 051.1 2 542.1 1 541.3 1 803.31 950.7瑕疵类
2.5 咖啡香气成分PCA
现有文献对不同烘焙度冷萃咖啡挥发性成分的研究鲜有报道,为进一步探究不同烘焙度冷萃和热萃咖啡挥发性成分的差异,将76种具有香气的挥发性化合物进行PCA。由图3A可知,12 组冷萃和热萃咖啡样品在PC1和PC2维度上有较好区分,PC1和PC2的贡献度分别为46.34%%和24.15%,浅烘咖啡(红线以上)主要分布于第1象限附近,中烘咖啡(红、绿线中间)主要分布于原点两侧,深烘咖啡(绿线以下)主要分布于第3象限附近,表明浅、中和深烘咖啡的挥发性物质贡献率具有明显差异,可以根据挥发性成分有效区分不同烘焙度的咖啡。与浅烘咖啡分布较近的主要挥发性成分有2-丁烯醛、香叶醇、糠醇、辛酸、亚油酸等,这些物质呈现香气以花香、甜味、油脂味为主;与中烘咖啡分布较近的主要挥发性成分有己醛、2,6-二乙基吡嗪、5-甲基糠醛等,呈现了花香、果味、坚果等香气;与深烘咖啡分布较近的主要挥发性成分明显多于前两者,3-乙基吡啶、甲基糠硫醇、2,5-二乙基吡嗪、3,5-二乙基-2-甲基吡嗪、1-甲基-2-吡咯甲醛、异戊酸肉桂酯、2,5-二甲基吡嗪等富含烟味、香料、焙烤、坚果类香气成分。此外,挥发性成分对苏门答腊豆咖啡的贡献率总体高于云南豆咖啡,且影响主要挥发性成分也不同。另一方面,中烘与深烘豆咖啡冷萃的样品点之间的离散度较热萃啡样品点的离散度更大,表明深烘咖啡豆对冷萃咖啡香气成分的影响更大。
由图3B可知,咖啡样品在PC1和PC3两个维度上有所区分,能反映原始数据的变异信息,其中PC1和PC3的贡献度分别为46.34%和14.19%。热萃咖啡(红圈)主要分布于PC1、PC3的正半轴而冷萃咖啡(绿圈)主要分布于PC1、PC3负半轴附近,而挥发性成分的分布规律是PC1负半轴明显高于正半轴,表明冷萃和热萃咖啡的挥发性物质贡献率具有差异,可以根据挥发性成分有效区分不同萃取方式的咖啡。其中与热萃咖啡分布较近的主要挥发性成分有甲基糠硫醇、榛子吡嗪、5-甲基糠醛、辛酸、吲哚、亚油酸、肉豆蔻酸等,这些物质主要呈现焙烤、油脂、蜡质、焦糖、动物味,与冷萃咖啡分布较近的挥发性成分更多,主要有2-丁酮、2-乙烯基呋喃、丙酮醇、2,6-二乙基吡嗪、2,5-二乙基吡嗪、香叶醇等,这些物质呈现果味、花香、甜味、坚果味等,因此冷萃和热萃咖啡在主要挥发性成分方面有较大差异,且香气呈现类型也有较大差别。另外,3-乙基吡啶、2,5-二乙基吡嗪等物质含量变化明显受到到烘焙度的影响,这与Caporaso等[37]关于25种非洲、美洲和亚洲豆的热萃咖啡香气成分研究结果相似。
此外,对冷萃咖啡样品和热萃咖啡样品分别进行PCA(图3C、D),从而分析不同烘焙度的咖啡豆在冷萃与热萃萃取液中挥发性成分影响的差异。由图3C可知,6 组冷萃咖啡样品在PC1和PC2维度上有明显区分,PC1和PC2的贡献度分别为54.65%和32.52%。浅烘冷萃咖啡(红线以上)主要分布于第2象限附近,中烘冷萃咖啡(红、绿线中间)主要分布于原点两侧,深烘冷萃咖啡(绿线以下)主要分布于第4象限附近,挥发性成分主要分布于PC1正半轴,表明不同烘焙度的冷萃咖啡的挥发性物质贡献率具有明显差异。与浅烘冷萃咖啡分布较近的主要挥发性成分有2-丁酮、香叶醇、辛酸(苏门答腊豆)和2-丁烯醛、亚油酸(云南豆);与中烘冷萃咖啡分布较近的主要挥发性成分有2,3-戊二酮、己醛、(Z)-芳樟醇氧化物(苏门答腊豆)和2,6-二乙基吡嗪、川芎嗪、吲哚(云南豆);与深烘冷萃咖啡分布较近的主要挥发性成分有2-乙烯基呋喃、2-乙酰呋喃、2-丙酰基呋喃(苏门答腊豆)和甲基糠硫醇、2,5-二乙基吡嗪、糠基甲基硫醚、异戊酸肉桂酯(云南豆)。由图3D可知,6 组热萃咖啡样品在PC1和PC2维度上有明显区分,PC1和PC2的贡献度分别为50.66%和34.33%。浅烘热萃咖啡(红线以下)主要分布于第3象限附近,中烘热萃咖啡(红、绿线中间)主要分布于原点两侧,深烘热萃咖啡(绿线以上)主要分布于第2象限附近,挥发性成分主要分布于PC1正半轴。与浅烘热萃咖啡分布较近的主要挥发性成分有香叶醇、糠醇、辛酸(苏门答腊豆)和丙酮醇、亚油酸(云南豆);与中烘热萃咖啡分布较近的主要挥发性成分有2,4,5-三甲基恶唑、2,3-戊二酮、苯酚(苏门答腊豆)和2,6-二乙基吡嗪、川芎嗪、吲哚(云南豆);与深烘热萃咖啡分布较近的主要挥发性成分有榛子吡嗪、乙酸糠醇酯、3,4-己烷二酮、2-甲基吡嗪(苏门答腊豆)和二甲基二硫、对甲酚、1-甲基吡咯、肉桂丙烯醛(云南豆)。
综合PCA结果表明,冷萃和热萃咖啡中代表性的挥发性成分差异较大。随着烘焙度增加,咖啡中烘焙坚果类、瑕疵类和干蒸馏类成分含量增加,这些成分对各组咖啡风味成分差异特征的贡献率也在增加,尤其瑕疵类香气占总香气成分比例上升显著,且这种影响在冷萃咖啡中更为明显,尤其是深度烘焙豆冷萃的咖啡液。
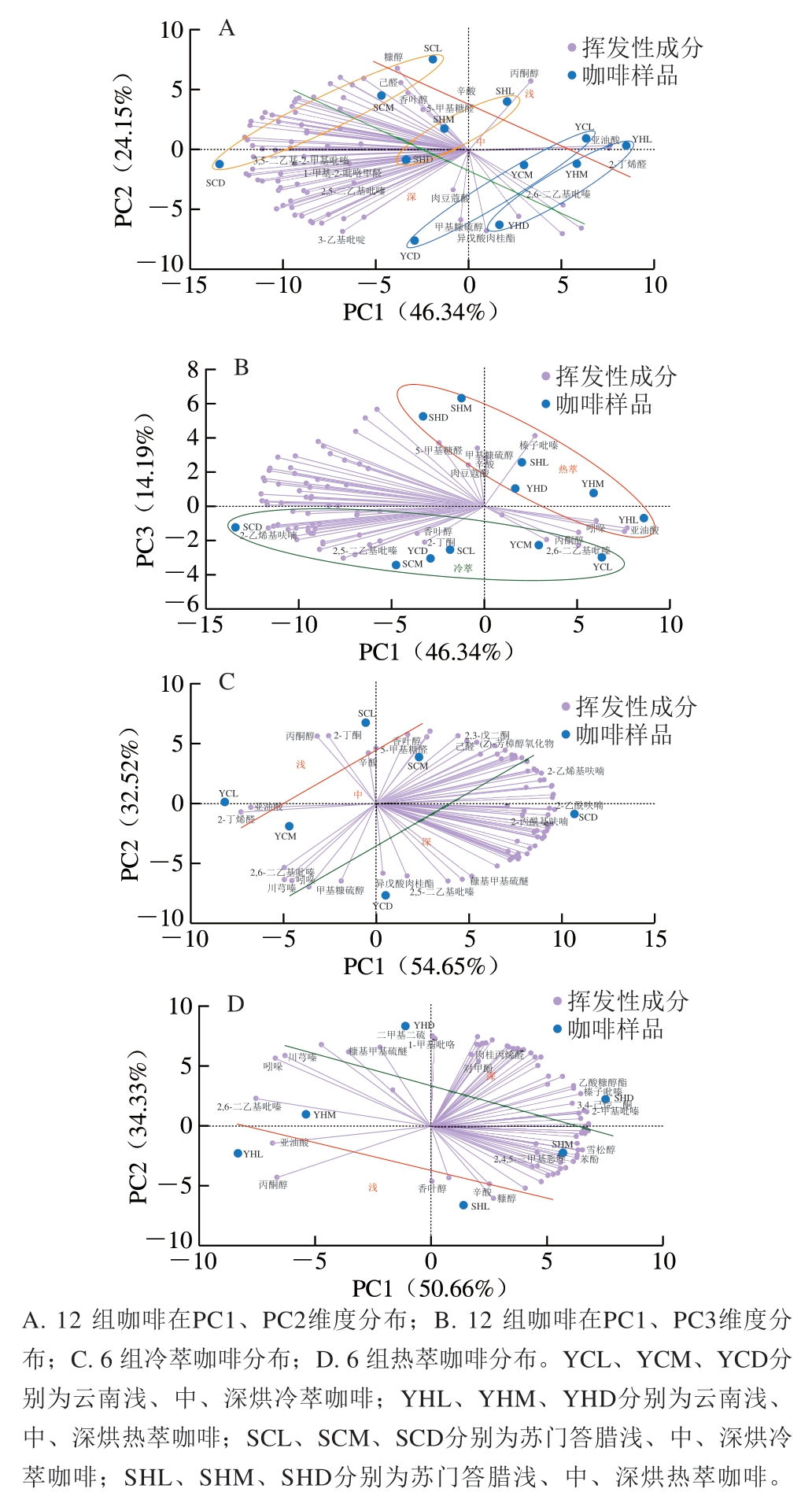
图3 不同烘焙度冷萃和热萃亚洲咖啡挥发性成分PCA
Fig. 3 PCA plots of volatile components in hot and cold brew coffee with different roasting degrees
3 结 论
以亚洲咖啡豆为研究对象,探究不同烘焙度对冷萃咖啡的理化性质、非挥发性成分、挥发性成分的影响,并与热萃咖啡进行比较分析。总体来说,烘焙度对冷萃与热萃咖啡的理化性质与非挥发性成分的影响较为相似,随着烘焙度增加,咖啡萃取液的浓度、萃取率均显著上升,可滴定酸、总酚、总糖、葫芦巴碱、绿原酸水平和抗氧化活性均显著下降(P<0.05),特别是深烘冷萃咖啡的DPPH自由基清除活性较热萃下降更为明显。在相同烘焙度下,冷萃咖啡的可滴定酸、总酚含量、抗氧化活性显著低于热萃咖啡,萃取率与总糖显著高于热萃咖啡,而冷萃与热萃不同萃取方式对咖啡因、葫芦巴碱、绿原酸含量的影响较弱。
萃取方式(冷萃、热萃)与烘焙度等因素均会影响咖啡萃取液中的挥发性成分组成,具有较明显差异。浅烘咖啡萃取液中的2-丁酮、2-丁烯醛等花果香类物质对冷萃方式的贡献率更高,而2-甲基吡嗪、糠醇等烘焙坚果类香气物质对热萃方式的贡献率更高。中烘咖啡萃取液中2,6-二乙基吡嗪、川芎嗪等以烘焙坚果类香气为主物质对冷萃和热萃方式均有较更高的贡献率。深烘咖啡萃取液中2-乙烯基呋喃、甲基糠硫醇、2,5-二乙基吡嗪、糠基甲基硫醚等物质对冷萃方式有较高的贡献率,二甲基二硫、对甲酚、1-甲基吡咯等物质对热萃方式的贡献率更高。在相同烘焙度下,冷萃咖啡中呈现花果香类的挥发性成分含量显著高于热萃咖啡。而随着烘焙度增加,咖啡中花果香类成分占比下降,烘焙坚果类、瑕疵类和干蒸馏类成分占比增加,尤其瑕疵类香气相对占比上升显著,且这种影响趋势在深烘冷萃咖啡中更为明显。因此,相较于热萃方式,烘焙度对冷萃咖啡挥发性成分具有更大的影响。
[1]MEHARI B, CHANDRAVANSHI B S, REDI-ABSHIRO M, et al.Polyphenol contents of green coffee beans from different regions of Ethiopia[J]. International Journal of Food Properties, 2021, 24(1): 17-27. DOI:10.1080/10942912.2020.1858866.
[2]丁莉, 侯媛媛. 中国咖啡产业形势分析及发展建议[J].热带农业科学, 2019, 39(3): 105-109. DOI:10.12008/j.issn.1009-2196.2019.03.018.
[3]RAO N Z, FULLER M, GRIM M D. Physiochemical characteristics of hot and cold brew coffee chemistry: the effects of roast level and brewing temperature on compound extraction[J]. Foods, 2020, 9(7):902. DOI:10.3390/foods9070902.
[4]CORDOBA N, PATAQUIVA L, OSORIO C, et al. Effect of grinding,extraction time and type of coffee on the physicochemical and flavour characteristics of cold brew coffee[J]. Scientific Reports, 2019, 9(1):1-12. DOI:10.1038/s41598-019-44886-w.
[5]ANDUEZA S, VILA M A, DE PEÑA M P, et al. Influence of coffee/water ratio on the final quality of espresso coffee[J]. Journal of the Science of Food and Agriculture, 2007, 87(4): 586-592. DOI:10.1002/jsfa.2720.
[6]LOPEZ-GALILEA I, DE PENA M P, CID C. Correlation of selected constituents with the total antioxidant capacity of coffee beverages:influence of the brewing procedure[J]. Journal of Agricultural and Food Chemistry, 2007, 55(15): 6110-6117. DOI:10.1021/jf070779x.
[7]CAPRIOLI G, CORTESE M, CRISTALLI G, et al. Optimization of espresso machine parameters through the analysis of coffee odorants by HS-SPME-GC/MS[J]. Food Chemistry, 2012, 135(3): 1127-1133.DOI:10.1016/j.foodchem.2012.06.024.
[8]周斌, 任洪涛. 烘焙程度对云南小粒咖啡香气品质的影响[J].食品研究与开发, 2014, 35(22): 68-73. DOI:10.3969/j.issn.1005-6521.2014.22.020.
[9]张丰, 董文江, 王凯丽, 等. 云南不同地区烘焙咖啡豆挥发性成分的HS-SPME/GC-MS分析[J]. 食品工业科技, 2015, 36(11): 273-280.DOI:10.13386/j.issn1002-0306.2015.11.047.
[10]吕文佳, 刘云, 杨剀舟, 等. 咖啡主要烘焙风味物质的形成及变化规律[J]. 食品工业科技, 2015, 36(3): 394-400. DOI:10.13386/j.issn1002-0306.2015.03.077.
[11]RAO N Z, FULLER M. Acidity and antioxidant activity of cold brew coffee[J]. Scientific Reports, 2018, 8(1): 1-9. DOI:10.1038/s41598-018-34392-w.
[12]TOCI A T, FARAH A. Volatile fingerprint of Brazilian defective coffee seeds: corroboration of potential marker compounds and identification of new low quality indicators[J]. Food Chemistry, 2014, 153: 298-314.DOI:10.1016/j.foodchem.2013.12.040.
[13]HEO J A, ADHIKARI K, CHOI K S, et al. Analysis of caffeine,chlorogenic acid, trigonelline, and volatile compounds in cold brew coffee using high-performance liquid chromatography and solid-phase microextraction-gas chromatography-mass spectrometry[J]. Foods,2020, 9(12): 1746. DOI:10.3390/foods9121746.
[14]邵金良, 刘兴勇, 杨东顺, 等. 咖啡及咖啡制品中葫芦巴碱, 绿原酸和咖啡因含量比较分析[J]. 山西农业科学, 2016, 44(2): 158-163.DOI:10.3969/j.issn.1002-2481.2016.02.07.
[15]LIANG J, CHAN K C, RISTENPART W D. An equilibrium desorption model for the strength and extraction yield of full immersion brewed coffee[J]. Scientific Reports, 2021, 11(1): 1-13. DOI:10.1038/s41598-021-85787-1.
[16]CORDOBA N, MORENO F L, OSORIO C, et al. Chemical and sensory evaluation of cold brew coffees using different roasting profiles and brewing methods[J]. Food Research International, 2021,141: 110-141. DOI:10.1016/j.foodres.2021.110141.
[17]高文军, 李卫红, 王喜明, 等. 3,5-二硝基水杨酸法测定蔓菁中还原糖和总糖含量[J]. 中国药业, 2020, 29(9): 113-116. DOI:10.3969/j.issn.1006-4931.2020.09.034.
[18]BILGE G. Investigating the effects of geographical origin, roasting degree, particle size and brewing method on the physicochemical and spectral properties of Arabica coffee by PCA analysis[J]. Journal of Food Science and Technology, 2020, 57(9): 3345-3354. DOI:10.1007/s13197-020-04367-9.
[19]全国信息与文献标准化技术委员会. 饮料中咖啡因的测定: GB 5009.139—2014[S]. 北京: 中国标准出版社, 2014: 1-4.
[20]全国信息与文献标准化技术委员会. 咖啡及制品中葫芦巴碱的测定: NY/T 3012—2016[S]. 北京: 中国标准出版社, 2016: 1-3.
[21]全国信息与文献标准化技术委员会. 保健食品中绿原酸的测定:GB/T 22250—2008[S]. 北京: 中国标准出版社, 2008: 1-3.
[22]GORECKI M, HALLMANN E. The antioxidant content of coffee and its in vitro activity as an effect of its production method and roasting and brewing time[J]. Antioxidants, 2020, 9(4): 308. DOI:10.3390/antiox9040308.
[23]CHEONG M W, TONG K H, ONG J J M, et al. Volatile composition and antioxidant capacity of Arabica coffee[J]. Food Research International, 2013, 51(1): 388-396. DOI:10.1016/j.foodres.2012.12.058.
[24]BONINO M, SCHELLINO R, RIZZI C, et al. Aroma compounds of an Italian wine (Ruché) by HS-SPME analysis coupled with GCITMS[J]. Food Chemistry, 2003, 80(1): 125-133. DOI:10.1016/S0308-8146(02)00340-0.
[25]SOMPORN C, KAMTUO A, THEERAKULPISUT P, et al. Effects of roasting degree on radical scavenging activity, phenolics and volatile compounds of Arabica coffee beans (Coffea arabica L. cv. Catimor)[J]. International Journal of Food Science & Technology, 2011, 46(11):2287-2296. DOI:10.1111/j.1365-2621.2011.02748.x.
[26]CANTARAGIU A M, IVAN A S, ALEXE P, et al. Effect of ground and roasted parameters on both the microstructure of Arabica coffee beans and coffee infusion: an imagistic study[J]. Journal of Science and Arts,2020, 20(4): 957-968. DOI:10.46939/J.Sci.Arts-20.4-b01.
[27]ALVES R C, COSTA A S G, JEREZ M, et al. Antiradical activity,phenolics profile, and hydroxymethylfurfural in espresso coffee:influence of technological factors[J]. Journal of Agricultural and Food Chemistry, 2010, 58(23): 12221-12229. DOI:10.1021/jf1031229.
[28]FUJIMOTO H, NARITA Y, IWAI K, et al. Bitterness compounds in coffee brew measured by analytical instruments and taste sensing system[J]. Food Chemistry, 2021, 342: 128228. DOI:10.1016/j.foodchem.2020.128228.
[29]BARBOSA M S G, FRANCISCO J S, DOS SANTOS SCHOLZ M B, et al. Dynamics of sensory perceptions in arabica coffee brews with different roasting degrees[J]. Journal of Culinary Science & Technology,2019, 17(5): 453-464. DOI:10.1080/15428052.2018.1489321.
[30]刘兴勇, 陈兴连, 杜丽娟, 等. 多因素交互作用导致烘焙咖啡中绿原酸快速降解[J]. 食品科学, 2021, 42(9): 7-14. DOI:10.7506/spkx1002-6630-20200521-259.
[31]FULLER M, RAO N Z. The effect of time, roasting temperature, and grind size on caffeine and chlorogenic acid concentrations in cold brew coffee[J]. Scientific Reports, 2017, 7(1): 1-9. DOI:10.1038/s41598-017-18247-4.
[32]陈钰莹, 孙红波, 宋萧萧, 等. 咖啡苦味特性研究进展[J]. 食品科学,2020, 41(9): 285-293. DOI:10.7506/spkx1002-6630-20190423-304.
[33]STEEN I, WAEHRENS S S, PETERSEN M A, et al. Influence of serving temperature on flavour perception and release of Bourbon Caturra coffee[J]. Food Chemistry, 2017, 219: 61-68. DOI:10.1016/j.foodchem.2016.09.113.
[34]SAMSONOWICZ M, REGULSKA E, KARPOWICZ D, et al.Antioxidant properties of coffee substitutes rich in polyphenols and minerals[J]. Food Chemistry, 2019, 278: 101-109. DOI:10.1016/j.foodchem.2018.11.057.
[35]王瑶, 王晓娜, 张雪辉, 等. 云南小粒咖啡类黑精的抗氧化及减肥功能[J]. 食品科学, 2019, 40(1): 183-189. DOI:10.7506/spkx1002-6630-20170917-242.
[36]陈仲娜, 谢妍纯, 谢欣妍. 云南阿拉比卡咖啡冷萃和热萃香气分析[J].饮料工业, 2019, 22(3): 44-52.
[37]CAPORASO N, WHITWORTH M B, CUI C, et al. Variability of single bean coffee volatile compounds of Arabica and robusta roasted coffees analysed by SPME-GC-MS[J]. Food Research International,2018, 108: 628-640. DOI:10.1016/j.foodres.2018.03.077.
[38]DE MELO PEREIRA G V, DE CARVALHO NETO D P, JÚNIOR A I M, et al. Exploring the impacts of postharvest processing on the aroma formation of coffee beans: a review[J]. Food Chemistry, 2019, 272:441-452. DOI:10.1016/j.foodchem.2018.08.061.