支链氨基酸(branched chain amino acid,BCAA)即L-缬氨酸、L-亮氨酸、L-异亮氨酸,参与动物和人类的蛋白质合成并广泛应用于食品、药品和动物饲料行业[1-4]。目前,用于BCAA生产的方法包括化学合成法、蛋白质水解法以及微生物发酵法[5-7]。而化学合成法以及蛋白质水解法存在合成过程操作复杂、副产物多、产率低等问题[8]。微生物发酵法由于其成本低、产量高、不需要金属催化剂、作用条件温和等优点而备受关注[9]。如今,通过代谢工程与合成生物学在微生物中的应用,改造代谢网络从而改变代谢流的方向控制产物的合成成为研究热点[10]。
乙酰羟基酸合酶(acetohydroxyacid synthase,AHAS)(EC 2.2.1.6)又称乙酰乳酸合酶,是BCAA生物合成途径中的第一步关键酶,属于丙酮酸氧化酶亚类[11],AHAS存在于植物、真菌、古生菌和细菌中,但不存在于动物中[12]。该酶具有两个底物结合位点,其中第1个结合位点与丙酮酸结合性较高,第2个结合位点可以与丙酮酸、2-酮丁酸(2-ketobutyric acid,2-KB)结合[13]。因此,该酶在BCAA的生产途径中起到关键性作用。AHAS是硫胺素二磷酸(thiamine diphosphate,ThDP)依赖性酶,行使功能时需要黄素腺嘌呤二核苷酸(flavin adenine dinucleotide,FAD)和二价金属离子,如Mg2+[14]。由BCAA在微生物体内的合成途径(图1)可知AHAS被多条代谢途径共享,并且该酶易受到末端产物(L-亮氨酸、L-缬氨酸、L-异亮氨酸)的反馈抑制[15],因此对该酶进行深入研究并进行改造以解除反馈抑制,对提高工业化生产BCAA的效率格外重要。对不同微生物体内AHAS结构以及性质的探索一直是研究热点,这为改造该酶并提高BCAA的生产提供了更多的可能性。
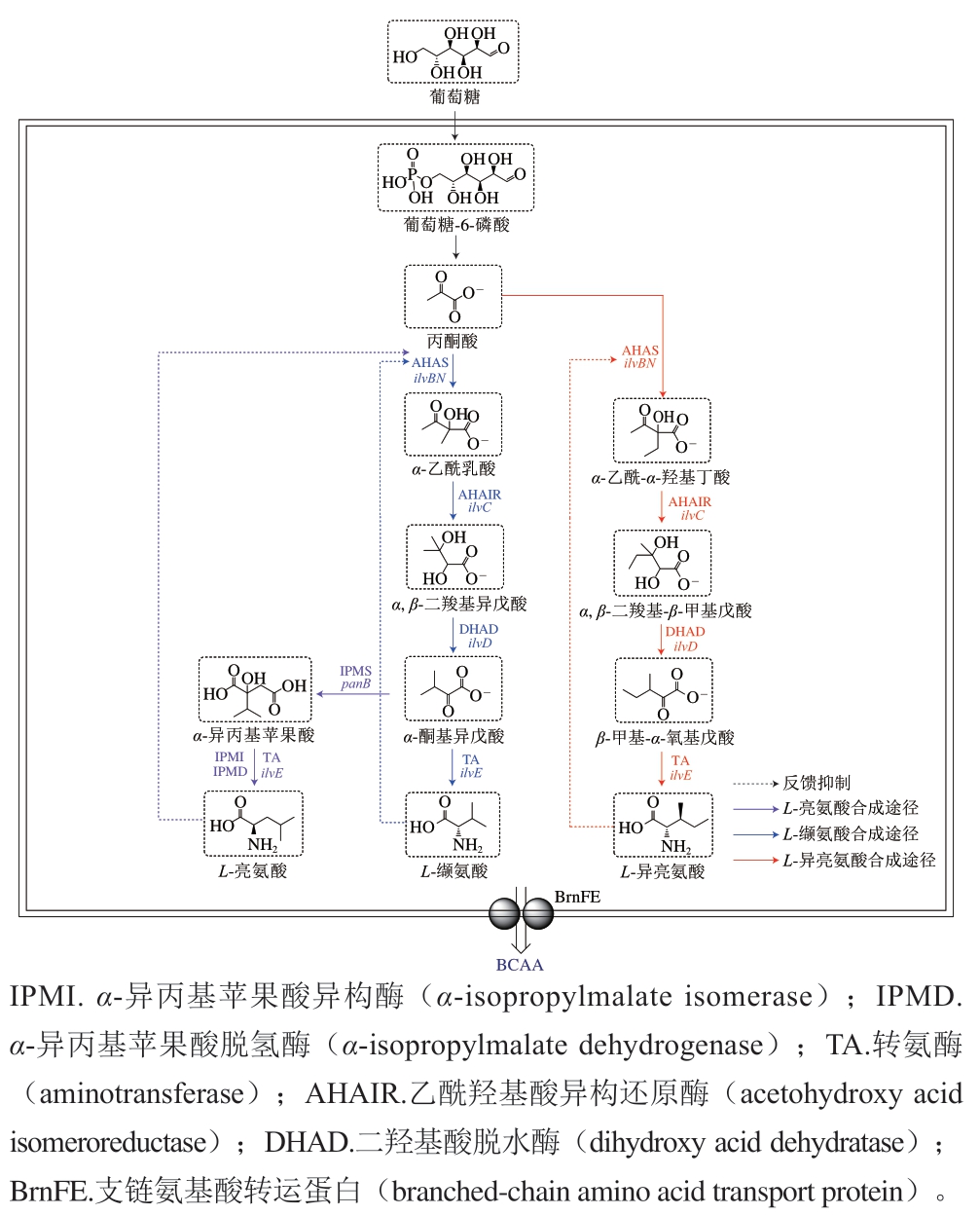
图1 微生物中的BCAA合成途径[15]
Fig. 1 BCAA pathways in microorganisms[15]
本文结合近几年国内外相关研究成果,总结并综述AHAS的结构、催化机理以及其现有的分子改造策略,展望未来的研究方向与改造策略,以期为深入研究该酶以及构建高产BCAA的工业菌株提供一定的借鉴。
1 AHAS的结构
AHAS由两个亚基组成,一个是含有催化位点的催化亚基(catalytic subunit,CSU),其分子质量大约为60 kDa,另一个是调节亚基(regulatory subunit,RSU),RSU在原核生物中分子质量约为9~17 kDa,真核生物中分子质量高达55 kDa[16-17]。RSU包含1 个结构域(ACT结构域)。该结构域是参与代谢、信号转导和溶质转运的保守结构基序,可以完全激活CSU的活性以及参与BCAA介导的反馈抑制[18-19]。RSU与CSU的偶联促进了CSU底物结合口袋的打开,进而导致酶的活化[20]。目前,部分物种AHAS的RSU和CSU的晶体结构及其复合体结构[19-21]已得到解析并公布于蛋白质数据库(Protein Data Bank,PDB)。
1.1 大肠杆菌AHAS的结构
AHAS首先在大肠杆菌中被发现[22],在大肠杆菌内存在3 种同工酶——AHAS I、AHAS II和AHAS III,3 种同工酶均是由两个大亚基和两个小亚基组合而成的四聚体酶,分别由基因ilvBN、ilvGM和ilvIH编码,其中ilvB、ilvG和ilvI编码AHAS的CSU,ilvN、ilvM和ilvH则编码AHAS的RSU[23]。同工酶AHAS I的RSU是1 种小分子质量蛋白质(96 个氨基酸残基),大约是其他细菌RSU大小的一半[17]。最近的研究发现AHAS I的RSU单体具有典型的铁氧化还原蛋白样折叠,中间有4 个β-折叠、3 个α-螺旋。AHAS I的全酶结构(PDB:6LPI)具有双重非晶体对称性,RSU二聚体位于CSU二聚体的顶部,来自RSU二聚体的4 个螺旋与CSU二聚体形成相互作用(图2A)[19]。Belenky等[24]发现AHAS I中的2 个氨基酸残基(Gln480和Leu476)与其他所有已知AHAS同源位置发现的氨基酸不同,这种差异赋予了AHAS I独特的性质。Xu Huiniu等[25]观察到了大肠杆菌中AHAS II与FAD、ThDP和Mg2+共结晶的CSU晶体并采集了其完整的X射线数据。Hill等[26]发现任何BCAA对该同工酶都没有反馈抑制作用,因为在其RSU编码序列中缺少与氨基酸结合的位点,例如ilvN中的G14或ilvH中的G20在ilvM中被Glu取代,ilvN中的N11或ilvH中的N17在ilvM中被Phe取代[17]。Kaplun等[21]成功地使大肠杆菌AHAS III 的RSU(PDB:2F1F)结晶化,并在1.75 Å分辨率下确定了其结构(图2B)。其RSU是具有紧密交织的两条链的同源二聚体,每个链由不同的N和C端结构域组成,这两个结构域都采用铁氧化还原样折叠。来自两条链的N端结构域组装形成1 个ACT结构域,与三磷酸甘油酸脱氢酶(3-phosphoglycerate dehydrogenase,3-PGDH)的C末端结构域非常接近。两个C端结构域组合在一起,使得它们的β-折叠大致背靠背定位,并垂直于N端ACT结构域的扩展β-折叠。
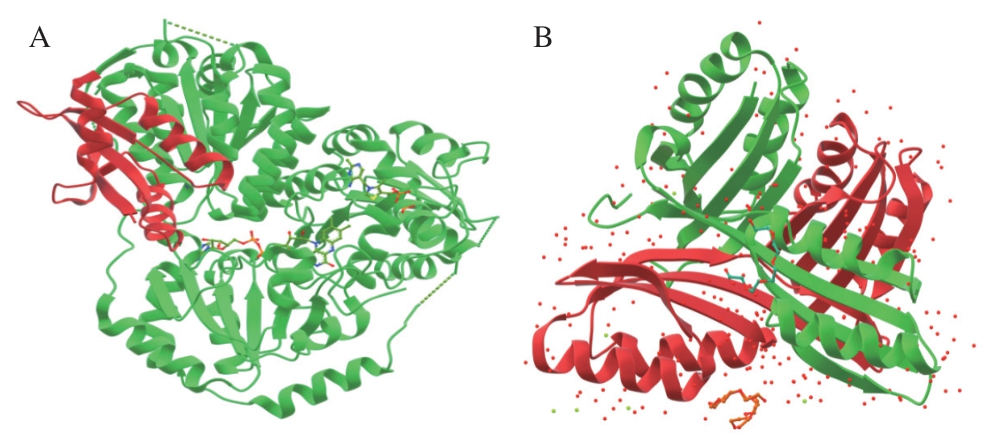
图2 大肠杆菌AHAS I全酶结构(A)[19]和大肠杆菌AHAS III 的RSU结构(B)[21]
Fig. 2 Structure of E. coli AHAS I holoenzyme (A)[19] and regulatory subunit structure of E. coli AHAS III (B)[21]
1.2 酿酒酵母与拟南芥AHAS的结构
Lonhienne等[20]发现了酿酒酵母AHAS(PDB:6U9D)全酶(Saccharomyces cerevisiae AHAS,ScAHAS)的晶体结构(图3A),并利用低温电子显微镜观察到了当L-赖氨酸存在或不存在时拟南芥的AHAS(PDB:6U9H)复合结构(Arabidopsis thaliana AHAS,AtAHAS)(图3B)。他们发现ScAHAS为十六聚体,ScAHAS中的RSU有4 个不同的区域:N-末端结构域及其扩展域,以及C-末端结构域与其扩展域。N-末端和C-末端结构域与细菌RSU同源二聚体的拓扑结构相似,该酶由8 个CSU和8 个RSU以马耳他十字形排列,8 个RSU形成1 个中央核心,4 个CSU二聚体连接到该核心上,4 个ATP对与RSU二聚体结合。AtAHAS复合物两个亚基中的大多数多肽都是可见的,RSU和CSU的整体布置类似于ScAHAS。不同的是,ScAHAS的8 个RSU的同源位置在AtAHAS中被4 个RSU所取代,每个RSU包含ScAHAS序列的两个伪重复序列并构成了中央核心。
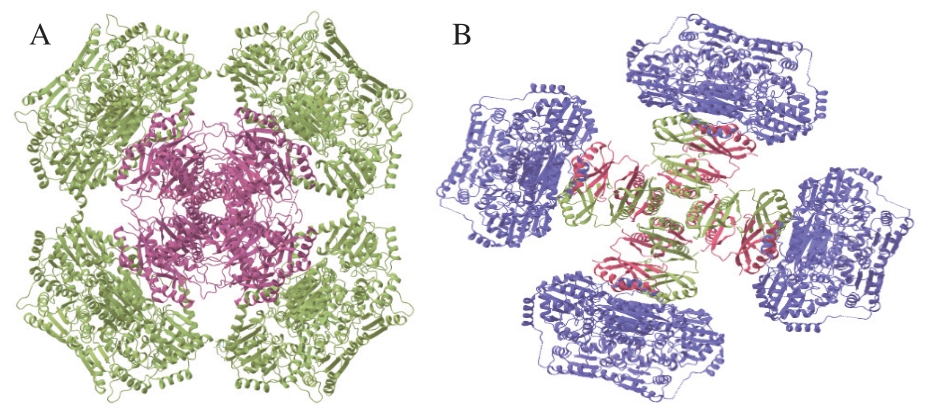
图3 酿酒酵母AHAS全酶结构(A)和拟南芥AHAS全酶结构(B)[20]
Fig. 3 Structure of Saccharomyces cerevisiae AHAS holoenzyme (A)and structure of Arabidopsis thaliana AHAS holoenzyme (B)[20]
1.3 CSU与RSU的联系
近几年,随着对大肠杆菌AHAS I与拟南芥、酿酒酵母AHAS全酶结构的揭示,CSU、RSU之间的相互作用模式也逐渐明晰。在大肠杆菌的AHAS I同工酶RSU二聚体的R32氨基酸残基和CSU二聚体中激活环的D120氨基酸残基之间存在一个高度保守的盐桥。当这个盐桥被破坏时会促进RSU与CSU的解离,从而显著降低3 种大肠杆菌AHAS亚型中AHAS全酶的活性(降低50%~80%),这种盐桥也可能在RSU激活CSU中发挥重要作用[19]。在ScAHAS中与CSU相互作用的RSU的主要区域是ACT结构域。ACT结构域的第1个α-螺旋(残基90~101)与活性位点Q环(残基191~204)形成盐桥R101(RSU)和D199(CSU)。该盐桥在ScAHAS复合体中高度保守。ACT结构域的第2个α-螺旋(残基129~140)与两个CSU之一的β结构域相互作用。在AtAHAS复合体中,当RSU与CSU结合时CSU二聚体发生收缩并稳定AtAHAS复合体中的CSU。AtAHAS复合体的R110(RSU)和R343(RSU)分别与CSU的d204(Q环)形成盐桥,该盐桥对AtAHAS复合体的稳定性是必不可少的。近几年,研究人员更多集中于对AHAS的CSU与RSU之间互作模式的分析探索。同时揭示AHAS的CSU和RSU晶体结构以及全酶复合体结构,为探索该酶的催化机理、在BCAA合成途径中的作用以及调控机制奠定了基础,同时也为该酶的分子改造策略开辟了思路。
2 AHAS催化机制与其在支链氨基酸合成途径的作用
2.1 AHAS催化机制
ThDP作为AHAS催化机制中必不可少的物质,是可以辅助催化糖代谢中碳碳键形成和断键反应的辅助因子。它由1 个4’氨基嘧啶环(4’-aminopyrimidine,AP)和1 个由亚甲基桥接的噻唑环组成[27-28]。两个芳香环都参与催化,其中噻唑环作为亲电共价催化剂,AP作为酸碱催化剂[29]。AHAS由1 个高度保守的谷氨酸残基激活,该残基使AP互变异构体的嘧啶环中1’-氮原子质子化,从而形成APH+。由于互变异构形式的1’,4’-亚氨基嘧啶(1’,4’-iminopyrimidine,IP)中ThDP的反应性结构(V构象),高度碱性的4’-亚氨基基团非常靠近第2位碳原子(催化中心)并产生叶立德中间体(图4)。
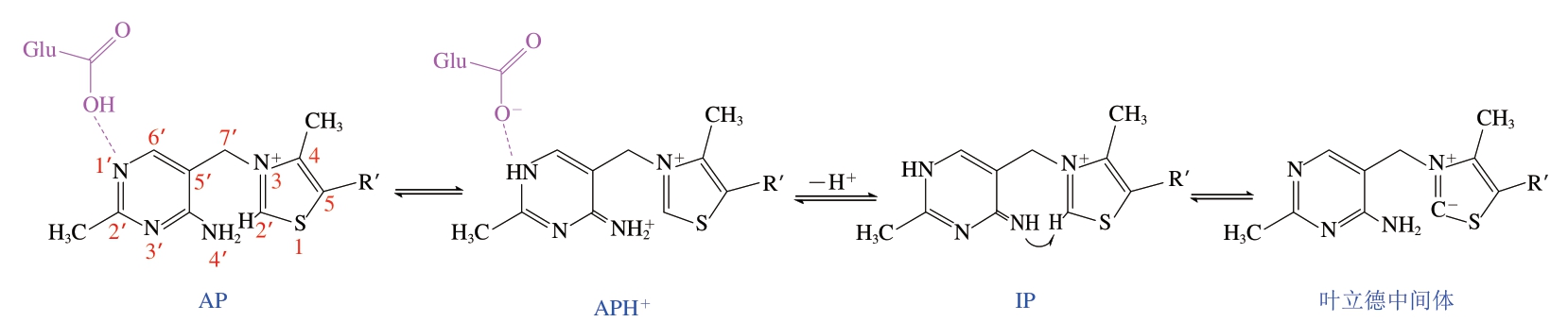
图4 ThDP的激活路径
Fig. 4 Activation pathway of thiamine diphosphate
Jana等[28]发现叶立德中间体具有亲核性质,亲核叶立德辅助C2原子对丙酮酸分子的Cα原子进行亲核攻击,从而形成乳酰-ThDP中间体(lactyl-ThDP,L-ThDP)。L-ThDP脱羧形成羟乙基-ThDP阴离子/烯胺中间体(hydroxyethyl-ThDP,HEThDP)。随后,2-酮酸底物(丙酮酸和2-KB)与该中间体反应形成复合物乙酰乳酸(acetolactate,AL)-ThDP。最后产物被释放,再次形成ThDP(图5)。
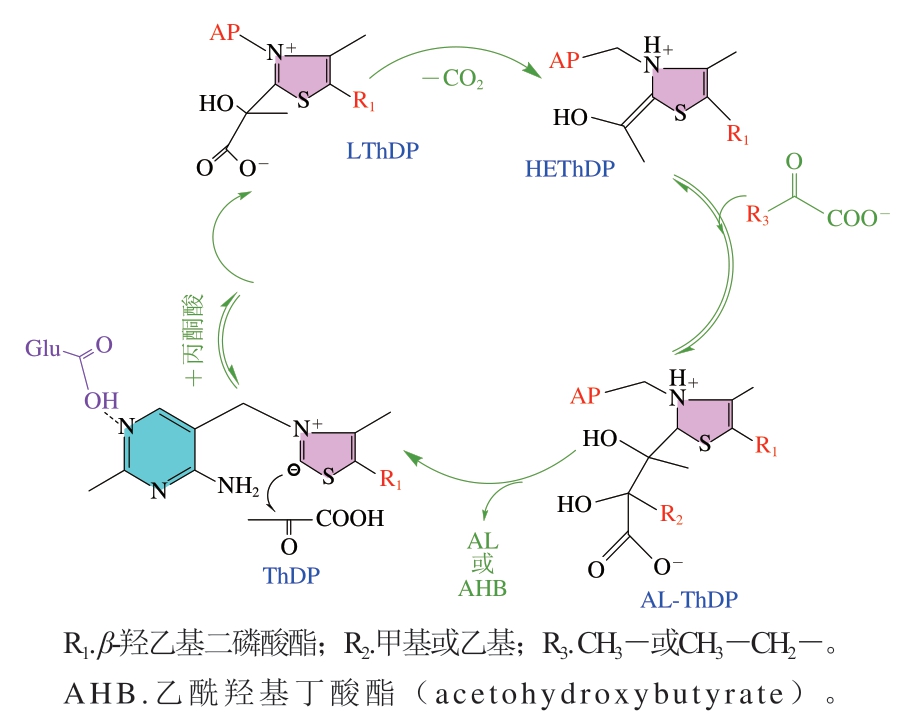
图5 AHAS的催化循环
Fig. 5 Catalytic cycle of AHAS
2.2 分子动力学/量子力学揭示AHAS催化机制
AHAS的催化反应机理以及反应过程中相关残基作用机制一直备受研究人员关注。对AHAS催化机制进行详细研究对于开发不同方法以及寻找新的残基位点从而改造AHAS使其在改善生物体内代谢网络中发挥重要作用是必不可少的。近几年,研究人员利用分子动力学模拟以及量子力学辅助实验以揭开详细的催化机制。
Lizana等[30]通过量子力学/分子动力学计算并探索了两种形式的叶立德的势能面,并探讨了L-ThDP生成的反应机理。他们观察到反应是通过碳化反应和质子转移同步进行的,两种形式的势能面都是在反应过程中完成从N1’原子去质子化到N1’原子质子化的转化,这一转化为最低能量的反应路径,活化能约为80 kJ/mol。丙酮酸和叶立德中间体之间的距离在反应机理中起到重要作用,因为它引发了碳化反应和质子转移。在前期研究中发现ThDP的N1’原子和Glu残基的相互作用对于AHAS的催化活性至关重要[31-32]。Baig等[33]利用分子动力学模拟发现,结核分枝杆菌AHAS的Gln86残基在催化Glu85侧链与维持ThDP的N1’原子所需的构象中发挥关键性作用,Ala、Asp和Gln这3 个残基取代保守的Glu85残基导致催化活性严重下降并进一步对ThDP的亲和力降低。因此Glu残基在AHAS的催化作用中起到了决定性作用。
催化循环的前3 个步骤在AHAS以及其他ThDP依赖酶中是常见的,而最后两个步骤仅存在于AHAS中。在最后两个步骤中需要至少1 个酸碱可电离基团,其参与丙酮酸或2-KB羰基的质子化和在释放产物时所需的羟基质子提取[34]。Jana等[35]通过分子动力学模拟发现催化循环的最后两步不需要额外的酸碱可电离基团来促进催化循环,并证实了HEThDP-中间体发挥可电离基团的作用,促进催化循环的碳化和产物形成。Mendoza等[36]利用量子力学/分子动力学研究了最后两个催化步骤,证实了碳化是通过分子内质子转移进行的,不需要额外的酸碱可电离基团,并且发现AHAS的Gln202残基通过静电作用稳定反应部位的催化性水分子,催化性水分子与反应物形成分子间氢键对碳化过程中的中间体AL-ThDP的形成作用巨大。
通过研究人员对AHAS的催化机理以及碳化反应中各中间步骤的逐渐探索,并结合理论模拟与实验分析,对理解该酶在BCAA合成途径的作用具有重要意义。
2.3 AHAS在支链氨基酸生产中的作用
AHAS催化丙酮酸的脱羧以及双碳中间体HEThDP-与2-KB的特异性缩合,形成AL或AHB[37]。它们是生物合成途径中通向合成BCAA的中间产物。如图6所示,AHAS在L-缬氨酸和L-亮氨酸的形成途径中催化两分子丙酮酸缩合形成AL,在L-异亮氨酸形成途径中催化丙酮酸和2-KB缩合形成AHB[12]。因为2-酮丁酸盐和丙酮酸盐之间的竞争决定了L-异亮氨酸和L-缬氨酸、L-亮氨酸形成的相对速率。大多数AHAS对酮丁酸盐比对丙酮酸盐更有亲和力[38],因此该酶在确定不同最终产物的相对通量方面发挥关键性作用。据报道,大肠杆菌AHAS I的两个氨基酸残基Gln480和Met476分别取代了其他AHAS中保守的Trp和Leu残基[39]。这种差异导致产物AHB的释放速度比AL快得多,并且该酶对2-KB没有底物特异性。Ibdah等[40]在大肠杆菌的AHAS II活性位点中鉴定出残基,这些残基会影响反应中产物关键步骤的速率,并且Trp464的突变会导致对2-KB偏好性的丧失。Tittmann等[41]在大肠杆菌AHAS II中观察到AHB比AL的形成更稳定,释放速率高出两倍以上,并提出该酶对2-KB的偏好性可能归因于这一性质。Sánchez等[42]结合量子力学、分子动力学分析发现,中间体HEThDP-与2-KB的反应分为两个步骤。第一步反应中,碳负离子对2-KB进行亲核攻击,HEThDP-的羟基向2-KB的羰基氧转移质子,并且碳化反应优先于质子转移;在第二步中叶立德中间体的再生伴随着产物的释放,进而再一次启动催化循环。Engel等[43]发现大肠杆菌的AHAS II中的Arg残基在2-KB特异性反应起到关键性作用,并发现该残基的诱变体Arg276在反应的第二阶段成为速率决定性因素。随着研究人员对AHAS在产物形成中作用研究的深入,发现该酶在不同的BCAA合成途径中是有差异的。这种对丙酮酸与2-KB结合的差异性为日后对该酶的分子改造提供了研究基础。未来,鉴定更多不同物种的AHAS中对产物连接速率起作用的残基并加以改造可能会对BCAA的产量有所影响。
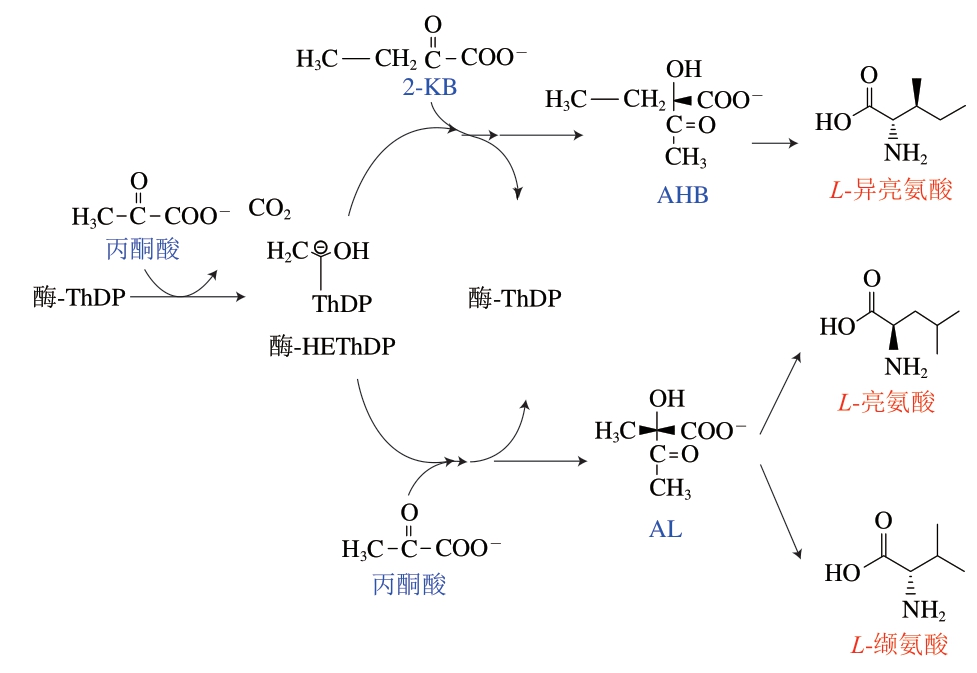
图6 AHAS催化的两种竞争性反应
Fig. 6 Two competing reactions catalyzed by AHAS
3 AHAS在氨基酸生产途径中的分子改造策略
在许多模式生物中,BCAA(L-缬氨酸、L-亮氨酸、L-异亮氨酸)的生产途径复杂,并且代谢网络中每一步酶的调节机制都极其精密,而AHAS作为第一步限速酶,更容易受到BCAA的反馈抑制[44]。不同BCAA对该酶的半抑制浓度(half-maximal inhibitory concentration,IC50):L-缬氨酸为0.9 mmol/L,L-异亮氨酸为3.1 mmol/L,L-亮氨酸为6.0 mmol/L[45]。目前,研究人员主要集中于研究通过弱化或消除AHAS的反馈抑制以及转录衰减[46]或者通过对该酶两种亚基的编码基因(ilvBN)采用过表达策略以提高酶活力,并与其他基因工程技术如基因敲除、提高辅因子供应等结合以提高BCAA的产量(表1)。
表1 AHAS分子改造策略
Table 1 Molecular modification strategies for AHAS
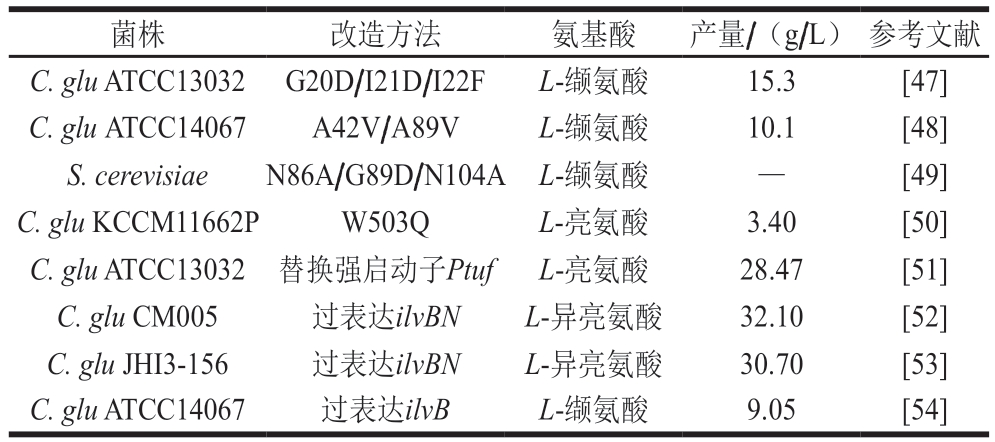
注:—.文献未报道。
菌株改造方法氨基酸 产量/(g/L)参考文献C. glu ATCC13032G20D/I21D/I22FL-缬氨酸15.3[47]C. glu ATCC14067A42V/A89VL-缬氨酸10.1[48]S. cerevisiaeN86A/G89D/N104A L-缬氨酸—[49]C. glu KCCM11662PW503Q L-亮氨酸3.40[50]C. glu ATCC13032替换强启动子PtufL-亮氨酸28.47[51]C. glu CM005过表达ilvBNL-异亮氨酸 32.10[52]C. glu JHI3-156过表达ilvBNL-异亮氨酸30.70[53]C. glu ATCC14067过表达ilvBL-缬氨酸9.05[54]
3.1 定点突变解除反馈抑制以及截短改造策略
微生物体内的BCAA代谢途径错综复杂,产物积累过量会影响酶活性以及细胞内代谢。研究人员集中利用定点突变对AHAS进行改造以解除反馈抑制。通过诱变AHAS结构中与BCAA结合的位点或者鉴定保守残基加以改造从而抵抗BCAA的抑制。Elsakova等[47]对谷氨酸棒杆菌中AHAS的RSU编码基因ilvN的20、21、22氨基酸位点进行突变,筛选出M13突变体,在10 mmol/L缬氨酸存在下,突变酶的特异性活性对比野生型提高76%。Guo Yanfeng等[48]选择AHAS的RSU中保守的A42、A89和K136残基进行定点诱变,并进一步进行双突变,最后A42V-A89V突变体几乎能完全抵抗3 种BCAA的抑制作用,即使在BCAA浓度为10 mmol/L时也能保持93%的活性。Lu Jingnan等[55]发现谷氨酸棒杆菌AHAS的RSU几种突变体(N11S、T34I、A36V、T104S、N11F、G14E、N29H)与野生型ilvB重组时可以降低BCAA的敏感性。Takpho等[49]则在ScAHAS中预测RSU的Asn86、Gly89和Asn104位于L-缬氨酸结合位点的附近,并成功构建Asn86Ala、Gly89Asp和Asn104Ala突变体,使细胞内L-缬氨酸产量比野生型高出约4 倍。
目前,大多数改造策略都是针对该酶的RSU。有报道指出对CSU的改造也可以解除BCAA的反馈抑制。Jeon等[50]对CSU进行改造,发现W503Q突变体可将L-亮氨酸产量提高到3.40 g/L,是野生型的1.1 倍。未来可以寻找更多CSU的可改造位点,或者与RSU协同突变提高酶催化活性与抗反馈抑制能力以增加BCAA的产量。不同于定点突变改造酶可以解除反馈抑制,在之前的报道中,研究人员观察到肉桂链霉菌AHAS的RSU会自发截短,该截短位置与AHAS III的RSU的108位氨基酸残基处于同源的位置,并且导致该酶对L-缬氨酸的敏感性丧失[56]。因此,在AHAS结构上采取截短策略同样可以降低BCAA对该酶的抑制。Mendel等[57]对大肠杆菌中AHAS同工酶AHAS III RSU的C端采用截短策略从而减弱了L-缬氨酸对该酶的反馈抑制。Wada等[58]在谷氨酸棒杆菌中采用C端截短策略,使L-缬氨酸的产量从野生型菌株的38.3 mmol/L增加到95.7 mmol/L。
3.2 调控基因表达策略
最近的研究表明,BCAA介导的反馈抑制会导致CSU和RSU的编码基因表达量显著下调[59],这也从基因表达水平上补充了反馈抑制机制。调控基因表达水平策略可以利用强启动子更换靶基因的天然启动子或者过表达目标酶的编码基因从而达到提高酶活力、改善代谢碳流并使BCAA高产的目的[60]。启动子是细胞转录调控的重要元件,利用启动子工程精确调控基因转录已成为非常重要的代谢工程策略[61]。Wang Yingyu等[51]利用强启动子Ptuf替代ilvBNC天然启动子,同时通过删除pyc和avtA基因并下调alaT基因的表达量,使L-亮氨酸产量高达(28.47±0.36)g/L。通过过表达AHAS的编码基因增强代谢途径碳流是目前最常用的分子改造策略。Liu Yadi等[62]对两株不同工程菌(谷氨酸棒杆菌IWJ001和谷氨酸棒杆菌VWB-1)中的基因ilvB和ilvN进行了测序。发现两种菌株中ilvN的序列相同,但ilvB的序列在413、1 211处碱基对不同,分别导致AHAS的CSU中第138、404位的氨基酸突变,ilvB的第138、404位残基在IWJ001中分别是丙氨酸和缬氨酸,但在VWB-1中分别是缬氨酸和丙氨酸。通过组合不同突变体并在谷氨酸棒杆菌中过表达,当过表达第138个残基为缬氨酸的CSU突变体时,L-缬氨酸产量高达25.93 g/L。张炎潮[52]通过在谷氨酸棒杆菌WM001中过表达已解除反馈抑制AHAS的ilvBN基因,并通过提高辅因子的供应从而强化L-异亮氨酸的碳途径,最后达到高产L-异亮氨酸的目的。Yin Lianghong等[53]在谷氨酸棒杆菌JHI3-156中过表达ilvBN与ilvA基因,使L-异亮氨酸产量达到30.7 g/L。
Niu Congwei等[63]观察到AHAS的CSU与RSU在异源活化中存在很强的异源关联,并且来自其他AHAS同工酶的RSU可以激活大肠杆菌 AHAS 的CSU。Zhao Yuefang等[64]构建了大肠杆菌AHAS III的RSU的截短突变体DN14-DC89,不仅可以激活大肠杆菌AHAS I和AHAS III的CSU,还可以激活来自酿酒酵母、拟南芥和梅花球菌的CSU。未来,可以通过改造大肠杆菌同工酶AHAS III的CSU并异源表达激活其他物种的AHAS达到高产BCAA的目的。目前CRISPR基因编辑技术已广泛应用于谷氨酸棒杆菌、大肠杆菌等模式生物中[65-68]。CRISPR系统作为一种RNA引导的内切核酸酶系统,在基因敲除、基因沉默和基因激活等方面逐渐成为最高效的手段[69]。近几年,CRISPR/Cas9基因编辑技术已成功应用于AHAS[70-72]。Wei Tao等[70]利用CRISPR碱基编辑系统对拟南芥的AHAS进行精确碱基编辑赋予拟南芥抗除草剂性。Wu Jian等[71]同样利用CRISPR技术对油菜AHAS的P197碱基进行编辑从而赋予其抗药性。Ran Yidong等[72]通过该技术成功地将S653N突变引入小麦的AHAS中,赋予其对咪唑啉酮类除草剂的抗性。虽然CRISPR基因编辑技术可以应用并高效改造AHAS,但目前主要集中于抗药、抗除草剂方面的应用,未来,可利用该技术改造AHAS以赋予该酶抗反馈抑制的特性,从而达到高产BCAA的目的是一个重要的研究方向。
4 结 语
AHAS作为BCAA合成途径中第一步共享酶,其重要性毋庸置疑。目前,该酶一直处于探索分析阶段。随着近几年几种不同微生物体AHAS全酶结构的揭示,使得对该酶的CSU、RSU互作模式有了更完善的认知体系,但是仍有许多问题未得到解决。
在结构方面,迄今为止仍有大部分物种AHAS的全酶结构以及两个亚基之间相互联系的结构机制还未得到解析,有研究表明植物体内存在多肽链与CSU相互作用调节其活性,但是目前在其他物种中还未发现可以与CSU相互作用的物质。在催化机制方面,AHAS对两种底物(丙酮酸、2-KB)的结合模式还需要鉴定更多的氨基酸残基来确定控制产物生成速率的性质,并且目前AHAS结合2-KB或丙酮酸的详细机制尚不清楚。现阶段,结合模拟分子对接以及分子动力学等方法对AHAS的催化循环中间反应物的研究仍然是有效的手段。目前手段并不能完全解除BCAA对该酶的反馈抑制,而且对该酶的改造策略主要集中在定点饱和突变以及C端截短策略,调控基因表达策略的研究较少。未来,可以利用启动子工程鉴定筛选更多的强启动子控制基因表达水平,从而提高酶的活性,改善生物体的代谢网络。也可以利用计算机辅助进行酶工程改造或者从该酶编码基因的转录水平以及翻译层面进行优化,如利用CRISPR基因编辑技术可以快速、高效地改造AHAS,精准靶向编码AHAS的CSU或RSU基因进行碱基编辑,基因编辑技术还可以在基因转录过程中引入激活基团从而提高酶的活性或者利用密码子优化技术,通过在该酶翻译过程中人工加入稀有密码子,引入非天然氨基酸,从而赋予该酶全新的表型,以此改善该酶的稳定性、特异性,并进一步降低其受到底物的反馈抑制。
[1]ZHANG S H, ZENG X F, REN M, et al. Novel metabolic and physiological functions of branched chain amino acids: a review[J].Journal of Animal Science and Biotechnology, 2017, 8(1): 10.DOI:10.1186/s40104-016-0139-z.
[2]简华锋, 章旭春, 董信阳, 等. 支链氨基酸在畜禽低蛋白质饲粮体系中的应用[J]. 动物营养学报, 2021, 33(8): 4285-4293. DOI:10.3969/j.issn.1006-267x.2021.08.009.
[3]谢小青, 刘亚贤, 陈顺, 等. 支链氨基酸在非酒精性脂肪性肝病发生发展中的作用[J]. 临床肝胆病杂志, 2022, 38(2): 439-442.DOI:10.3969/j.issn.1001-5256.2022.02.037.
[4]PLOTKIN D L, DELCASTILLO K, VANEVER D W, et al. Isolated leucine and branched-chain amino acid supplementation for enhancing muscular strength and hypertrophy: a narrative review[J]. International Journal of Sport Nutrition and Exercise Metabolism, 2021, 31(3): 292-301. DOI:10.1123/ijsnem.2020-0356.
[5]SUZUKI M, SATO T, SHIRAI H, et al. Powerful low-molecularweight gelators based on L-valine and L-isoleucine with various terminal groups[J]. New Journal of Chemistry, 2006, 30(8): 1184-1191. DOI:10.1039/b604847a.
[6]ROLF W, WICHMANN R, CHRISTIAN W, et al. Continuous enzymatic transformation in an enzyme membrane reactor with simultaneous NAD(H) regeneration[J]. Biotechnology and Bioengineering, 2004,23(12): 2789-2802. DOI:10.1002/bit.260231213.
[7]WANG X Y. Strategy for improving L-isoleucine production efficiency in Corynebacterium glutamicum[J]. Applied Microbiology and Biotechnology,2019, 103(5): 2101-2111. DOI:10.1007/s00253-019-09632-2.
[8]陈志超, 刘云鹏, 徐庆阳, 等. 支链氨基酸生物合成及其生产菌的研究进展[J]. 发酵科技通讯, 2020, 49(3): 161-170. DOI:10.16774/j.cnki.issn.1674-2214.2020.03.007.
[9]孔帅, 方应浩, 周航, 等. 微生物发酵法生产L-异亮氨酸的研究进展[J]. 中国酿造, 2020, 39(9): 30-36. DOI:10.11882/j.issn.0254-5071.2020.09.006.
[10]MONTANO L, DURAN L, AVALOS J. Physiological limitations and opportunities in microbial metabolic engineering[J]. Nature Reviews Microbiology, 2022, 20(1): 35-48. DOI:10.1038/s41579-021-00600-0.
[11]DUGGLEBY R G. Domain relationships in thiamine diphosphatedependent enzymes[J]. Accounts of Chemical Research, 2006, 39(8):550-557. DOI:10.1021/ar068022z.
[12]LIU Y D, LI Y N, WANG X Y. Acetohydroxyacid synthases: evolution,structure, and function[J]. Applied Microbiology and Biotechnology,2016, 100(20): 8633-8649. DOI:10.1007/s00253-016-7809-9.
[13]CHIPMAN D, BARAK Z, SCHLOSS J V. Biosynthesis of 2-aceto-2-hydroxy acids: acetolactate synthases and acetohydroxyacid synthases[J]. Biochimica et Biophysica Acta (BBA)-Protein Structure and Molecular Enzymology, 1998, 1385(2): 401-419. DOI:10.1016/s0167-4838(98)00083-1.
[14]PUE N, GUDDAT L W. Acetohydroxyacid synthase: a target for antimicrobial drug discovery[J]. Journal of Molecular Biology, 2014,20(5): 740-753. DOI:10.2174/13816128113199990009.
[15]ERAM M S, MA K. Pyruvate decarboxylase activity of the acetohydroxyacid synthase of Thermotoga maritima[J]. Biochemistry and Biophysics Reports, 2016, 7: 394-399. DOI:10.1016/j.bbrep.2016.07.008.
[16]LIU Y D, LI Y Y, WANG X Y. Molecular evolution of acetohydroxyacid synthase in bacteria[J]. MicrobiologyOpen, 2017,6(6): 524. DOI:10.1002/mbo3.524.
[17]BARAK Z, CHIPMAN D M. Allosteric regulation in acetohydroxyacid synthases (AHAS): different structures and kinetic behavior in isozymes in the same organisms[J]. Archives of Biochemistry and Biophysics, 2012, 519(2): 167-174. DOI:10.1016/j.abb.2011.11.025.
[18]CHEN H, SAKSA K, ZHAO F, et al. Genetic analysis of pathway regulation for enhancing branched-chain amino acid biosynthesis in plants[J]. The Plant Journal, 2010, 63(4): 573-583. DOI:10.1111/j.1365-313X.2010.04261.x.
[19]ZHANG Y Y, LI Y, LIU X, et al. Molecular architecture of the acetohydroxyacid synthase holoenzyme[J]. Biochemical Journal, 2020,477(13): 2439-2449. DOI:10.1042/BCJ20200292.
[20]LONHIENNE T, LOW Y S, GARCIA M D, et al. Structures of fungal and plant acetohydroxyacid synthases[J]. Nature, 2020, 586: 317-321.DOI:10.1038/s41586-020-2514-3.
[21]KAPLUN A, VYAZMENSKY M, ZHERDEV Y, et al. Structure of the regulatory subunit of acetohydroxyacid synthase isozyme III from Escherichia coli[J]. Journal of Molecular Biology, 2006, 357(3): 951-963. DOI:10.1016/j.jmb.2005.12.077.
[22]WEK R C. The nucleotide sequence of the ilvBN operon of Escherichia coli[J]. Nucleic Acids Research, 1985, 13(11): 3995-4010.DOI:10.1093/nar/13.11.3995.
[23]VYAZMENSKY M, ZHERDEV Y, SLUTZKER A, et al. Interactions between large and small subunits of different acetohydroxyacid synthase isozymes of Escherichia coli[J]. Biochemistry, 2009, 48(36):8731-8737. DOI:10.1021/bi9009488.
[24]BELENKY I, STEINMETZ A, VYAZMENSKY M, et al. Many of the functional differences between acetohydroxyacid synthase (AHAS)isozyme I and other AHASS are a result of the rapid formation and breakdown of the covalent acetolactate-thiamin diphosphate adduct in AHAS I[J]. The FEBS Journal, 2012, 279(11): 1967-1979.DOI:10.1111/j.1742-4658.2012.08577.x.
[25]XU Huiniu, LIU Xiang, ZHOU Yanfei, et al. Preliminary X-ray crystallographic studies of the catalytic subunit of Escherichia coli AHAS II with its cofactors[J]. Structural Biology Communications,2011, 67(6): 659-661. DOI:10.1107/s1744309111008839.
[26]HILL M, PANG S, DUGGLEBY G R. Purification of Escherichia coli acetohydroxyacid synthase isoenzyme II and reconstitution of active enzyme from its individual pure subunits[J]. Biochemical Journal,1997, 327(3): 891-898. DOI:10.1042/bj3270891.
[27]KLUGER R, TITTMANN K. Diphosphate catalysis: enzymic and nonenzymic covalent intermediates[J]. Chemical Reviews, 2008,108(6): 1797-1833. DOI:10.1021/cr068444m.
[28]JANA G A, DELGADO E J. Electron density reactivity indexes of the tautomeric/ionization forms of thiamin diphosphate[J]. Journal of Molecular Modeling, 2013, 19(9): 3799-3803. DOI:10.1007/s00894-013-1908-7.
[29]BALAKRISHNAN A, PARAMASIVAM S, CHAKRABORTY S, et al.Solid-state nuclear magnetic resonance studies delineate the role of the protein in activation of both aromatic rings of thiamin[J]. Journal of the American Chemical Society, 2012, 134(1): 665-672. DOI:10.1021/ja209856x.
[30]LIZANA I, JANA G A, DELGADO E J. New insights on the reaction pathway leading to lactyl-ThDP: a theoretical approach[J]. Journal of Molecular Modeling, 2015, 55(8): 1640-1644. DOI:10.1021/acs.jcim.5b00197.
[31]VYAZMENSKY M, STEINMETZ A, MEYER D, et al. Significant catalytic roles for Glu47 and Gln110 in all four of the C-C bondmaking and -breaking steps of the reactions of acetohydroxyacid synthase II[J]. Biochemistry, 2011, 50(15): 3250-3260. DOI:10.1021/bi102051h.
[32]WIKNER C, MESHALKINA L, NILSSON U, et al. Analysis of an invariant cofactor-protein interaction in thiamin diphosphatedependent enzymes by site-directed mutagenesis. Glutamic acid 418 in transketolase is essential for catalysis[J]. Journal of Biological Chemistry, 1994, 269(51): 32144-32150. DOI:10.1093/nar/22.25.5773.
[33]BAIG I A, MOON J Y, KIM M S, et al. Structural and functional significance of the highly-conserved residues in Mycobacterium tuberculosis acetohydroxyacid synthase[J]. Enzyme and Microbial Technology, 2014, 58/59: 52-59. DOI:10.1016/j.enzmictec.2014.02.009.
[34]MCCOURT J A, DUGGLEBY R G. Acetohydroxyacid synthase and its role in the biosynthetic pathway for branched-chain amino acids[J].Amino Acids, 2006, 31(2): 173-210. DOI:10.1007/s00726-005-0297-3.
[35]JANA G, JIMENEZ V, VILLA F J, et al. Computational study on the carboligation reaction of acetohidroxyacid synthase: new approach on the role of the HETHDP- intermediate[J]. Proteins-Structure Function and Bioinformatics, 2010, 78(7): 1774-1788. DOI:10.1002/prot.22693.
[36]MENDOZA F, MEDINA F E, JIMENEZ V A, et al. The catalytic role of Gln202 in the carboligation reaction mechanism of yeast AHAS: a QM/MM study[J]. Journal of Chemical Information, 2019, 60(2): 915-922. DOI:10.1021/acs.jcim.9b00863.
[37]CHIPMAN D M, DUGGLEBY R G, TITTMANN K. Mechanisms of acetohydroxyacid synthases[J]. Current Opinion in Chemical Biology,2006, 10(1): 88. DOI:10.1016/j.cbpa.2006.01.016.
[38]GOLLOP N, DAMRI B, CHIPMAN D M, et al. Physiological implications of the substrate specificities of acetohydroxy acid synthases from varied organisms[J]. Journal of Bacteriology, 1990,172(6): 3444-3449. DOI:10.1128/jb.172.6.3444-3449.1990.
[39]GEDI V, YOON M Y. Bacterial acetohydroxyacid synthase and its inhibitors: a summary of their structure, biological activity and current status[J]. The FEBS Journal, 2012, 279(6): 946-963. DOI:10.1111/j.1742-4658.2012.08505.x.
[40]IBDAH M, BARILAN A, LIVNAH O, et al. Homology modeling of the structure of bacterial acetohydroxy acid synthase and examination of the active site by site-directed mutagenesis[J]. Biochemistry, 1996,35(50): 16282-16291. DOI:10.1021/bi961588i.
[41]TITTMANN K, VYAZMENSKY M, HUBNER G, et al. The carboligation reaction of acetohydroxyacid synthase II: steadystate intermediate distributions in wild type and mutants by NMR[J]. Proceedings of The National Academy of Sciences of The United States of America, 2005, 102(3): 553-558. DOI:10.1073/pnas.0408210101.
[42]SÁNCHEZ L A, GONZALO W, DELGADO E J. A QM/MM study on the reaction pathway leading to 2-aceto-2-hydroxybutyrate in the catalytic cycle of AHAS[J]. Journal of Computational Chemistry,2014, 35(6): 488-494. DOI:10.1002/jcc.23523.
[43]ENGEL S, VYAZMENSKY M, VINOGRADOV M, et al. Role of a conserved arginine in the mechanism of acetohydroxyacid synthase:catalysis of condensation with a specific ketoacid substrate[J]. Journal of Biological Chemistry, 2004, 279(23): 24803-24812. DOI:10.1074/jbc.M401667200.
[44]MENDEL S, ELKAYAM T, SELLA C, et al. Acetohydroxyacid synthase: a proposed structure for regulatory subunits supported by evidence from mutagenesis[J]. Journal of Molecular Biology, 2001,307(1): 465-477. DOI:10.1006/jmbi.2000.4413.
[45]LEYVAL D, UY D, DELAUNAY S, et al. Characterisation of the enzyme activities involved in the valine biosynthetic pathway in a valine-producing strain of Corynebacterium glutamicum[J]. Journal of Biotechnology, 2003, 104(1): 241-252. DOI:10.1016/S0168-1656(3)00162-7.
[46]YU S, ZHENG B, CHEN Z, et al. Metabolic engineering of Corynebacterium glutamicum for producing branched chain amino acids[J]. Microbial Cell Factories, 2021, 20(1): 230. DOI:10.1186/s12934-021-01721-0.
[47]ELISAKOVA V, PATEK M, HOLATKO J, et al. Feedbackresistant acetohydroxy acid synthase increases valine production in Corynebacterium glutamicum[J]. Applied and Environmental Microbiology, 2005, 71(1): 207-213. DOI:10.1128/AEM.71.1.207-213.2005.
[48]GUO Yanfeng, HAN Mei, YAN Weiliu, et al. Generation of branchedchain amino acids resistant Corynebacterium glutamicum acetohydroxy acid synthase by site-directed mutagenesis[J]. Biotechnology and Bioprocess Engineering, 2014, 19(3): 456-467. DOI:10.1007/s12257-013-0843-x.
[49]TAKPHO N, WATANABE D, TAKAGI H. High-level production of valine by expression of the feedback inhibition-insensitive acetohydroxyacid synthase in Saccharomyces cerevisiae[J]. Metabolic Engineering, 2018, 46: 60-67. DOI:10.1016/j.ymben.2018.02.011.
[50]JEON A J, SONG B C, JI H L, et al. Acetohydroxy acid synthase variant, microorganism comprising the same, and method of producing L-branched-chain amino acid using the same: EP18832634[P]. (2019-05-04)[2022-05-16]. https://patentscope2.wipo.int/search/en/detail.jsf?docId=KR241270554.
[51]WANG Yingyu, SHI Ke, CHEN Peidong, et al. Rational modification of the carbon metabolism of Corynebacterium glutamicum to enhance L-leucine production[J]. Journal of Industrial Microbiology and Biotechnology, 2020, 47(6/7): 485-495. DOI:10.1007/s10295-020-02282-8.
[52]张炎潮. 代谢工程改造谷氨酸棒状杆菌生产L-异亮氨酸[D]. 无锡:江南大学, 2020: 20-30.
[53]YIN Lianghong, HU Xiaoqing, XU Daqing, et al. Co-expression of feedback-resistant threonine dehydratase and acetohydroxy acid synthase increase L-isoleucine production in Corynebacterium glutamicum[J]. Metabolic Engineering, 2012, 14(5): 542-550.DOI:10.1016/j.ymben.2012.06.002.
[54]GUO Y, HAN M, XU J, et al. Analysis of acetohydroxyacid synthase variants from branched-chain amino acids-producing strains and their effects on the synthesis of branched-chain amino acids in Corynebacterium glutamicum[J]. Protein Expression and Purification,2015, 109(2): 106-112. DOI:10.1016/j.pep.2015.02.006.
[55]LU Jingnan, CHRISTOPHER J, PLASSMEIER J K, et al.Characterization and modification of enzymes in the 2-ketoisovalerate biosynthesis pathway of Ralstonia eutropha H16[J]. Applied Microbiology and Biotechnology, 2015, 99(2): 761-774. DOI:10.1007/s00253-014-5965-3.
[56]KOPECKY J, JANATA J, POSPISIL S, et al. Mutations in two distinct regions of acetolactate synthase regulatory subunit from Streptomyces cinnamonensis result in the lack of sensitivity to end-product inhibition[J]. Biochemical and Biophysical Research Communications,1999, 266(1): 162-166. DOI:10.1006/bbrc.1999.1792.
[57]MENDEL S, VINOGRADOV M, VYAZMENSKY M, et al. The N-terminal domain of the regulatory subunit is sufficient for complete activation of acetohydroxyacid synthase III from Escherichia coli[J].Journal of Molecular Biology, 2003, 325(2): 275-284. DOI:10.1016/S0022-2836(2)01142-7.
[58]WADA M, HIJIKATA N, AOKI R, et al. Enhanced valine production in Corynebacterium glutamicum with defective H+-ATPase and C-terminal truncated acetohydroxyacid synthase[J]. Bioscience, Biotechnology, and Biochemistry, 2008, 72(11): 2959-2965. DOI:10.1271/bbb.80434.
[59]SHAO S, LI B, SUN Q, et al. Acetolactate synthases regulatory subunit and catalytic subunit genes Vdilvs are involved in BCAA biosynthesis, microscletotial and conidial formation and virulence in Verticillium dahliae[J]. Fungal Genetics and Biology, 2022, 159:103667. DOI:10.1016/j.fgb.2022.103667.
[60]王钰, 郑平, 孙际宾. 谷氨酸棒杆菌的代谢工程使能技术研究进展[J]. 生物工程学报, 2021, 37(5): 1603-1618. DOI:10.13345/j.cjb.200649.
[61]刘莫识, 刘娇, 孙冠男, 等. 谷氨酸棒杆菌人工合成启动子文库的构建及应用[J]. 生物工程学报, 2022, 38(2): 831-842. DOI:10.13345/j.cjb.210202.
[62]LIU Yadi, WANG Xiaoyuan, ZHAN Jie, et al. The 138th residue of acetohydroxyacid synthase in Corynebacterium glutamicum is important for the substrate binding specificity[J].Microbial Technology, 2019, 129(2): 109357. DOI:10.1016/j.enzmictec.2019.06.001.
[63]NIU Congwei, WEI Feng, ZHOU Yanfei, et al. Homologous and heterologous interactions between catalytic and regulatory subunits of Escherichia coli acetohydroxyacid synthase I and III[J]. Science China Chemistry, 2009, 52(9): 1362-1371. DOI:10.1007/s11426-009-0213-x.
[64]ZHAO Yuefang, NIU Congwei, WEN Xin, et al. The minimum activation peptide from ilvH can activate the catalytic subunit of AHAS from different species[J]. Chembiochem, 2013, 14(6): 746-752.DOI:10.1002/cbic.201200680.
[65]GAUTTAM R, SEIBOLD G M, MUELLER P, et al. A simple dualinducible CRISPR interference system for multiple gene targeting in Corynebacterium glutamicum[J]. Plasmid, 2019, 103(3): 25-35.DOI:10.1016/j.plasmid.2019.04.001.
[66]FONTANA J, DONG C, KIATTISEWEE C, et al. Effective CRISPRamediated control of gene expression in bacteria must overcome strict target site requirements[J]. Nature Communications, 2020, 11(1):1618. DOI:10.1038/s41467-020-15454-y.
[67]CHUNG M E, YEH I H, SUNG L Y, et al. Enhanced integration of large DNA into E. coli chromosome by CRISPR/Cas9[J].Biotechnology and Bioengineering, 2017, 114(1): 172-183.DOI:10.1002/bit.26056.
[68]HASHEMI A. CRISPR-CAS9/CRISPRi tools for cell factory construction in E. coli[J]. World Journal of Microbiology and Biotechnology, 2020, 36(7): 13. DOI:10.1007/s11274-020-02872-9.
[69]龙梦飞, 徐美娟, 张显, 等. 合成生物学与代谢工程在谷氨酸棒杆菌产氨基酸中的应用[J]. 中国科学: 生命科学, 2019, 49(5): 541-552.DOI:10.1360/N052018-00248.
[70]WEI Tao, WEN Xin, NIU Congwei, et al. Design of acetohydroxyacid synthase herbicide-resistant germplasm through MB-QSAR and CRISPR/CAS9-mediated base-editing approaches[J]. Journal of Agricultural and Food Chemistry, 2022, 70(9): 2817-2824.DOI:10.1021/acs.jafc.1c07180.
[71]WU Jian, CHEN Chen, XIAN Guiyu, et al. Engineering herbicideresistant oilseed rape by CRISPR/CAS9-mediated cytosine baseediting[J]. Plant Biotechnology Journal, 2020, 18(9): 1857-1859.DOI:10.1111/pbi.13368.
[72]RAN Yidong, PATRON N, KAY P, et al. Zinc finger nuclease-mediated precision genome editing of an endogenous gene in hexaploid bread wheat (Triticum aestivum) using a DNA repair template[J]. Plant Biotechnology Journal, 2018, 16(12): 2088-2101. DOI:10.1111/pbi.12941.