健康奶牛分娩后3 d内所分泌的乳汁称为牛初乳,3 d后所产乳汁称为成熟乳,初乳与成熟乳的组成成分和含量均存在较大差异,初乳色泽微黄、质地浓稠,乳味浓重并具有特殊的苦味和腥味。牛初乳富含免疫球蛋白(immunoglobulins,Igs)、乳铁蛋白、溶菌酶、乳过氧化物酶、低聚糖、抗菌肽和生长因子等多种活性成分[1],对犊牛的营养代谢、胃肠道生长发育、内分泌功能等均具有重要作用。人类食用牛初乳已有上千年历史,古印度人就将牛初乳制成糖果食用[2];在几百年前,北欧斯卡纳地区利用牛初乳制成初乳布丁或甜品,并一直延续至今;在抗生素出现以前,美国人将牛初乳作为抗病食物使用[3]。越来越多的动物和临床试验证明,牛初乳具有增强免疫力、缓解胃肠道不适、抑菌以及修复黏膜等多种生物学活性[4]。然而,牛初乳富含的Igs、乳铁蛋白等活性组分热稳定性相对较差,易受杀菌、干燥等生产加工的影响而发生热变性,导致牛初乳功能活性和品质下降[5]。因此,在加工过程中保持牛初乳活性成分的天然结构和功能至关重要。
本文重点对牛初乳的营养成分、功能特性和加工稳定性等进行综述,旨在为牛初乳的开发及产业应用提供科学依据。
1 牛初乳的独特营养特性
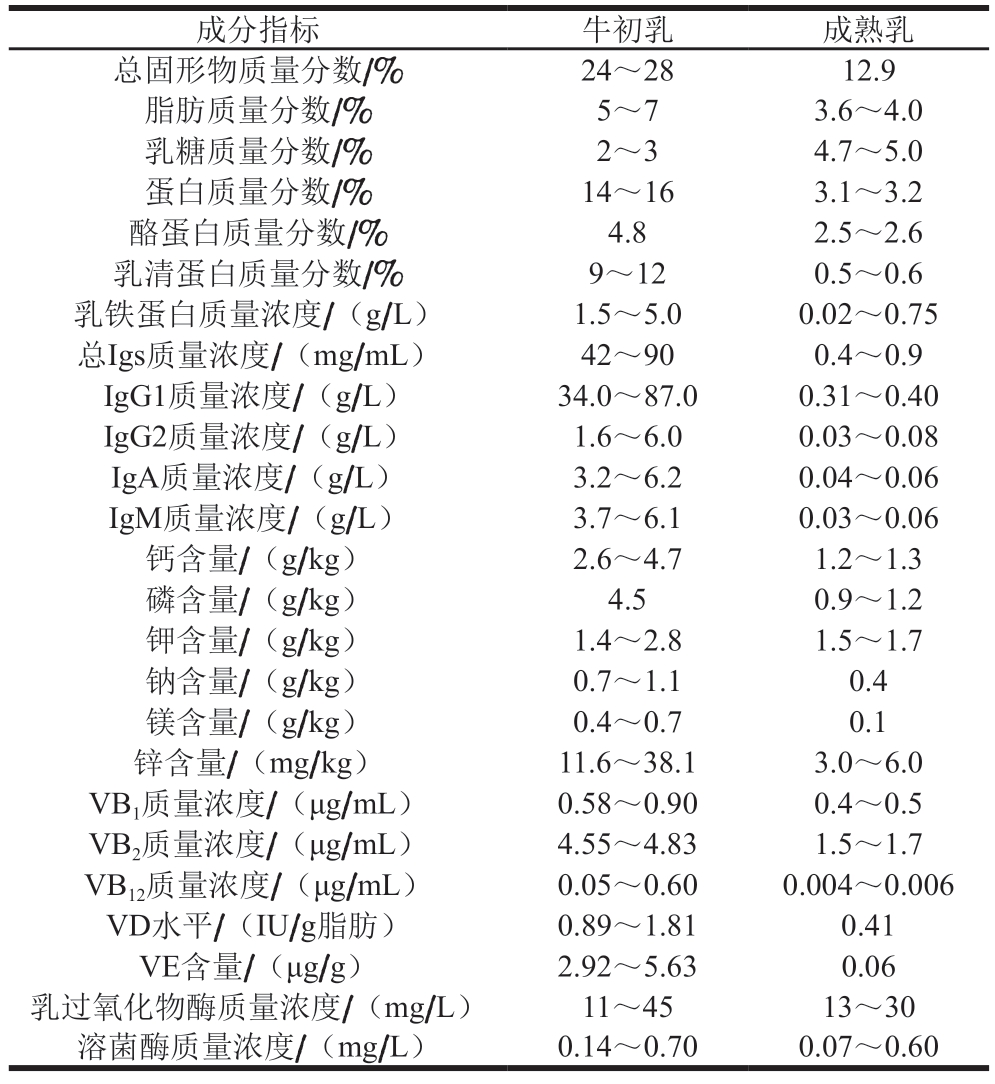
牛初乳的营养素种类和含量与成熟乳相比存在较大差异,其酪蛋白、乳清蛋白(Igs、乳铁蛋白等)、脂肪、维生素、矿物质、生长因子等含量较高,特别是IgG和乳铁蛋白含量远远高于成熟乳,分别约为成熟乳的75~280 倍和2~250 倍[6],而乳糖含量相对较低(表1)。除乳糖外,牛初乳中的其他营养素均在产犊后前3 d逐渐下降,特别是乳清蛋白含量下降最快,产犊3 d后的乳中乳清蛋白含量接近成熟乳[1](图1);此外,如图2所示,牛初乳中Igs、表皮生长因子(epidermal growth factor,EGF)和胰岛素样生长因子1(insulin-like growth factor,IGF1)等活性成分的含量也在产犊后3 d内逐渐下降[6-7]。牛初乳中大多数维生素含量通常高于成熟乳,尤其是VB2、VB12、VE和VD;牛初乳的必需矿物质如钙、磷、镁、锌含量也高于成熟乳。此外,牛初乳的其他活性成分如乳脂肪球膜也随着泌乳期的延长而发生改变。这些营养素组成和含量的不同使牛初乳较成熟乳具有更多的生物学功能。
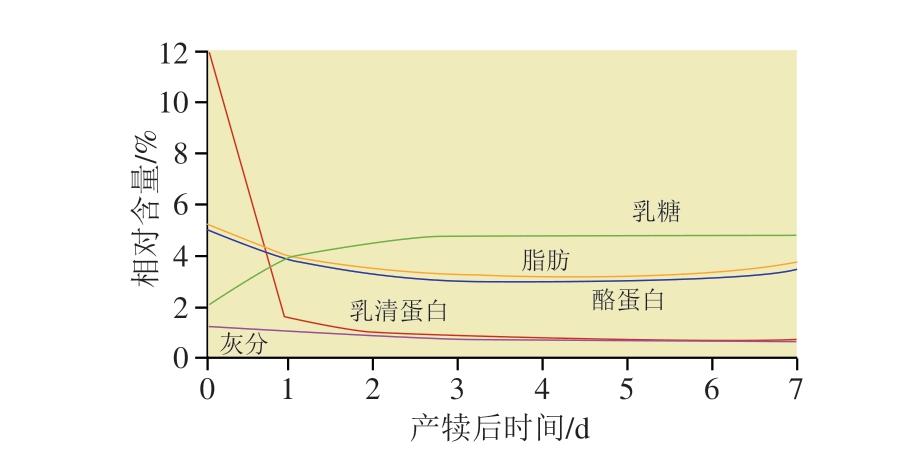
图1 乳成分含量随产犊后时间的变化[8]
Fig.1 Changes in the composition of bovine milk after parturition[8]
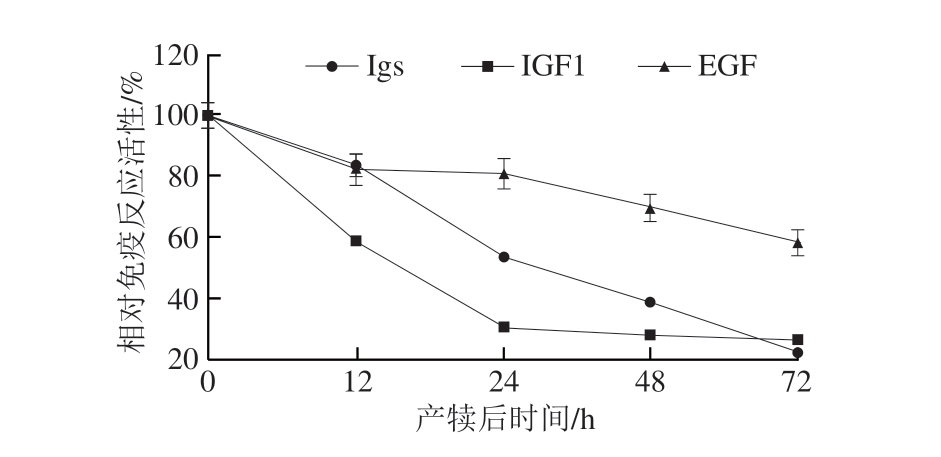
图2 乳中Igs和生长因子含量随产犊后时间的变化[7]
Fig.2 Changes in Igs and growth factor constituents of bovine milk with time after parturition[7]
表1 牛初乳营养组成及其与成熟乳对比[6]
Table 1 Comparison of various nutrients in colostrum and mature milk[6]
1.1 牛初乳富含Igs、乳铁蛋白等活性蛋白质
牛初乳的蛋白质含量显著高于成熟乳,初乳和成熟乳的蛋白质量分数分别约为15%和3%。在蛋白质组成方面,成熟乳的酪蛋白和乳清蛋白分别占总蛋白的80%和20%,而牛初乳的乳清蛋白占比相对较高,酪蛋白和乳清蛋白的比例为40∶60,此比例与人乳更相近[9],较高的乳清蛋白含量和比例赋予初乳更高的蛋白质消化利用率。
乳清蛋白含有多种功能性蛋白质,是婴幼儿配方乳粉和功能食品的重要原料。牛乳中Igs主要包括IgG、IgM、IgA和IgD,成熟乳的Igs质量浓度为0.4~0.9 mg/mL,而初乳中Igs质量浓度则高达42~90 mg/mL。其中,IgG1占初乳Igs的75%以上,其次是IgM、IgA和IgG2[1]。牛初乳中高含量的Igs能够阻止病原体与宿主细胞的结合、激活免疫T细胞和B细胞以及诱导IgA的产生,不仅能够为机体提供被动免疫,还能调节适应性和先天免疫系统[10]。此外,牛初乳Igs的免疫调节功能不局限于犊牛,对人类等其他哺乳动物的病原体同样具有清除作用[10]。
乳铁蛋白是一种铁结合糖蛋白,具有抗氧化、抗肿瘤、抑菌、提高免疫力以及调节肠道健康和骨骼健康等多种生物活性[11],这些活性多与乳铁蛋白的N-糖链有关。牛初乳的乳铁蛋白质量浓度约为1.5~5.0 mg/mL,其在成熟乳中含量显著下降,约为0.02~0.35 mg/mL[12];不同泌乳期牛乳中乳铁蛋白的N-糖组学研究结果表明,随着泌乳期延长,乳铁蛋白总N-糖链的种类和含量显著下降,唾液酸化N-糖链α-2,3-和α-2,6-连接异构体的种类也逐渐减少,关于乳铁蛋白糖基化差异所造成的生物学功能差异仍需进一步探究[13]。
骨桥蛋白(osteopontin,OPN)是一种高度磷酸化的酸性糖蛋白,含有RGD(精氨酸-甘氨酸-天冬氨酸)和CD44结合位点,具有调节机体免疫、促进神经发育以及改善肠道健康等多种功能。人乳中OPN含量较高,与人乳相比,牛成熟乳和婴幼儿配方乳粉中的OPN含量较低,分别约为19 mg/L和9 mg/L[14]。在婴幼儿配方乳粉中添加牛乳源OPN可以一定程度缩小其与母乳之间的差距。牛初乳中OPN含量更为丰富,约为200 mg/L,而在产后5 d,OPN含量则不足其初始浓度的10%[15],说明牛初乳是牛乳源OPN的优质来源。
综上所述,牛初乳乳清蛋白中含有更为丰富的活性蛋白,使其具有更多的生物学功能,是一种优质的功能性乳基料。除蛋白组成外,牛初乳和成熟乳的氨基酸组成也存在较大差异。牛初乳中含有更高含量的丝氨酸和精氨酸[16]。丝氨酸在多种生理进程中均发挥重要作用,如参与核苷酸、蛋白质、神经递质合成以及促进肌肉发育等,并且是细胞膜的重要组成成分[17];精氨酸则以蛋白质精氨酸甲基化的形式参与蛋白质-RNA、蛋白质-DNA和蛋白质-蛋白质之间的相互作用以及维持蛋白质稳定等[18]。富含丝氨酸和精氨酸的蛋白质之间有很强的相互作用,并且参与蛋白激酶的磷酸化和前信使RNA的可变剪接等生理进程[19]。此外,牛初乳中组氨酸和牛磺酸的含量显著高于成熟乳[14],组氨酸和牛磺酸不仅参与知觉和信号传输,并且能够促进婴幼儿神经系统发育,因此牛初乳中高含量的组氨酸和牛磺酸可以为婴幼儿的大脑和认知功能发育提供一定的营养支持[20-21]。苏氨酸能够促进T淋巴细胞增殖,增强婴幼儿的免疫功能,促进婴幼儿生长。牛初乳中苏氨酸含量约为成熟乳的6.9 倍,因此牛初乳中高含量的苏氨酸是其具有良好免疫调节功能的原因之一[16]。
1.2 牛初乳富含不饱和脂肪酸
乳脂肪为新生儿提供约50%的能量和必需脂肪酸,在新生儿的生长发育和代谢过程中发挥重要功能[22]。乳脂肪含有400多种脂肪酸,是组成最复杂的天然脂质。牛乳中的脂肪酸主要来源于膳食摄入、瘤胃的生物氢化以及乳腺的脂质合成作用,并且随着泌乳期的延长而发生变化。牛初乳的脂肪质量分数为5%~7%,显著高于成熟乳。此外,不同泌乳期牛乳脂肪的脂肪酸组成存在很大差异。牛初乳饱和脂肪酸含量约占总脂肪酸65%~75%,单不饱和脂肪酸约占24%~28%,多不饱和脂肪酸(polyunsaturated fatty acids,PUFAs)约占4%~5%[23-24]。PUFAs对婴幼儿生长、器官形成和神经发育等均具有重要作用。牛初乳的亚油酸、二十碳五烯酸(eicosapentaenoic acid,EPA)、二十二碳六烯酸(docosahexaenoic acid,DHA)、二十二碳五烯酸、花生四烯酸(arachidonic acid,ARA)以及PUFAs总量均显著高于成熟乳[25-26]。DHA、EPA和ARA对于新生儿的大脑发育至关重要,其中DHA是大脑的重要成分之一,约占大脑脂质的60%,是神经元生长必不可少的营养物质[27],在妊娠期、哺乳期以及婴幼儿时期补充DHA、EPA和ARA能够促进新生儿神经发育、提高认知功能[28-30]。n-3 PUFAs可通过调节肠道菌群,增加丙酸盐等短链脂肪酸的产生,增强肠道屏障功能,缓解肠道功能紊乱[31-32]。此外,DHA和EPA还能够调节T淋巴细胞功能,促进自然杀伤细胞的生成,调节机体免疫反应[33]。因此,牛初乳特殊的脂肪酸组成赋予其维持肠道稳态、促进神经发育、增强免疫等多种生物学功能。
利用脂质组学技术分析牛初乳和成熟乳的脂质组成,发现两种不同泌乳期的牛乳存在63 种差异脂质,其中牛初乳中有5 种甘油磷脂酰乙醇胺、1 种磷脂酰甘油和15 种甘油三酯的含量显著高于成熟乳;而成熟乳中有1 种双磷脂酰甘油、9 种甘油二酯、2 种甘油磷脂酰胆碱、9 种双己糖神经酰胺、3 种己糖神经酰胺、3 种甘油磷脂酸、12 种磷脂酰乙醇胺和3 种甘油三酯的含量高于牛初乳,这些差异脂质主要与甘油磷脂、鞘脂类和甘油酯类代谢途径有关[34],而由这些差异脂质所引起的生物学功能差异尚待进一步探究。
1.3 牛初乳是类母乳低聚糖的天然来源
母乳低聚糖是天然存在于母乳且含量仅次于乳糖和脂肪的第三大营养素,因具有多种重要的生理功能而受到广泛关注。鉴于母乳低聚糖规模化生产限制和法规要求,目前主要将低聚半乳糖和低聚果糖等母乳低聚糖替代品应用于婴幼儿配方食品生产。但低聚半乳糖和低聚果糖等母乳低聚糖替代品结构简单,不含有母乳低聚糖特有的岩藻糖和唾液酸结构[35]。近年来,牛乳低聚糖因与母乳低聚糖具有相似的结构和功能而引起重视。牛乳低聚糖一般由3~15 个单糖通过糖苷键共价连接形成,且70%以上的牛乳低聚糖含有一个或多个酸性唾液酸残基,其中唾液酸乳糖(sialyllactose,SL)和唾液酸乳糖胺(sialyllactosamine,SLN)含量最为丰富[36]。牛乳低聚糖可以阻止病原菌对肠上皮细胞的黏附[37],并为有益菌的生长提供碳源,促进肠道发育、维持肠道健康[38]。牛初乳的低聚糖质量浓度约为1 g/L,随着泌乳期的延长而逐渐下降[39];3’-SL、6’-SL、6’-SLN和二唾液酸乳糖(disialyllactose,DSL)是牛初乳中主要的低聚糖,3’-SL占低聚糖总量的70%[40]。牛初乳中3’-SL、6’-SL、6’-SLN和DSL的水平在牛分娩后最高,分别可达681、243、239、201 mg/mL,并在产后48 h迅速下降[41-42]。因此,牛初乳是牛乳低聚糖的优质来源,开发牛初乳低聚糖模拟母乳低聚糖并应用于配方食品和功能食品,既能够满足对食品营养的需求,还能提高牛乳附加值。
1.4 牛初乳乳脂肪球膜与成熟乳之间的差异
乳脂肪球膜(milk fat globule membrane,MFGM)是包裹在乳脂肪液滴表面,由磷脂和特异性膜蛋白等组成的复杂3 层膜,具有促进神经发育、提高认知能力、增强免疫力、维持肠道健康以及改善糖脂代谢等多种生物学功能[43-44]。人乳MFGM和牛乳MFGM具有高度的结构和功能同源性,从牛乳中分离的MFGM已被添加到婴幼儿配方乳粉中,以更好地满足婴幼儿生长发育的健康需求[45]。牛乳MFGM的含量和组成受泌乳期、饲料和乳牛健康状况等多种因素影响。利用蛋白组学技术比较不同泌乳期牛乳MFGM蛋白种类和功能的差异,发现初乳MFGM的差异蛋白主要涉及半乳糖代谢和脂质形成等通路,而成熟乳MFGM差异蛋白则主要与脂质代谢和过氧化物酶体增殖物激活受体信号通路有关[46];牛初乳和成熟乳MFGM的N-糖蛋白比较分析结果表明,牛初乳MFGM的免疫相关N-糖蛋白与成熟乳存在显著差异[47],这与牛初乳较强的免疫调节功能有关。此外,乳脂肪球的大小与泌乳期呈负相关,不同泌乳期人乳MFGM脂质组成和脂肪球微观结构存在差异[48],关于不同泌乳期牛乳MFGM脂质组成和功能差异的研究较少。因此,后续研究需进一步明确牛初乳和成熟乳MFGM组成与生物学功能差异,以更好地指导牛乳MFGM在功能性食品和婴幼儿配方乳粉中的应用[45]。
1.5 牛初乳富含多种生长因子
牛初乳含有多种具有生长发育促进作用的生长因子,如EGF、IGFI和IGFII、转化生长因子(transforming growth factor,TGF)β1和TGFβ2、成纤维细胞生长因子(fibroblast growth factor,FGF)和血小板衍生生长因子等,目前已发现牛初乳中有20多种肽类生长因子,在促进肠道发育、调节免疫等方面发挥协同作用[6]。牛初乳中生长因子水平在产后最初几个小时最高,并随着泌乳期的延长而显著下降[49]。
IGFs是牛初乳中含量最高的生长因子,其中IGFI和IGFII的质量浓度分别约为50~2 000 μg/L和200~600 μg/L,主要以游离形式存在;在成熟乳中,IGFI和IGFII的质量浓度均低于10 μg/L,主要以结合形式存在[50]。牛乳和人乳IGFs具有100%的序列同源性。IGFs具有促进细胞增殖分化、骨骼肌细胞生长发育、神经再生、加速骨骼愈合、促进肠道发育、增加葡萄糖利用以及介导生长激素的促生长作用等多种生物活性[51]。牛初乳中TGFβ含量较高,约为成熟乳的20 倍,TGFβ有35 个亚基,在免疫调节、细胞增殖、维持胃肠道完整性以及促进骨骼发育等方面均具有重要作用[52]。EGF含有53 个氨基酸残基,具有加速伤口愈合、调节炎症反应、促进胃肠道组织修复以及细胞增殖分化等功能[52]。将EGF与早产儿的胃液孵育后,EGF仍能保持完整,但是EGF在成年人胃液中不稳定,会降解形成E G F 4 9,造成其生物学活性降低[53]。EGF对肠消化的稳定性则依赖于是否存在其他食物蛋白,空腹时摄入EGF会被胰蛋白酶快速降解,而当其与酪蛋白等其他蛋白共存时,EGF则可以保持其原有活性,说明牛乳酪蛋白等可以在一定程度上保护EGF,使其摄入后能正常发挥生物学功能[54]。
2 牛初乳的特殊组成赋予其多种生物学功能
2.1 调节免疫
牛初乳含有Igs、乳铁蛋白、骨桥蛋白、抗菌肽等多种免疫活性成分,可以作为增强免疫功能的天然营养来源。在生命早期肠道发育尚未成熟,牛初乳IgG可以完整地到达肠道,发挥抗菌和免疫调节功能。一项在埃及开展的双盲实验将80 名早产儿随机分为对照组和牛初乳干预组,牛初乳组婴儿CD4+CD25+FOXP3+T淋巴细胞的比例明显升高,并且早产儿败血症的严重程度和死亡率均显著下降[55]。牛初乳的IgA质量浓度较高,为3.2~6.2 g/L。IgA可以保护机体黏膜,IgA缺乏导致呼吸道和胃肠道感染。土耳其的一项临床研究发现,摄入牛初乳1 周可以显著缓解IgA缺乏儿童的病毒性呼吸道感染,表明牛初乳对儿童的呼吸道和消化道黏膜具有较好的保护效果[56];一项在丹麦开展的临床试验发现,对急性淋巴细胞白血病儿童补充牛初乳可有效保护化疗对口腔黏膜的损伤[57]。一项埃及开展的临床试验表明,牛初乳可以有效地预防儿童反复性呼吸道感染和腹泻的发生,减少此类感染所导致的住院频率[58]。牛初乳对慢性疾病患者、运动员等特殊群体同样具有一定的免疫保护作用。高危心血管疾病患者连续摄入2 个月牛初乳可以有效预防流感的发生[59]。运动员由于长期的力量训练,常出现免疫力下降以及上呼吸道感染等症状,牛初乳能够有效降低运动员上呼吸道感染的时间和发生频率,增加运动员唾液中分泌型IgA的含量[60],增强血液中吞噬细胞活性[61]。
牛乳Igs、骨桥蛋白和乳铁蛋白等具有免疫调节功能的活性蛋白会随着泌乳时间的延长而逐渐下降。因此,严格控制牛初乳收集的时间、保证牛初乳产品组成和品质的一致性至关重要。
2.2 改善肠道健康
黏膜屏障损伤及其引起的炎症反应是腹泻、坏死性结肠炎等多种胃肠道疾病的典型特征。上皮细胞修复作用对于黏膜屏障重建具有重要生理意义,此过程需要IGF、EGF以及TGF等多种肽类生长因子的参与。牛初乳是多种生长因子的天然来源,具有增强上皮细胞修复的功能,这一特点决定了其在黏膜损伤类胃肠道疾病的潜在治疗作用。当肠道损伤后,伤口周围存活的细胞能够迁移至损伤区域重新形成连续的肠上皮,对肠道进行修复。体外细胞实验表明,牛初乳能够促进Caco-2细胞的体外增殖活性,并且促进其向损伤部位的迁移[6]。动物实验表明,牛初乳及其活性组分可以有效降低促炎细胞因子的水平,缓解由非类固醇类抗炎药物、2,4,6-三硝基苯磺酸和葡聚糖硫酸钠等化学药物引起的肠炎症状,修复肠黏膜,改善肠道屏障功能[62-65]。坏死性结肠炎是造成早产儿死亡的重要诱因。早产仔猪进行牛初乳干预后,坏死性结肠炎症状明显得到缓解,IL-1β和IL-8等炎症因子水平降低,远端小肠绒毛高度和刷状缘酶活性增加,促进早产仔猪的乳糖吸收[66]。人群实验表明,牛初乳可以通过促进黏膜修复,提高结肠炎患者组织评分,缓解结肠炎症[67],加速克罗恩病儿童的康复[68]。牛初乳还可缓解由轮状病毒和大肠杆菌等引起的儿童腹泻,减少腹泻和呕吐次数[69-70]。运动员在训练过程中常出现肠道通透性增强等胃肠道疾病。一项双盲安慰剂对照实验结果表明,运动员连续每天补充500 mg牛初乳,20 d后其粪便连蛋白含量降低,肠道通透性下降,肠道屏障功能改善[71]。波兰的一项随机双盲对照试验证明,分娩后2 h和24 h所产牛初乳能够显著降低运动员的肠道通透性,但是分娩后72 h所产牛初乳干预组较对照组则无明显改善作用,说明泌乳期是影响牛初乳肠道保护功能的重要因素[72]。因此,牛初乳可以直接作用于消化道黏膜,加速胃肠道疾病的康复并减少相关并发症,可作为腹泻、肠炎等胃肠道疾病的辅助治疗手段。
除黏膜屏障外,肠道菌群作为生物屏障在多种胃肠道疾病的发生和发展过程中同样发挥重要作用。牛初乳含有丰富的Igs、乳铁蛋白、低聚糖等,可以有效促进益生菌的生长及其在肠道的定植。Igs能够增加双歧杆菌对人结肠癌细胞HT-29的黏附,表明牛乳IgG可作为促进人体肠道有益菌生长和定植的功能性原料[73]。在体外培养条件下,乳铁蛋白能够抑制有害致病菌的增殖,而对益生菌的生长无明显影响[74]。牛初乳低聚糖可以通过调节糖基转移酶和聚糖合成相关基因的表达,促进双歧杆菌在HT-29结肠癌细胞表面的定植,并且对病原菌的定植没有影响[75]。这些研究结果表明牛初乳具有调节肠道菌群的潜在功能。
2.3 改善骨骼健康
牛初乳中含有乳铁蛋白、Igs、IGF和TGF等多种活性成分,使其具有改善骨骼健康的功能。与普通配方乳粉喂养组相比,牛初乳对幼年恒河猴的体质量、身高和脂肪组织质量等无显著影响,但可以有效增加幼年恒河猴的骨密度,有益于骨骼发育[76]。对青春期大鼠灌胃牛初乳1~30 kDa活性组分,干预6.2 周后,大鼠骨密度显著增加,并且血清生长激素和IGF1的水平升高,表明牛初乳活性组分能够通过调节青春期大鼠的内分泌促进骨骼生长[77]。研究发现,去卵巢雌性大鼠和去势雄性大鼠每天分别灌胃1.5 g和2 g牛初乳,4 个月后大鼠骨组织中骨保护素、血管内皮生长因子A和FGF2等表达水平显著升高,骨生成能力增强,骨组织显微结构得到改善[78]。人群实验表明,中老年人(>50 岁)每天补充60 g牛初乳粉,经8 周后,受试者腿部抗压强度增加,并且尿液中N-端肽含量明显下降,说明牛初乳粉能够抑制中老年人的骨吸收,增强其骨骼强度[79]。因此,牛初乳不仅具有促进骨骼生长发育的潜力,而且能够有效改善因衰老引起的骨质流失。
关于牛初乳中发挥骨保护作用的活性组分和作用机制也有深入研究。牛初乳能够有效缓解糖皮质激素对MC3T3-E1前成骨细胞的氧化损伤,抑制前成骨细胞凋亡[80];去除酪蛋白的脱脂牛初乳可以有效促进间充质干细胞向成骨细胞分化,增加钙盐沉积,增强骨生成能力[81]。这些结果说明,牛初乳可以通过增强成骨细胞的活性和功能,促进骨生成作用,发挥骨保护功能。Du Ming等[82]利用膜过滤等方法获得富含乳铁蛋白、EGF和IGF等活性组分的牛初乳酸性蛋白(bovine colostrum acidic proteins,BCAP),并以50 mg/d的剂量干预去卵巢大鼠12 周,结果显示BCAP可以有效增强大鼠的骨密度,减少骨流失,改善骨微结构退化,缓解绝经后骨质疏松症。近年来,越来越多的研究开始关注外泌体对骨骼健康的作用。牛初乳外泌体可以有效降低抗酒石酸酸性磷酸酶的活性,抑制破骨细胞的分化,外泌体还可以调节糖皮质激素诱导小鼠的肠道菌群,改善糖皮质激素诱导的骨质疏松症,表明外泌体是牛初乳发挥改善骨骼健康作用的有效成分之一[83]。综上,牛初乳中富含的乳铁蛋白、生长因子和外泌体等活性成分协同作用,不仅能够促进骨生成,还能抑制骨吸收,使其可成为一种有益于骨骼生长发育和骨骼健康的营养补充剂。
2.4 提高运动能力
牛初乳具有提高运动表现、促进运动恢复等功能。在抗阻训练中,牛初乳补充组运动员的肌肉质量和力量较安慰剂组显著增加[84]。足球运动员在训练后,以3.2 g/d的剂量补充牛初乳,6 周后运动员蹲跳训练后恢复得更快,肌酸激酶和IL-6水平更低,说明牛初乳能够在一定程度上加速运动恢复、提高运动能力[85]。自行车运动员每天补充10 g浓缩牛初乳粉6 周后,运动员在5 d的加强训练中表现更好[86];以20 g/d和60 g/d的剂量连续补充牛初乳8 周均能显著增强自行车运动员的运动耐力,但是两个剂量组间无显著差异[87]。因此,牛初乳能够增强运动员的运动表现、提高运动耐力、加速运动恢复,是一种天然、优质的运动营养食品,其潜在机制可能与牛初乳增加机体代谢缓冲能力、增强免疫功能等有关[88]。
2.5 降低血糖和血脂
牛初乳及其活性组分还具有降血糖、降血脂和护肝等功能。2型糖尿病患者每天摄入5 g牛初乳4 周后,血糖、胆固醇和甘油三酯水平显著下降[89]。利用超滤富集分娩后24 h牛初乳的IGF1组分,并以50 μg/kg mb的剂量干预链脲佐菌素诱导的糖尿病小鼠,4 周后糖尿病小鼠血糖水平显著降低,体质量明显增加,肾脏和肝脏质量明显下降,表明牛初乳的IGF1组分可以用于糖尿病患者的辅助治疗[90]。非酒精性脂肪肝炎和胰岛素抵抗患者服用Imm124-E(一种IgG增强的牛初乳提取物)30 d后,血清中胰高血糖素样肽-1、脂联素水平和调节性T细胞数目显著增加,血糖紊乱和肝脏脂质变性程度得到改善[91]。胰岛素抵抗、糖尿病和非酒精性脂肪肝等疾病均涉及肠道屏障功能受损、炎症反应等病理进程,牛初乳的免疫调节、肠道黏膜保护和改善肠道菌群功能可能是其改善上述疾病的作用机制,而具体的分子机制仍需进一步探究。
2.6 促进皮肤健康
牛初乳还能够促进皮肤的修复,其不仅能够促进人角质细胞的增殖和迁移[92],还能通过激活PI3K/PLC-γ/PKCα信号通路,促进人初代角质细胞从增殖向分化状态的转变,增加角质细胞分化早期和晚期标志蛋白的表达,促进丝聚合蛋白的成熟[93];此外,通过外敷牛初乳粉可以缩短皮肤外伤愈合时间,降低患者的疼痛反应[94],表明牛初乳可作为皮肤类疾病的辅助治疗手段。
3 牛初乳活性成分的加工稳定性
牛初乳中的Igs、乳铁蛋白、生长因子等活性成分极易受热处理、干燥等加工条件的影响,牛初乳活性成分和生物学功能的保留程度是评价牛初乳相关产品品质的重要指标。
3.1 不同杀菌方式对牛初乳活性成分稳定性的影响
热处理是乳品加工的重要生产环节,主要目的在于杀死微生物和使酶失活,对于保证乳制品安全以及延长货架期至关重要。目前,乳制品生产中基于热处理的杀菌方式主要有两种:超高温瞬时灭菌(ultrahigh temperature,UHT)和巴氏杀菌。UHT的条件为135 ℃下杀菌2~5 s,UHT能够有效杀灭多种微生物和孢子,延长产品在室温下的货架期,但会导致牛初乳中IgG几乎完全失活,并破坏多种其他活性成分[95],说明UHT不适用于牛初乳相关产品的生产。巴氏杀菌分为高温短时(high-temperature short-time,HTST)和低温长时(low-temperature long-time,LTLT)巴氏杀菌。HTST杀菌条件为72~85 ℃下加热15 s,而LTLT杀菌条件为63 ℃下加热至少30 min。两种巴氏杀菌工艺均会造成Igs发生不同程度的损失,其中HTST会造成约25%的Igs变性[96],LTLT则导致约12.3%的IgG损失[97],但是经两种杀菌工艺获得的牛初乳均能促进肠道上皮细胞的增殖,促进脂多糖刺激条件下肠道上皮细胞免疫调节因子的分泌[98]。因此,生产者可根据生产和贮藏需求,选择合适的巴氏杀菌工艺,在保证牛初乳产品安全的同时最大程度地保留生物活性组分,满足消费者对高质量牛初乳产品的需求。
3.2 基于膜过滤技术的非热除菌方式有利于牛初乳活性成分的保持
基于膜过滤的除菌方式也是液态牛初乳产品生产的主要工艺之一。与传统的热处理杀菌相比,膜过滤除菌工艺可全程低温,不仅能够有效控制并除去牛初乳中的病原菌,还能保护Igs和生长因子等功效成分。脱脂牛初乳经1.4 μm和0.8 μm孔径的滤膜处理后好氧嗜温菌总数分别降至104 CFU/mL和10 CFU/mL以下,并且这两种孔径的滤膜均能使牛初乳IgG的保留率达到70%~90%[99]。将膜过滤与热处理结合不仅能够有效控制牛初乳中的病原菌,还能最大程度地保持牛初乳的品质,在50 ℃条件下用0.22 μm孔径滤膜过滤脱脂牛初乳,所得滤液可达到接近无菌的状态,且IgG保留率高达90%[100]。采用微滤和超滤结合的多级膜分离技术,不仅能够保证牛初乳的微生物安全性,还能定向富集牛初乳TGF-β等活性组分[101],开发具有特定生物功能的牛初乳产品,满足不同消费者的需求。因此,膜分离等低热处理技术更有利于保持和富集初乳活性成分。
3.3 不同干燥方式对牛初乳活性成分稳定性的影响
干燥是乳制品生产的重要环节之一。干燥后产品水分活度的下降能够有效抑制微生物的生长,减缓化学反应,防止乳品品质下降,延长货架期,也更利于乳品的贮藏、包装和运输等。目前,生产牛初乳粉的方式主要有喷雾干燥和冷冻干燥两种。冷冻干燥引起的蛋白质变性程度低,对TGF-β2和IGFI等生长因子和抗体的保留程度高[102],对IgG的破坏程度小[103],但干燥效率低、规模小、自动化程度较低、生产成本高[5]。喷雾干燥则是乳粉类产品生产中应用最广泛的干燥方式,具有规模大、耗时短、成本低等优点,分为低温喷雾干燥和高温喷雾干燥。高温喷雾干燥工艺操作温度较高,进样口温度可高达180 ℃,易导致乳铁蛋白、Igs和TGF-β等热敏性活性成分的损失[104],因此高温喷雾干燥在牛初乳粉生产中的应用具有一定的局限性。相比于传统喷雾干燥,低温干燥工艺则更有利于牛初乳活性成分的保持[105]。低温喷雾干燥利用温度较低且含湿量极低的空气作为载体,快速去除物料中的水分,可减少传统喷雾干燥过程中高温引起的蛋白变性和热敏性活性成分的破坏[106]。
总地来说,牛初乳粉的生产要经历从生乳收集、贮藏、运输到脱脂、杀菌、干燥等各个过程,而每个环节对于终产品的营养性、安全性、活性物质稳定性都至关重要,终产品的品质取决于各环节的质量控制。因此,初乳粉的质量和品质取决于整个生产加工流程。
4 牛初乳的人群适用性
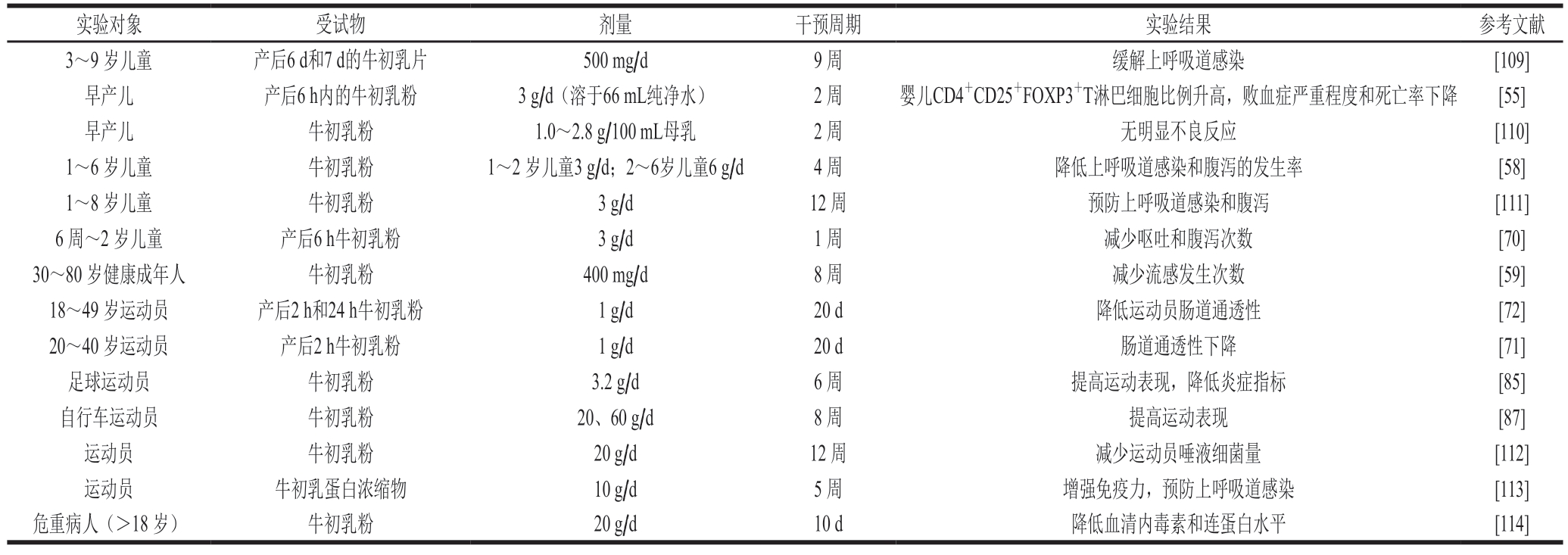
人类食用牛初乳的历史已有上千年,近几十年来,牛初乳也一直被作为功能性乳基料,在全球范围内用于饮品、乳制品等生产。牛初乳作为一种天然动物源食品,与其他天然乳品、大豆制品、蜂蜜等食品一样含有微量的内源性激素,但是不含外源性激素。牛初乳中天然存在的内源性激素主要为脂溶性激素,会随着牛初乳生产过程中脱脂、杀菌、干燥等工艺流失[107]。实际上人体每日从饮食中摄入的激素水平远低于自身产生的内源性激素。临床试验也证明了儿童、非孕妇成人和运动员等在一定剂量范围内摄入牛初乳的安全性,其中儿童的摄入剂量范围约为500 mg/d~3 g/d,成年人和运动员的摄入剂量范围约为400 mg/d~20 g/d(表2)。因此,科学合理地摄入牛初乳不仅能为青少年儿童的身体健康和生长发育提供营养支持[9],还能满足中老年人、运动员等特殊人群的营养和健康需求[108]。
表2 牛初乳临床试验
Table 2 Clinical experiments of bovine colostrum
目前,既不能在婴幼儿配方食品和其他食品中使用牛初乳,也不能在膳食补充剂中使用牛初乳的代表性国家为日本;不能在婴幼儿配方食品和其他食品中使用,但能在膳食补充剂中添加牛初乳的代表性国家包括新西兰和澳大利亚;美国仅不允许在1 岁以下的婴幼儿配方食品中使用,其他食品和膳食补充剂均可添加牛初乳;欧盟除婴幼儿配方食品外,也不允许在3 岁以上的配方食品中使用牛初乳,其他非配方食品和膳食补充剂均可使用;此外,越南、韩国和中国台湾等经过备案审批后,牛初乳可以被添加于各类食品中。2012年,我国原卫生部在《牛初乳类产品适用标准问题的复函》中表示,婴幼儿配方食品中不得添加牛初乳以及用牛初乳为原料生产的乳制品,而在其他普通食品中可以按照相关食品标准添加牛初乳为原料的乳制品。目前,随着牛初乳安全性和功能性评价体系的不断完善、我国牛初乳行业不断规范,牛初乳及相关产品将被越来越多的消费者所接受,牛初乳行业将迎来崭新阶段。
5 结语
牛初乳富含乳铁蛋白、Igs、低聚糖、生长因子和微量营养素等多种活性成分,是天然功能因子的优质来源。大量证据表明,牛初乳中活性组分协同作用,具有调节免疫、改善肠道健康、促进骨骼健康、增强运动能力等多种生物功能。随着“十四五”规划中“健康中国”建设的全面推进和人民生活水平的提高,消费者对于功能性乳制品的需求日益增加,我国牛初乳市场容量也将持续扩大。将牛初乳与磷脂、益生菌、多酚以及PUFAs等功能性成分复配,针对不同群体开发精准营养产品,不仅能够促进牛初乳产品市场的多元化,丰富消费者的选择,也能更好地为人民的健康保驾护航。
[1] MCGRATH B A,FOX P F,MCSWEENEY P L H,et al.Composition and properties of bovine colostrum: a review[J].Dairy Science &Technology,2016,96(2):133-158.DOI:10.1007/s13594-015-0258-x.
[2] RAJAMANICKAM K,JAYASHREE G,LEELA V,et al.Current and future prospects of colostrum-Indian ethnic food supplement[J].Journal of Dairy Science and Technology,2016,5(3): 23-28.DOI:10.37591/rrjodst.v5i3.454.
[3] SCAMMELL A W.Production and uses of colostrum[J].Australian Journal of Dairy Technology,2001,56(2): 74-82.
[4] SANGILD P T,VONDEROHE C,HEBIB V M,et al.Potential benefits of bovine colostrum in pediatric nutrition and health[J].Nutrients,2021,13(8): 2551.DOI:10.3390/nu13082551.
[5] KAPLAN M,ARSLAN A,DUMAN H,et al.Production of bovine colostrum for human consumption to improve health[J].Frontiers in Pharmacology,2022,12: 796824.DOI:10.3389/fphar.2021.796824.
[6] PLAYFORD R J,WEISER M J.Bovine colostrum: its constituents and uses[J].Nutrients,2021,13(1): 265.DOI:10.3390/nu13010265/.
[7] BYLUND G.Dairy processing handbook[M/OL].Sweden: Tetra Pak,1995: 331-352.https://dairyprocessinghandbook.tetrapak.com/.
[8] PLAYFORD R J,CATTELL M,MARCHBANK T.Marked variability in bioactivity between commercially available bovine colostrum for human use;implications for clinical trials[J].PLoS ONE,2020,15(6): e234719.DOI:10.1371/journal.pone.0234719.
[9] SANGILD P T,VONDEROHE C,MELENDEZ HEBIB V,et al.Potential benefits of bovine colostrum in pediatric nutrition and health[J].Nutrients,2021,13(8): 2551.DOI:10.3390/nu13082551.
[10] ULFMAN L H,LEUSEN J H W,SAVELKOUL H F J,et al.Effects of bovine immunoglobulins on immune function,allergy,and infection[J].Frontiers in Nutrition,2018,5: 52.DOI:10.3389/fnut.2018.00052.
[11] ZHAO X,XU X X,LIU Y,et al.The in vitro protective role of bovine lactoferrin on intestinal epithelial barrier[J].Molecules,2019,24(1):7-13.DOI:10.3390/molecules24010148.
[12] DONOVAN S M,ODLE J.Growth factors in milk as mediators of infant development[J].Annual Review of Nutrition,1994,14: 147-167.DOI:10.1146/annurev.nu.14.070194.001051.
[13] JIA Y,LU Y,WANG X,et al.Mass spectrometry based quantitative and qualitative analyses reveal N-glycan changes of bovine lactoferrin at different stages of lactation[J].LWT-Food Science and Technology,2021,147: 111626.DOI:10.1016/j.lwt.2021.111626.
[14] JIANG R,LÖNNERDAL B.Osteopontin in human milk and infant formula affects infant plasma osteopontin concentrations[J].Pediatric Research,2019,85(4): 502-505.DOI:10.1038/s41390-018-0271-x.
[15] KUMURA H,MIURA A,SATO E,et al.Susceptibility of bovine osteopontin to chymosin[J].Journal of Dairy Research,2004,71(4):500-504.DOI:10.1017/S0022029904000391.
[16] LI M,LI W,KONG F,et al.Metabolomics methods to analyze full spectrum of amino acids in different domains of bovine colostrum and mature milk[J].European Food Research and Technology,2020,246(1): 213-224.DOI:10.1007/s00217-019-03385-y.
[17] TABATABAIE L,KLOMP L W,BERGER R,et al.L-Serine synthesis in the central nervous system: a review on serine deficiency disorders[J].Molecular Genetics and Metabolism,2010,99(3): 256-262.DOI:10.1016/j.ymgme.2009.10.012.
[18] LEE Y,STALLCUP M R.Minireview: protein arginine methylation of nonhistone proteins in transcriptional regulation[J].Molecular Endocrinology,2009,23(4): 425-433.DOI:10.1210/me.2008-0380.
[19] GHOSH G,ADAMS J A.Phosphorylation mechanism and structure of serine-arginine protein kinases[J].FEBS Journal,2011,278(4): 587-597.DOI:10.1111/j.1742-4658.2010.07992.x.
[20] MULLER-TIDOW C,WANG W,IDOS G E,et al.Cyclin A1 directly interacts with B-myb and cyclin A1/cdk2 phosphorylate B-myb at functionally important serine and threonine residues: tissue-specific regulation of B-myb function[J].Blood,2001,97(7): 2091-2097.DOI:10.1182/blood.V97.7.2091.
[21] EL IDRISSI A.Taurine regulation of neuroendocrine function[J].Advances in Experimental Medicine and Biology,2019,1155: 977-985.DOI:10.1007/978-981-13-8023-5_81.
[22] DELPLANQUE B,GIBSON R,KOLETZKO B,et al.Lipid quality in infant nutrition: current knowledge and future opportunities[J].Journal of Pediatric Gastroenterology &Nutrition,2015,61(1): 8-17.DOI:10.1097/MPG.0000000000000818.
[23] CONTARINI G,POVOLO M,PELIZZOLA V,et al.Bovine colostrum: changes in lipid constituents in the first 5 days after parturition[J].Journal of Dairy Science,2014,97(8): 5065-5072.DOI:10.3168/jds.2013-7517.
[24] O’CALLAGHAN T F,O’DONOVAN M,MURPHY J P,et al.Evolution of the bovine milk fatty acid profile-from colostrum to milk five days post parturition[J].International Dairy Journal,2020,104:104655.DOI:10.1016/j.idairyj.2020.104655.
[25] WILMS J N,HARE K S,FISCHER-TLUSTOS A J,et al.Fatty acid profile characterization in colostrum,transition milk,and mature milk of primi-and multiparous cows during the first week of lactation[J].Journal of Dairy Science,2022,105(3): 2612-2630.DOI:10.3168/jds.2021-20880.
[26] CONTARINI G,POVOLO M,PELIZZOLA V,et al.Bovine colostrum: changes in lipid constituents in the first 5 days after parturition[J].Journal of Dairy Science,2014,97(8): 5065-5072.DOI:10.3168/jds.2013-7517.
[27] KHALID W,GILL P,ARSHAD M S,et al.Functional behavior of DHA and EPA in the formation of babies brain at different stages of age,and protect from different brain-related diseases[J].International Journal of Food Properties,2022,25(1): 1021-1044.DOI:10.1080/109 42912.2022.2070642.
[28] JANSSEN C I F,ZERBI V,MUTSAERS M P C,et al.Impact of dietary n-3 polyunsaturated fatty acids on cognition,motor skills and hippocampal neurogenesis in developing C57BL/6J mice[J].The Journal of Nutritional Biochemistry,2015,26(1): 24-35.DOI:0.1016/j.jnutbio.2014.08.002.
[29] BASAK S,DUTTAROY A K.Maternal PUFAs,placental epigenetics,and their relevance to fetal growth and brain development[J].Reproductive Sciences,2022,8: 1-15.DOI:10.1007/s43032-022-00989-w.
[30] SUN J,ZHANG W.Supplementation with dietary omega-3 PUFA mitigates fetal brain inflammation and mitochondrial damage caused by high doses of sodium nitrite in maternal rats[J].PLoS ONE,2022,17(3): e266084.DOI:10.1371/journal.pone.0266084.
[31] SHAMA S,LIU W.Omega-3 fatty acids and gut microbiota: a reciprocal interaction in nonalcoholic fatty liver disease[J].Digestive Diseases and Sciences,2020,65(3): 906-910.DOI:10.1007/s10620-020-06117-5.
[32] BIDU C,ESCOULA Q,BELLENGER S,et al.The transplantation of omega 3 PUFA-altered gut microbiota of fat-1 mice to wild-type littermates prevents obesity and associated metabolic disorders[J].Diabetes,2019,68(1): 1512-1524.DOI:10.2337/db19-er01a.
[33] ZALOGA G P.Narrative review of n-3 polyunsaturated fatty acid supplementation upon immune functions,resolution molecules and lipid peroxidation[J].Nutrients,2021,13(2): 662.DOI:10.3390/nu13020662.
[34] LI M,LI Q,KANG S,et al.Characterization and comparison of lipids in bovine colostrum and mature milk based on UHPLC-QTOFMS lipidomics[J].Food Research International,2020,136: 109490.DOI:10.1016/j.foodres.2020.109490.
[35] CATENZA K F,DONKOR K K.Recent approaches for the quantitative analysis of functional oligosaccharides used in the food industry: a review[J].Food Chemistry,2021,355: 129416.DOI:10.1016/j.foodchem.2021.129416.
[36] TAO N,DEPETERS E J,FREEMAN S,et al.Bovine milk glycome[J].Journal of Dairy Science,2008,91: 3768-3778.DOI:10.3168/jds.2008-1305.
[37] SOHANPAL B K,EL-LABANY S,LAHOOTI M,et al.Integrated regulatory responses of fimB to N-acetylneuraminic (sialic) acid and GlcNAc in Escherichia coli K-12[J].Proceedings of the National Academy of Sciences,2004,101(46): 16322-16327.DOI:10.1073/pnas.0405821101.
[38] FISCHER A J,MALMUTHUGE N,GUAN L L,et al.Short communication: the effect of heat treatment of bovine colostrum on the concentration of oligosaccharides in colostrum and in the intestine of neonatal male Holstein calves[J].Journal of Dairy Science,2018,101(1): 401-407.DOI:10.3168/jds.2017-13533.
[39] URASHIMA T,TAUFIK E,FUKUDA K,et al.Recent advances in studies on milk oligosaccharides of cows and other domestic farm animals[J].Bioscience Biotechnology and Biochemistry,2013,77(3):455-466.DOI:10.1271/bbb.120810.
[40] FISCHER-TLUSTOS A J,HERTOGS K,VAN NIEKERK J K,et al.Oligosaccharide concentrations in colostrum,transition milk,and mature milk of primi-and multiparous Holstein cows during the first week of lactation[J].Journal of Dairy Science,2020,103(4): 3683-3695.DOI:10.3168/jds.2019-17357.
[41] NAKAMURA T,KAWASE H,KIMURA K,et al.Concentrations of sialyloligosaccharides in bovine colostrum and milk during the prepartum and early lactation[J].Journal of Dairy Science,2003,86(4): 1315-1320.DOI:10.3168/jds.S0022-0302(03)73715-1.
[42] MCJARROW P,VAN AMELSFORT-SCHOONBEEK J.Bovine sialyl oligosaccharides: seasonal variations in their concentrations in milk,and a comparison of the colostrums of Jersey and Friesian cows[J].International Dairy Journal,2004,14(7): 571-579.DOI:10.1016/j.idairyj.2003.11.006.
[43] LI T,GONG H,YUAN Q,et al.Supplementation of polar lipidsenriched milk fat globule membrane in high-fat diet-fed rats during pregnancy and lactation promotes brown/beige adipocyte development and prevents obesity in male offspring[J].The FASEB Journal,2020,34(3): 4619-4634.DOI:10.1096/fj.201901867RRR.
[44] YUAN Q C,GONG H,DU M,et al.Supplementation of milk polar lipids to obese dams improves neurodevelopment and cognitive function in male offspring[J].The FASEB Journal,2021,35(4):e21454.DOI:10.1096/fj.202001974RRR.
[45] SANGILD P T,VONDEROHE C,MELENDEZ HEBIB V,et al.Potential benefits of bovine colostrum in pediatric nutrition and health[J].Nutrients,2021,13(8): 2551.DOI:10.3390/nu13082551.
[46] JIA W,ZHANG R,ZHU Z,et al.A high-throughput comparative proteomics of milk fat globule membrane reveals breed and lactation stages specific variation in protein abundance and functional differences between milk of saanen dairy goat and holstein bovine[J].Frontiers in Nutrition,2021,8: 680683.DOI:10.3389/fnut.2021.680683.
[47] CAO X,ZHENG Y,WU S,et al.Characterization and comparison of milk fat globule membrane N-glycoproteomes from human and bovine colostrum and mature milk[J].Food &Function,2019,10(8): 5046-5058.DOI:10.1039/c9fo00686a.
[48] ZOU X,GUO Z,HUANG J,et al.Human milk fat globules from different stages of lactation: a lipid composition analysis and microstructure characterization[J].Journal of Agricultural and Food Chemistry,2012,60(29): 7158-7167.DOI:10.1021/jf3013597.
[49] BASTIAN S E,DUNBAR A J,PRIEBE I K,et al.Measurement of betacellulin levels in bovine serum,colostrum and milk[J].Journal of Endocrinology,2001,168(1): 203-212.DOI:10.1677/joe.0.1680203.
[50] MCGRATH B A,FOX P F,MCSWEENEY P L H,et al.Composition and properties of bovine colostrum: a review[J].Dairy Science &Technology,2015,96(2): 133-158.DOI:10.1007/s13594-015-0258-x.
[51] RABINOVSKY E D,DRAGHIA-AKLI R.Insulin-like growth factor I plasmid therapy promotes in vivo angiogenesis[J].Molecular Therapy,2004,9(1): 46-55.DOI:10.1016/j.ymthe.2003.10.003.
[52] MEHRA R,SINGH R,NAYAN V,et al.Nutritional attributes of bovine colostrum components in human health and disease: a comprehensive review[J].Food Bioscience,2021,40: 100907.DOI:10.1016/j.fbio.2021.100907.
[53] PLAYFORD R J,MARCHBANK T,CALNAN D P,et al.Epidermal growth factor is digested to smaller,less active forms in acidic gastric juice[J].Gastroenterology,1995,108(1): 92-101.DOI:10.1016/0016-5085(95)90012-8.
[54] PLAYFORD R J,WOODMAN A C,CLARK P,et al.Effect of luminal growth factor preservation on intestinal growth[J].Lancet,1993,341(8849): 843-848.DOI:10.1016/0140-6736(93)93057-8.
[55] ISMAIL R I H,AWAD H A,IMAM S S,et al.Gut priming with bovine colostrum and T regulatory cells in preterm neonates: a randomized controlled trial[J].Pediatric Research,2021,90(3): 650-656.DOI:10.1038/s41390-020-01344-y.
[56] PATIROGLU T,KONDOLOT M.The effect of bovine colostrum on viral upper respiratory tract infections in children with immunoglobulin A deficiency[J].Clinical Respiratory Journal,2013,7(1): 21-26.DOI:10.1111/j.1752-699X.2011.00268.x.
[57] RATHE M,DE PIETRI S,WEHNER P S,et al.Bovine colostrum against chemotherapy-induced gastrointestinal toxicity in children with acute lymphoblastic leukemia: a randomized,double-blind,placebocontrolled trial[J].Journal of Parenteral and Enteral Nutrition,2020,44(2): 337-347.DOI:10.1002/jpen.1528.
[58] SAAD K,ABO-ELELA M G M,EL-BASEER K A A,et al.Effects of bovine colostrum on recurrent respiratory tract infections and diarrhea in children[J].Medicine,2016,95(37): e4560.DOI:10.1097/MD.0000000000004560.
[59] CESARONE M R,BELCARO G,DI RENZO A,et al.Prevention of influenza episodes with colostrum compared with vaccination in healthy and high-risk cardiovascular subjects: the epidemiologic study in San Valentino[J].Clinical and Applied Thrombosis-Hemostasis,2007,13(2): 130-136.DOI:10.1177/1076029606295957.
[60] CROOKS C V,WALL C R,CROSS M L,et al.The effect of bovine colostrum supplementation on salivary IgA in distance runners[J].International Journal of Sport Nutrition and Exercise Metabolism,2006,16(1): 47-64.DOI:10.1123/ijsnem.16.1.47.
[61] JENSEN G S,PATEL D,BENSON K F.A novel extract from bovine colostrum whey supports innate immune functions.II.Rapid changes in cellular immune function in humans[J].Preventive Medicine,2012,54: S124-S129.DOI:10.1016/j.ypmed.2012.01.004.
[62] CAIRANGZHUOMA,YAMAMOTO M,MURANISHI H,et al.Skimmed,sterilized,and concentrated bovine late colostrum promotes both prevention and recovery from intestinal tissue damage in mice[J].Journal of Dairy Science,2013,96(3): 1347-1355.DOI:10.3168/jds.2012-5701.
[63] FILIPESCU I E,LEONARDI L,MENCHETTI L,et al.Preventive effects of bovine colostrum supplementation in TNBS-induced colitis in mice[J].PLoS ONE,2018,13(8): e202929.DOI:10.1371/journal.pone.0202929.
[64] KANWAR J R,KANWAR R K,STATHOPOULOS S,et al.Comparative activities of milk components in reversing chronic colitis[J].Journal of Dairy Science,2016,99(4): 2488-2501.DOI:10.3168/jds.2015-10122.
[65] SPALINGER M R,ATROTT K,BAEBLER K,et al.Administration of the hyper-immune bovine colostrum extract IMM-124E ameliorates experimental murine colitis[J].Journal of Crohn’s and Colitis,2019,13(6): 785-797.DOI:10.1093/ecco-jcc/jjy213.
[66] STØY A C F,HEEGAARD P M H,THYMANN T,et al.Bovine colostrum improves intestinal function following formula-induced gut inflammation in preterm pigs[J].Clinical Nutrition,2014,33(2): 322-329.DOI:10.1016/j.clnu.2013.05.013.
[67] KHAN Z,MACDONALD C,WICKS A C,et al.Use of the‘nutriceutical’,bovine colostrum,for the treatment of distal colitis:results from an initial study[J].Alimentary Pharmacology &Therapeutics,2002,16(11): 1917-1922.DOI:10.1046/j.1365-2036.2002.01354.x.
[68] RUBIO A,PIGNEUR B,GARNIER-LENGLINÉ H,et al.The efficacy of exclusive nutritional therapy in paediatric Crohn’s disease,comparing fractionated oral vs.continuous enteral feeding[J].Alimentary Pharmacology &Therapeutics,2011,33(12): 1332-1339.DOI:10.1111/j.1365-2036.2011.04662.x.
[69] LI J,XU Y,JIANG J,et al.Bovine colostrum and product intervention associated with relief of childhood infectious diarrhea[J].Scientific Reports,2019,9(1): 3093.DOI:10.1038/s41598-019-39644-x.
[70] BARAKAT S H,MEHEISSEN M A,OMAR O M,et al.Bovine colostrum in the treatment of acute diarrhea in children: a doubleblinded randomized controlled trial[J].Journal of Tropical Pediatrics,2019,66(1): 46-55.DOI:10.1093/tropej/fmz029.
[71] HAŁASA M,MACIEJEWSKA D,BAŚKIEWICZ-HAŁASA M,et al.Oral supplementation with bovine colostrum decreases intestinal permeability and stool concentrations of zonulin in athletes[J].Nutrients,2017,9(4): 370.DOI:10.3390/nu9040370.
[72] HAŁASA M,MACIEJEWSKA-MARKIEWICZ D,BAŚKIEWICZHAŁASA M,et al.Post-delivery milking delay influence on the effect of oral supplementation with bovine colostrum as measured with intestinal permeability test[J].Medicina,2020,56(10): 495.DOI:10.3390/medicina56100495.
[73] MORRIN S T,MCCARTHY G,KENNEDY D,et al.Immunoglobulin G from bovine milk primes intestinal epithelial cells for increased colonization of bifidobacteria[J].AMB Express,2020,10(1): 20-43.DOI:10.1186/s13568-020-01048-w.
[74] TIAN H,MADDOX I S,FERGUSON L R,et al.Influence of bovine lactoferrin on selected probiotic bacteria and intestinal pathogens[J].BioMetals,2010,23(3): 593-596.DOI:10.1007/s10534-010-9318-0.
[75] MORRIN S T,LANE J A,MAROTTA M,et al.Bovine colostrumdriven modulation of intestinal epithelial cells for increased commensal colonisation[J].Applied Microbiology and Biotechnology,2019,103(6): 2745-2758.DOI:10.1007/s00253-019-09642-0.
[76] TAY N,TAN Y C,CHNG K,et al.Effect of human milk formula with bovine colostrum supplementation on bone mineral density in infant cynomolgus macaques[J].Journal of Developmental Origins of Health and Disease,2018,9(2): 172-181.DOI:10.1017/S2040174417000812.
[77] LEE J R B C,KWON S H,KIM H M,et al.Effect of a growth protein-colostrum fraction on bone development in juvenile rats[J].Bioscience,Biotechnology,and Biochemistry,2008,72(1): 1-6.DOI:10.1271/bbb.60695.
[78] KYDONAKI E K,FREITAS L,FONSECA B M,et al.Bovine colostrum supplementation improves bone metabolism in an osteoporosis-induced animal model[J].Nutrients,2021,13(9): 2981.DOI:10.3390/nu13092981.
[79] DUFF W R D,CHILIBECK P D,ROOKE J J,et al.The Effect of bovine colostrum supplementation in older adults during resistance training[J].International Journal of Sport Nutrition and Exercise Metabolism,2014,24(3): 276-285.DOI:10.1123/ijsnem.2013-0182.
[80] MARTIN-ARAGON S,BERMEJO-BESCÓS P,BENEDÍ J,et al.A neuroprotective bovine colostrum attenuates apoptosis in dexamethasone-treated MC3T3-E1 osteoblastic cells[J].International Journal of Molecular Sciences,2021,22(19): 10195.DOI:10.3390/ijms221910195.
[81] MUSSANO F,BARTORELLI C A,BROSSA A,et al.Presence of osteoinductive factors in bovine colostrum[J].Bioscience Biotechnology and Biochemistry,2014,78(4): 662-671.DOI:10.1080/09168451.2014.896733.
[82] DU Ming,XU Weili,YI Huaxi,et al.Protective effects of bovine colostrum acid proteins on bone loss of ovariectomized rats and the ingredients identification[J].Molecular Nutrition &Food Research,2011,55(2): 220-228.DOI:10.1002/mnfr.200900593.
[83] YUN B,MABURUTSE B E,KANG M,et al.Short communication:Dietary bovine milk-derived exosomes improve bone health in an osteoporosis-induced mouse model[J].Journal of Dairy Science,2020,103(9): 7752-7760.DOI:10.3168/jds.2019-17501.
[84] ANTONIO J,SANDERS M S,VAN GAMMEREN D.The effects of bovine colostrum supplementation on body composition and exercise performance in active men and women[J].Nutrition,2001,17(3): 243-247.DOI:10.1016/S0899-9007(00)00552-9.
[85] KOTSIS Y,MIKELLIDI A,ARESTI C,et al.A low-dose,6-week bovine colostrum supplementation maintains performance and attenuates inflammatory indices following a Loughborough Intermittent Shuttle Test in soccer players[J].European Journal of Nutrition,2018,57(3): 1181-1195.DOI:10.1007/s00394-017-1401-7.
[86] SHING C M,JENKINS D G,STEVENSON L,et al.The influence of bovine colostrum supplementation on exercise performance in highly trained cyclists[J].British Journal of Sports Medicine,2006,40(9):797-801.DOI:10.1136/bjsm.2006.027946.
[87] COOMBES J S,CONACHER M,AUSTEN S K,et al.Dose effects of oral bovine colostrum on physical work capacity in cyclists[J].Medicine and Science in Sports and Exercise,2002,34(7): 1184-1188.DOI:10.1097/00005768-200207000-00020.
[88] DAVISON G.The use of bovine colostrum in sport and exercise[J].Nutrients,2021,13(6): 1789.DOI:10.3390/nu13061789.
[89] KIM J H,JUNG W S,CHOI N,et al.Health-promoting effects of bovine colostrum in type 2 diabetic patients can reduce blood glucose,cholesterol,triglyceride and ketones[J].The Journal of Nutritional Biochemistry,2009,20(4): 298-303.DOI:10.1016/j.jnutbio.2008.04.002.
[90] HWANG K,HWANG Y,HA W,et al.Oral administration of insulinlike growth factor-I from colostral whey reduces blood glucose in streptozotocin-induced diabetic mice[J].British Journal of Nutrition,2012,108(1): 39-45.DOI:10.1017/S0007114511005198.
[91] MIZRAHI M,SHABAT Y,BEN Y A,et al.Alleviation of insulin resistance and liver damage by oral administration of Imm124-E is mediated by increased Tregs and associated with increased serum GLP-1 and adiponectin: results of a phase I/II clinical trial in NASH[J].Journal of Inflammation Research,2012,5: 141-150.DOI:10.2147/JIR.S35227.
[92] KOVACS D,CARDINALI G,ASPITE N,et al.Bovine colostrum promotes growth and migration of the human keratinocyte HaCaT cell line[J].Growth Factors,2009,27(6): 448-455.DOI:10.3109/08977190903211077.
[93] KOVACS D,MARESCA V,FLORI E,et al.Bovine colostrum induces the differentiation of human primary keratinocytes[J].The FASEB Journal,2020,34(5): 6302-6321.DOI:10.1096/fj.201900103RRR.
[94] KSHIRSAGAR A Y.A comparative study of colostrum dressing versus conventional dressing in deep wounds[J].Journal of Clinical and Diagnostic Research,2015,9(4): PC01-PC04.DOI:10.7860/JCDR/2015/12004.5739.
[95] LICHAN E,KUMMER A,LOSSO J N,et al.Stability of bovine immunoglobulins to thermal-treatment and processing[J].Food Research International,1995,28(1): 9-16.DOI:10.1016/0963-9969(95)93325-O.
[96] STABEL J R,HURD S,CALVENTE L,et al.Destruction of Mycobacterium paratuberculosis,Salmonella spp.,and Mycoplasma spp.in raw milk by a commercial on-farm high-temperature,shorttime pasteurizer[J].Journal of Dairy Science,2004,87(7): 2177-2183.DOI:10.3168/jds.S0022-0302(04)70038-7.
[97] MEYLAN M,RINGS D M,SHULAW W P,et al.Survival of Mycobacterium paratuberculosis and preservation of immunoglobulin G in bovine colostrum under experimental conditions simulating pasteurization[J].American Journal of Veterinary Research,1996,57(11): 1580-1585.DOI:10.3354/dao027157.
[98] NGUYEN D N,CURRIE A J,REN S,et al.Heat treatment and irradiation reduce anti-bacterial and immune-modulatory properties of bovine colostrum[J].Journal of Functional Foods,2019,57: 182-189.DOI:10.1016/j.jff.2019.04.012.
[99] GOSCH T,APPRICH S,KNEIFEL W,et al.A combination of microfiltration and high pressure treatment for the elimination of bacteria in bovine colostrum[J].International Dairy Journal,2014,34(1): 41-46.DOI:10.1016/j.idairyj.2013.06.014.
[100] BORAD S G,SINGH A K,KAPILA S,et al.Influence of unit operations on immunoglobulins and thermal stability of colostrum fractions[J].International Dairy Journal,2019,93: 85-91.DOI:10.1016/j.idairyj.2019.02.007.
[101] OLLIKAINEN P,MUURONEN K,TIKANMÄKI R.Effect of pasteurization on the distribution of bovine milk transforming growth factor-β2 in casein and whey fractions during micro-and ultrafiltration processes[J].International Dairy Journal,2012,26(2): 141-146.DOI:10.1016/j.idairyj.2012.04.004.
[102] KUMAR M,UPRIT S.Bovine colostrum: neonate to nutraceuticals[J].Research Journal of Animal Husbandry &Dairy Science,2015,5(1): 23-19.
[103] SOTUDEH S,RABBANI KHORASGANI M,ETEMADIFAR Z,et al.Effects of spray-drying,freeze-drying and pasteurization on microbiological quality and IgG level of bovine colostrum[J].Journal of Food Quality and Hazards Control,2018,5(2): 54-60.DOI:10.29252/jfqhc.5.2.5.
[104] STY A C,SANGILD P T,SKOVGAARD K,et al.Spray dried,pasteurised bovine colostrum protects against gut dysfunction and inflammation in preterm pigs[J].Journal of Pediatric Gastroenterology and Nutrition,2016,63(2): 280-287.DOI:10.1097/MPG.0000000000001056.
[105] ELFSTRAND L,LINDMARK-MANSSON H,PAULSSON M,et al.Immunoglobulins,growth factors and growth hormone in bovine colostrum and the effects of processing[J].International Dairy Journal,2002,12(11): 879-887.DOI:10.1016/S0958-6946(02)00089-4.
[106] DE OLIVEIRA A H,MATA M E R M,FORTES M,et al.Influence of spray drying conditions on the properties of whole goat milk[J].Drying Technology,2021,39(6): 726-737. DOI:10.1080/07373937.2020.1714647.
[107] BARREIRO R,REGAL P,DIAZ-BAO M,et al.Analysis of naturally occurring steroid hormones in infant formulas by HPLC-MS/MS and contribution to dietary intake[J].Foods,2015,4(4): 605.DOI:10.3390/foods4040605.
[108] GUBERTI M,BOTTI S,CAPUZZO M T,et al.Bovine colostrum applications in sick and healthy people: a systematic review[J].Nutrients,2021,13(7): 2194.DOI:10.3390/nu13072194.
[109] UCHIDA K,YAMAGUCKI H,KAWASAKI M,et al.Bovine late colostrum (colostrum 6 or 7 days after parturition) supplement reduces symptoms of upper respiratory tract infection in infant[J].Journal of Japanese Society of Clinical Nutrition,2010,31: 122-127.
[110] LI Y,JUHL S M,YE X,et al.A stepwise,pilot study of bovine colostrum to supplement the first enteral feeding in preterm infants(precolos): study protocol and initial results[J].Frontiers in Pediatrics,2017,5: 42.DOI:10.3389/fped.2017.00042.
[111] PATEL K,RANA R.Pedimune in recurrent respiratory infection and diarrhoea: the Indian experience: the pride study[J].Indian Journal of Pediatrics,2006,73(7): 585-591.DOI:10.1007/BF02759923.
[112] JONES A W,CAMERON S J S,THATCHER R,et al.Effects of bovine colostrum supplementation on upper respiratory illness in active males[J].Brain,Behavior,and Immunity,2014,39: 194-203.DOI:10.1016/j.bbi.2013.10.032.
[113] SHING C M,PEAKE J,SUZUKI K,et al.Effects of bovine colostrum supplementation on immune variables in highly trained cyclists[J].Journal of Applied Physiology,2007,102(3): 1113-1122.DOI:10.1152/japplphysiol.00553.2006.
[114] ESLAMIAN G,ARDEHALI S H,BAGHESTANI A R,et al.Effects of early enteral bovine colostrum supplementation on intestinal permeability in critically ill patients: a randomized,doubleblind,placebo-controlled study[J].Nutrition,2019,60: 106-111.DOI:10.1016/j.nut.2018.10.013.