大豆中含有丰富的蛋白质及多种人体必需氨基酸,是一种重要的植物性蛋白资源,常被加工成各种食品,如酱油、豆豉和豆浆等[1]。同时,大豆还可以作为保健品及医药制品的原料[2]。然而,大豆在部分国家是优先过敏原[3]。据统计,大豆过敏影响了大约0.2%~0.4%的人群[4-5],其在儿童中的过敏率高达13%[6]。随着植物基食品种类及大豆副产品的逐渐增加,大豆过敏的发病率也在不断上升[7]。据相关报道,引发大豆过敏反应的阈值水平在0.001 3~500 mg[8]。现阶段,食物过敏是第四大公共卫生问题[8-9],而大豆过敏是一种重要的食物过敏反应。食物过敏大多是由免疫球蛋白(immunoglobulin,Ig)E介导的速发型过敏反应,当过敏性人群二次接触过敏原时,会刺激人体产生一系列免疫性反应,其机理为过敏原特异性IgE与肥大细胞表面上的高亲和力IgE受体(receptor I for the Fc fragment of IgE,FcεRI)相交联[10],使细胞内已有的或新合成的白细胞介素(interleukin,IL)-3、IL-5、IL-13等细胞因子释放,并通过刺激嗜碱性粒细胞等其他炎症细胞激发过敏反应。由此引发皮肤、呼吸道及消化道症状,如皮疹、荨麻疹、哮喘、腹泻、腹痛等[11],严重时可导致过敏性休克[12]。
由于食品工业的高速发展及食品加工程度的不断深化,食物中的组分越来越复杂,其中微量过敏原成分的存在使得食物过敏的发生率不断增加。食物过敏主要发生在工业化国家[13],多数工业化国家均强制性要求商家将大豆、花生、牛奶、鸡蛋等主要食品过敏原在食品标签中有所显示[14]。目前,除对麸质的含量进行规范外,大多数过敏原的标识仅存在于定性阶段,即标明了“含有”或者“可能含有”[15]。当前,由于缺少对食品过敏的有效治疗手段,所以敏感人群要严格避免摄入含有一种或多种过敏原的食物。然而,大豆及其副产品广泛添加于许多素食和肉类食品中,通过饮食避免食物过敏变得较为困难。因此,对于大豆致敏蛋白特性的深入了解及研究快速、精确和标准化的过敏原检测方法具有重要的实际意义。
1 大豆主要致敏蛋白及结构特性
根据超速离心分类法,大豆蛋白可分为4 种主要蛋白质,分别为2S、7S、11S及15S球蛋白组分[15]。大豆中已有38 种过敏原被识别[16-18],根据致敏蛋白的组分含量及其致敏能力的差异,β-伴大豆球蛋白、大豆球蛋白、Gly m Bd 30K、Gly m Bd 28K被列为主要致敏成分[19]。
1.1 β-伴大豆球蛋白
β-伴大豆球蛋白属于贮藏蛋白,其含量约占大豆总蛋白的30%[20],分子质量约为210 ku,属于7S球蛋白。由α’(~71 ku)、α(~67 ku)和β(~50 ku)3 种亚基通过疏水相互作用及静电相互作用连接形成三聚体糖蛋白[21]。亚基α和α’由延伸区和核心区组成,其延伸区的氨基酸数量分别为125及141。而β亚基仅有一个核心区[15,22],其氨基酸数量为418。3 种亚基随机组合形成3 种同三聚体(如α3、α’3、β3)和7 种异三聚体(如αα’2、α2α’、αα’α2、α’2β、α’β2、α2β、αβ2),其中β3的立体图如图1所示[23]。研究发现这3 种亚基都有不同程度的致敏性,其中β-伴大豆球蛋白的α亚基能被23%的患者血清识别,并且这3 种亚基之间具有较高的同源性[24]。其中,对于核心区,α与α’的同源性为90.4%,α与β的同源性为76.2%,α’与β的同源性为75.5%[16-17];而α和α’之间的延伸区具有57.3%的序列同一性[25]。
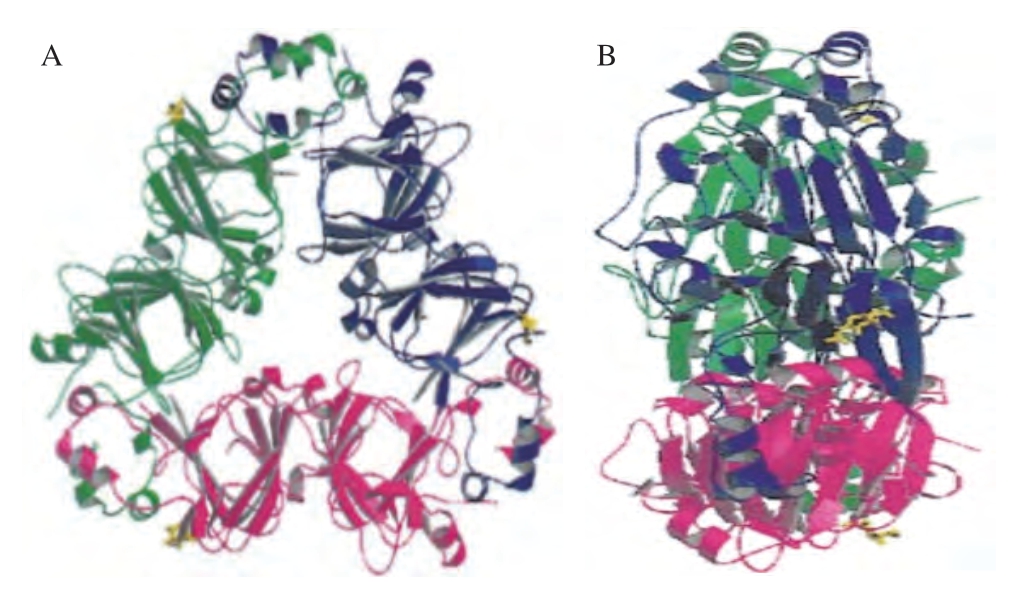
图1 β-伴大豆球蛋白β3的透视图[23]
Fig.1 Ribbon diagrams of β-conglycinin β3[23]
A.俯视图;B.侧视图(90°);图2同。
1.2 大豆球蛋白
大豆球蛋白也是一种贮藏蛋白,约占大豆总蛋白含量的19.5%~23.1%[18-19],其分子质量约为360 ku,属于11S球蛋白。大豆球蛋白由氢键连接的5 个主要亚基对组成,其主要亚基对根据氨基酸序列可以分为两组(组1包括A1aB1b、A1bB2、A2B1a;组2包括A3B4、A5A4B3)[26],每个亚基对的分子质量约60 ku。目前已知的大豆球蛋白酸性多肽链有6 种:A1a、A1b、A2、A3、A4和A5,其分子质量为35~40 ku;碱性多肽链有5种:B1a、B1b、B2、B3和B4,其分子质量均为22 ku。除了A5A4B3以外,其他亚基对均由1 个酸性A肽链和1 个碱性B肽链通过二硫键组成A-S-S-B单体形式[27]。研究表明,酸性多肽链与碱性多肽链的结合并不是随机的,而是形成独特的酸性-碱性对[28]。Badley等[29]利用电子显微镜和X射线散射技术,首次揭示了大豆球蛋白的四级结构,阐明大豆球蛋白的物理形状是一个低扁圆柱体,其尺寸为11.0 nm×11.0 nm×7.5 nm,其中两个三聚体位于另一个三聚体之上,从而形成大豆球蛋白六聚体。同时两个三聚体通过静电作用相互连接,而三聚体中的亚单元则主要通过疏水力结合。迄今为止,仅有含A3B4亚单位的大豆球蛋白同型六聚体被确定了晶体结构,如图2所示[30]。在不同的离子强度、pH环境及热处理条件下,大豆球蛋白可被解离为亚基、成分多肽和半分子形式,但是天然状态下大豆球蛋白的分子结构十分紧密,一般难以被酶解和催化[31]。针对致敏性而言,大豆球蛋白的致敏性弱于β-伴大豆球蛋白[24-25],其中大豆球蛋白碱性多肽链的致敏性较弱,而酸性多肽链的致敏性较强,原因是酸性多肽链与IgE、IgM、IgA有较强的结合活性。
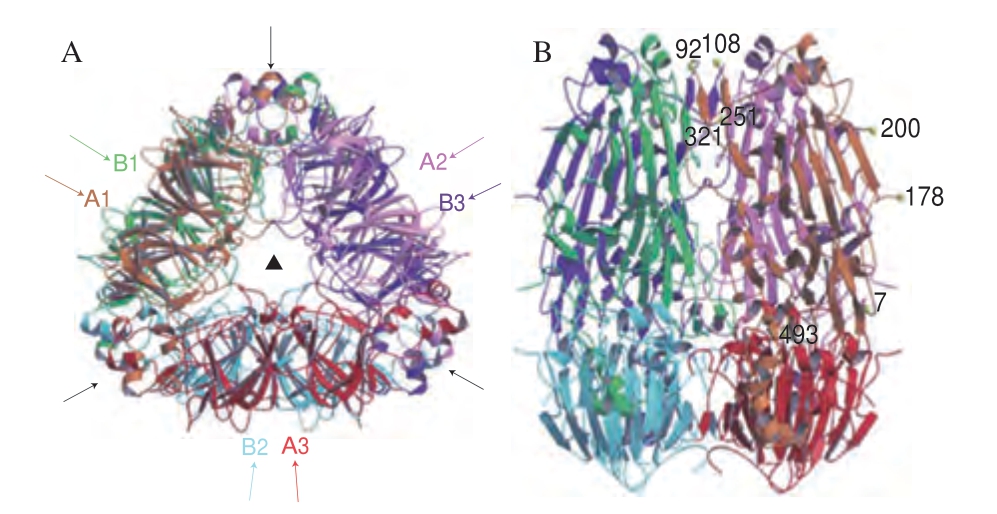
图2 大豆球蛋白A3B4的透视图[30]
Fig.2 Ribbon diagrams of glycinin A3B4[30]
1.3 Gly m Bd 30K
Gly m Bd 30K,又称P34,是一种半胱氨酸蛋白酶,广泛存在于大豆细胞液泡中[32]。Gly m Bd 30K是单体蛋白,其氨基酸数量为379 个,分子质量为34 ku,属于7S球蛋白,约占大豆总蛋白含量的1%[18],其结构如图3所示[33]。研究发现,66.5%的大豆过敏患者对Gly m Bd 30K识别并产生过敏反应,因此认为其属于大豆中的主要致敏蛋白[19,34]。同时,Gly m Bd 30K是一种糖蛋白,其N端170位氨基酸处是一个多糖链结合位点。研究表明,蛋白质的糖基化位置在其致敏性方面发挥重要作用[35-36],因此Gly m Bd 30K存在一定致敏性。
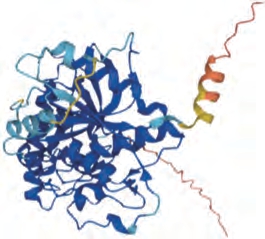
图3 Gly m Bd 30K的透视图[33]
Fig.3 Ribbon diagram of Gly m Bd 30K[33]
1.4 Gly m Bd 28K
Gly m Bd 28 K是由473 个氨基酸残基组成的糖蛋白[27-28],其分子质量为26 ku,等电点为6.1,主要存在于7S球蛋白中,约占大豆总蛋白含量的0.5%[37],其蛋白结构如图4所示[38]。23%的大豆过敏患者可以对Gly m Bd 28K产生过敏反应[34],其致敏表位最主要反映在其N端氨基酸序列:FHDDEGGDKKSPKSLFLMSSTR[19,38],其多糖结合位点位于多肽链20位天冬酰胺处,该多糖由甘露糖、N-乙酰氨基葡萄糖、木糖及海藻糖以物质的量比3∶2∶1∶1组成[39]。研究表明,去糖基化后Gly m Bd 28K的致敏性完全消失[18]。
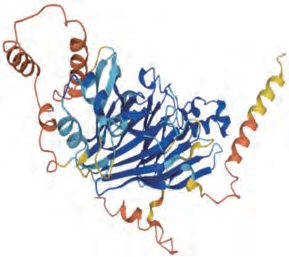
图4 Gly m Bd 28K的透视图[38]
Fig.4 Ribbon diagram of Gly m Bd 28K[38]
2 检测技术
根据识别物质的不同,目前食品过敏原的检测技术可分为基于蛋白水平和基于核酸水平的检测技术。基于蛋白质水平的检测技术包括酶联免疫吸附测定(enzymelinked immunosorbent assay,ELISA)、免疫印迹法(Western blotting)、免疫层析法、质谱法及生物传感器法;基于核酸水平的检测技术有实时定量聚合酶链式反应(quantitative real-time polymerase chain reaction,qPCR)、环介导等温扩增(loop-mediated isothermal amplification,LAMP)技术。本文主要介绍当前大豆过敏原检测方法的基本原理、优缺点及实际应用,为后续研究提供依据。
2.1 基于蛋白水平的检测技术
2.1.1 ELISA
ELISA基于抗原-抗体的特异性结合对过敏原进行免疫测定,通过间接指标对过敏原含量进行定性或定量检测,不需要复杂或昂贵的设备[40]。ELISA作为常见的免疫学检测技术,已广泛应用于大豆中主要抗原蛋白的检测[41]。ELISA根据固定抗原方法的不同,可分为直接法和间接法,其中间接法包括夹心法及竞争法,不同ELISA方法的原理示意图如图5所示。Xi Jun等[42]建立了一种基于自制的重组蛋白Gly m Bd 28K及单克隆抗体的竞争性ELISA法测定食品样品中的Gly m Bd 28K,其检测限为0.235 μg/L,平均回收率为96.73%。Ma Xi等[43]基于自制的单克隆抗体4B2,建立了竞争性ELISA法检测大豆球蛋白,其检测限为0.3 ng/mL,定量线性范围为0.3~11.2 ng/mL。Segura-Gil等[44]开发出可检测β-伴大豆球蛋白的两种检测方法,结果显示间接竞争ELISA法及夹心ELISA法的检测限分别为30 ng/mL及0.90 ng/mL,定量线性范围分别为10~3 000 ng/mL及2~15 ng/mL。Smirnova等[45]建立了检测食品中大豆原料的竞争性ELISA法,以大豆胰蛋白酶抑制剂为识别物质,该方法的检测时长为60 min,检测限为3.5 ng/mL,定量线性范围为7.7~110 ng/mL,研究结果证明该方法可用于检测肉类食品中的大豆过敏成分。夹心ELISA法检测灵敏度明显高于竞争性ELISA法,但更适合于未加工大豆蛋白的检测,而竞争性ELISA法则更适合检测加工后的大豆制品[46]。基于单克隆抗体所建立的ELISA法检测精准度高于基于多克隆抗体的ELISA法[47]。
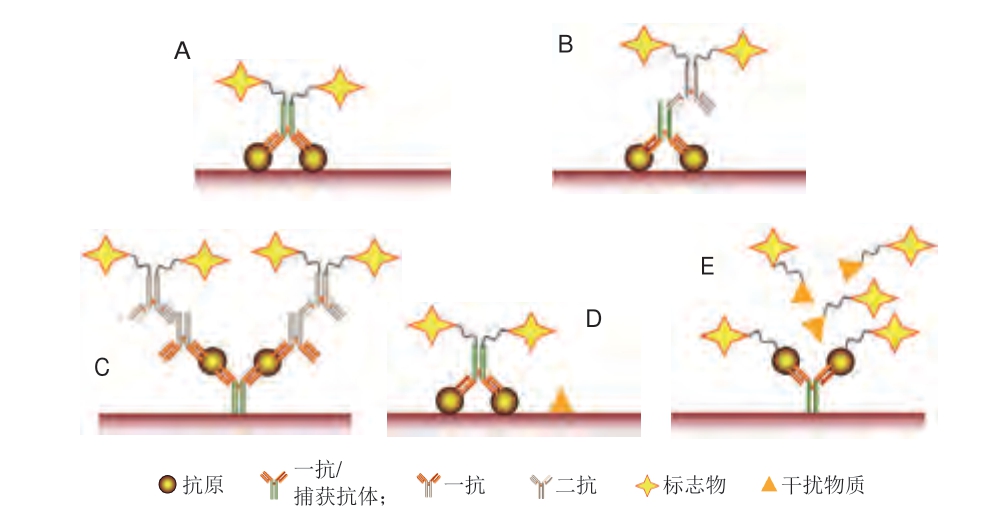
图5 ELISA的检测原理
Fig.5 Principle of enzyme-linked immunosorbent assay
A.直接ELISA法;B.间接ELISA法;C.夹心式ELISA法;D.含标记抗体的竞争性ELISA法;E.含标记抗原的竞争性ELISA法。
2.1.2 免疫印迹法
免疫印迹法又称蛋白质印迹法,是基于抗体的特异性来鉴定抗原的有效检测方法。首先进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfatepolyacrylamide gel electrophoresis,SDS-PAGE),随后将聚丙烯酰胺凝胶上的蛋白质样品电转移至聚偏二氟乙烯膜(polyvinylidene fluoride,PVDF)上。利用一抗作为“探针”,用标记的二抗进行“显色”,对样品进行检测与分析[48],免疫印迹法的具体步骤及原理如图6所示。Matsuo等[49]基于免疫印迹法,以IgE结合能力为指标,对比了转基因大豆及非转基因大豆的过敏原性,结果显示这两种大豆之间并无致敏性差异。免疫印迹法兼具电泳的高分辨力及免疫测定法的高特异性及敏感性等优点,可用于抗原的定性和半定量检测[50]。相比于ELISA,免疫印迹法的灵敏度较低,对检测样品中的大豆过敏原仅能进行定性或半定量检测,但是其可以追踪不同食物加工阶段产物中所有蛋白和肽段图谱。此外,免疫印迹法可以有效避免由于蛋白抑制剂的存在导致的检测结果假阴性现象[50]。
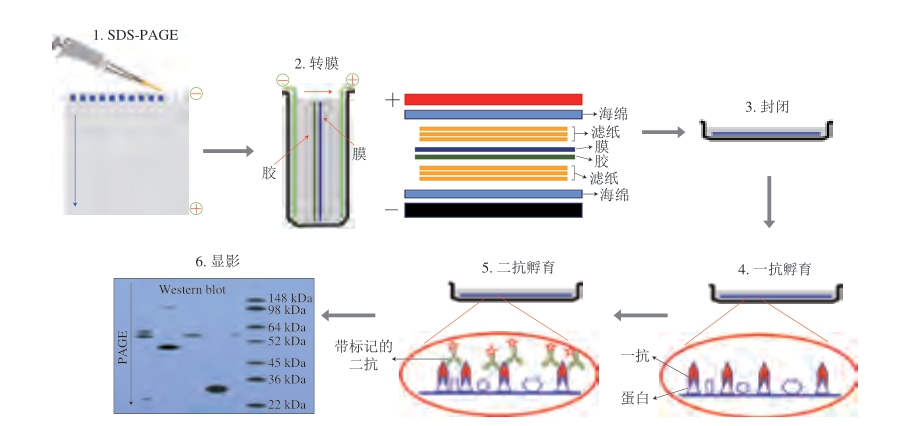
图6 免疫印迹法的检测原理
Fig.6 Principle of Western blotting
2.1.3 免疫层析法
免疫层析法基于抗原-抗体的特异性结合,首先将抗体预包被于硝化纤维素(nitrocellulose,NC)膜上,待测样品通过毛细作用涌动到预包被抗体区域时被捕获,使用酶标或胶体金作为检测标志物,从而得到可视化结果,以纤维素膜上显色条带及其颜色的深浅等作为评价指标,从而实现过敏原的定性或定量检测[48],检测原理如图7所示。Wang Yao等[51]建立了胶体金标记的试纸条并应用于奶粉中大豆球蛋白的检测,利用自制的多克隆抗体及胶体金标记的多克隆抗体,成功组装了可精准检测大豆球蛋白的试纸条,最低检测限为46.1 ng/mL,定量线性范围为50~3 200 ng/mL。Wang Yao等[52]利用胶体金标记的小鼠抗β-伴大豆球蛋白单克隆抗体和兔抗β-伴大豆球蛋白多克隆抗体,建立了基于夹心法的快速侧向流动胶体金免疫分析试纸条,以专门鉴定大豆过敏原β-伴大豆球蛋白,检测时间为10 min,检测限为1.66 mg/kg。该检测方法显示出对β-伴大豆球蛋白的高特异性,并且与其他食品过敏原没有交叉反应。该检测试纸条对奶粉样品中β-伴大豆球蛋白的检测范围在80.8%~89.2%之间。相比于ELISA法,免疫层析法虽然检测时间较短,但是其精准度较低。免疫层析法操作简单、用时较短,通过增加检测线(T线)可以进行高通量检测。为了有效提高免疫层析法的灵敏度,未来可以将单克隆抗体与新型材料标志物如荧光量子点相结合。
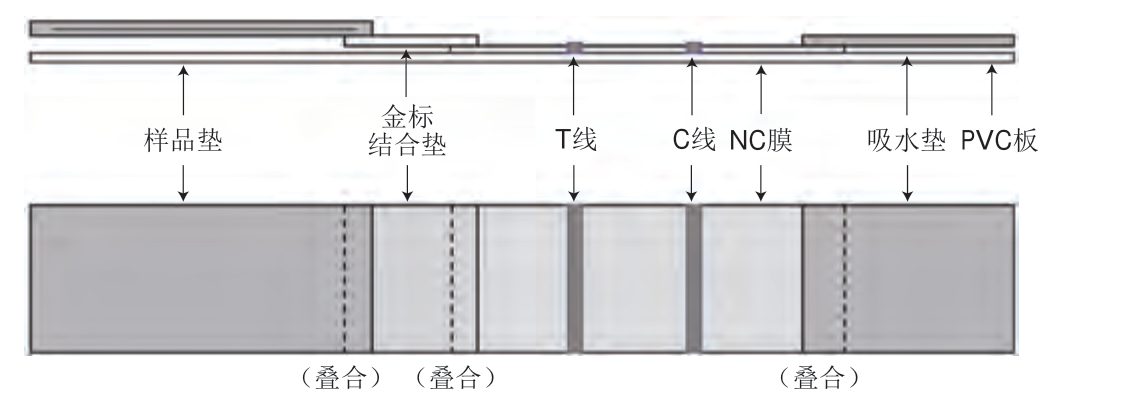
图7 免疫层析法的检测原理
Fig.7 Principle of immunochromatograpgy
T线.检测线;C线.质控线;PVC.聚氯乙烯(polyvinyl chloride)。
2.1.4 生物传感器
生物传感器通过生物识别元件识别并响应食物中的过敏原,再由换能器将其转化为定量的光电信号来实现检测[53],其工作原理如图8所示。根据换能器的不同,生物传感器可以分为光学生物传感器、电化学生物传感器及压电传感器三类。作为一类新的检测方法,它具有快速、灵敏度高、自动化程度高、实时监测等优点,近年来已被广泛应用于食物过敏原方面的检测。Sundhoro等[54]将分子印迹聚合物(molecularly imprinted polymers,MIPs)固定到丝网印刷电极上,并将其与电化学生物传感器相结合,以实现对大豆球蛋白精准、高效的检测,其检测限为0.1 mg/L。Wang Wei等[55]开发出无标记的芯片,用以检测Gly m Bd 30K在食品基质中的含量,其可在15 min内检测出1 mg/mL的Gly m Bd 30K。生物传感器技术兼具免疫检测技术及光电技术的优点,在大豆过敏原检测中,选用最佳生物传感器并扩大检测范围是未来的发展热点之一。此外,为了更好地检测大豆过敏原,高灵敏度、集成化、微型化及商业化的生物传感器也是未来研究的主要方向之一。
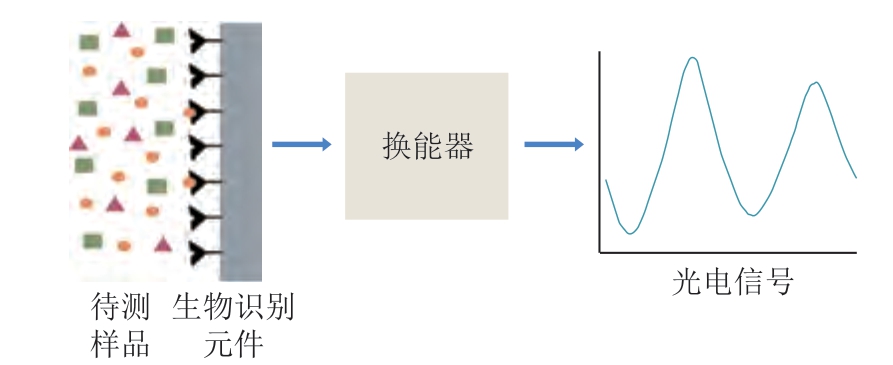
图8 生物传感器的检测原理
Fig.8 Principle of biosensor
2.1.5 质谱法
液相色谱串联质谱(liquid chromatography-tandem mass spectrometry,LC-MS/MS)法检测的基本原理是样品通过离子源从而被电离成不同带电粒子,利用加速电场使带电粒子进入质量分析器,接着在电场及磁场的双重作用下,将不同质荷比(m/z)的离子分离并计算其分子质量,最后通过计算机对蛋白质或肽段进行鉴定分析[39-40],其工作原理如图9所示。Chen Shimin等[56]成功建立质谱法,筛选出大豆中11 种过敏原的特征标识肽段,为食品中大豆过敏原的检测提供了技术支撑。Montowska等[57]基于LC-MS/MS法检测寿司中的大豆、牛奶及鸡蛋清3 种食物中过敏原的含量,结果显示大豆及鸡蛋清中过敏原的检测限为0.45%(m/m),牛奶中过敏原的检测限为0.14%(m/m)。Gu Shuqing等[58]成功建立了LC-MS/MS检测方法,对巧克力基质中含有的8 种过敏原进行多重检测,对牛奶、大豆、花生、坚果的检测限分别为0.2~0.4、1.0~4、2.5~4、1~3 μg/g,并且其加标回收率为60.1%~92.4%,表明所建立的检测方法有效且精准。质谱方法虽然克服了免疫学技术遇到的问题,即在食品加工处理后导致蛋白质的结构发生变化后,无法有效、精准地检测过敏原,但其需要使用昂贵的设备,维护成本很高,而且需要由训练有素的人员操作[58]。现阶段,由于质谱法具有检测灵敏度高、检测时间短、检测用量少及可进行分离鉴定等特点,已广泛应用于大豆过敏的检测中。
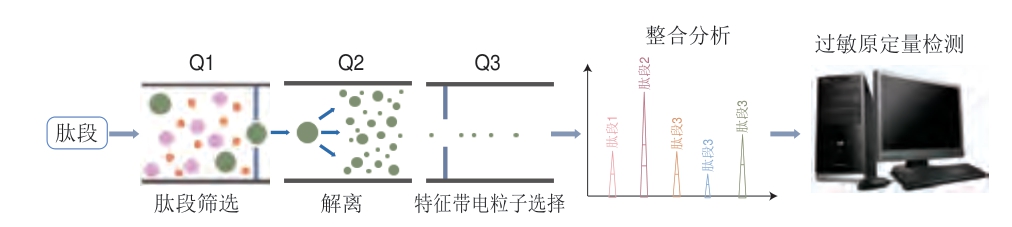
图9 LC-MS/MS的检测原理
Fig.9 Principle of liquid chromatography-tandem mass spectrometry
2.2 基于核酸水平的检测技术
2.2.1 qPCR
PCR技术是一种在体外将少量初始样品中的目的基因进行大量扩增的核酸合成技术。随着科学技术的发展,qPCR技术也开始在过敏原检测中有所应用[59-60]。随着荧光化学物质的发展,基于其荧光特性实时定量监测扩增过程即为qPCR技术,其利用体外大量扩增的核酸产物来进行样品检测。可在PCR体系中加入荧光基团,通过所产生的荧光信号变化来动态监测整个反应过程[46]。qPCR是在食品过敏原检测中应用最为广泛的一项基因水平检测技术。qPCR的特异性和灵敏度均优于普通PCR,在进行定性分析的同时,实现了在复杂食品基质中对多重过敏原的定量分析。兰海鸥[61]成功建立了qPCR方法,可精准检测出大豆、核桃及花生的过敏成分,其最低检测限均为0.01 ng/μL。张舒亚等[62]以大豆主要过敏蛋白P34为靶标,建立并优化了特异性强、灵敏度高的qPCR检测方法,最低检测限为10 mg/kg。Ladenburger等[63]成功研发出两种可应用于定量检测花生及大豆的竞争性qPCR检测方法,建立了针对其线粒体DNA序列的PCR引物及探针,其定量检测范围是1~100 mg/L,该检测方法可定量检测商业食品中微量的花生和大豆。然而利用PCR检测大豆过敏原容易出现假阳性或假阴性结果,因此PCR在大豆过敏原检测中的应用有所局限。
2.2.2 LAMP技术
LAMP技术是根据6~8 种不同的靶基因DNA序列开发设计出4~6 种特异性引物,60~65 ℃恒温下在链置换DNA聚合酶作用下进行大量扩增,短时间内可实现靶基因的特异性显著扩增[64]。LAMP的分析检测结果通过反应体系中样品颜色等变化进行评估。与传统的PCR和qPCR检测方法相比,LAMP具有许多优点,如恒温扩增、反应时间短、检测结果可通过肉眼判断等。该方法最主要的难点在于引物的设计,其直接决定了检测方法的准确性[49]。张舒亚等[65]成功设计6 条引物,建立了LAMP检测方法,可在60 ℃、40 min内成功检出大豆过敏原成分,灵敏度可达0.01%。Allgöwer等[66]利用多拷贝基因ORF160b的循环介导等温扩增引物,结合侧向流动免疫法评估LAMP在复杂食品基质中检测大豆成分的精准度,并且与基于抗体的侧向流动免疫法的检测结果进行比较。结果显示,LAMP-侧向流动免疫法可精准、重复地检测出3 种代表性基质(煮熟的香肠、巧克力、速溶番茄汤)中10 mg/kg的大豆成分,然而两种商业侧向流动免疫法阳性检测线的清晰显示需大豆成分含量在10~102 mg/kg之间,且可见度可能会受到食品基质的影响。因此,基于DNA的LAMP-侧向流动免疫法是一种操作简单的大豆致敏原检测方法,其显示出比商业侧向流动免疫法更高的灵敏度及特异性。
2.3 不同检测方法的对比
随着全球范围内食品多样性的增加,食品中可能含有的过敏原含量及种类不断上升,检测难度不断升高,总结和认识现有检测方法的优势与不足(表1),对于食品中不同过敏原的快速精准检测具有重要作用。
表1 不同检测方法的对比
Table 1 Comparison of different testing methods

分类检测方法优势不足蛋白质类ELISA操作相对简便,应用广泛易出现假阳性结果免疫层析法快速、高效检测过程复杂,检测时间长免疫印迹法检测时间较短实验结果差异性较大质谱法灵敏度高,可同时检测多种过敏原需要专业仪器及专业人员生物传感器法成本低、灵敏度高、可自动化检测对样品前处理要求较高核酸类qPCR灵敏度高、检测结果精准易出现假阳性结果LAMP技术检测效率高、检测速度快需要设计特异性引物
3 结 语
在全球范围内,食物过敏尚无特效疗法,但大豆过敏患者人数逐年升高。由于大豆具有较高的营养价值及良好的功能特性,且其在食品工业中应用广泛,所以明确大豆中的主要致敏蛋白及其结构,建立灵敏、高效的检测方法对于预防大豆过敏相当重要。目前应用的检测技术中,ELISA、质谱技术及qPCR检测方法应用最为广泛,但是检测结果容易受到食品加工技术及食品基质的影响。此外,食品加工过程中过敏原的分子结构变化、样品前处理中的有机溶剂残留等因素均会影响抗原-抗体的特异性结合,导致检测结果不准确。由于食品在加工、包装、运输过程中可能发生交叉污染,所以精准检测复杂食品基质中的隐藏过敏原成分极为重要。随着食品工业的快速发展,研究高通量且可现场检测的方法十分必要。在现有检测技术的基础上,应用新型生物传感器及纳米材料开发出便捷、高效、精准的过敏原检测技术极具实际意义。
[1] 周明明, 张明俊, 王俊, 等.大豆(Glycine max(L.)Merr.)致敏蛋白Gly m Bd 30K检测方法及低致敏优异种质鉴定[J].植物遗传资源学报,2021, 22(1): 149-156.DOI:10.13430/j.cnki.jpgr.20200618001.
[2] DUKE W W.Soy bean as a possible important source of allergy[J].Journal of Allergy, 1934, 5(3): 300-302.DOI:10.1016/S0021-8707(34)90228-8.
[3] World Health Organization.Risk assessment of food allergens part 1: review and validation of codex alimentarius priority allergen list through risk assessment: meeting report[M].Geneva: World Health Organization, 2000: 128.
[4] SAVAGE J H, BS A J K, MATSUI E C.The natural history of soy allergy[J].Journal of Allergy and Clinical Immunology, 2010, 125(3):683-686.DOI:10.1016/j.jaci.2009.12.994.
[5] EFSA Panel on Dietetic Products, Nutrition and Allergies.Opinion of the scientific panel on dietetic products, nutrition and allergies (NDA)on a request from the commission related to the tolerable upper intake level of fluoride[J].EFSA Journal, 2005, 3(3): 192.DOI:10.2903/j.efsa.2005.192.
[6] SAEED H, GAGNON C, COBER E, et al.Using patient serum to epitope map soybean glycinins reveals common epitopes shared with many legumes and tree nuts[J].Molecular Immunology, 2016, 70:125-133.DOI:10.1016/j.molimm.2015.12.008.
[7] RIASCOS J J, WEISSINGER S M, WEISSINGER A K, et al.The seed biotinylated protein of soybean (Glycine max): a boiling-resistant new allergen (Gly m 7) with the capacity to induce IgE-mediated allergic responses[J].Journal of Agricultural and Food Chemistry,2016, 64(19): 3890-3900.DOI:10.1021/acs.jafc.5b05873.
[8] AMPONSAH A, NAYAK B.Evaluation of the efficiency of three extraction conditions for the immunochemical detection of allergenic soy proteins in different food matrices[J].Journal of the Science of Food and Agriculture, 2018, 98(6): 2378-2384.DOI:10.1002/jsfa.8729.
[9] KHEDRI M, RAMEZANI M, RAFATPANAH H, et al.Detection of food-born allergens with aptamer-based biosensors[J].TrAC Trends in Analytical Chemistry, 2018, 103: 126-136.DOI:10.1016/j.trac.2018.04.001.
[10] DE JONG N W, WICHERS H J.Update on nutrition and food allergy[J].Nutrients, 2022, 14(10): 2137.DOI:10.3390/nu14102137.
[11] ZHOU Jinru, QI Qinqin, WANG Chong, et al.Surface plasmon resonance (SPR) biosensors for food allergen detection in food matrices[J].Biosensors and Bioelectronics, 2019, 142: 111449.DOI:10.1016/j.bios.2019.111449.
[12] 毕源, 周忻, 孙娜, 等.两种方法评价食品过敏原潜在致敏性的对比分析[J].食品科学, 2013, 34(15): 313-317.DOI:10.7506/spkx1002-6630-201315065.
[13] PILOLLI R, NITRIDE C, GILLARD N, et al.Critical review on proteotypic peptide marker tracing for six allergenic ingredients in incurred foods by mass spectrometry[J].Food Research International,2019, 128: 108747.DOI:10.1016/j.foodres.2019.108747.
[14] 周淑红.国外关于食品过敏标签的现状及启示[J].世界农业,2007(6): 67-68.DOI:10.3969/j.issn.1002-4433.2007.06.022.
[15] SUI X, ZHANG T, JIANG L.Soy protein: molecular structure revisited and recent advances in processing technologies[J].Annual Review of Food Science and Technology, 2021, 12(1): 119-147.DOI:10.1146/annurev-food-062220-104405.
[16] BATISTA R, MARTINS I, JENÖ P, et al.A Proteomic study to identify soya allergens-the human response to transgenic versus non-transgenic soya samples[J].International Archives of Allergy and Immunology,2007, 144(1): 29-38.DOI:10.1159/000102611.
[17] L’HOCINE L, BOYE J I.Allergenicity of soybean: new developments in identification of allergenic proteins, crossreactivities and hypoallergenization technologies[J].Critical Reviews in Food Science and Nutrition, 2007, 47(2): 127-143.DOI:10.1080/10408390600626487.
[18] 祖琴琴, 华萍, 龚育清, 等.基于食品物理加工技术对大豆过敏原的影响[J].食品工业科技, 2014, 35(5): 360-364.DOI:10.13386/j.issn1002-0306.2014.05.064.
[19] OGAWA T, BANDO N, TSUJI H, et al.Investigation of the IgEbinding proteins in soybeans by immunoblotting with the sera of the soybean-sensitive patients with atopic dermatitis[J].Journal of Nutritional Science and Vitaminology, 1991, 37(6): 555-565.DOI:10.3177/jnsv.37.555.
[20] 朱婷伟, 布冠好, 陈复生, 等.β-伴大豆球蛋白间接竞争ELISA检测方法建立[J].粮食与油脂, 2014, 27(9): 63-66.DOI:10.3969/j.issn.1008-9578.2014.09.017.
[21] HOU H J, CHANG K C.Structural characteristics of purified β-conglycinin from soybeans stored under four conditions[J].Journal of Agricultural and Food Chemistry, 2004, 52(26): 7931-7937.DOI:10.1021/jf049430p.
[22] 于寒松, 单单单, 吕博, 等.大豆β-伴大豆球蛋白和大豆球蛋白的研究现状及未来发展趋势[J/OL].吉林农业大学学报, 2021:1-19.[2023-06-14].http://kns.cnki.net/kcms/detail/22.1100.S.20210415.1437.003.html.
[23] MARUYAMA N, ADACHI M, TAKAHASHI K, et al.Crystal structures of recombinant and native soybean β-conglycinin β homotrimers: crystal structures of soybean β-conglycinin β homotrimers[J].European Journal of Biochemistry, 2001, 268(12):3595-3604.DOI:10.1046/j.1432-1327.2001.02268.x.
[24] 王梦莉, 高美须, 姜小燕, 等.大豆过敏原在低盐固态酱油酿造过程中的降解规律[J].食品工业科技, 2020, 41(24): 197-202.DOI:10.13386/j.issn1002-0306.2020120240.
[25] MARUYAMA N, KATSUBE T, WADA Y, et al.The roles of the N-linked glycans and extension regions of soybean β-conglycinin in folding, assembly and structural features[J].European Journal of Biochemistry, 1998, 282(2): 854-862.DOI:10.1046/j.1432-1327.1998.2580854.x.
[26] MARUYAMA N, MATSUOKA Y, YOKOYAMA K, et al.A vacuolar sorting receptor-independent sorting mechanism for storage vacuoles in soybean seeds[J].Scientific Reports, 2018, 8(1): 1108.DOI:10.1038/s41598-017-18697-w.
[27] SINGH A, MEENA M, KUMAR D, et al.Structural and functional analysis of various globulin proteins from soy seed[J].Critical Reviews in Food Science and Nutrition, 2021, 55(11): 1491-1502.DOI:10.1080/10408398.2012.700340.
[28] SCOTT M P, JUNG R, MUNTZ K, et al.A protease responsible for post-translational cleavage of a conserved Asn-Gly linkage in glycinin,the major seed storage protein of soybean[J].Proceedings of the National Academy of Sciences, 1992, 89(2): 658-662.DOI:10.1073/pnas.89.2.658.
[29] BADLEY R A, ATKINSON D, HAUSER H, et al.The structure,physical and chemical properties of the soy bean protein glycinin[J].Biochimica et Biophysica Acta (BBA)-Protein Structure, 1975, 412(2):214-228.DOI:10.1016/0005-2795(75)90036-7.
[30] ADACHI M, KANAMORI J, MASUDA T, et al.Crystal structure of soybean 11S globulin: glycinin A3B4 homohexamer[J].Proceedings of the National Academy of Sciences of the United States of America,2003, 100(12): 7390-7400.DOI:10.1073/pnas.0832158100.
[31] 王梦莉.大豆蛋白过敏原在酱油酿造和发芽过程中的降解规律[D].北京: 中国农业科学院, 2020: 3-4.
[32] KALINSKI A, WEISEMANN J M, MATTHEWS B F, et al.Molecular cloning of a protein associated with soybean seed oil bodies that is similar to thiol proteases of the papain family[J].Journal of Biological Chemistry, 1990, 265(23): 13843-13848.DOI:10.1016/0008-6215(90)80036-3.
[33] JOSEPH L M, HYMOWITZ T, SCHMIDT M A, et al.Evaluation of glycine germplasm for nulls of the immunodominant allergen P34/Gly m Bd 30K[J].Crop Science, 2006, 46(4): 1755-1763.DOI:10.2135/cropsci2005.12-0500.
[34] SAMOTO M, FUKUDA Y, TAKAHASHI K, et al.Substantially complete removal of three major allergenic soybean proteins (Gly m Bd 30K, Gly m Bd 28K, and the α-subunit of conglycinin) from soy protein by using a mutant soybean, Tohoku 124[J].Bioscience,Biotechnology, and Biochemistry, 1997, 61(12): 2148-2150.DOI:10.1271/bbb.61.2148.
[35] BANDO N, TSUJI H, YAMANISHI R, et al.Identification of the glycosylation site of a major soybean allergen, Gly m Bd 30K[J].Bioscience, Biotechnology, and Biochemistry, 1996, 60(2): 347-348.DOI:10.1271/bbb.60.347.
[36] 布冠好, 张楠, 陈复生.大豆蛋白-木糖复合物的抗原性、致敏性及结构特性研究[J].现代食品科技, 2015, 31(11): 33-38; 91.DOI:10.13982/j.mfst.1673-9078.2015.11.006.
[37] XIANG Ping, HAAS E J, ZEECE M G, et al.C-Terminal 23 kDa polypeptide of soybean Gly m Bd 28 K is a potential allergen[J].Planta, 2004, 220(1): 56-63.DOI:10.1007/s00425-004-1313-7.
[38] TSUJI H, HIEMORI M, KIMOTO M, et al.Cloning of cDNA encoding a soybean allergen, Gly m Bd 28K[J].Biochimica et Biophysica Acta (BBA)-Gene Structure and Expression, 2001,1518(1/2): 178-182.DOI:10.1016/S0167-4781(00)00310-9.
[39] TSUJI H, BANDO N, HIEMORI M, et al.Purification and characterization of soybean allergen Gly m Bd 28K[J].Bioscience, Biotechnology, and Biochemistry, 1997, 61(6): 942-947.DOI:10.1271/bbb.61.942.
[40] KONSTANTINOU G N.Enzyme-linked immunosorbent assay(ELISA)[M].New York: Springer, 1592: 79-94.
[41] 宁亚维, 杨正, 马梦戈, 等.食品中常见过敏原及检测技术研究进展[J].食品科学, 2021, 42(15): 319-328.DOI:10.7506/spkx1002-6630-20200614-191.
[42] XI Jun, SHI Qiaoqiao.Development of an indirect competitive ELISA kit for the detection of soybean allergenic protein Gly m Bd 28K[J].Food Analytical Methods, 2016, 9(11): 2998-3005.DOI:10.1007/s12161-016-0493-7.
[43] MA Xi, SUN Peng, HE Pingli, et al.Development of monoclonal antibodies and a competitive ELISA detection method for glycinin,an allergen in soybean[J].Food Chemistry, 2010, 121(2): 546-551.DOI:10.1016/j.foodchem.2009.12.045.
[44] SEGURA-GIL I, BLÁZQUEZ-SORO A, GALÁN-MALO P, et al.Development of sandwich and competitive ELISA formats to determine β-conglycinin: evaluation of their performance to detect soy in processed food[J].Food Control, 2019, 103: 78-85.DOI:10.1016/j.foodcont.2019.03.035.
[45] SMIRNOVA N I, ZVEREVA E A, ZHERDEV A V, et al.Development of immunoenzyme assay for detection of soybean raw material in food products[J].Applied Biochemistry and Microbiology, 2020, 56(4):483-487.DOI:10.1134/S0003683820040158.
[46] 刘宾.大豆主要致敏原的免疫检测研究[D].北京: 中国农业科学院,2011: 11-13.
[47] 黄玉霞, 梁金玲, WANG L, 等.食品中花生过敏原及其检测方法的研究进展[J].食品工业科技, 2018, 39(22): 314-318; 327.
[48] 杨阳, 何欣蓉, 何少贵, 等.食品中过敏原及其检测方法的研究进展[J].食品安全质量检测学报, 2021, 12(14): 5497-5506.DOI:10.19812/j.cnki.jfsq11-5956/ts.2021.14.001.
[49] MATSUO A, MATSUSHITA K, FUKUZUMI A, et al.Comparison of various soybean allergen levels in genetically and non-genetically modified soybeans[J].Foods, 2020, 9(4): 522.DOI:10.3390/foods9040522.
[50] 布冠好, 朱婷伟, 陈复生, 等.大豆球蛋白间接竞争ELISA检测方法的建立[J].河南工业大学学报(自然科学版), 2014, 35(4): 1-5; 11.DOI:10.16433/j.cnki.issn1673-2383.2014.04.005.
[51] WANG Yao, DENG Ruiguang, ZHANG Gaiping, et al.Rapid and sensitive detection of the food allergen glycinin in powdered milk using a lateral flow colloidal gold immunoassay strip test[J].Journal of Agricultural and Food Chemistry, 2015, 63(8): 2172-2178.DOI:10.1021/jf5052128.
[52] WANG Yao, LI Zhaozhou, PEI Yafeng, et al.Establishment of a lateral flow colloidal gold immunoassay strip for the rapid detection of soybean allergen β-conglycinin[J].Food Analytical Methods, 2017,10(7): 2429-2435.DOI:10.1007/s12161-017-0800-y.
[53] 叶茂, 李欣, 武涌, 等.生物传感器检测食物过敏原的研究进展[J].食品工业科技, 2021, 42(18): 397-406.DOI:10.13386/j.issn1002-0306.2020080167.
[54] SUNDHORO M, AGNIHOTRA S R, AMBERGER B, et al.An electrochemical molecularly imprinted polymer sensor for rapid and selective food allergen detection[J].Food Chemistry, 2021, 344:128648.DOI:10.1016/j.foodchem.2020.128648.
[55] WANG Wei, ZHU Xudong, TENG Shuang, et al.Label-free biochips for rapid detection of soybean allergen GlymBd 30K (P34) in foods[J].Tropical Journal of Pharmaceutical Research, 2017, 16(4): 755-760.DOI:10.4314/tjpr.v16i4.3.
[56] CHEN Shimin, YANG C, DOWNS M.Targeted mass spectrometry quantification of total soy protein residues from commercially processed ingredients for food allergen management[J].Journal of Proteomics, 2021,239: 104194.DOI:10.1016/j.jprot.2021.104194.
[57] MONTOWSKA M, FORNAL E, PIĄTEK M, et al.Mass spectrometry detection of protein allergenic additives in emulsion-type pork sausages[J].Food Control, 2019, 104: 122-131.DOI:10.1016/j.foodcont.2019.04.022.
[58] GU Shuqing, CHEN Niannian, ZHOU Yao, et al.A rapid solidphase extraction combined with liquid chromatography-tandem mass spectrometry for simultaneous screening of multiple allergens in chocolates[J].Food Control, 2018, 84: 89-96.DOI:10.1016/j.foodcont.2017.07.033.
[59] DE LA CRUZ S, LÓPEZ-CALLEJA I, MARTÍN R, et al.Recent advances in the detection of allergens in foods[J].Methods in Molecular Biology, 2017, 1592: 263-295.DOI:10.1007/978-1-4939-6925-8_20.
[60] 丁博群, 刘珊娜.荧光定量PCR技术在食品快速检测中的应用[J].食品工业科技, 2021, 42(7): 366-373.DOI:10.13386/j.issn1002-0306.2020050185.
[61] 兰海鸥.大豆、核桃、花生过敏原基因三重实时荧光检测方法的建立及应用[D].兰州: 西北民族大学, 2020: 38-48.
[62] 张舒亚, 于翠, 宋青, 等.食品过敏原大豆P34蛋白基因的实时荧光PCR检测[J].中国油料作物学报, 2012, 34(6): 661-665.
[63] LADENBURGER E M, DEHMER M, GRÜNBERG R, et al.Highly sensitive matrix-independent quantification of major food allergens peanut and soy by competitive real-time PCR targeting mitochondrial DNA[J].Journal of AOAC International, 2018, 101(1): 170-184.DOI:10.5740/jaoacint.17-0406.
[64] SHEU S C, TSOU P C, LIEN Y Y, et al.Development of loopmediated isothermal amplification (LAMP) assays for the rapid detection of allergic peanut in processed food[J].Food Chemistry,2018, 257: 67-74.DOI:10.1016/j.foodchem.2018.02.124.
[65] 张舒亚, 李富威, 于翠, 等.环介导等温扩增法检测食品过敏原大豆成分[J].食品安全质量检测学报, 2013, 4(2): 451-456.DOI:10.19812/j.cnki.jfsq11-5956/ts.2013.02.028.
[66] ALLGÖWER S M, HARTMANN C A, LIPINSKI C, et al.LAMPLFD based on isothermal amplification of multicopy gene ORF160b:applicability for highly sensitive low-tech screening of allergenic soybean (Glycine max) in food[J].Foods, 2020, 9(12): 1741.DOI:10.3390/FOODS9121741.