食醋具有悠久的历史,目前已发展成为世界各国人民餐桌上必不可少的调味品。食醋的酿造主要依赖于微生物的发酵作用,微生物经过特殊的生化活动将富含糖分的原料转化为乙酸、乳酸等有机酸,并伴随多种风味物质和功能性成分的生成,这造就了食醋独特的风味[1]。
中国传统食醋的发酵是一个多菌种参与下的复杂化学变化过程,发酵体系(醋醅)中的微生物可能来自原料、曲、种子以及自然环境,多种微生物共同形成稳定的群落结构是保证食醋品质的基础[2]。然而,自然接种、开放式的发酵工艺不利于得到品质稳定的食醋产品,为实现食醋产业的转型与升级,需要对传统发酵模式进行改良。醋醅中丰富的微生物群落是形成食醋独特风味品质最关键的影响因素,研究其群落结构、功能及群落成员间的互作关系对明晰发酵机理和有效调控发酵进程具有重要意义。
近年来,学者们针对食醋中微生物群落的结构和演替规律、主要酿造微生物的功能等方面开展了大量的研究工作,有助于初步认识发酵过程中微生物所扮演的角色,但是推动如此复杂的生物群体向特定方向演替的动力以及群体成员间的联系对发酵结果产生的影响仍不明确[3]。为此,有关食醋中微生物相互作用关系的研究逐渐成为热点。笔者认为,发酵体系内微生物的代谢作用及一系列基于代谢产物的种间互作关系是形成食醋优良风味的关键,利用微生物的相互作用关系对食醋品质进行定向调控是食醋产业转型升级的重要发展方向。本文以传统食醋发酵体系中的关键微生物为研究对象,总结了传统发酵食醋中微生物群落演替规律以及核心微生物间相互作用关系的研究进展(图1),并为该领域未来的研究方向提出一些建议。以期从新的角度更为全面地揭示微生物对发酵过程的影响,同时希望能够对微生物群落定向调控技术、合成微生物群落技术等手段的发展和产业化应用提供参考。
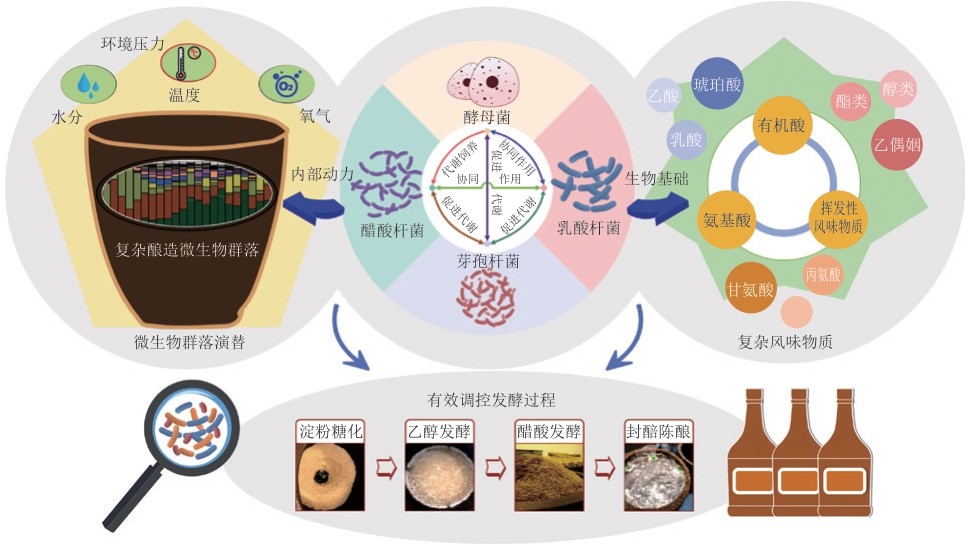
图1 传统食醋发酵体系中微生物群落及相互作用关系
Fig.1 Microbial communities and their interaction in traditional vinegar fermentation process
1 传统发酵食醋中微生物多样性及演替规律
对传统发酵食醋中微生物群落结构的研究有助于了解微生物间相互作用关系,明确微生物在发酵过程中所发挥的作用,对于改进生产工艺。提高生产效率以及新技术的研发和应用具有重要意义。近年来,对传统食醋发酵过程中微生物群落结构的研究随时间的推移愈发深入。
1.1 传统发酵食醋中微生物群落的基本结构
食醋的酿造是由多种微生物共同参与的生物转化过程。随着发酵的进行,微生物不断生长、繁殖,伴随着微生物与环境、微生物与微生物之间复杂的相互作用,最终自发形成稳定的群落结构,同时产生大量的风味物质和功能因子[4]。传统发酵食醋粗放式多菌种混合发酵的工艺特点使得发酵过程中微生物的种类更加多样,要探究微生物的相互作用关系对发酵的影响,首先要从解析微生物群落结构开始,这有助于有效定位参与食醋发酵过程的主要功能微生物。
近年来,随着分子生物学、分子生态学等先进技术的发展,有关食醋中微生物群落的研究愈发丰富。为从整体上把握相关文献的数量变化及时序规律,本文在Web of Science核心数据库中按照TS=(((“*vinegar*”)NOT(“wood-vinegar”)AND(“*bacteria*”))OR((“*vinegar*”)NOT(“woodvinegar”)AND(“*bacterial*”))OR((“*vinegar*”)NOT(“wood-vinegar”)AND(“*microbe*”))OR((“*vinegar*”)NOT(“wood-vinegar”)AND(“*microbiota*”)))进行高级检索,时间跨度选择“2011—2021”,最终共得到591 篇有关食醋中微生物群落的出版文献,分别通过Origin和CiteSpace V软件对检索结果进行时序数量统计和关键词共现分析(图2)。
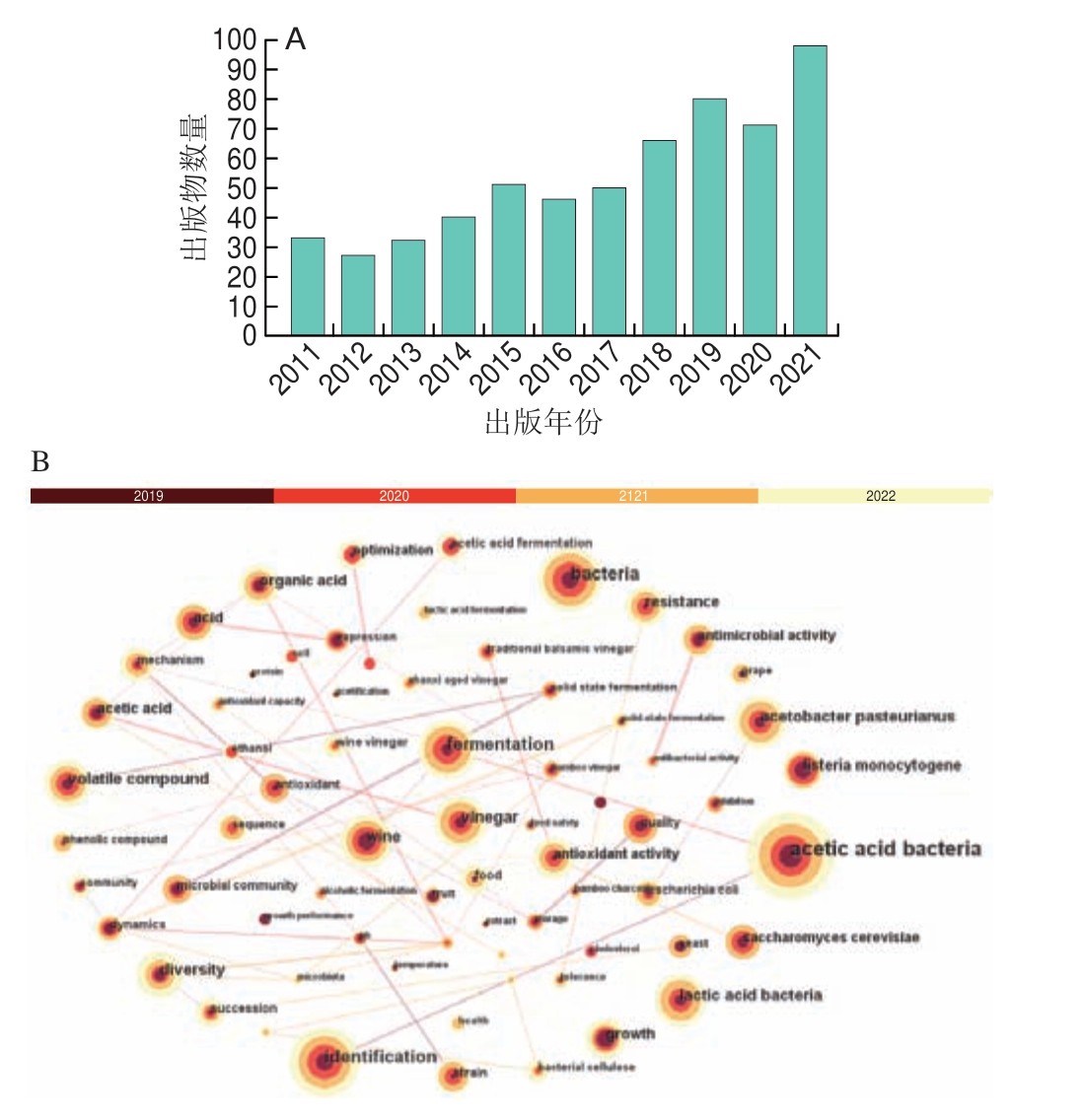
图2 传统发酵食醋中微生物群落相关研究发文数量趋势图(A)及关键词共现图(B)
Fig.2 Annual trend in the number of research papers (A) about and keywords co-occurrence map (B) of microbial communities in traditional fermented vinegar
某一研究领域在特定时间段内研究热度的变化可以通过发文数量的变化直观地体现。由图2A可以看出,相关研究数量在整体上呈现逐年递增的趋势,近2 年发文量保持着较高水平,说明对于该领域的研究仍存在较大发展空间;在关键词共现图中,结点越大则该关键词的词频越高,由图2B可知,该领域近年来的研究热点主要包括食醋中微生物的鉴定与定量、微生物群落的多样性及演替规律以及发酵微生物对发酵过程的影响等。在对前人研究成果进行充分学习和整理的基础上,本文对几种代表性食醋中的主要微生物进行了总结(表1)。
表1 传统发酵食醋中的主要微生物
Table 1 Major microbes in traditional fermented vinegar

传统发酵食醋 主要微生物 参考文献山西老陈醋真菌:Saccharomyces、Saccharomycopsis、Alternaria细菌:Acetobacter、Lactobacillus、Weissella、Streptococcus、Pantoea、Pediococcus、Lactococcus、Komagataeibacter、Kroppenstedtia[5-8]镇江香醋真菌:Aspergillus、Alternaria、Cryptococcus、Rhodotorula、Debaryomyces、Sporobolomyces、Candida、Saccharomyces细菌:Acetobacter、Lactobacillus[9-10]四川麸醋 真菌:Aspergillus、Penicillium、Saccharomyces、Saccharomycopsis、Issatchenkia细菌:Acetobacter、Lactobacillus、Gluconacetobacter [11]福建红曲醋 真菌:Saccharomycopsis、Sterigmatomyces、Yarrowia细菌:Acetobacter、Lactobacillus [12-13]天津独流老醋 真菌:Aspergillus、Saccharomycopsis、Pichia细菌:Acetobacter、Lactobacillus、Gluconacetobacter、Nostoc [14]凉州熏醋 真菌:Aspergillus、Alternaria、Saccharomyces细菌:Acetobacter、Lactobacillus [15]
如表1 所示,在传统发酵食醋中占主导地位的细菌为醋酸杆菌属(A c e t o b a c t e r)和乳酸杆菌属(Lactobacillus),发酵初期醋酸杆菌的丰度一般较低(5%~8%),而由于乳酸杆菌多来自于酒醪,在发酵初期大多保持着较高的丰度(30%~90%),随发酵的进行,醋酸杆菌的种群数量快速上升并最终保持较高水平,乳酸杆菌种群数量的变化趋势则在不同种类食醋中呈现出一定的差异性,醋酸杆菌和乳酸杆菌在达到最大丰度时的占比范围分别为30%~85%和50%~90%[7,9-10,15]。而在传统发酵食醋中主要的真菌种类则存在较大差异,例如,山西老陈醋和镇江香醋酿造过程中优势真菌属为酵母菌属(Saccharomyces),四川麸醋和天津独流陈醋中曲霉属(Aspergillus)居于主导地位,而凉州熏醋酿造过程中的优势真菌属则为链格孢属(Alternaria),这可能是地理气候、酿造原料和工艺等因素的差异所导致[16]。
深入了解发酵过程中微生物群落结构的变化规律有助于明晰核心微生物在发酵体系中所扮演的角色,对于定向调控食醋风味和保障食醋品质都具有重要意义。而山西老陈醋、镇江香醋作为中国传统醋的杰出代表,在该方面的研究较为丰富。
1.2 山西老陈醋中微生物多样性及演替规律
山西老陈醋作为传统发酵食醋的代表之一,其酿制过程一般涉及制曲、淀粉糖化、乙醇发酵、醋酸发酵4 个主要阶段,在对山西老陈醋微生物群落的研究过程中,最先建立的是对大曲中微生物群落结构的认识。Mucor、Absidia是大曲中的优势霉菌,主要负责酿制过程中淀粉、蛋白质等生物大分子的水解;Candida、Hansenula、Saccharomyces等酵母菌则与大曲产酯类和醇类的功能有关;醋酸杆菌、乳酸杆菌和芽孢杆菌是大曲中的主要细菌,能够产生大量的有机酸、氨基酸和酯类物质,具有增强食醋风味和调节食醋口感等作用[17]。
随着研究的深入,山西老陈醋酿制过程中微生物群落的结构和演替规律得以揭示。有研究者采用变性梯度凝胶电泳(denaturing gradient gel electrophoresis,DGGE)研究山西老陈醋大曲及其他发酵阶段微生物群落的多样性和动态演替规律,发现大曲中部分真菌如Streptomyces、Eurotium、Monascus、Pichia和Bacillus、Staphylococcus等在乙醇发酵阶段消失,Weissella、Lactobacillus、Streptococcus、Saccharomyces在乙醇发酵后期居于主导地位。随着发酵的进行,Weissella等微生物转向消亡,而Acetobacter、Lactobacillus、Saccharomycopsis、Alternaria在醋酸发酵阶段保持了较高丰度[6]。随着高通量测序技术和组学技术在发酵领域的应用,山西老陈醋中微生物群落的演替规律及其与风味物质的关系愈发明确。山西老陈醋醋酸发酵过程可分为3 个阶段(早期:第0~4天;中期:第5~21天;后期:第22~26天)。在早期,Pantoea、Pediococcus、Lactococcus、Rhizobium的数量显著增加,且主要与发酵过程中体系内的醇、醛、酮、酯等挥发性物质的含量有关;在中期,Lactobacillus成为优势菌,乳酸杆菌的存在导致体系内乳酸含量迅速上升;当发酵进行至后期时,乳酸杆菌数量显著减少,Acetobacter、Komagataeibacter、Kroppenstedtia居于主导地位,促进了食醋中有机酸特别是乙酸的积累以及醛类、酯类、乙偶姻等风味物质的生成。值得关注的是,相较于采用DGGE方法所得到的检测结果,研究者通过第2代测序技术首次在醋酸发酵阶段发现Lactococcus和Komagataeibacter[7],说明采用传统纯培养技术探索发酵过程中菌群结构仍存在一定局限性,随着第2代测序技术的发展,传统发酵食醋中微生物群落的结构和演替规律将被更为全面地揭示。山西老陈醋不同发酵阶段微生物群落的演替规律及主要微生物所占比例如图3所示。
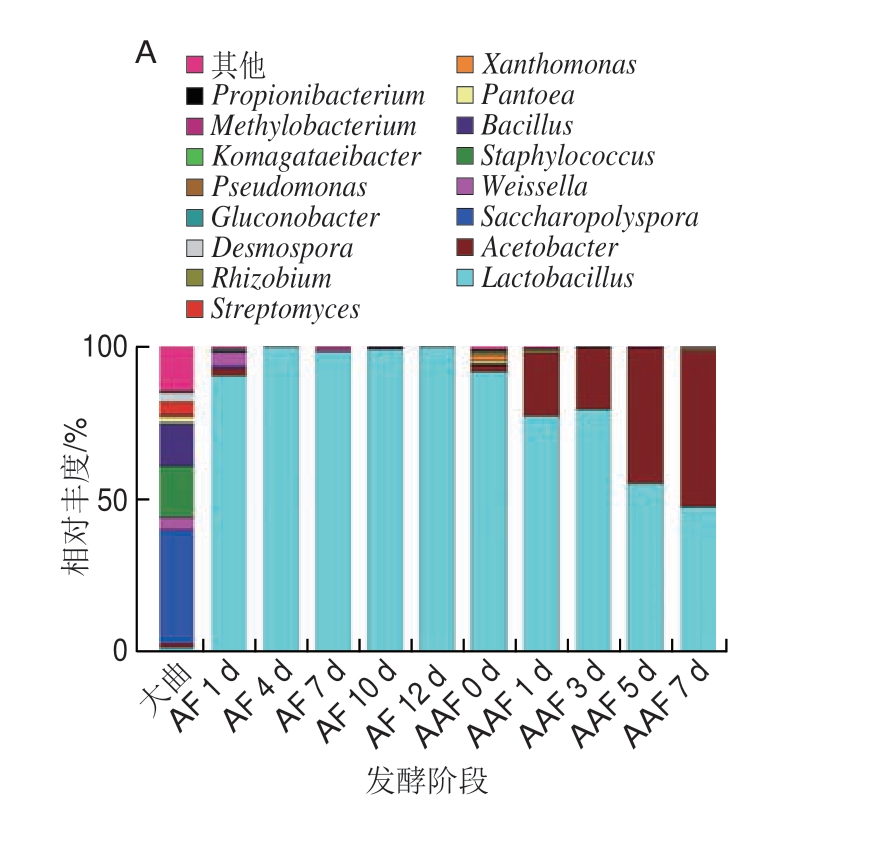
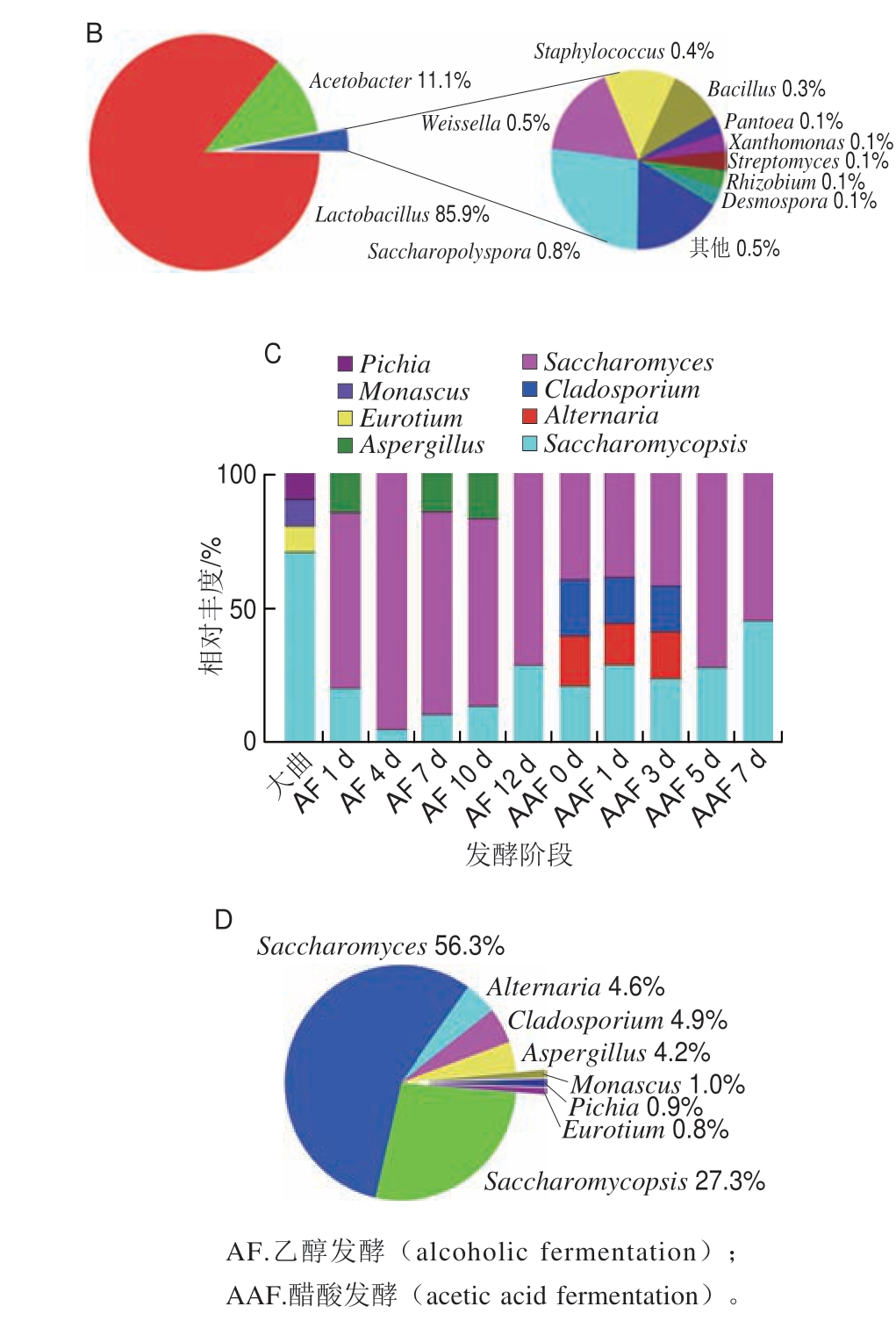
图3 山西老陈醋不同发酵阶段微生物群落的演替规律(A、C)及主要微生物所占比例(B、D)[8]
Fig.3 Succession of microbial community in different fermentation stages of Shanxi aged vinegar (A and C) and proportion of major microorganisms (B and D)[8]
1.3 镇江香醋中微生物多样性及演替规律
镇江香醋是我国最具代表性的四大名醋之一,其酿制过程主要采用固态分层发酵工艺,成品经陈酿后具有香气浓郁、酸而不涩的特点[18]。早期对香醋中微生物群落的研究依赖于纯培养技术,但由于受到培养条件、种群丰度等因素的限制,目前在实验室中仅能够得到少部分与产酸、产气、致浑浊、致腐败等因素相关的微生物,主要为醋酸杆菌、乳酸杆菌和芽孢杆菌等[19-20]。
传统研究方法的局限性导致了人们对香醋中微生物群落结构的认识不足,近年来,随着免培养技术在食品发酵领域的应用范围不断拓宽,香醋中微生物群落结构也变得更加清晰。通过免培养法对镇江香醋中微生物群落结构进行分析,发现醋醅中除含有丰富的醋酸杆菌和乳酸杆菌外,还存在Sinorhizobium、Enterobacter、Gluconacetobacter等此前采用纯培养方法未能检测到的物种[21]。但免培养的DGGE法由于检测通量较小,能够得到的操作分类单元(operational taxonomic units,OTUs)仍十分有限。
随着第2代测序技术的出现,食醋中的微生物群落信息得以被深入挖掘,从而有效揭示了醋酸发酵过程中微生物群落的演替规律。通过对醋酸发酵过程中微生物群落的动态变化进行检测,研究者发现Acetobacter和Lactobacillus是发酵过程中的主要细菌,其中Lactobacillus主要来源于酒醪,其相对丰度在发酵初期呈上升趋势,并在发酵第8天达到最大,而后逐渐降低。Acetobacter则主要来源于醋醅,其相对丰度在发酵前期较低,但始终呈上升趋势,在发酵第8天左右超过乳酸杆菌,在发酵后期占据主导地位;真菌群落则主要以Aspergillus和Alternaria为主,Aspergillus的相对丰度随着发酵开始逐渐上升,并在发酵第7天后趋于稳定。Alternaria在发酵前3 d迅速生长,并在第4~7天始终保持着高丰度,之后其相对丰度开始迅速下降并维持在较低水平,直至发酵结束[9]。组学技术的发展为进一步揭示发酵过程中菌群的功能及演替规律提供了新的工具,有研究者利用宏基因组学技术分析了镇江香醋醋酸发酵阶段微生物群落的结构和功能,不仅明确了醋酸阶段的优势细菌和优势真菌,Acetobacter、Lactobacillus等7 个核心微生物与香醋中挥发性风味物质的关系也被揭示[10](图4)。测序技术的发展使得醋醅中微生物群落显示出了比以往更丰富的多样性和更高的物种丰度,证实了醋酸发酵过程是一个由多种微生物共同参与的复杂进程[22]。在发酵过程中微生物群落的演替规律与风味物质变化规律展现出了惊人的一致性,发酵体系中微生物间存在的复杂互作关系可能是促成这种变化规律的动力之一,对此需要更进一步的研究和探索。
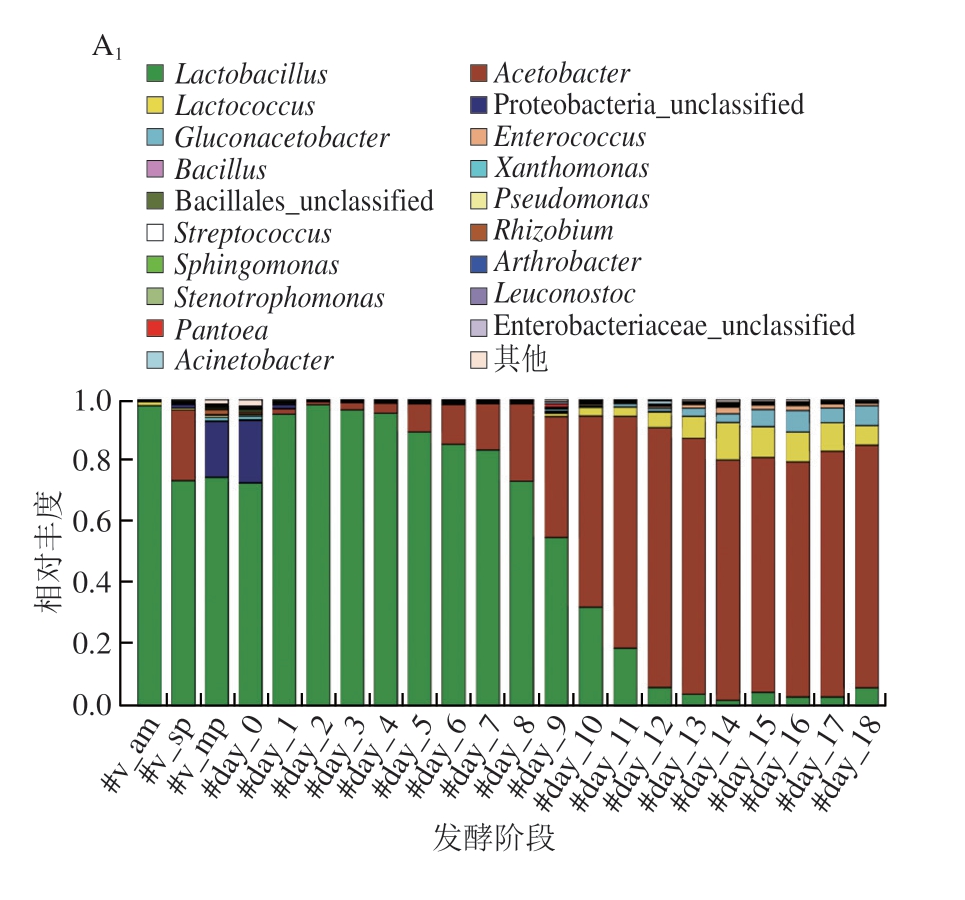
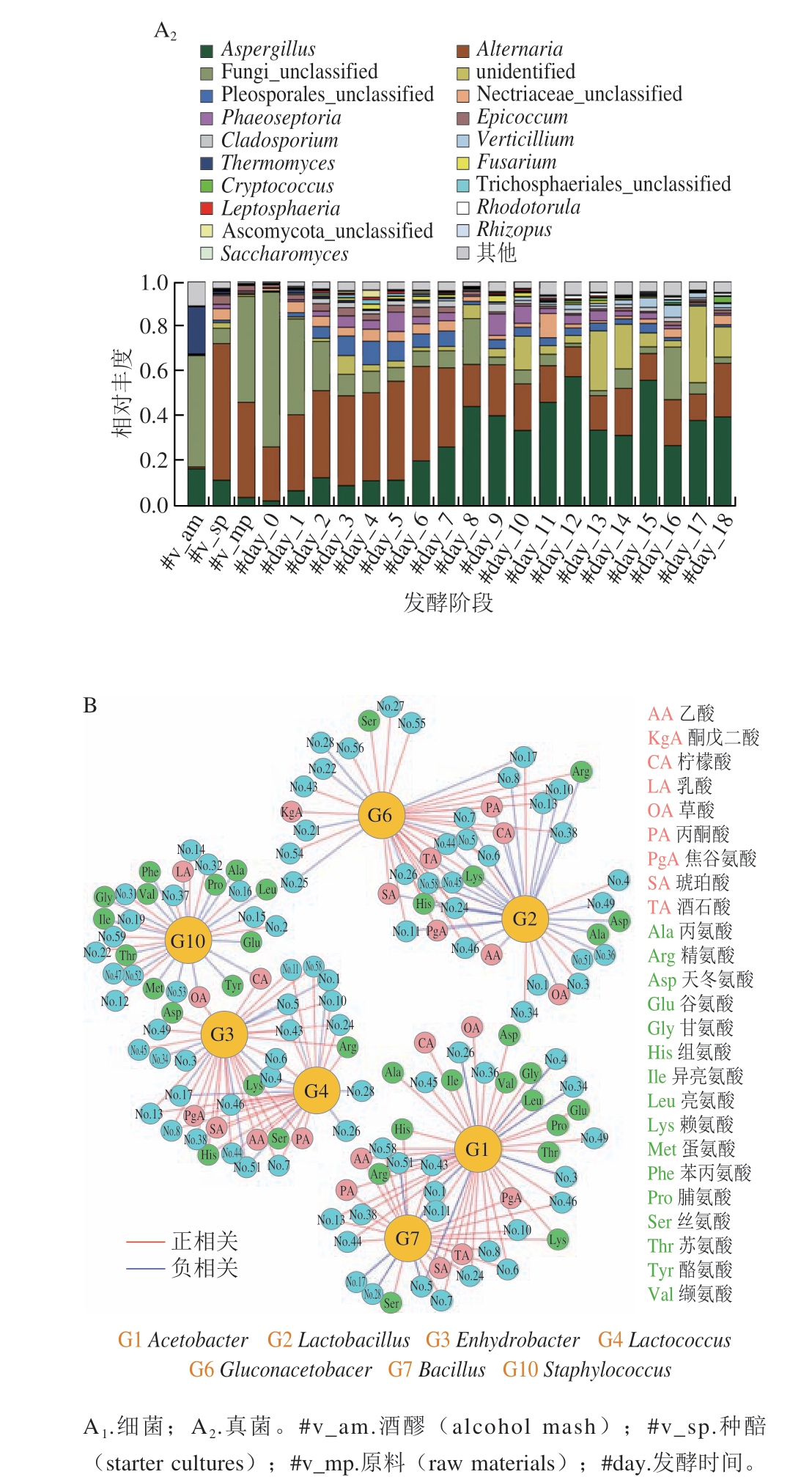
图4 镇江香醋中微生物群落结构(A)及核心功能微生物分析(B)[9-10]
Fig.4 Distribution of microbiota (A) and analysis of core microbiota (B)in Zhenjiang aromatic vinegar[9-10]
2 传统发酵食醋中微生物间相互作用
在微生物主导下的发酵体系中,微生物之间存在的复杂相互作用关系是群落保持稳定以及产生风味物质的重要基础[23]。在食醋酿造过程中,醋醅中的微生物与环境、微生物与微生物之间的相互作用共同构成了一个不断演替变化且相对稳定的内环境[24],然而,体系内微生物组成过于复杂也为探究其中某几种微生物间的相互影响带来了困难。目前,国内外研究者大都基于纯培养微生物在异位以及模拟原位条件下的共培养结果对固态发酵食醋中微生物的相互作用关系及其内在机制进行解析,所涉及的微生物主要包括酵母菌与醋酸杆菌、酵母菌与乳酸杆菌、乳酸杆菌与醋酸杆菌、芽孢杆菌与醋酸杆菌和乳酸杆菌等。其中,酵母菌作为酒曲中的主要微生物,在制酒阶段发挥了重要作用,酵母菌与其他微生物之间的互作关系大多在发酵前期对食醋品质产生影响[25-28]。随着酿造进行至醋酸发酵阶段,乳酸杆菌和醋酸杆菌成为优势微生物,二者间的互作关系在整个互作体系中居于主导地位。此外,芽孢杆菌等低丰度微生物在整个发酵过程中始终存在,芽孢杆菌与醋醅中优势微生物之间的互作关系及其对食醋品质的影响同样值得探究[29-30]。
2.1 酵母菌与其他微生物之间的相互作用关系
传统固态发酵食醋在引入醋酸杆菌进行醋酸发酵之前,往往需要先向糯米、高粱等原料中加入大曲、酒药等发酵剂进行乙醇发酵,大曲和酒药作为乙醇发酵阶段重要的糖化剂和发酵剂,其中含有丰富的微生物群落,主要包括霉菌、酵母菌和细菌3 类,对于上述微生物各自在乙醇发酵中的作用则可表述为霉菌的糖化作用、酵母菌的发酵作用和细菌的生香作用[31]。酵母菌作为乙醇发酵阶段不可或缺的一种微生物,能够通过厌氧发酵将原料中的糖转化为乙醇和二氧化碳,是推动发酵进程的重要动力[27]。
2.1.1 酵母菌的发酵作用为醋酸杆菌提供充足底物
酵母菌在乙醇发酵阶段将糖转化为乙醇,醋酸杆菌再利用乙醇代谢产生乙酸,该过程基于代谢产物呈递的简单相互作用模型如图5所示。Chakraborty等[32]发现,Saccharomyces cerevisisae与Acetobacter aceti混合培养能够显著提高食醋生产过程中的产量和生产效率。Wang Zhi等[33]发现Saccharomyces cerevisiae和Acetobacter pasteurianus在发酵罐中混合培养具有高产乙酸特性,并探索了二者在发酵罐中共培养的最佳发酵条件。这主要是由于酿酒酵母是一种发酵型酵母,能够通过自身发酵作用分解糖并产生乙醇,所产生的乙醇作为醋酸杆菌发酵的底物促进了醋酸杆菌的生长发育,进而促进了乙酸等有机酸在食醋中的积累。
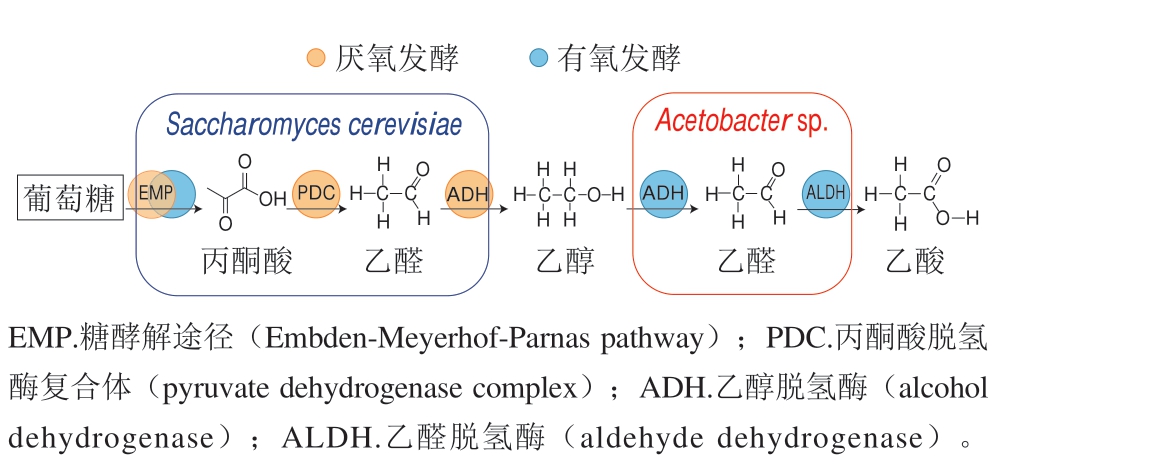
图5 传统发酵食醋中酵母菌与醋酸杆菌间营养级联示意图
Fig.5 Schematic diagram of trophic cascade between yeast and acetic acid bacteria in traditional vinegar fermentation process
2.1.2 酵母菌与乳酸杆菌之间的相互作用促进风味物质的形成
为探究乙醇发酵阶段酵母菌与乳酸杆菌间相互作用关系对食醋品质的影响,蒋忠等[28]以大米为原料,进行了乳酸杆菌和酵母菌的共生发酵实验,结果表明,酵母菌和乳酸杆菌在一定条件下共培养有利于提高发酵体系中乙醇和乳酸的含量。Chen Yang等[34]比较了由S. cerevisiae和Lactobacillus plantarum混合发酵与S. cerevisiae单菌发酵(对照)所得橘子果醋品质的差异,发现S. cerevisiae和L. plantarum混合发酵所得果醋中甲酸、乳酸等有机酸和酯类、醇类、醛类等风味物质的含量均高于对照。同时,相较于单菌发酵,混合发酵还能够显著提高果醋的抗氧化活性和氨基酸等滋味物质的含量。李雅茹[27]经筛选得到山西老陈醋发酵过程中性能优良的酵母菌S. cerevisiae JL421和乳酸杆菌L. plantarum JL7并将二者进行共培养发酵,发现与纯培养相比,共培养条件下体系中总酸含量明显升高,有机酸、乙酸乙酯、异戊醇等风味物质的种类和浓度明显增加,乙偶姻等特征性功能成分的含量较纯培养也有了明显提升。由此推断,乳酸杆菌的加入不仅可能会对酵母菌的发酵活动具有一定促进作用,同时也有利于乳酸杆菌自身生产有机酸和挥发性风味物质。
值得注意的是,酵母菌和乳酸杆菌同样是中国传统酒饮料酿造过程中主要的功能性微生物,对传统酒饮料中二者相互作用关系的研究有助于进一步了解其对发酵进程的影响。熊君燕等[35]研究清香型白酒固态发酵过程中主要酵母菌和乳酸杆菌的相互作用时发现,乳酸杆菌和酵母菌共培养会对乙醇产量和代谢产物的组成产生影响,并且这种影响会因菌种选择的不同而表现为促进或抑制两种不同形式。这可能是由于共培养过程中乳酸杆菌发酵产酸抑制了某些不耐酸酵母菌的生长[36],而另一些酵母菌如毕赤酵母可以产生大量酯类物质,因此对低pH值、高渗环境适应力较强[37]。另外,由于共培养还存在营养物质的竞争和代谢产物的交换,这可能是导致不同培养组合中微生物生长状态和风味物质组成不同的另一原因。与上述研究结果类似,洪家丽等[38]研究乳酸杆菌对黄酒酿造过程中酵母菌的生长及风味物质的影响,发现除干酪乳杆菌外,实验所选用的多种乳酸杆菌对酵母菌的生长均有促进作用,同时对黄酒中特征风味物质的含量及感官品质的提升具有积极影响。
基于以上分析,乙醇发酵过程中乳酸杆菌和酵母菌间的相互作用可能会促使乳酸、乙酸乙酯等风味物质以及乙偶姻等功能性因子在成熟酒醪中积累,并随着酒醪一起参与醋酸发酵过程,在乙醇发酵阶段选择合适的菌种进行微生物强化将会对食醋品质的提升产生积极影响。
2.2 乳酸杆菌与醋酸杆菌之间的相互作用关系
2.2.1 乳酸杆菌与醋酸杆菌间相互作用的多样性乳酸杆菌和醋酸杆菌均为醋酸发酵过程中重要的功能微生物。前期研究表明,乳酸杆菌和醋酸杆菌不仅在数量上占据着绝对的优势,也是乙酸、乳酸等有机酸以及乙酸乙酯、2,3-丁二酮等多种风味物质的重要生物来源[39],二者间的相互作用关系会对发酵结果产生一定影响。
为探究这种影响,牟俊[40]利用微生物培养的方法研究了山西老陈醋中主要乳酸杆菌Lactobacillus helveticus与醋酸杆菌A. pasteurianus间的相互作用。在共培养过程中,A. pasteurianus和L. helveticus呈现出一种一方对另一方存在有害影响从而促进自身生长代谢的偏害共生关系;与之相反,Zhang Meng等[41]发现在共培养过程中,L. plantarum对A. pasteurianus的正常生长活动影响很小,推测L. plantarum和A. pasteurianus对碳源的需求不同,L. plantarum以葡萄糖为主要的能量来源,而A. pasteurianus则主要通过代谢体系中的乙醇维持自身的生长发育。上述研究者在进行乳酸杆菌与醋酸杆菌共培养实验时均以某单一菌株为实验对象,而实验菌株选择的不同可能是导致实验结果存在较大差异的原因。同样以乳酸杆菌和醋酸杆菌为研究对象,孙红等[42]在研究由镇江香醋醋醅中分离得到的醋酸杆菌和乳酸杆菌间相互作用关系时发现,不同种乳酸杆菌和醋酸杆菌在共培养过程中所表现出的相互作用关系有所差异。同时,该研究者还通过比较相同的两种菌株在异位和模拟原位条件下共培养对代谢产生的影响,发现Acetobacter pomorum G15-6和L. helveticus M3-1、L. plantarum M10-1等菌株共培养在异位和模拟原位条件下表现出了不同的代谢情况。因此,该研究者推断,乳酸杆菌和醋酸杆菌间的相互作用存在种间特异性和环境特异性,即同一发酵环境下,不同种醋酸杆菌和乳酸杆菌之间存在多种相互作用关系,相同菌种之间的相互作用关系也可能因为发酵环境的变化而发生改变。该结论与此前的猜测一致,即乳酸杆菌与醋酸杆菌之间存在多种相互作用关系,这种差异形成的原因可能是菌种组合的多样性,同时也说明在发酵过程中可以通过对发酵菌株进行筛选,定向引导发酵向有益于提高食醋品质的方向进行。
2.2.2 乳酸杆菌与醋酸杆菌之间的相互作用关系对食醋品质的影响
食醋发酵过程中乳酸杆菌与醋酸杆菌间的相互作用大多产生积极、正向的结果,因此,乳酸杆菌和醋酸杆菌的菌种组合作为一种有效的微生物强化剂受到广泛关注。Zhang Qiang等[43]通过分析天津独流陈醋酿造过程中细菌与发酵的关系,提出醋酸杆菌、乳酸杆菌和片球菌是独流陈醋发酵过程中的主要功能菌,并在后续实验中将Pediococcus acidilactici AAF1-5作为微生物强化剂添加至发酵醋醅中,结果发现P. acidilactici AAF1-5的加入能够促进醋醅中醋酸杆菌和乳酸杆菌的生长及风味物质的积累,与对照组相比,食醋中不挥发性酸、乳酸和氨基酸含量分别提高了53%、14%、32%,有效提高了食醋品质。Lu Zhenming等[44]通过应用宏基因组测序技术和克隆文库分析,在物种水平上揭示了醋醅中丁二酮/乙偶姻代谢途径的微生物分布差异,从代谢物交流的角度解析了该代谢途径中微生物的互作模式,发现巴氏醋杆菌和乳酸杆菌可能是产生乙偶姻的主要功能菌。在后续共培养实验中,研究者发现A. pasteurianus G3-2与Lactobacillus brevis 4-22及A. pasteurianus G3-2与Lactobacillus fermentum M10-3的共培养组合能够显著提高体系内乙偶姻的含量,将A. pasteurianus G3-2、L. brevis 4-22等菌株添加至原位状态下的发酵醋醅中,可使醋醅中乙偶姻的含量得到显著提高。其中,相较于对照组((6.8±0.1)mg/g),添加A. pasteurianus G3-2与L. f e r m e n t u m M 1 0-3 的醋醅中乙偶姻含量高达(12.5±1.2)mg/g,证明醋酸杆菌和乳酸杆菌间的互作关系对食醋品质具有积极影响。与之类似,Chai Lijuan等[45]探讨了传统谷物醋醋酸发酵过程中醋酸杆菌和乳酸杆菌用作生物强化剂的发酵潜力,研究者将从醋醅中分离出的5 株乳酸杆菌和1 株醋酸杆菌分别进行纯培养和共培养,以比较不同培养方式下其代谢产物的差异,发现实验所选用的L. plantarum M1-6和A. pasteurianus G3-2在共培养条件下能够通过协同作用高产乙偶姻。将两种菌株应用于原位条件下的生物强化实验中,发现向醋醅中接种L. plantarum M1-6和A. pasteurianus G3-2后,食醋中乙酸、乳酸、乙偶姻、乙酸乙酯、乳酸乙酯、川芎嗪等特征风味物质和功能因子的含量明显提高,进一步证实了乳酸杆菌和醋酸杆菌作为微生物强化剂应用于食醋酿造的潜力。
传统食品发酵体系中生物强化战略的关键在于通过利用微生物的互作关系对酿造微生物群落实现有效调控,具体可以表述为:分析微生物群落的结构和功能,分离关键核心微生物;解析发酵体系中功能性微生物群落的互作关系;在此基础上,预测并验证这些关键核心微生物的代谢特征,在实际生产中对其生产效率进行进一步评估;最终目标是构建具有良好发酵性能的多细胞功能体系,以实现缩短发酵时间、提高发酵速度、提升产品品质等目标。
2.2.3 乳酸杆菌与醋酸杆菌共发酵提升食醋品质的作用机制
乳酸杆菌与醋酸杆菌之间的相互作用关系多通过代谢产物实现,随着组学技术的发展和风味物质检测手段的完善,二者通过代谢相互作用影响食醋品质的作用机制愈发明确。酶是一种具有催化活性的代谢产物,其催化作用在微生物代谢活动中扮演了重要角色。酶参与相互作用的案例之一为对谷物醋中乳酸含量的调节,Chai Lijuan等[46]探究了传统谷物醋发酵过程中L-/D-型乳酸积累的微生物强化和调控,在此过程中,研究者发现乳酸杆菌为醋酸发酵过程中乳酸的主要生产者,然而随着发酵的进行和乳酸的积累,醋醅中的醋酸杆菌能够通过分泌乳酸脱氢酶催化乳酸逆转化为丙酮酸,从而调节成品醋中L-/D-型乳酸含量(图6)。该结论在另一项研究中得到验证,并判断醋酸杆菌所分泌的乳酸脱氢酶为膜结合酶[47]。此外,乳酸杆菌与醋酸杆菌共培养过程中体系2,3-丁二酮水平的提高也被认为与酶有关,在二者共培养过程中,随着体系内乙酸、乳酸及柠檬酸等代谢产物的积累,丙酮酸/2,3-丁二酮这一代谢通路中编码多种相关酶基因的表达得到促进,进而提高了终产物2,3-丁二酮的含量[42,44]。2,3-丁二酮是生成乙偶姻的重要前体物质,因此推测该代谢通路可能是乳酸杆菌与醋酸杆菌共培养能够高产乙偶姻的主要原因。另有研究者发现在共培养过程中,乳酸杆菌胞外代谢产物中的某种蛋白可能具有氨肽酶的功能特性,能够在发酵过程中通过水解蛋白产生游离氨基酸作为醋酸杆菌生长代谢所需的营养物质,从而促进醋酸杆菌的发酵作用[48]。有机酸是食醋发酵过程中另一种特征代谢产物,乳酸杆菌、醋酸杆菌能够产生丰富的有机酸,发酵体系内有机酸的积累又可能反过来影响微生物的代谢活动,最终影响食醋中氨基酸、乙偶姻等风味物质的含量。例如,在山西老陈醋醋酸发酵过程中醋酸杆菌能够高产乙酸,体系中乙酸的积累能够促进醋醅中乳酸杆菌和醋酸杆菌的磷酸戊糖途径以及氨基酸、核酸和能量的代谢,产生大量氨态氮,从而有助于微生物抵御高酸性的外部环境,多余的氨类物质则会因浓度梯度向胞外迁移,最终促进多种氨基酸在食醋中的积累[49]。

图6 醋酸发酵阶段的乳酸和乙醇代谢途径[46]
Fig.6 Metabolic pathways of lactic acid and ethanol in acetic acid fermentation stage[46]
综上所述,首先,乳酸杆菌与醋酸杆菌之间的相互作用关系有利于促进体系中乙酸、乳酸等有机酸的快速积累和对其定向调控;其次,共培养条件下某些酶活力的增强和相关基因的强表达有利于促进特定代谢通路的表达,从而提高体系内功能性成分的含量;由微生物产酸引起的胁迫作用和代谢产生的生物酶能够提高食醋中氨基酸类风味物质的含量,从而使食醋具有更加丰富的滋味。综上,乳酸杆菌与醋酸杆菌间的相互作用关系是形成食醋优良品质的重要因素,二者联合应用于食醋酿造将具有很大的发展潜力。
2.3 芽孢杆菌与醋酸杆菌、乳酸杆菌之间的相互作用关系
现有研究表明,部分在体系中微量存在的微生物种群同样对提高食醋品质具有重要意义。芽孢杆菌作为重要的发酵微生物,能够通过自身代谢作用产生大量的乙偶姻,最终提高体系中川芎嗪等功能性物质的含量[50](图7)。
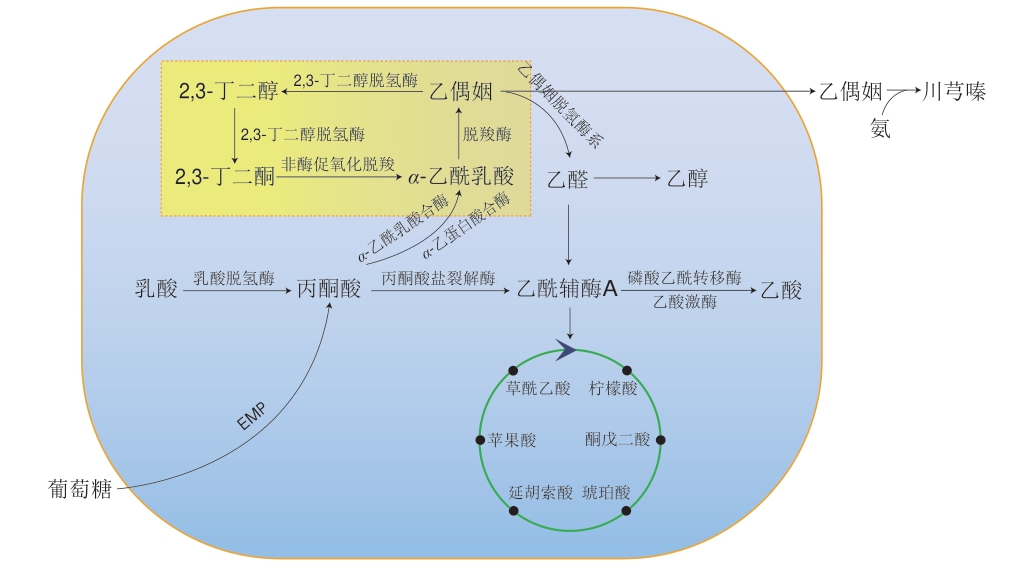
图7 芽孢杆菌代谢产生乙偶姻以及川芎嗪的机制[50]
Fig.7 Mechanisms of acetoin and tetramethylpyrazine production in Bacillus sp.[50]
贾瑞娟等[51]将筛选自山西老陈醋中的优良芽孢杆菌与醋酸杆菌和乳酸杆菌共培养,发现多株菌株共培养条件下,体系中挥发性香气成分含量和种类最为丰富,具有水果香气的乙酸乙酯、香蕉香气的异戊酸乙酯等山西老陈醋特征挥发性风味物质含量明显优于各菌株纯培养,二者在食醋中的含量分别提高了78.65%和49.26%,证明优良芽孢杆菌与醋酸杆菌、乳酸杆菌协同发酵有利于山西老陈醋风味的形成。Zhang Liqiang等[52]在研究Bacillus amyloliquefaciens对四川麸醋品质的影响时发现,当B. amyloliquefaciens被用作生物强化剂添加至四川麸醋发酵大曲中后,大曲中有机酸和风味物质含量有所提高;值得关注的是,改良后大曲中乙偶姻和川芎嗪含量明显高于对照组,说明B. amyloliquefaciens参与发酵能够有效提高食醋中乙偶姻及川芎嗪等功能性物质的含量。在后续研究中发现,这种改变可能源自菌种自身的代谢特性,芽孢杆菌属中多个菌种已被证明可以通过EMP代谢产生丙酮酸,丙酮酸缩合产生α-乙酰乳酸[29],α-乙酰乳酸是2,3-丁二醇-2,3-丁二酮-3-羟基-2-丁酮生物合成途径的重要前体物质[39],芽孢杆菌能够通过该代谢途径大量合成乙偶姻;另一种假设认为醋醅中的乳酸杆菌等微生物能够将生物大分子分解为小分子物质,该生命活动为芽孢杆菌提供了高浓度的代谢底物,促使芽孢杆菌产生大量2,3-丁二酮[53];另外,有研究者认为醋酸发酵过程中乳酸杆菌和醋酸杆菌代谢产生的乳酸、乙酸、柠檬酸等有机酸的积累也可能有利于促进丙酮酸/2,3-丁二酮代谢通路的表达,最终提高体系中双乙酰和乙偶姻的含量[54]。
芽孢杆菌作为一种高产风味物质和功能因子的微生物,其在食醋酿造过程中有较好的应用前景,且其微生物强化作用对发酵食品品质的积极影响已经在白酒酿造中得到了充分验证[55-56]。但同样需要认识到,食醋醋醅和白酒大曲在外部环境、所含成分、微生物结构上都存在较大差异,所筛选的芽孢杆菌能否与醋醅中原始菌群和谐共生、能否适应醋醅所提供的高酸性环境以及对终产物品质的影响等都是衡量其能否被用于生物强化所需考虑的因素。
3 结 语
微生物群落及其相互作用关系是形成传统发酵食醋风味品质的关键,近年来,研究者们对此开展了丰富的研究。本文综述了传统发酵食醋中微生物群落的结构及核心功能微生物间存在的多种相互作用,同时对微生物互作关系对食醋品质的影响进行了总结。
微生物广泛存在于食醋酿造过程中,微生物群落之间复杂的相互作用关系是维持其结构稳定的基础[57],但是要完全解析食醋中各种微生物间复杂的相互作用关系还比较困难,合成微生物群落的产业化应用条件还不够完备,目前研究还存在以下几方面欠缺:1)对于醋醅环境中微量存在或不可培养的微生物对发酵所做贡献的研究较少;2)缺少对发酵区系中整个微生物群落内部互作机制的系统性研究;3)对合成微生物群落在实际生产中应用条件的探索不够全面。当前对于微生物强化的实验步骤已经较为明确,可以总结为:预测核心功能微生物、基因组引导核心功能微生物分离、实际生产验证3 个步骤,但对于生物强化过程中的强化时间、强化接种量等条件因素仍缺乏深入探讨。相信随着微生物培养技术和组学技术的不断发展,微生物群落间复杂的互作关系将得到进一步完善,相关发酵技术也将随着研究的深入不断进步。
[1] CHIN W, AZWAN M, SHAZRUL F, et al.Varieties, production,composition and health benefits of vinegars: a review[J].Food Chemistry, 2017, 221: 1621-1630.DOI:10.1016/j.foodchem.2016.10.128.
[2] LU Zhenming, WANG Zongmin, ZHANG Xiaojuan, et al.Microbial ecology of cereal vinegar fermentation: insights for driving the ecosystem function[J].Current Opinion in Biotechnology, 2018, 49:88-93.DOI:10.1016/j.copbio.2017.07.006.
[3] 魏军林, 聂尧, 杜海, 等.营养相互作用对传统发酵食品微生物群落构建的推动作用研究进展[J].微生物学通报, 2021, 48(11): 4412-4424.DOI:10.13344/j.microbiol.china.210227.
[4] BLASCHE S, KIM Y, MARS R, et al.Metabolic cooperation and spatiotemporal niche partitioning in a Kefir microbial community[J].Nature Microbiology, 2021, 6(2): 196-208.DOI:10.1038/s41564-020-00816-5.
[5] WU Jiajia, MA Yingkun, ZHANG Fenfen, et al.Biodiversity of yeasts, lactic acid bacteria and acetic acid bacteria in the fermentation of “Shanxi aged vinegar”, a traditional Chinese vinegar[J].Food Microbiology, 2012, 30(1): 289-297.DOI:10.1016/j.fm.2011.08.010.
[6] NIE Zhiqiang, ZHENG Yu, DU Hongfu, et al.Dynamics and diversity of microbial community succession in traditional fermentation of Shanxi aged vinegar[J].Food Microbiology, 2015, 47(1): 62-68.DOI:10.1016/j.fm.2014.11.006.
[7] ZHU Yunping, ZHANG Feifei, ZHANG Chengnan, et al.Dynamic microbial succession of Shanxi aged vinegar and its correlation with flavor metabolites during different stages of acetic acid fermentation[J].Scientific Reports, 2018, 8: 8612.DOI:10.1038/s41598-018-26787-6.
[8] NIE Zhiqiang, ZHENG Yu, XIE Sankuan, et al.Unraveling the correlation between microbiota succession and metabolite changes in traditional Shanxi aged vinegar[J].Scientific Reports, 2017, 7: 9240.DOI:10.1038/s41598-017-09850-6.
[9] 王宗敏.镇江香醋醋酸发酵阶段菌群结构变化与风味物质组成之间的相关性研究[D].无锡: 江南大学, 2016: 12-24; 26-37.
[10] WANG Zongmin, LU Zhenming, SHI Jinsong, et al.Exploring flavour-producing core microbiota in multispecies solid-state fermentation of traditional Chinese vinegar[J].Scientific Reports,2016, 6: 26818.DOI:10.1038/srep26818.
[11] 彭杨, 张奶英, 何利, 等.基于PCR-DGGE技术的四川麸醋固态发酵过程中微生物群落分析[J].现代食品科技, 2016, 32(8): 155;171-177.DOI:10.13982/j.mfst.1673-9078.2016.8.026.
[12] 黄祖新.福建红曲醋发酵液的细菌群落结构分析[J].福建师范大学学报(自然科学版), 2015, 31(3): 76-82.
[13] JIANG Yajun, LV Xucong, ZHANG Chong, et al.Microbial dynamics and flavor formation during the traditional brewing of Monascus vinegar[J].Food Research International, 2019, 125: 108531.DOI:10.1016/j.foodres.2019.108531.
[14] NIE Zhiqiang, ZHENG Yu, WANG Min, et al.Exploring microbial succession and diversity during solid-state fermentation of Tianjin Duliu mature vinegar[J].Bioresource Technology, 2013, 148: 325-333.DOI:10.1016/j.biortech.2013.08.152.
[15] YUN Jianmin, ZHAO Fengqin, ZHANG Wenwen, et al.Monitoring the microbial community succession and diversity of Liangzhou fumigated vinegar during solid-state fermentation with next-generation sequencing[J].Annals of Microbiology, 2019, 69(3): 279-289.DOI:10.1007/s13213-018-1418-z.
[16] ZHANG Qiang, FU Chuanxue, ZHAO Cuimei, et al.Monitoring microbial succession and metabolic activity during manual and mechanical solid-state fermentation of Chinese cereal vinegar[J].LWT-Food Science and Technology, 2020, 133: 109868.DOI:10.1016/j.lwt.2020.109868.
[17] 武晋海.山西老陈醋大曲微生物种类及主要生物活性的研究[D].太谷: 山西农业大学, 2004: 17-19; 27-36.
[18] 包启安.镇江香醋传统生产工艺的剖析[J].中国酿造, 2000(4): 1-4.
[19] 林祖申.多菌种发酵是提高酱油、食醋质量的重要途径[J].中国酿造, 2005(6): 1-5.DOI:10.3969/j.issn.0254-5071.2005.06.001.
[20] 郑宇, 牛纪伟, 张祥龙, 等.传统食醋中潜在污染微生物的分离鉴定[J].现代食品科技, 2016, 32(11): 327; 334-339.DOI:10.13982/j.mfst.1673-9078.2016.11.050.
[21] XU Wei, HUANG Zhiyong, ZHANG Xiaojun, et al.Monitoring the microbial community during solid-state acetic acid fermentation of Zhenjiang aromatic vinegar[J].Food Microbiology, 2011, 28(6): 1175-1181.DOI:10.1016/j.fm.2011.03.011.
[22] 聂志强, 韩玥, 郑宇, 等.宏基因组学技术分析传统食醋发酵过程微生物多样性[J].食品科学, 2013, 34(15): 198-203.DOI:10.7506/spkx1002-6630-201315041.
[23] SMID E, LACROIX C.Microbe-microbe interactions in mixed culture food fermentations[J].Current Opinion in Biotechnology, 2013, 24(2):148-154.DOI:10.1016/j.copbio.2012.11.007.
[24] 姚尚杰, 金垚, 周荣清, 等.传统发酵食品中微生物间相互作用及应用[J].生物产业技术, 2019(4): 48-54.DOI:10.3969/j.issn.1674-0319.2019.04.007.
[25] 罗青春, 郑佳, 赵东, 等.浓香型白酒中优势乳酸菌和酵母菌间的相互关系[J].应用与环境生物学报, 2019, 25(5): 1192-1199.DOI:10.19675/j.cnki.1006-687x.2018.12031.
[26] LI Sha, LI Pan, LIU Xiong, et al.Bacterial dynamics and metabolite changes in solid-state acetic acid fermentation of Shanxi aged vinegar[J].Applied Microbiology and Biotechnology, 2016, 100(10):4395-4411.DOI:10.1007/s00253-016-7284-3.
[27] 李雅茹.山西老陈醋源优良酵母菌和乳酸菌的筛选、互作及应用研究[D].太谷: 山西农业大学, 2019: 17-37.
[28] 蒋忠, 冯文利, 王伟, 等.乳酸菌和酵母菌共酵改善食醋品质的研究[J].中国酿造, 2015, 34(9): 104-108.DOI:10.11882/j.issn.0254-5071.2015.09.025.
[29] 张颖, 李霄霄, 李景辉, 等.高产四甲基吡嗪芽孢杆菌的筛选及其对酱香型白酒堆积过程的影响[J].食品工业科技, 2022, 43(2): 142-149.DOI:10.13386/j.issn1002-0306.2021050066.
[30] 李豆南, 邱树毅.酱香大曲微生物菌群结构及微生物功能研究概述[J].中国酿造, 2017, 36(1): 5-11.DOI:10.11882/j.issn.0254-5071.2017.01.002.
[31] WU Qun, ZHU Wei’an, WANG Wei, et al.Effect of yeast species on the terpenoids profile of Chinese light-style liquor[J].Food Chemistry,2015, 168: 390-395.DOI:10.1016/j.foodchem.2014.07.069.
[32] CHAKRABORTY K, SAHA S, RAYCHAUDHURI U, et al.Vinegar from Bael (Aegle marmelos): a mixed culture approach[J].Indian Chemical Engineer, 2018, 60(4): 1-12.DOI:10.1080/00194506.2017.1376601.
[33] WANG Zhi, YAN Mei, CHEN Xiong, et al.Mixed culture of Saccharomyces cerevisiae and Acetobacter pasteurianus for acetic acid production[J].Biochemical Engineering Journal, 2013, 79: 41-45.DOI:10.1016/j.bej.2013.06.019.
[34] CHEN Yang, HUANG Yao, BAI Ye, et al.Effects of mixed cultures of Saccharomyces cerevisiae and Lactobacillus plantarum in alcoholic fermentation on the physicochemical and sensory properties of citrus vinegar[J].LWT-Food Science and Technology, 2017, 84: 753-763.DOI:10.1016/j.lwt.2017.06.032.
[35] 熊君燕, 李小东, 谢圣凯, 等.清香型白酒中乳酸菌和酵母菌的相互作用[J].微生物学通报, 2017, 44(8): 1767-1776.DOI:10.13344/j.microbiol.china.160917.
[36] PASSOTH V, FREDLUND E, DRUVEFORS U, et al.Biotechnology,physiology and genetics of the yeast Pichia anomala[J].FEMS Yeast Research, 2006, 6(1): 3-13.DOI:10.1111/j.1567-1364.2005.00004.x.
[37] 林良才, 白茹, 高滢, 等.高耐性库德里阿兹威氏毕赤酵母的筛选及应用[J].食品与发酵工业, 2023, 49(3): 60-67.DOI:10.13995/j.cnki.11-1802/ts.031854.
[38] 洪家丽, 陈敏, 周文斌, 等.乳酸菌对红曲黄酒酿造过程酵母菌生长及风味物质形成的影响[J].中国食品学报, 2020, 20(1): 91-100.DOI:10.16429/j.1009-7848.2020.01.012.
[39] WU Linhuan, LU Zhenming, ZHANG Xiaojuan, et al.Metagenomics reveals flavour metabolic network of cereal vinegar microbiota[J].Food Microbiology, 2017, 62: 23-31.DOI:10.1016/j.fm.2016.09.010.
[40] 牟俊.山西老陈醋醋酸发酵阶段乳酸菌和醋酸菌相互作用研究[D].天津: 天津科技大学, 2018: 26-33.
[41] ZHANG Meng, LI Xingjiang, MU Dongdong, et al.Co-fermentation metabolism characteristics of apple vinegar with Acetobacter pasteurianus and Lactobacillus plantarum[J].Journal of Food Processing and Preservation, 2022, 46: e16605.DOI:10.1111/jfpp.16605.
[42] 孙红, 柴丽娟, 陆震鸣, 等.镇江香醋核心酿造微生物醋酸杆菌和乳酸杆菌共培养对生长代谢的影响[J].微生物学报, 2021, 61(7):2065-2076.DOI:10.13343/j.cnki.wsxb.20200537.
[43] ZHANG Qiang, ZHAO Cuimei, WANG Xiaobin, et al.Bioaugmentation by Pediococcus acidilactici AAF1-5 improves the bacterial activity and diversity of cereal vinegar under solidstate fermentation[J].Frontiers in Microbiology, 2021, 11: 603721.DOI:10.3389/fmicb.2020.603721.
[44] LU Zhenming, LIU Na, WANG Lijuan, et al.Elucidating and regulating the acetoin production role of microbial functional groups in multispecies acetic acid fermentation[J].Applied and Environmental Microbiology, 2016, 82(19): 5860-5868.DOI:10.1128/aem.01331-16.
[45] CHAI Lijuan, QIU Ting, LU Zhenming, et al.Modulating microbiota metabolism via bioaugmentation with Lactobacillus casei and Acetobacter pasteurianus to enhance acetoin accumulation during cereal vinegar fermentation[J].Food Research International, 2020,138: 109737.DOI:10.1016/j.foodres.2020.109737.
[46] CHAI Lijuan, SHEN Mina, SUN Jia, et al.Deciphering the D-/L-lactate-producing microbiota and manipulating their accumulation during solid-state fermentation of cereal vinegar[J].Food Microbiology, 2020, 92: 103559.DOI:10.1016/j.fm.2020.103559.
[47] RAJ K C, INGRAM L O, MAUPIN-FURLOW J A.Pyruvate decarboxylase: a key enzyme for the oxidative metabolism of lactic acid by Acetobacter pasteurianus[J].Archives of Microbiology, 2001,176(6): 443-451.DOI:10.1007/s002030100348.
[48] 刘静.食醋发酵条件下乳酸菌对醋酸菌生长代谢的影响[D].天津:天津科技大学, 2020: 34-41.
[49] XIE Sankuan, ZHAO Cuimei, FAN Bingqian, et al.Metabolic network of ammonium in cereal vinegar solid-state fermentation and its response to acid stress[J].Food Microbiology, 2021, 95: 103684.DOI:10.1016/j.fm.2020.103684.
[50] 徐岩, 吴群, 范文来, 等.中国白酒中四甲基吡嗪的微生物产生途径的发现与证实[J].酿酒科技, 2011(7): 37-40.DOI:10.13746/j.njkj.2011.07.001.
[51] 贾瑞娟, 陈旭峰, 胡开燕, 等.山西老陈醋优良芽孢菌与醋酸菌、乳酸菌的相互作用[J].中国食品学报, 2021, 21(9): 57-70.DOI:10.16429/j.1009-7848.2021.09.007.
[52] ZHANG Liqiang, HUANG Jun, ZHOU Rongqing, et al.Evaluating the feasibility of fermentation starter inoculated with Bacillus amyloliquefaciens for improving acetoin and tetramethylpyrazine in Baoning bran vinegar[J].International Journal of Food Microbiology,2017, 255: 42-50.DOI:10.1016/j.ijfoodmicro.2017.05.021.
[53] PEYER L C, ZANNINI E, ARENDT E K.Lactic acid bacteria as sensory biomodulators for fermented cereal-based beverages[J].Trends in Food Science & Technology, 2016, 54: 17-25.DOI:10.1016/j.tifs.2016.05.009.
[54] COMASIO A, HARTH H, WECKX S, et al.The addition of citrate stimulates the production of acetoin and diacetyl by a citratepositive Lactobacillus crustorum strain during wheat sourdough fermentation[J].International Journal of Food Microbiology, 2019,289: 88-105.DOI:10.1016/j.ijfoodmicro.2018.08.030.
[55] 张荣, 徐岩, 范文来, 等.酱香大曲中地衣芽孢杆菌及其特征风味代谢产物的分析研究[J].工业微生物, 2010, 40(3): 7-12.DOI:10.3969/j.issn.1001-6678.2010.03.002.
[56] ZHU Bingfeng, XU Yan, FAN Wenlai.High-yield fermentative preparation of tetramethylpyrazine by Bacillus sp.using an endogenous precursor approach[J].Journal of Industrial Microbiology &Biotechnology, 2010, 37(2): 179-186.DOI:10.1007/s10295-009-0661-5.
[57] SMID E J, LACROIX C.Microbe-microbe interactions in mixed culture food fermentations[J].Current Opinion in Biotechnology,2013, 24(2): 148-154.DOI:10.1016/j.copbio.2012.11.007.