作为新型功能性食品的潜在来源,生物活性肽等生物活性化合物引起了众多研究者的兴趣。生物活性肽是一种对身体功能有积极影响并可能影响健康的特定氨基酸片段,是由几个至十几个氨基酸通过共价键(也称为酰胺键或肽键)连接而成的有机物质,虽然不同分子片段的复杂程度有所差异,但生物活性肽的分子质量都在6 000 Da以下[1]。生物活性肽可以是天然来源的,也可以是蛋白质片段中的特定氨基酸序列,其在亲本蛋白质的序列中是无活性的,但是通过不同技术释放后可以呈现出不同的活性。生物活性肽和蛋白质在生物体的代谢功能中能展现出优异的类激素或药物活性,从而在人体健康方面发挥积极作用。根据生物活性的差异生物活性肽可以分为抗高血压肽、抗氧化肽、抗血栓肽、降胆固醇肽、降血压肽、抗菌肽、免疫调节肽、细胞调节肽、矿物质结合肽等[2]。
从植物、动物等原料中获得蛋白质是蛋白质工程的难点之一,加上蛋白质分子大多拥有复杂的三维结构[3],这使得蛋白质在向生物活性肽的转化过程中存在阻碍。为了解决这些难点,众多研究者正致力于优化样品制备的条件,如优化蛋白质酶消化的温度、时间、pH值;联合使用多种蛋白酶消化、添加有机溶剂等[4]。除此之外,研究者越来越关注使用新技术,如超高压、超声波、脉冲电场、微波辅助萃取和亚临界水水解等[5]以辅助制备生物活性肽。
超高压处理也被称为高压处理或高压静压处理,是一种非热加工技术[6]。近年来,超高压技术在食品工业中得到更广泛的应用(图1),研究证明,将超高压技术应用于蛋白质改性和生物活性肽制备,能有效解决蛋白质提取、活性肽制备及应用上的困难。本文重点综述超高压技术在肽和蛋白质的提取、消化、生成等方面的应用,还概述生物活性肽的类型、来源和生物活性,以期为深入应用超高压技术辅助蛋白质改性和活性肽制备提供理论依据。
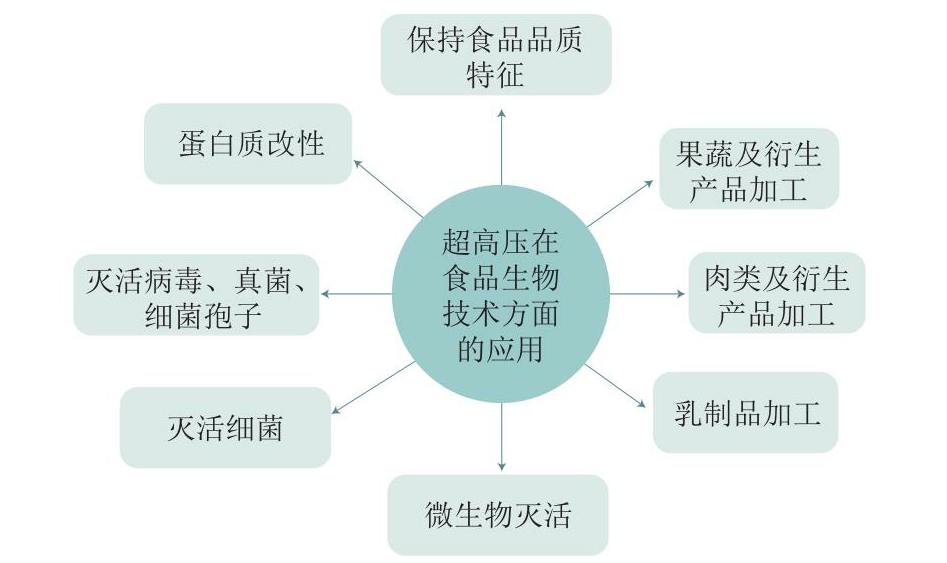
图1 超高压技术在食品加工领域的应用[5]
Fig.1 Application of ultra-high pressure in food processing[5]
1 生物活性肽
食品中存在的大量营养素中,肽和蛋白质扮演着重要的角色,它们不仅可以作为能量来源和氨基酸来源,一些肽还表现出独特的生物活性。
生物活性肽一般以植物、动物或海洋生物为原料,再通过一定的技术制备获得。植物原料如谷物(小麦、大麦、大米、黑麦、燕麦、小米、高粱和玉米)、大豆、蘑菇、南瓜和苋菜等都是优质的生物活性肽来源。其中,小麦和大麦的谷物蛋白极具多样性且具有最丰富的潜在生物活性[7]。牛乳、鸡蛋和肉类等动物来源的原料也是制备活性肽的优质来源[8],除此之外动物的副产品也常被作为制备活性肽的原料,牛乳奶酪和乳制品是生物活性肽的主要来源[9]。近年来,海洋生物资源成为了药物研究和保健品应用中新型活性成分的重要来源。一方面,研究证实,海水鱼蛋白水解物及其肽具有优越的生物活性;另一方面,由海洋生物(被囊动物、海绵、软珊瑚、海兔、裸鳃类动物、苔藓虫、海蛞蝓、被囊类动物、海绵、软体动物)制备的活性肽具有一系列生物活性(如酶抑制、免疫调节、抗菌、抗氧化、抗血栓、降胆固醇和抗高血压等)[10]。多肽及其用途的变革如图2所示。
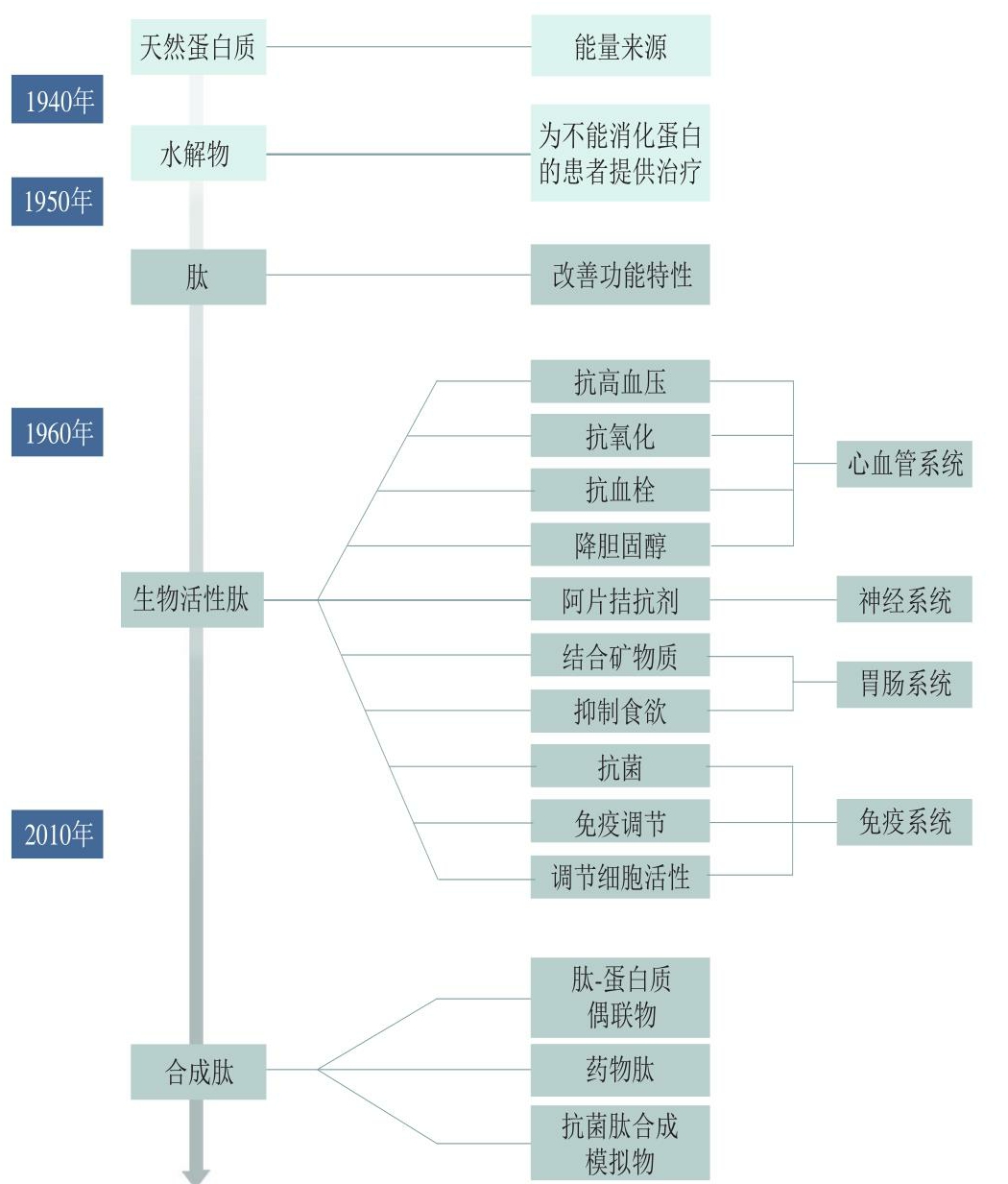
图2 多肽及其用途的变革[11]
Fig.2 Changes in peptides and their purposes[11]
生物活性肽的制备方法主要有化学提取法、微生物发酵法、生物合成法和酶解法[11],4 种提取方法的优缺点如图3所示。
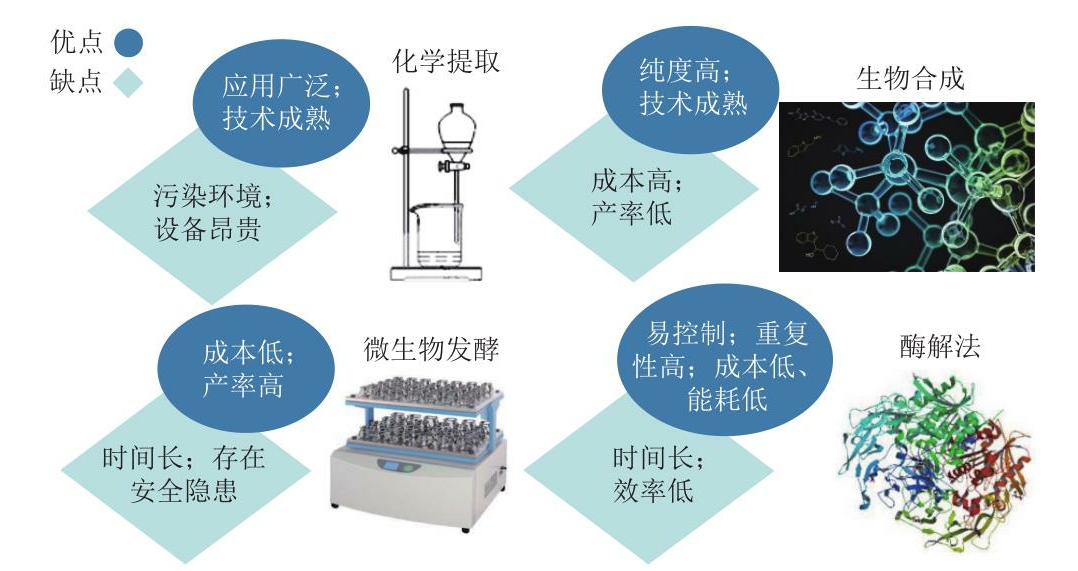
图3 生物活性肽制备方法的优缺点[11]
Fig.3 Advantages and disadvantages of bioactive peptide preparation methods[11]
2 超高压技术的作用原理
食品原料打包后置于盛满水的压力作用腔内,利用水作为传压介质,样品在高压作用腔内受到100~1 000 MPa压力[12]。如图4所示,食品原料在超高压技术处理工程中,某些性质发生改变主要归因于2 个机制——帕斯卡原理和勒夏特列原理[13]。帕斯卡原理指相同的压力会立即且均等地施加给食品物料,与传统的热处理工艺相比,超高压技术能保证食品的质地、形状、色泽,还能保证食品的风味和营养特性;勒夏特列原理指在超高压处理过程中,食品物料会随着压力的方向发生移动,其体积减小,食品体系的平衡和体积变化速率、分子构象都发生一定程度的改变。
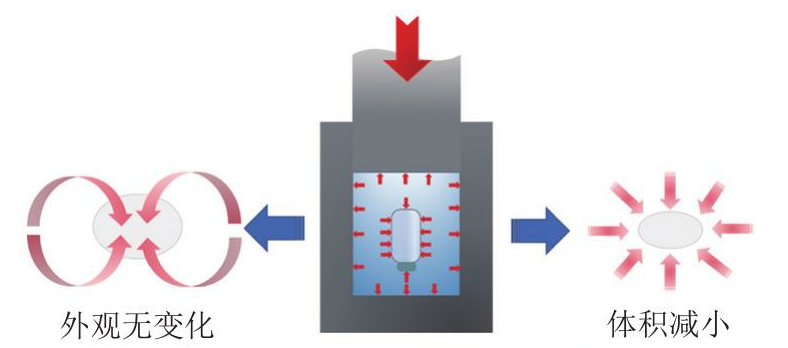
图4 超高压技术的作用原理
Fig.4 Working principle of ultra-high pressure
3 超高压技术的应用
超高压处理是一个瞬时过程,通过水这个压力传递介质,影响蛋白质的二、三、四级结构,快速破坏蛋白质的共价键,蛋白质肽链折叠改变,分子结构发生变化,从而达到不同的应用目的[14]。不同压力对蛋白质结构有不同程度的影响,研究表明,在不超过150 MPa的压力条件下使低聚蛋白质结构解离,分子体积减小,有时蛋白质体积变化很大;当压力超过150 MPa时,会促使蛋白质伸展,并能使解离的低聚体亚基再发生聚合[15]。近年来,众多学者致力于研究超高压等新技术制备活性肽及其下游产品(合成肽)。超高压技术在蛋白质和活性肽领域的应用如图5所示。值得注意的是,众多研究表明,较长处理时间的过高压力处理会产生高温和高压条件,使蛋白质或肽的一级序列发生改变,其状态将不利于后续工作。因此,后期研究应重点关注超高压处理条件的优化。
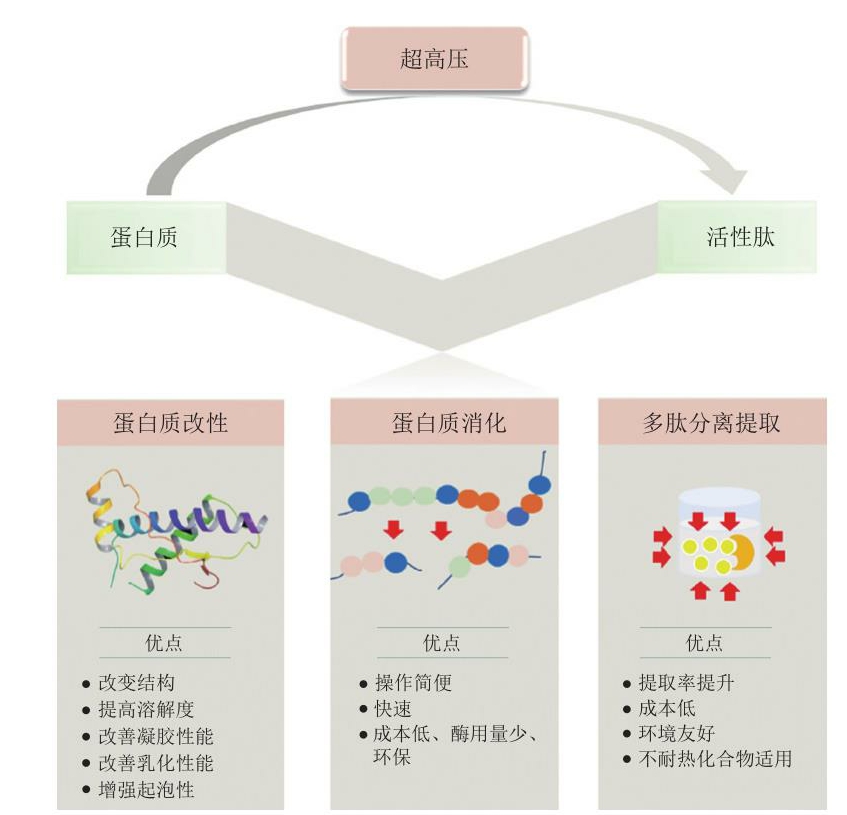
图5 超高压技术在蛋白质改性、消化和活性肽分离提取领域的应用
Fig.5 Application of ultra-high pressure in modification and digestion of proteins as well as separation and extraction of peptides
3.1 超高压技术在蛋白质改性中的应用
蛋白质改性是蛋白质工程中重要的一个环节,超高压可以解离非共价键、离子键、疏水键和氢键,从而改变蛋白质的结构,压力的变化会引起蛋白质的局部或整体变化,并最终通过改变稳定天然蛋白质折叠构象的相互作用而导致蛋白质发生变性(图6),从而达到蛋白质改性的目的[16]。超高压处理对蛋白质改性作用主要体现在对蛋白质结构、水合性质(溶解性、持水性)、表面性质(乳化性、起泡性)、流体动力学性质(凝胶性)的影响。
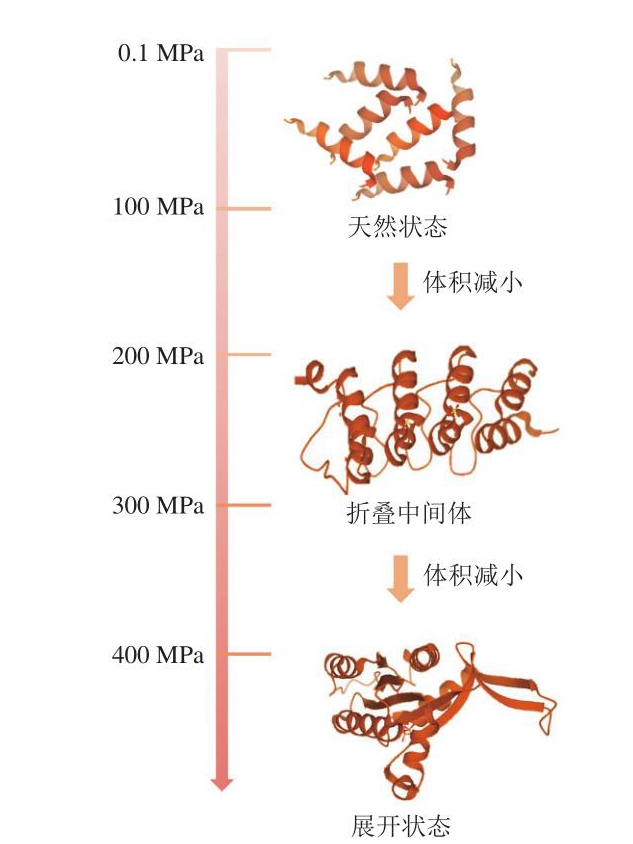
图6 压力诱导蛋白质变性的机理示意图
Fig.6 Schematic diagram of the mechanism of pressure-induced protein denaturation
3.1.1 蛋白质结构
超高压主要会对蛋白质的二、三、四级结构产生不同程度的影响,对蛋白质的一级结构影响不显著[17]。蛋白质的一级结构是指构成蛋白质肽链的氨基酸残基的线形排列顺序,有时也称为残基的序列。氨基酸序列决定了蛋白质的一级结构,由于酰胺键是共价键,因此压力对其影响小。蛋白质的二级结构是指多肽链上主链骨架中各个肽段所形成的规则或无规则构象,包括α-螺旋、β-折叠、β-转角、无规卷曲,其间靠羰基和氨基之间形成的氢键来稳定,氢键是非共价键,压力很容易对其产生影响。巩雪等[18]研究100、200、300 MPa压力对扇贝肌结构影响,结果表明,与常压处理组相比,随着压力的增加,肌蛋白的二级结构发生了比较明显的变化:α-螺旋结构含量下降,β-折叠、β-转角和无规卷曲结构的含量逐渐增加;林素丽[19]在100~500 MPa的压力下处理米糠蛋白10 min,圆二色光谱分析结果表明,处理后的米糠蛋白中α-螺旋结构含量增多。二者研究结果的差异可能缘于蛋白质来源不同,可以明确的是超高压对蛋白质的二级结构有明显的影响,而压力对不同来源蛋白质二级结构的影响存在差异。蛋白质的三级结构是指二级结构的蛋白质其线性多肽链进一步折叠成为紧密结构时的三维空间排列,当具有三级结构的蛋白质亚基之间通过非共价键缔合后就形成蛋白质的四级结构。内源荧光强度、表面疏水性、活性巯基含量能反映蛋白质三级结构的变化,研究表明,随着超高压处理压力的增大,表面疏水性、活性巯基含量升高,相对内源荧光强度也发生变化,这表明蛋白质的三级结构在压力作用下发生改变。蛋白质的四级结构主要通过疏水相互作用来稳定,疏水相互作用对压力十分敏感,100~200 MPa的压力能分解蛋白质低聚物,同时使蛋白质的体积变小,即超高压处理会导致蛋白质解聚,并破坏连接的多肽链之间的疏水键,导致多肽链分离。
3.1.2 水合性质
蛋白质的水合性质指的是蛋白质分子中极性基团或肽键与水分子相互结合的性质,其通过蛋白质的肽键(偶极-偶极或氢键)或氨基酸侧链(离子的极性甚至非极性基团)同水分子之间的相互作用来实现[20]。研究证明,超高压处理会破坏蛋白质中非共价键的平衡并暴露二硫键、疏水基团和其他官能团,这些官能团可以拉伸蛋白质分子并影响蛋白质的水合性质。随处理压力的增加,一般而言,当超高压的作用压力在0~600 MPa时,随处理压力的增加,蛋白质溶解性呈现先下降后上升的趋势[21],但蛋白种类的差异和蛋白所处的环境会影响其溶解性,黄薇[22]研究发现,利用200、400、600 MPa压力处理小麦蛋白时,随着作用压力的上升,面筋蛋白和麦醇溶蛋白的溶解性下降,但麦谷蛋白的溶解性则升高;戴彩霞等[23]研究结果表明,200、400、600 MPa的压力处理菜籽蛋白时,pH 9下菜籽蛋白的溶解性(71.23%)最好。Cao Baiying等[24]利用高静水压处理从松子中提取的蛋白质,结果表明当压力在400 MPa时,球蛋白的持水能力从2.33 g/g增加到3.43 g/g。值得注意的是,蛋白质分子结构和组成的差异会使压力对蛋白质分子的持水能力的影响存在差异,黄薇[22]研究发现,与未处理的样品相比,200 MPa压力处理面筋蛋白的持水性下降,但是分别使用400、600 MPa压力处理后,面筋蛋白的持水性无显著性变化;麦醇溶蛋白的持水性随压力的增加而上升,麦谷蛋白经200、400 MPa高压处理后持水性下降,但当作用压力提升到600 MPa时,麦谷蛋白的持水性增加。
3.1.3 表面性质
蛋白质是两亲分子,它能自发地迁移到空气-水界面或油-水界面,这便是蛋白质的表面性质,乳化性和起泡性是典型的表面性质[25]。蛋白质乳化作用最重要的特征是其能够向油-水界面扩散和在界面的吸附能力。起泡性通常是气泡在连续的液相或含可溶性表面活性剂的半固相中形成的分散体系。周一鸣等[26]研究结果表明:与未处理的样品相比,当利用500 MPa压力作用于荞麦蛋白30 min时,乳化性(67.3 m2/g)、起泡性(91.5%)分别提高了33.0%、16.1%。吴溪[27]发现当压力作用于大豆分离蛋白时,大豆分离蛋白发生聚集,使蛋白的黏度和表面张力提升,大豆分离蛋白的起泡性得以提升,另一方面,压力使疏水基团暴露,蛋白质分子的表面柔顺性增强,分子间的聚集速率加快,蛋白的起泡能力也增强;乳化能力的提高则归因于超高压破坏蛋白质分子内部疏水相互作用,使得蛋白质的空间结构改变。有研究发现超高压处理时间对蛋白质的表面性质影响不显著,但蛋白质所处的溶液pH值会明显影响其表面性质[28],在碱性环境中进行压力处理能增强蛋白质的起泡性,在酸性环境中压力处理能增强泡沫稳定性。
3.1.4 流体动力学性质
流体动力学性质包括弹性、黏度、黏附性、内聚性、咀嚼性、凝胶性等,这些性质通常与蛋白质的大小、形状和柔顺性有关。此处着重介绍超高压对蛋白质凝胶特性的影响。变性的蛋白质分子聚集并形成有序的蛋白质网络的过程成为凝胶作用,凝胶是一种介于固体和液体之间的中间相,实质上是非稳态流体的一种稀释体系。凝胶通常与疏水相互作用的吸引和静电排斥作用之间的平衡有关,这两种力决定了蛋白质-蛋白质相互作用和蛋白质-溶剂相互作用[29]。王炳智[30]研究100~400 MPa压力对小麦面筋蛋白的凝胶特性的影响,实验结果表明利用300 MPa高压处理小麦面筋蛋白时,凝胶强度达到最大值((93.80±1.93)g),这是因为超高压处理使蛋白质分子结构展开,分子间疏水相互作用增强,形成三维网络结构,凝胶强度增加;当作用压力增加至400 MPa时,蛋白质分子发生部分聚集,蛋白质分子间的相互作用降低,凝胶强度下降。此外,超高压处理还可以暴露蛋白质分子内的巯基,从而促进二硫键的形成,疏水基团和二硫键的存在可以加强分子间网络结构,促进不可逆凝胶的形成[31]。Lu Wangwei等[32]在0~400 MPa 压力处理15 min的条件下制备罗非鱼鱼糜凝胶,发现超高压处理的鱼糜凝胶致密而柔韧,拉曼光谱实验结果证实了二硫键在罗非鱼鱼糜凝胶的形成中起重要作用。
3.2 超高压技术在蛋白质消化中的应用
一般来说,蛋白质消化是使用蛋白水解酶或酸水解蛋白质,食品中常见的水解蛋白酶有胃蛋白酶、胰蛋白酶、胰凝乳蛋白酶、木瓜蛋白酶和嗜热菌蛋白酶[33],蛋白质消化是利用蛋白质制备生物活性肽的重要步骤。但是,利用蛋白酶或酸水解蛋白质前需要消耗较长的时间来对样品进行前处理,除此之外,由于蛋白质的基质异质性,消化过程很难重复统一,因此蛋白质的消化是多肽制备过程中的主要瓶颈之一。在蛋白质消化前对其进行处理能提高消化效率,超高压是常见前处理方式之一,此外亚临界水水解、微波、超声波也是现阶段研究常用的新兴前处理方式[34]。超高压对蛋白质的消化起促进作用归因于:压力使蛋白质分子间和分子内二硫键和疏水键的重排;压力诱导裂解位点暴露,蛋白质去折叠的程度增加,天然蛋白质有着复杂的空间结构,经超高压处理后,酶与蛋白质分子接触位点数量增加,蛋白质消化率得以提高。Franck等[34]使用不同超高压(100、300 MPa)分别预处理亚麻籽蛋白5、10 min后,利用胰蛋白酶对亚麻籽蛋白进行水解,结果表明:300 MPa压力下处理会导致亚麻籽蛋白结构不稳定程度提高,超高压处理均能增加500~1 500 Da肽的相对丰度,在300 MPa下处理5 min和10 min,亚麻籽蛋白水解物的抗氧化活性分别提高了39%和55%。然而,也有研究表明,当施加的压力高达400~500 MPa时,蛋白质会因聚集而导致后续消化得到的活性肽含量降低。Chao Dongfang等[35]研究发现利用200 MPa预处理豌豆分离蛋白时,蛋白质去折叠层度和疏水基团的暴露量增多,对血管紧张素转化酶(angiotensin converting enzyme,ACE)抑制肽的释放有促进作用,但是当压力提升到400、600 MPa时,高压预处理对ACE抑制肽的释放产生了相反的效果。此外,超高压处理后蛋白质消化性的增强也归因于压力作用下蛋白质对酶或对底物-酶相互作用效果增强,相互接触更紧密[36]。
3.3 超高压技术在肽的分离/提取中的应用
目前超高压技术已被应用于不同来源蛋白质生物活性肽的分离提取(表1),这些蛋白质基质包括亚麻籽蛋白[34]、卵清蛋白[37]、扁豆蛋白[6]、大豆分离蛋白[38]、甘薯蛋白[39-40]、蘑菇脚蛋白[41]、β-乳球蛋白[42]、黑豆蛋白[43]、酪蛋白[44]、罗非鱼蛋白[45]等。Boukil等[46]利用400~600 MPa的压力处理β-乳球蛋白,处理后β-乳球蛋白的构象发生变化,疏水基团暴露,游离巯基的反应活性增加,胰蛋白酶水解提高了生物活性肽的产量;Al-Ruwaih等[47]发现高压处理(300~600 MPa、15 min)菜豆蛋白有助于其被碱性蛋白酶水解,水解产物的抗氧化活性显著提高。因此,超高压处理对肽的分离、提取有积极促进作用。
表1 超高压处理在生物活性肽分离提取中的应用
Table 1 Applications of ultra-high pressure in separation and extraction of bioactive peptides
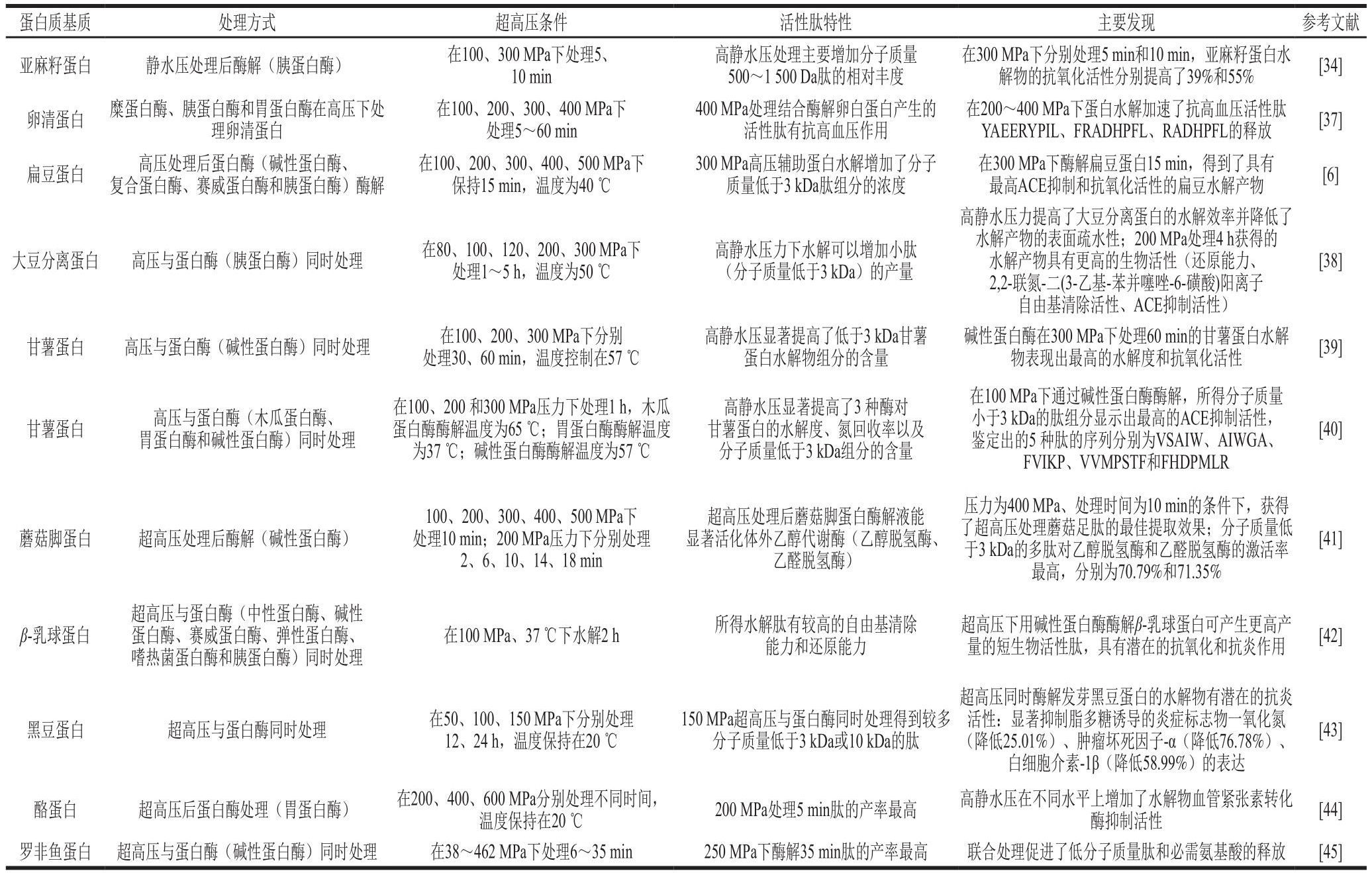
蛋白质基质 处理方式 超高压条件 活性肽特性 主要发现 参考文献亚麻籽蛋白 静水压处理后酶解(胰蛋白酶) 在100、300 MPa下处理5、10 min高静水压处理主要增加分子质量500~1 500 Da肽的相对丰度在300 MPa下分别处理5 min和10 min,亚麻籽蛋白水解物的抗氧化活性分别提高了39%和55% [34]卵清蛋白 糜蛋白酶、胰蛋白酶和胃蛋白酶在高压下处理卵清蛋白在100、200、300、400 MPa下处理5~60 min 400 MPa处理结合酶解卵白蛋白产生的活性肽有抗高血压作用在200~400 MPa下蛋白水解加速了抗高血压活性肽YAEERYPIL、FRADHPFL、RADHPFL的释放 [37]扁豆蛋白 高压处理后蛋白酶(碱性蛋白酶、复合蛋白酶、赛威蛋白酶和胰蛋白酶)酶解在100、200、300、400、500 MPa下保持15 min,温度为40 ℃300 MPa高压辅助蛋白水解增加了分子质量低于3 kDa肽组分的浓度在300 MPa下酶解扁豆蛋白15 min,得到了具有最高ACE抑制和抗氧化活性的扁豆水解产物 [6]大豆分离蛋白 高压与蛋白酶(胰蛋白酶)同时处理 在80、100、120、200、300 MPa下处理1~5 h,温度为50 ℃高静水压力下水解可以增加小肽(分子质量低于3 kDa)的产量高静水压力提高了大豆分离蛋白的水解效率并降低了水解产物的表面疏水性;200 MPa处理4 h获得的水解产物具有更高的生物活性(还原能力、2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)阳离子自由基清除活性、ACE抑制活性)[38]甘薯蛋白 高压与蛋白酶(碱性蛋白酶)同时处理 在100、200、300 MPa下分别处理30、60 min,温度控制在57 ℃高静水压显著提高了低于3 kDa甘薯蛋白水解物组分的含量碱性蛋白酶在300 MPa下处理60 min的甘薯蛋白水解物表现出最高的水解度和抗氧化活性 [39]甘薯蛋白 高压与蛋白酶(木瓜蛋白酶、胃蛋白酶和碱性蛋白酶)同时处理在100、200 和300 MPa压力下处理1 h,木瓜蛋白酶酶解温度为65 ℃;胃蛋白酶酶解温度为37 ℃;碱性蛋白酶酶解温度为57 ℃高静水压显著提高了3 种酶对甘薯蛋白的水解度、氮回收率以及分子质量低于3 kDa组分的含量在100 MPa下通过碱性蛋白酶酶解,所得分子质量小于3 kDa的肽组分显示出最高的ACE抑制活性,鉴定出的5 种肽的序列分别为VSAIW、AIWGA、FVIKP、VVMPSTF和FHDPMLR[40]蘑菇脚蛋白 超高压处理后酶解(碱性蛋白酶)100、200、300、400、500 MPa下处理10 min;200 MPa压力下分别处理2、6、10、14、18 min超高压处理后蘑菇脚蛋白酶解液能显著活化体外乙醇代谢酶(乙醇脱氢酶、乙醛脱氢酶)压力为400 MPa、处理时间为10 min的条件下,获得了超高压处理蘑菇足肽的最佳提取效果;分子质量低于3 kDa的多肽对乙醇脱氢酶和乙醛脱氢酶的激活率最高,分别为70.79%和71.35%[41]β-乳球蛋白超高压与蛋白酶(中性蛋白酶、碱性蛋白酶、赛威蛋白酶、弹性蛋白酶、嗜热菌蛋白酶和胰蛋白酶)同时处理在100 MPa、37 ℃下水解2 h 所得水解肽有较高的自由基清除能力和还原能力超高压下用碱性蛋白酶酶解β-乳球蛋白可产生更高产量的短生物活性肽,具有潜在的抗氧化和抗炎作用 [42]黑豆蛋白 超高压与蛋白酶同时处理 在50、100、150 MPa下分别处理12、24 h,温度保持在20 ℃150 MPa超高压与蛋白酶同时处理得到较多分子质量低于3 kDa或10 kDa的肽超高压同时酶解发芽黑豆蛋白的水解物有潜在的抗炎活性:显著抑制脂多糖诱导的炎症标志物一氧化氮(降低25.01%)、肿瘤坏死因子-α(降低76.78%)、白细胞介素-1β(降低58.99%)的表达[43]酪蛋白 超高压后蛋白酶处理(胃蛋白酶) 在200、400、600 MPa分别处理不同时间,温度保持在20 ℃ 200 MPa处理5 min肽的产率最高 高静水压在不同水平上增加了水解物血管紧张素转化酶抑制活性 [44]罗非鱼蛋白 超高压与蛋白酶(碱性蛋白酶)同时处理 在38~462 MPa下处理6~35 min 250 MPa下酶解35 min肽的产率最高 联合处理促进了低分子质量肽和必需氨基酸的释放 [45]
3.4 超高压技术在抗氧化肽制备中的应用
过量的自由基会产生氧化应激效应,这可能会降低高脂食物的品质,缩短食物的保质期,同时氧化损伤可能引起多种慢性疾病,如糖尿病、阿尔茨海默病、关节炎、心脏病和癌症等。抗氧化肽的潜在作用机制主要包括清除氧自由基、螯合金属离子、抑制脂质过氧化反应、激活机体的抗氧化防御系统[11]。抗氧化肽的来源包括鹰嘴豆[48]、乳清蛋白[49]、小麦面筋蛋白[50]、亚麻籽蛋白[34]、扁豆蛋白[6]、甘薯蛋白[39]、β-乳球蛋白[42]、酪蛋白[44]等。一般来说,这些多肽可以通过原料蛋白酶解制备,常用酶的来源包括微生物源(碱性蛋白酶、中性蛋白酶和风味酶)、动物源(胃蛋白酶和胰蛋白酶)和植物源(菠萝蛋白酶和木瓜蛋白酶)。庞佳坤[49]使用超高压预处理来提高乳清蛋白蛋白的分解,以产生抗氧化肽,400 MPa超高压处理处理30 min对乳清蛋白二级、三级结构的影响最显著,得到抗氧化肽的2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)阳离子自由基清除率达到65.18%。盛小波[51]研究了超高压处理对乳清蛋白水解抗氧化活性的影响,结果表明300 MPa超高压处理30 min时,乳清蛋白的水解度达30.33%,所得乳清蛋白肽中分子质量低于3 kDa的组分III抗氧化活性较强。李艳红[48]研究发现超高压处理压力显著影响抗氧化肽的释放,100~200 MPa压力处理对鹰嘴豆蛋白水解程度无显著影响,当压力上升到300 MPa时可提高酶解速率,但当压力增加至400~600 MPa时酶解速率降低。以上研究表明,一定的超高压处理压力和作用时间对抗氧化肽的制备具有积极影响,但具体的制备工艺需要优化。
4 结 语
蛋白质和生物活性多肽具有丰富的功能性质以及与人体健康相关的多种生物活性,已受到广泛的关注,然而,生物活性多肽的商业化开发仍然具有挑战性。最近的研究表明,一方面,超高压可以对蛋白质进行改性,以改善蛋白质的结构和功能性质;另一方面,超高压可以促进生物活性多肽的产生,超高压处理后的蛋白质能够更高效地转化成生物活性多肽。综上所述,超高压技术是一种蛋白质改性和制备生物活性多肽的可行技术。未来还需要更多的研究,以促进超高压技术在蛋白质和多肽领域的应用。
[1]陆佳俊, 刘春娥, 黄昆仑, 等.海洋食品中海洋多糖、生物活性肽与皂苷类化合物改善代谢综合征的机制[J].中国食品学报, 2021,21(9): 346-351.DOI:10.16429/j.1009-7848.2021.09.038.
[2]黄沐晨, 杨傅佳, 陈旭, 等.海洋源生物活性肽的构效关系与作用机理研究进展[J].食品科学, 2021, 42(19): 271-280.DOI:10.7506/spkx1002-6630-20200702-035.
[3]吴丰旭.蛋白-蛋白/小分子相互作用的分子模拟新方法研究[D].武汉: 华中师范大学, 2019: 51.
[4]PINO F R, CARPIO F J E, GUADIX E M.Bioactive fish hydrolysates resistance to food processing[J].LWT-Food Science and Technology,2020, 117: 108670.DOI:10.1016/j.lwt.2019.108670.
[5]KESKIN U S, FOROUGH J, WU J P.Novel technologies for the production of bioactive peptides[J].Trends in Food Science &Technology, 2021, 108: 27-39.DOI:10.1016/J.TIFS.2020.12.002.
[6]MORA P G, PENAS E, FRIAS J, et al.High-pressure improves enzymatic proteolysis and the release of peptides with angiotensin I converting enzyme inhibitory and antioxidant activities from lentil proteins[J].Food Chemistry, 2015, 171: 224-232.DOI:10.1016/j.foodchem.2014.08.116.
[7]刘铭, 刘玉环, 王允圃, 等.制备、纯化和鉴定生物活性肽的研究进展及应用[J].食品与发酵工业, 2016, 42(4): 244-251.DOI:10.13995/j.cnki.11-1802/ts.201604045.
[8]王玉帅.动物源活性肽调节拟南芥生长的活性及机理研究[D].福州: 福州大学, 2017: 2-5.
[9]赵烜影, 刘振民, 雍靖怡, 等.乳源生物活性肽研究进展[J].乳业科学与技术, 2021, 44(6): 51-57.DOI:10.15922/j.cnki.jdst.2021.06.010.
[10]KADAM S U, TIWARI B K, ÁLVARES C, et al.Ultrasound applications for the extraction, identification and delivery of food proteins and bioactive peptides[J].Trends in Food Science &Technology, 2015, 46(1): 60-67.DOI:10.1016/j.tifs.2015.07.012.
[11]WEN C T, ZHANG J X, ZHANG H H, et al.Plant protein-derived antioxidant peptides: isolation, identification, mechanism of action and application in food systems: a review[J].Trends in Food Science &Technology, 2020, 105: 308-322.DOI:10.1016/j.tifs.2020.09.019.
[12]陈启航, 文丽华, 陈小娥, 等.超高压辅助脱壳对虾夷扇贝肌原纤维蛋白生化特性及结构的影响[J].食品科学, 2021, 42(11): 102-107.DOI:10.7506/spkx1002-6630-20200603-040.
[13]赵飞.物理预处理对大豆分离蛋白结构和理化性质的影响机制[D].泰安: 山东农业大学, 2019: 9.
[14]王硕, 黄薇, 王金荣, 等.食品非热加工技术: 超高压在蛋白质和淀粉改性中的应用[J].中国食品学报, 2015, 15(6): 1-13.DOI:10.16429/j.1009-7848.2015.06.001.
[15]NADERI N, HOUSE J D, POULIOT Y, et al.Effects of high hydrostatic pressure processing on hen egg compounds and egg products[J].Comprehensive Reviews in Food Science and Food Safety, 2017, 16(4): 707-720.DOI:10.1111/1541-4337.12273.
[16]郑海波.高压下加热处理对鸡肉糜凝胶品质的影响及机制研究[D].南京: 南京农业大学, 2018: 13-24.
[17]党慧杰.超高压协同酶水解对乳清分离蛋白理化及致敏性的影响[D].上海: 上海海洋大学, 2021: 9.
[18]巩雪, 常江, 李丹婷, 等.超高压对扇贝界面闭壳肌结构的影响[J].食品科学, 2021, 42(13): 87-93.DOI:10.7506/spkx1002-6630-20200623-314.
[19]林素丽.超高压处理对米糠蛋白功能及结构特性的影响研究[D].杭州: 浙江大学, 2017: 28.
[20]王莹, 王瑛瑶, 刘建学, 等.花生蛋白水合性质的研究进展[J].食品工业科技, 2014, 35(13): 374-377.DOI:10.13386/j.issn1002-0306.2014.13.073.
[21]SPERONI F, BEAUMAL V, LAMBALLERIE M D, et al.Gelation of soybean proteins induced by sequential high-pressure and thermal treatments[J].Food Hydrocolloids, 2009, 23: 1433-1442.DOI:10.1016/j.foodhyd.2008.11.008.
[22]黄薇.超高压对小麦面筋蛋白改性及应用的研究[D].天津: 天津科技大学, 2016: 22-25.
[23]戴彩霞, 何荣.超高压和加热处理对菜籽蛋白功能性质和结构的影响研究[J].中国油脂, 2019, 44(7): 68-74.DOI:10.3969/j.issn.1003-7969.2019.07.015.
[24]CAO Baiying, LI Fang, LIU Chunlei, et al.Effects of high hydrostatic pressure on the functional and rheological properties of the protein fraction extracted from pine nuts[J].Food Science and Technology International, 2018, 24(1): 53-66.DOI:10.1177/1082013217726883.
[25]王碧璇.利用大豆蛋白制备大豆蛋白基表面活性剂的研究[D].柳州: 广西科技大学, 2019: 2-3.
[26]周一鸣, 杜丽娜, 李云龙, 等.高静水压和热处理对荞麦蛋白功能性质的影响[J].食品科学, 2021, 42(5): 77-83.DOI:10.7506/spkx1002-6630-20200210-084.
[27]吴溪.超高压辅助木瓜蛋白酶改善大豆分离蛋白起泡性及其应用[D].哈尔滨: 东北农业大学, 2017: 28-31.
[28]杜丽娜.超高压处理对荞麦13S球蛋白结构与功能特性的影响[D].上海: 上海应用技术大学, 2020: 26-27.
[29]王盼盼.食品中蛋白质的功能特性综述[J].肉类研究, 2010, 24(5):62-71.
[30]王炳智.高压与TG酶处理对小麦面筋蛋白的凝胶性影响研究[D].合肥: 合肥工业大学, 2019: 24-28.
[31]MA R R, LIU H P, LI Y H, et al.Effects of high hydrostatic pressure treatment: characterization of eel (Anguilla japonica) surimi, structure,and angiotensin-converting enzyme inhibitory activity of myofibrillar protein[J].Food and Bioprocess Technology, 2021, 14: 1641-1639.DOI:10.1007/S11947-021-02658-3.
[32]LU Wangwei, QIN Yuyue, RUAN Zheng.Effects of high hydrostatic pressure on color, texture, microstructure, and proteins of the tilapia(Orechromis niloticus) surimi gels[J].Journal of Texture Studies, 2020,52(2): 177-186.DOI:10.1111/jtxs.12572.
[33]李希宇, 林伟玲, 杨怀谷, 等.不同蛋白酶水解牛肉蛋白产物的ACE抑制活力比较[J].现代食品科技, 2021, 37(10): 197-204; 161.DOI:10.13982/j.mfst.1673-9078.2021.10.0212.
[34]FRANCK M, PERREAULT V, SUWAL S, et al.High hydrostatic pressure-assisted enzymatic hydrolysis improved protein digestion of flaxseed protein isolate and generation of peptides with antioxidant activity[J].Food Research International, 2019, 115: 467-473.DOI:10.1016/j.foodres.2018.10.034.
[35]CHAO Dongfang, HE Rong, JUNG S, et al.Effect of pressure or temperature pretreatment of isolated pea protein on properties of the enzymatic hydrolysates[J].Food Research International, 2013, 54(2):1528-1534.DOI:10.1016/j.foodres.2013.09.020.
[36]TOLDRA M, PARES D, SAGUER E, et al.Hemoglobin hydrolysates from porcine blood obtained through enzymatic hydrolysis assisted by high hydrostatic pressure processing[J].Innovative Food Science and Emerging Technologies, 2011, 12(4): 435-442.DOI:10.1016/j.ifset.2011.05.002.
[37]QUIROS A, CHICHON R, RECIO I, et al.The use of high hydrostatic pressure to promote the proteolysis and release of bioactive peptides from ovalbumin[J].Food Chemistry, 2006, 104(4): 1734-1739.DOI:10.1016/j.foodchem.2006.10.050.
[38]GUAN H N, DIAO X Q, JIANG F, et al.The enzymatic hydrolysis of soy protein isolate by corolase PP under high hydrostatic pressure and its effect on bioactivity and characteristics of hydrolysates[J].Food Chemistry, 2018, 245: 89-96.DOI:10.1016/j.foodchem.2017.08.081.
[39]ZHANG M, MU T H.Identification and characterization of antioxidant peptides from sweet potato protein hydrolysates by alcalase under high hydrostatic pressure[J].Innovative Food Science and Emerging Technologies, 2017, 43: 92-101.DOI:10.1016/j.ifset.2017.08.001.
[40]NAZIR M A, MU T H, ZHANG M.Preparation and identification of angiotensin I-converting enzyme inhibitory peptides from sweet potato protein by enzymatic hydrolysis under high hydrostatic pressure[J].International Journal of Food Science & Technology, 2020, 55(2): 482-489.DOI:10.1111/ijfs.14291.
[41]ZHAO R J, HUO C Y, QIAN Y, et al.Ultra-high-pressure processing improves proteolysis and release of bioactive peptides with activation activities on alcohol metabolic enzymes in vitro from mushroom foot protein[J].Food Chemistry, 2017, 231: 25-32.DOI:10.1016/j.foodchem.2017.03.058.
[42]BAMDAD F, BARK S, KWON C H, et al.Anti-inflammatory and antioxidant properties of peptides released from β-lactoglobulin by high hydrostatic pressure-assisted enzymatic hydrolysis[J].Molecules,2017, 22(6): 949.DOI:10.3390/molecules22060949.
[43]KIM Y M, JANG T G, OH N S, et al.Characteristics and in vitro antiinflammatory activities of protein extracts from pre-germinated black soybean [Glycine max (L.)]treated with high hydrostatic pressure[J].Innovative Food Science and Emerging Technologies, 2017, 43: 84-91.DOI:10.1016/j.ifset.2017.07.027.
[44]HU G L, ZHENG Y R, LIU Z M, et al.Effects of high hydrostatic pressure, ultraviolet light-C, and far-infrared treatments on the digestibility, antioxidant and antihypertensive activity of α-casein[J].Food Chemistry, 2017, 221: 1860-1866.DOI:10.1016/j.foodchem.2016.10.088.
[45]HEMKER A K, NGUYEN L T, KARWE M, et al.Effects of pressureassisted enzymatic hydrolysis on functional and bioactive properties of tilapia (Oreochromis niloticus) by-product protein hydrolysates[J].LWT-Food Science and Technology, 2020, 122: 109003.DOI:10.1016/j.lwt.2019.109003.
[46]BOUKIL A, SUWAL S, CHAMBERLAND J, et al.Ultrafiltration performance and recovery of bioactive peptides after fractionation of tryptic hydrolysate generated from pressure-treated β-lactoglobulin[J].Journal of Membrane Science, 2018, 556: 42-53.DOI:10.1016/j.memsci.2018.03.079.
[47]AL-RUWAIH N, AHMED J, MULLA M F, et al.High-pressure assisted enzymatic proteolysis of kidney beans protein isolates and characterization of hydrolysates by functional, structural, rheological and antioxidant properties[J].LWT-Food Science and Technology,2018, 100: 231-236.DOI:10.1016/j.lwt.2018.10.074.
[48]李艳红.鹰嘴豆蛋白酶解物的制备及其抗氧化肽的研究[D].无锡:江南大学, 2008: 1.
[49]庞佳坤.超高压协同酶解对乳清蛋白理化及功能特性的影响[D].上海: 上海海洋大学, 2020: 1-3.
[50]乔晓林.酶解小麦面筋蛋白制备抗氧化肽工艺优化[D].西安: 陕西科技大学, 2014: 1.
[51]盛小波.超高压处理对牛乳清蛋白水解及其产物抗氧化活性的影响[D].北京: 中国农业科学院, 2011: 30-34.