粗壮女贞苦丁茶(Ligustrum robustum (Rxob.)Blume)是我国传统的植物代用茶和药食同源植物,对人体无毒无害,目前在我国四川、贵州、云南及重庆等地有广泛的种植,其相关产品(口服含片、泡袋剂和软饮料等)占有一定的市场份额[1-3]。现代医学研究表明苦丁茶具有泻火生津、清热解毒和杀菌消炎等作用。据报道,粗壮女贞苦丁茶富含酚类物质,具有多种临床药理作用和保健功效,如:抗氧化、镇痛消炎,降血压、降血脂和增强免疫力等[4]。然而,酚类物质暴露于空气中或者处于不适宜的pH环境时,会发生聚合或者降解,使其抗氧化能力等活性功效降低。同时,酚类物质需要经人体消化吸收才能在人体内发挥其生物活性,而人体消化系统的水基环境以及低pH值的胃液限制了人体对酚类物质的吸收[5]。包埋可以保护生物活性物质,有利于延长活性物质的释放,并提高其稳定性和生物活性。目前,相关领域已有大量研究着重于开发和设计高分子聚合物,用于负载和保护敏感的酚类物质,然而高昂的原料价格和制作成本,以及合成类物质潜在的毒性限制了其在食品工业的推广和应用[6-8]。因此,无毒无害、价格低廉的食品级缓释载体的选择、设计及开发,对于酚类物质在食品及生物医药领域的高效利用具有深远意义[6]。
淀粉作为植物光合作用的主要能量储存形式,不仅是食品加工业中的常见原料,同时因其具有来源广泛、天然易得、无毒无害、价格低廉及生物相容性好等特性,可作为微胶囊壁材及包裹药剂缓释基材等的原料,对于活性益生菌及敏感药物的保护具有显著的效果[7-9]。有研究表明,淀粉能够通过物理及化学作用与酚类等生物活性物质发生相互作用,从而保护其免受环境不良因素的破坏[10]。
虽然已有研究对淀粉缓释载体进行了探索,但基于淀粉对苦丁茶提取物在水基环境及人体消化环境中的缓释及活性保护作用的内容鲜有报道。本实验以粗壮女贞苦丁茶和小麦淀粉作为研究对象,提取、鉴定粗壮女贞苦丁茶中的活性成分测定其抗氧化活性,并探究小麦淀粉对粗壮女贞苦丁茶提取物(Ligustrum robustum (Rxob.)Blume extract,LRE)的负载能力、抗氧化活性保护效果及在体外模拟消化系统中的缓释能力,以期为LRE在淀粉功能性食品及保健品中的开发利用提供理论与实验参考。
1 材料与方法
1.1 材料与试剂
粗壮女贞苦丁茶(干物质,泸州市梅山茶叶有限公司)和小麦淀粉(食品级,中粮集团有限公司)购于四川成都当地市场,密封常温避光保存备用。
1,1-二苯基-2-三硝基苯肼(1,1-dipheny l-2-picrylhydrazyl,DPPH)、Folin-Ciocalteu试剂、α-淀粉酶、胃蛋白酶 上海阿拉丁试剂公司;碳酸钠、没食子酸、无水乙醇、磷酸二氢钠、磷酸氢二钠、铁氰化钾、三氯乙酸、三氯化铁、氯化钠、氯化钾、氢氧化钠、浓盐酸(均为国产分析纯)成都金山化学试剂有限公司;实验用水为蒸馏水。
1.2 仪器与设备
SHB-III型循环水式多用真空泵 郑州长城科工贸有限公司;RE-52AA型旋转蒸发器 上海亚荣生化仪器厂;LGJ-30F型真空冷冻干燥机 宁波新艺超声设备有限公司;1290-6460型高效液相色谱-质谱联用仪、400-MR DD2型核磁共振波谱仪 美国安捷伦科技有限公司;UV-1800BPC紫外-可见分光光度计 上海美谱达仪器有限公司;GZX-GF101-2-BS型电热恒温鼓风干燥箱上海跃进医疗器械有限公司;GL-20G-C型高速冷冻离心机上海安亭科学仪器厂;ODS-3反相柱 日本GL-Science公司。
1.3 方法
1.3.1 LRE的制备
将苦丁茶叶破碎得到粗茶粉,取750 g(干基)粗茶粉与5500 mL蒸馏水混合,25 ℃搅拌提取24 h,对提取液真空减压抽滤,所得滤液于50 ℃真空浓缩至2000 mL,浓缩液于5000 r/min、25 ℃离心15 min,取上清液于-65~-55 ℃干燥48 h得提取物90.98 g(该条件下提取率为12.13%),所得LRE置于-20 ℃,密封冷冻保存备用[4]。
1.3.2 LRE的总酚含量测定
采用福林-酚法进行测定。分别吸取0.1 mL不同质量浓度(0.1、0.2、0.3、0.4、0.5、0.6 mg/mL)的没食子酸标准溶液与2 mL碳酸钠溶液(20 mg/mL)混匀,25 ℃孵育2 min,加入0.9 mL用蒸馏水1∶1稀释的Folin-Ciocalteu试剂溶液,混匀,25 ℃避光孵育30 min,于750 nm波长测定反应溶液的吸光度,使用Origin 8.0绘制没食子酸标准曲线并进行线性拟合,建立总酚质量浓度(x,mg/mL)与溶液吸光度(y)回归方程:y=1.21411x-0.0173,R2=0.9939。取0.1 mL的LRE溶液(5 mg/mL)替代没食子酸标准溶液,并按上述步骤反应,将测得吸光度代入回归方程,计算得到LRE的总酚含量(以没食子酸当量计算)为(178±1.64)mg/g。
1.3.3 LRE主要成分鉴定
1.3.3.1 高效液相色谱-质谱联用仪法[11-13]。
色谱条件:使用ODS-3反相柱(Inertsil PREPODS-3,4.6 mm×250 mm,5 μm);流动相:A为甲醇,B为0.1%甲酸溶液;洗脱程序:0~10 min,0%~50% A、100%~50% B;10~15 min,50%~60% A、50%~40% B;15~20 min,60%~70% A、40%~30% B;20~25 min,70%~80% A、30%~20% B;25~30 min,80%~90% A、20%~10% B;30~33 min,90%~100% A、10%~0% B;检测波长为280 nm;参比波长为360 nm;柱温为25 ℃;进样量为20 μL;样品质量浓度为10 mg/mL(超纯水作溶剂,0.45 μm滤膜过滤)。
质谱条件:扫描范围m/z 50~1200;毛细管电压140 V;干燥气流速1 L/min;干燥温度200 ℃;雾化气压14 psi;离子化方式为电喷雾电离,负离子模式。
1.3.3.2 核磁共振法[11-13]
取2 mg经高效液相色谱分离和制备得到的各主要洗脱峰物质,经重水(D2O)交换和氘代甲醇(CD3OD)溶解至均一状态,于25 ℃测定样品的核磁共振氢谱(共振频率400 MHz)和核磁共振碳谱(共振频率100 MHz)。使用MestReNova软件(version 12.0.1 for Windows,Mestrelab Research SL.,Galicia,Spain)对样品核磁共振图谱的数据进行获取和处理。
1.3.4 LRE体外抗氧化活性的测定
1.3.4.1 对DPPH自由基的清除能力
用95%乙醇溶液配制浓度为0.1 mmol/L的DPPH自由基溶液,现配现用。取2 mL 不同质量浓度(0.01~0.08 mg/mL)的LRE溶液与2 mL DPPH自由基溶液混合,25 ℃避光孵育30 min后,于517 nm处测定反应溶液的吸光度,并以95%乙醇溶液作为空白对照,计算LRE对DPPH自由基清除能力的半数有效浓度(concentration for 50% of maximal effect,EC50)。DPPH自由基清除率计算公式如下[14]:
1.3.4.2 还原能力的测定
取2.5 mL不同质量浓度(0.1~0.3 mg/mL)的LRE溶液,分别加入2.5 mL磷酸缓冲液(0.2 mmol/L,pH 6.6)和2.5 mL铁氰化钾溶液(1 g/100 mL),混匀后于50 ℃孵育20 min,迅速冷却,然后加入2.5 mL三氯乙酸溶液(10 g/100 mL),混匀,25 ℃、3000 r/min离心10 min,取2.5 mL上清液,向其中加入2.5 mL蒸馏水和0.5 mL三氯化铁溶液(0.1 g/100 mL),混匀后测定反应溶液在700 nm处的吸光度[14]。
1.3.5 小麦淀粉负载LRE的能力及稳定性的测定
向10 mL蒸馏水中分别加入0.24 g LRE和不同添加量(0.0、0.2、0.4、0.6、0.8、1.0 g和1.2 g,干物质)的小麦淀粉,随后沸水浴30 min,其间不断搅拌。然后,冰水浴60 min经冷冻干燥机干燥处理。将所得冻干样品全部粉碎并完全分散于60 mL蒸馏水,于37 ℃孵育,并分别连续搅拌0.5、1.0、2.0、3.0、5.0、7.0 h和9.0 h。随后,取不同孵育时间的样品进行离心过滤(25 ℃、4000 r/min离心10 min),收集滤液,用福林-酚法测定其总酚含量[15]。同时,以未添加LRE但经过相同处理的样品作为空白对照。以总酚累计释放量表征小麦淀粉对LRE的负载能力及负载稳定性,计算公式如下:
1.3.6 小麦淀粉对LRE抗氧化活性的影响
1.3.6.1 DPPH自由基清除能力
向2 g/100 mL(干物质)的淀粉悬浊液中加入LRE使其质量浓度达到0.06 mg/mL,于沸水浴中连续搅拌30 min,随后迅速转入冰水中冷却至室温(25 ℃)。使用1.3.4.1节方法测定样品初始的DPPH自由基清除能力。随后将样品转入含有均匀气孔的容器内,并将其置于60 ℃的鼓风干燥箱内分别孵育12、24、36、48 h和60 h。此外,每间隔6 h向容器内补充一次被蒸发掉的水分,并搅拌均匀;取不同孵育时间的样品,测定其DPPH自由基清除能力,且每次取样前使用高速匀浆机对样品进行均质化处理(8500 r/min,均质2 min)。同时,以未添加LRE但经过相同处理的样品作为空白对照。样品DPPH自由基清除能力的变化以相对清除能力表征,计算公式如下[14]:

1.3.6.2 还原能力
向2 g/100 mL(干物质)的淀粉悬浊液中加入LRE使其质量浓度达到0.5 mg/mL,于沸水浴中连续搅拌30 min,随后迅速转入冰水中冷却至室温(25 ℃)。使用1.3.4.2节方法,测定样品初始的还原能力,按照1.3.6.1节所示方法对样品进行处理及取样。样品还原能力的变化以相对还原能力的改变进行表征,计算公式[14]如下:

1.3.7 LRE在体外消化系统中释放速度的测定
采用口腔消化模拟和胃部消化模拟测定LRE在体外消化系统中的释放速度。人工唾液的配制:向1000 mL蒸馏水中分别加入1.594 g氯化钠、0.202 g氯化钾和5 g α-淀粉酶,搅拌均匀即得人工唾液。人工胃液的配制:取234 mL浓盐酸(质量分数约37%),加水稀释至1000 mL得所用稀盐酸。取16.4 mL稀盐酸,分别加入800 mL蒸馏水和10 g胃蛋白酶,搅拌均匀后定容至1000 mL即得人工胃液[16]。
向10 mL蒸馏水中分别加入0.24 g LRE和不同添加量(0.0、0.2、0.4、0.6、0.8、1.0 g和1.2 g,干物质)的小麦淀粉,于沸水浴中连续搅拌30 min。然后,于冰水浴中放置60 min后制得测试样品。此外,模拟体外消化前,将体外消化液(人工唾液和人工胃液)和测试样品预热至37 ℃。体外消化模拟程序如下:首先,向测试样品中加入10 mL人工唾液,于37 ℃振荡孵育10 min,以模拟口腔消化。随后向完成口腔消化模拟的样品中加入10 mL人工胃液,于37 ℃分别振荡孵育30、60、90、120 min,以模拟胃部消化[16]。然后,收集各消化阶段的样品,于4 ℃、10000 r/min离心15 min,收集上清液,于672 nm波长处测定上清液的吸光度,代入LRE质量浓度(x,mg/mL)与吸光度(y)之间的回归方程中:y=0.13298x-0.0442,R2=0.99784,以计算从淀粉中释放进入至消化液中的LRE含量,而LRE累计释放量按下式计算:
1.4 数据处理与分析
每组实验重复进行3 次,结果以![]() 表示。采用Origin 2018软件(OriginLab Corporation,MA,USA)进行作图。采用SPSS 20.0软件(SPSS Inc.,Chicago,IL,USA)进行统计学分析(ANOVA),差异显著,P<0.05。
表示。采用Origin 2018软件(OriginLab Corporation,MA,USA)进行作图。采用SPSS 20.0软件(SPSS Inc.,Chicago,IL,USA)进行统计学分析(ANOVA),差异显著,P<0.05。
2 结果与分析
2.1 LRE主要成分的分析
由图1可知,LRE中有3 个主要的成分,其质谱和核磁数据如下:
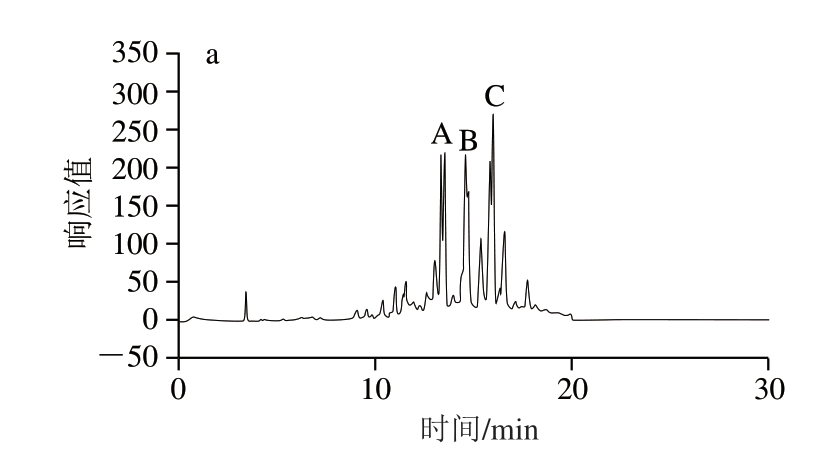
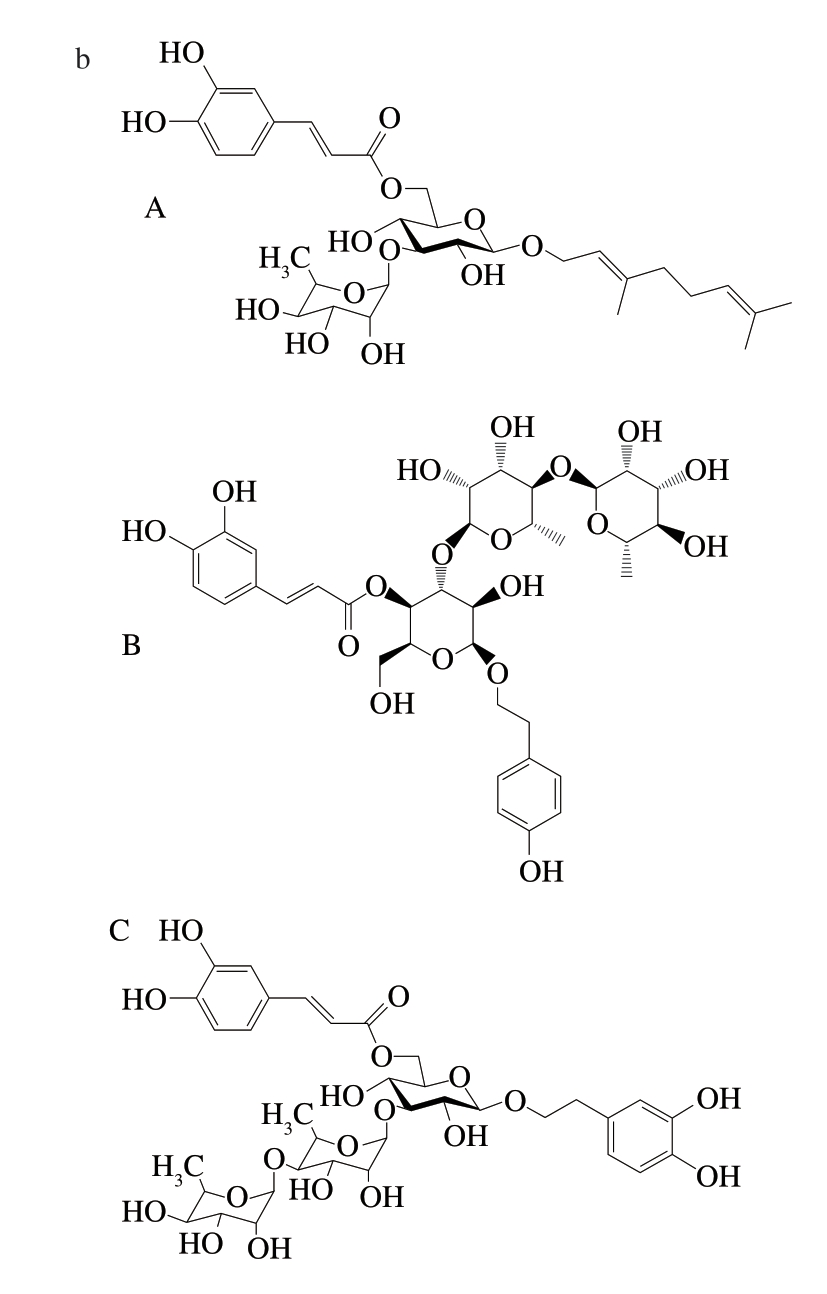
图1 LRE主要成分的分离(a)及结构鉴定(b)
Fig.1 Isolation (a) and identification (b) of the major components of LRE
洗脱峰A对应的物质:质谱给出准分子离子峰m/z 623 [M-H]-。1H-NMR(CD3OD,600 MHz):δ 7.62(1H,d,J=15.9 Hz,H-7''')、7.08(1H,d,J=2.3 Hz,H-2''')、6.94(1H,dd,J=8.3,2.1 Hz,H-5''')、6.82(1H,d,J=8.1 Hz,H-6''')、6.23(1H,d,J=15.7 Hz,H-8''')、5.38(1H,t,J=7.1 Hz,H-2)、5.06(1H,t,J=6.5 Hz,H-6)、4.39(1H,dd,J=12.1,7.3 Hz,H-1a)、4.22(1H,dd,J=11.5,7.3 Hz,H-1b)、2.15(2H,t,J=6.5 Hz,H-5)、1.97(2H,t,J=7.5 Hz,H-4)、1.74(6H,s,H-8,10)、1.58(3H,s,H-9);13C-NMR(CD3OD,150 MHz):δ 168.6(C=O)、150.2(C-4''')、148.2(C-8''')、147.1(C-3''')、141.9(C-3)、133.6(C-7)、127.4(C-1''')、125.7(C-6)、123.5(C-6''')、121.3(C-2)、116.8(C-5''')、115.1(C-2''')、114.6(C-7''')、103.4(C-1')、102.3(C-1'')、82.1(C-3')、76.5(C-2',5')、73.6(C-4'')、72.3(C-2'')、71.9(C-3'')、70.6(C-4')、69.9(C-5'')、67.2(C-1)、62.8(C-6')、41.1(C-4)、27.3(C-5)、25.7(C-8)、18.8(C-6'')、17.4(C-9)、16.3(C-10)。分析结果可知该物质分子式为C31H44O13,参考文献[11]可知,该物质为粗壮女贞苷B(3.87 mg/g)。
洗脱峰B 对应的物质:质谱给出准分子离子峰m/z:753 [M-H]-。1H-NMR(CD3OD,600 MHz):δ 7.81(1H,d,J=15.7 Hz,H-7'''')、7.32(2H,d,J=8.7 Hz,H2-2,6)、7.28(1H,d,J=2.2 Hz,H-2'''')、7.17(1H,dd,J=2.2,8.3 Hz,H-6'''')、7.05(1H,d,J=8.3 Hz,H-5'''')、6.92(2H,d,J=8.7 Hz,H2-3,5)、6.52(1H,d,J=15.7 Hz,H-8'''')、5.36(1H,d,J=1.6 Hz,H-1'')、5.23(1H,d,J=1.7 Hz,H-1''')、5.15(1H,t,J=9.5 Hz,H-4')、4.45(1H,d,J=7.3 Hz,H-1')、4.12(1H,m,Hb-8)、3.93(1H,m,Ha-8)、3.11(2H,t,J=6.7 Hz,H2-7)、1.31(3H,d,J=6.5 Hz,H3-6'')、1.23(3H,d,J=6.4 Hz,H3-6''');13C-NMR(CD3OD,150 MHz):δ 168.7(C=O)、156.9(C-4)、150.7(C-4'''')、148.3(C-7'''')、146.9(C-3'''')、131.6(C-2,6)、130.8(C-1)、127.7(C-1'''')、124.5(C-6'''')、117.3(C-5'''')、116.5(C-3,5)、115.7(C-2'''')、115.1(C-8'''')、105.1(C-1')、104.3(C-1'')、102.5(C-1''')、81.9(C-4'')、81.4(C-3')、76.9(C-5')、76.2(C-2')、75.1(C-4''')、74.2(C-2''')、72.9(C-3''')、72.5(C-2'')、72.2(C-8)、71.1(C-3'')、70.2(C-4')、69.4(C-5'',5''')、63.1(C-6')、37.3(C-7)、19.2(C-6'')、18.3(C-6''')。分析结果可知该物质分子式为C35H46O18,参考文献[12]可知,该物质为粗壮女贞苷N(3.32 mg/g)。
洗脱峰C对应的物质:质谱给出准分子离子峰m/z 759[M-H]-。1H-NMR(CD3OD,600 MHz):δ 7.58(1H,d,J=15.9 Hz,H-7'''')、7.05(1H,d,J=1.9 Hz,H-2'''')、6.89(1H,dd,J=8.4,1.9 Hz,H-6'''')、6.78(1H,d,J=8.4 Hz,H-5'''')、6.69(1H,d,J=2.1 Hz,H-2)、6.64(1H,d,J=8.2 Hz,H-5)、6.56(1H,dd,J=8.0,2.0 Hz,H-6)、6.28(1H,d,J=15.8 Hz,H-8'''')、5.19(1H,s,H-1'')、5.18(1H,s,H-1''')、4.51(1H,dd,J=12.0,1.8 Hz,H-6'a)、4.35(1H,d,J=8.1 Hz,H-1')、4.34(1H,J=11.9,6.3 Hz,H-6'b)、4.13(1H,dd,J=9.5,6.2 Hz,H-5'')、3.98(1H,m,H-2'')、3.98(1H,m,H-8a)、3.87(1H,m,H-2''')、3.87(1H,m,H-3'')、3.74(1H,m,H-8b)、3.73(1H,m,H-5''')、3.58(1H,m,H-3''')、3.56(1H,m,H-5')、3.54(1H,m,H-4'')、3.51(1H,m,H-3')、3.43(1H,m,J=9.9 Hz,H-4')、3.42(1H,m,H-4''')、3.33(1H,m,H-2')、2.78(1H,t,J=7.5 Hz,H-7)、1.28(3H,d,J=6.5 Hz,H-6''')、1.26(3H,d,J=6.5 Hz,H-6'');13C-NMR(CD3OD,150 MHz):δ 169.7(C-9'''')、150.2(C-4'''')、147.8(C-7'''')、146.9(C-3'''')、146.3(C-4)、144.9(C-3)、132.1(C-1)、127.6(C-1'''')、124.3(C-6'''')、121.5(C-6)、117.8(C-2)、116.8(C-5)、116.4(C-5'''')、115.7(C-2'''')、115.1(C-8'''')、105.1(C-1')、103.5(C-1'')、102.8(C-1''')、83.4(C-3')、81.9(C-4'')、75.9(C-2')、75.3(C-5')、74.1(C-4''')、73.5(C-2''')、73.1(C-3'')、72.9(C-8)、72.6(C-2'')、72.3(C-3''')、71.1(C-4')、70.2(C-5''')、68.5(C-5'')、65.1(C-6')、37.2(C-7)、19.3(C-6'')、17.5(C-6''')。分析结果可知该物质分子式为C35H46O19,参考文献[13]可知,该物质为紫茎女贞苷J(4.69 mg/g)。
结果表明,LRE中最主要的3 种物质分别为粗壮女贞苷B、粗壮女贞苷N和紫茎女贞苷J。
2.2 LRE的体外抗氧化活性
2.2.1 DPPH自由基清除能力
DPPH自由基清除实验已成为评价天然产物抗氧化活性的一种常用方法[17-18]。LRE的DPPH自由基清除能力如图2所示。
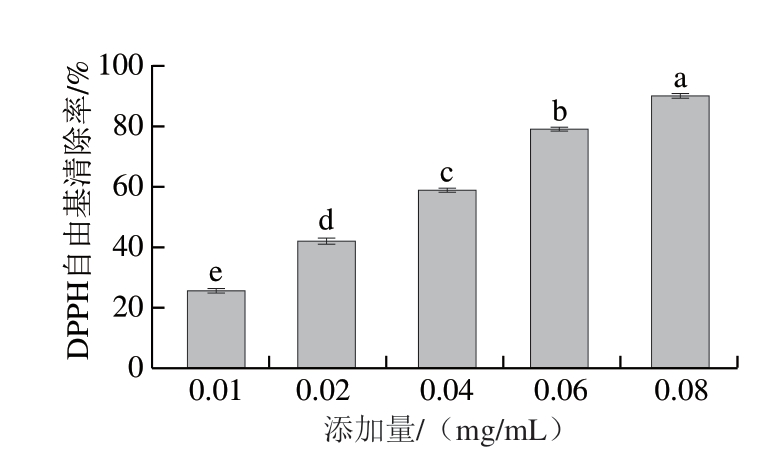
图2 LRE对DPPH自由基的清除能力
Fig.2 DPPH radical scavenging capacity of LRE
不同字母表示差异显著(P<0.05)。下同。
由图2可知,LRE能够有效清除体系的DPPH自由基,不同添加量的LRE对DPPH自由基具有不同清除效果。当LRE添加量由0.01 mg/mL提高至0.08 mg/mL时,LRE对DPPH自由基清除率由25.52%增加至90.15%,表现出明显的剂量效应关系。此外,其EC50值为0.03 mg/mL。LRE有较高的总酚含量,且主要含有粗壮女贞苷B、粗壮女贞苷N和紫茎女贞苷J 3 种酚类成分,其结构中含有大量的活性酚羟基,在反应体系中可以通过电子转移反应淬灭体系中的自由基,发挥良好的抗氧化能力。
2.2.2 还原能力
还原能力是物质抗氧化活性的重要表现,又能对其清除自由基等抗氧化能力作出合理解释[19]。LRE的还原能力如图3所示。
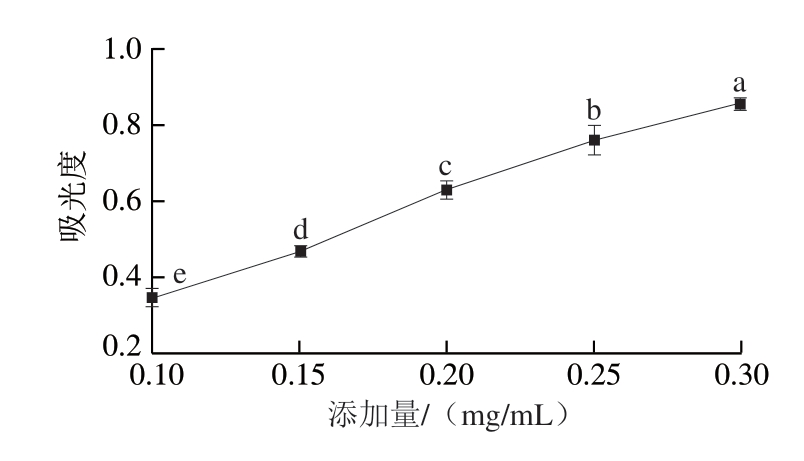
图3 LRE的还原能力
Fig.3 Reducing power of LRE
由图3可知,随着LRE添加质量浓度的增大,其吸光度逐渐增大,表明实验体系所产生的显色物质普鲁士蓝逐渐增多[20],LRE展现出较强的还原能力。结合前述实验结果分析可知,LRE中含有大量的酚类化合物,其结构中具有以酚羟基为代表的多种活性基团,可在氧化还原反应中给出电子,表现出良好的还原能力,从而清除体系中的自由基,降低体系的氧化态势,发挥优良的抗氧化作用。
2.3 小麦淀粉负载LRE的能力及稳定性分析
淀粉的糖羟基能够结合酚类物质,而随着淀粉使用量的增大,淀粉立体网状凝胶结构逐渐形成,使其表现出包埋和负载物质的能力[21]。小麦淀粉对LRE的负载能力及负载稳定性如图4所示。
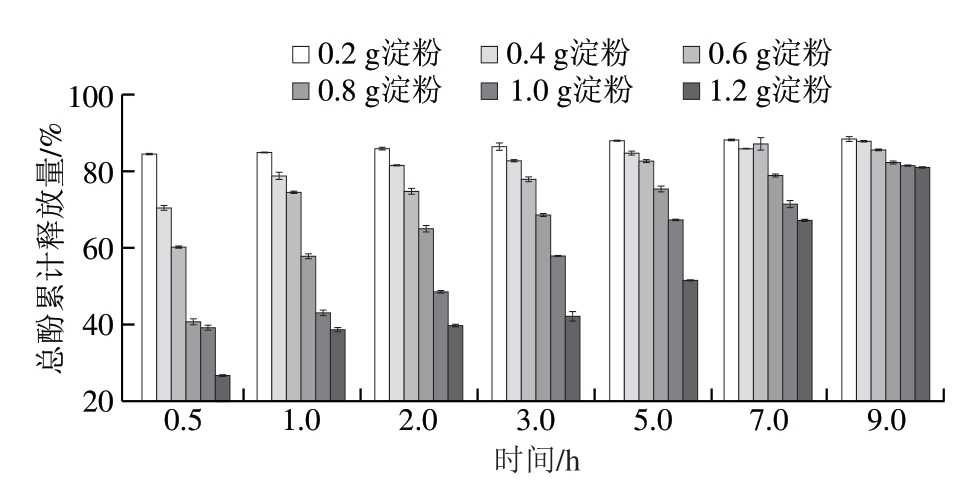
图4 小麦淀粉对LRE的负载能力及负载稳定性
Fig.4 Loading capacity and stability of wheat starch for LRE
由图4可见,淀粉的添加降低了LRE中总酚累计释放量,且与淀粉的添加量呈现剂量效应关系。小麦淀粉添加量越高,其对LRE的负载能力越强,水溶液中释放出的酚类物质越少。此外,随着采样时间的延长,所有样品中总酚累计释放量均增大,然而在最高淀粉添加量(1.2 g)的样品中,其总酚的累计释放量在任一采样时间处均低于其他组,表明在测试添加量梯度范围内(0.2~1.2 g),淀粉添加量越高,其对LRE的负载能力越稳定。有研究表明,在糊化过程中,淀粉颗粒的半结晶结构逐渐被破坏,颗粒内淀粉分子分散在水溶液中,当温度降低时,淀粉分子相互缠绕发生重结晶现象,而淀粉添加量增大会增加淀粉分子的碰撞机会和交联程度,导致淀粉凝胶的形成[21]。此外,有研究表明,淀粉分子可以通过氢键及疏水相互作用与多酚物质发生相互作用并结合[21],故随着淀粉添加量的增加及糖羟基的增多,淀粉与酚类物质之间形成更连续的氢键网络结构,更多的淀粉链可用于缠绕、结合及包埋多酚类物质。结果表明,一定浓度的淀粉可以通过物理包裹及氢键结合等方式负载LRE,从而达到在环境中缓慢释放LRE的效果。同时,淀粉对LRE的负载及包埋或许可以起到物理屏障一样的保护作用,避免pH值敏感、热敏感及光敏感活性物受到不良环境的影响。
2.4 小麦淀粉对LRE抗氧化活性的保护作用
基于小麦淀粉对LRE的负载作用,在60 ℃通风环境下,加速LRE的氧化,并以DPPH自由基清除能力及还原能力的衰减速率表征小麦淀粉对LRE抗氧化能力的影响。由图5可见,储存12 h后,LRE溶液的DPPH自由基清除能力下降至初始清除能力的93.73%,即储存12 h后LRE溶液的DPPH自由基相对清除能力为93.73%,随着储存时间的延长,LRE溶液的DPPH自由基清除能力逐渐下降。当储存60 h后,LRE溶液的DPPH自由基相对清除能力下降至4.53%,而小麦淀粉的存在减缓了LRE溶液的DPPH自由基相对清除能力的衰减,并且在任一储存周期内,添加淀粉样品的DPPH自由基相对清除能力均强于未添加淀粉的样品。同时,由图6可知,设定储存周期内,添加淀粉的LRE溶液的相对还原能力均高于未添加淀粉的LRE溶液,可见淀粉的存在显著抑制了样品还原能力的下降。有研究表明,茶叶中的酚类物质在高温环境下特别是存在水溶液中时较易被空气氧化[22-23]。此外,茶叶中酚类物质的氧化过程中,其酚羟基会解离脱氢形成醌类物质,而茶叶多酚的氧化和醌类物质的形成均会降低其抗氧化能力[22-24]。然而,糊化后淀粉分子间交联所产生的物理空隙以及淀粉分子通过分子间作用力与酚类的结合,在一定程度上保护了酚类化合物免受氧化聚合反应的影响,从而延缓其抗氧化能力的下降[25]。结果表明,小麦淀粉可抑制LRE的自由基清除作用和还原能力的降低,维持LRE的抗氧化活性。
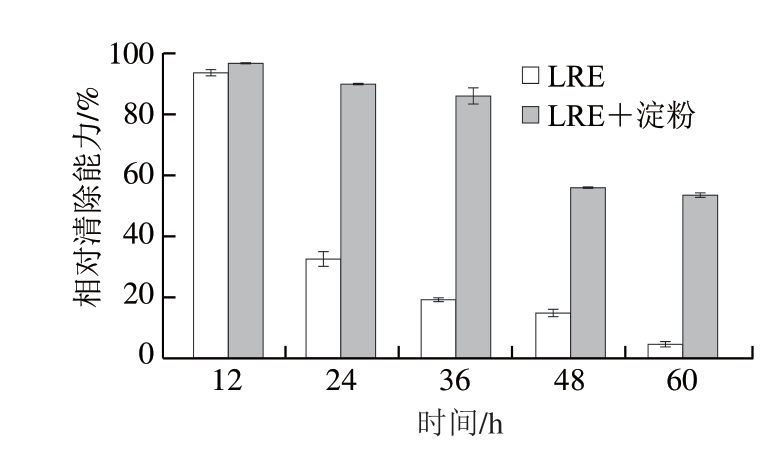
图5 小麦淀粉对LRE的DPPH自由基清除能力的影响
Fig.5 Effect of wheat starch on the DPPH radical scavenging capacity of LRE
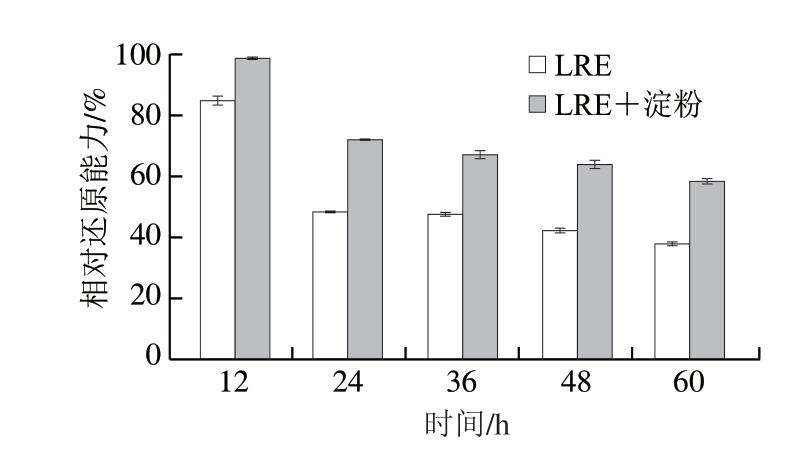
图6 小麦淀粉对LRE还原能力的影响
Fig.6 Effect of wheat starch on the reducing power of LRE
2.5 小麦淀粉对LRE在体外消化系统中的缓释作用
基于小麦淀粉对LRE的负载和保护作用,进一步探究了小麦淀粉对LRE在体外消化系统中的缓释作用。由图7可知,与添加0.2 g淀粉的样品组相比,较高量淀粉的添加显著降低了LRE累计释放量。添加1.2 g淀粉的样品组中,LRE在模拟口腔消化中(10 min处)的累计释放量降低至15.12%。此外,较高量淀粉的添加显著降低了LRE在模拟胃部消化中的累计释放量,减缓了LRE在模拟胃部消化滞留阶段的释放速率。结合相关文献可知[26],淀粉分子形成的三维网状结构可以包裹和负载酚类化合物。同时,淀粉分子还能通过氢键及疏水相互作用等方式与酚类物质结合形成复合物,从而延缓酚类物质的释放率和释放速率。此外,由淀粉分子形成的“屏障”将优先被消化液和消化酶分解,从而一定程度上保护LRE免受胃酸及酶的侵害。同时,由于淀粉彻底消化的发生场所在人体小肠内,故淀粉具有护送LRE进入小肠的能力[27-29]。结果表明,小麦淀粉能够延缓LRE在人体口腔和胃部消化系统中的释放量及释放速率,有益于其在人体内生物利用度的提高和生物活性的发挥。
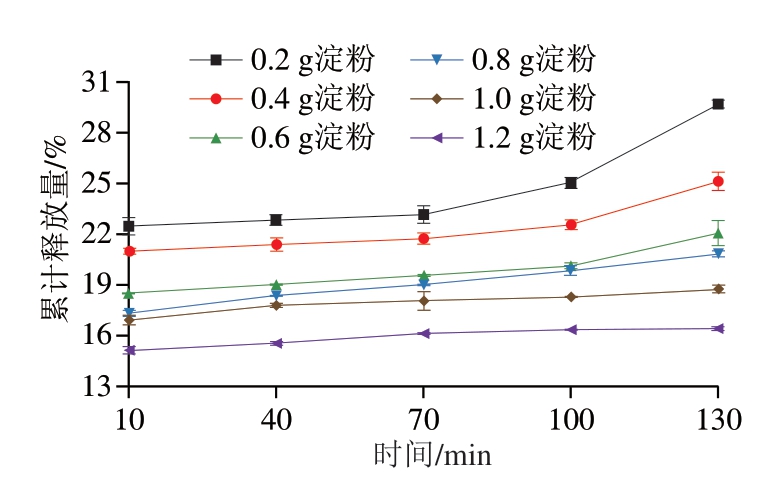
图7 小麦淀粉对LRE在体外消化系统中释放速度的影响
Fig.7 Effect of wheat starch on the release rate of LRE in in vitro digestive system
3 结论
LRE中的3 种主要成分分别为粗壮女贞苷B、粗壮女贞苷N和紫茎女贞苷J。LRE具有良好的DPPH自由基清除能力和还原能力,表现出良好的抗氧化活性,而小麦淀粉的添加能够负载和包埋LRE,保护LRE的抗氧化功效,并降低LRE在模拟口腔及模拟胃部的释放速率及释放量。本研究为苦丁茶资源及淀粉基负载材料在食品、生物医药领域的高效利用及相关产品的创新研发提供了实验基础。
[1]王世清,郑亚玉.贵州苦丁茶品种考证及资源调查: 一[J].中国民族民间医药杂志,2002,55(2): 107-108.DOI:10.3969/j.issn.1007-8517.2002.02.034.
[2]张敬杰,潘炉台,杨立勇,等.粗壮女贞药理作用初探[J].中国民族民间医药杂志,2004,69(4): 241-243.DOI:10.3969/j.issn.1007-8517.2004.04.033.
[3]LAU K M,HE Z D,DONG H,et al.Anti-oxidative,anti-inflammatory and hepato-protective effects of Ligustrum robustum[J].Journal of Ethnopharmacology,2002,83(1): 63-71.DOI:10.1016/s0378-8741(02)00192-7.
[4]于志龙,张曾,祝瑞雪,等.粗壮女贞苦丁茶提取物的抗氧化活性研究[J].中国食品学报,2017,17(10): 234-240.DOI:10.16429/j.1009-7848.2017.10.031.
[5]HERAS R M L,PINAZO A,HEREDIA A,et al.Evaluation studies of persimmon plant (Diospyros kaki) for physiological benefits and bioaccessibility of antioxidants by in vitro simulated gastrointestinal digestion[J].Food Chemistry,2017,214: 478-485.DOI:10.1016/j.foodchem.2016.07.104.
[6]WU Q,ZHOU J.The application of polyphenols in food preservation[J].Advances in Food and Nutrition Research,2021,98:35-99.DOI:10.1016/bs.afnr.2021.02.005.
[7]CATALINA C,ALEKNDRA N,NESTOR U,et al.Influence of thermoplasticized starch on physical-chemical properties of new biodegradable carriers intended for forest industry[J].International Journal of Biological Macromolecules,2018,122: 924-929.DOI:10.1016/j.ijbiomac.2018.11.026.
[8]YUE H,QIU B,JIA M,et al.Development and optimization of spray-dried functional oil microcapsules: oxidation stability and release kinetics[J].Food Science &Nutrition,2020,8(9): 4730-4738.DOI:10.1002/fsn3.1684.
[9]ARSHAD,H,ALI T M,HASNAIN A.Physical and functional properties of fried donuts incorporated with nutmeg microcapsules composed of gum-arabic and sorghum starch as wall materials[J].Journal of Food Measurement and Characterization,2019,13(4):3060-3068.DOI:10.1007/s11694-019-00228-y.
[10]曾铭,李蟠莹,胡鹏,等.多酚对淀粉理化性质影响的研究进展[J].食品工业科技,2018,39(22): 334-340.DOI:10.13386/j.issn1002-0306.2018.22.058.
[11]TIAN J,ZHANG H J,SUN H D,et al.Monoterpenoid glycosides from Ligustrum robustum[J].Phytochemistry,1998,48(6): 1013-1018.DOI:10.1016/S0031-9422(97)00472-X.
[12]HE Z D,LAU K M,BUT P P H,et al.Antioxidative glycosides from the leaves of Ligustrum robustum[J].Journal of Natural Products,2003,66(6): 851-854.DOI:10.1021/np020568g.
[13]FAN L,LIAO C H,LI S G,et al.Phenylethanoid and secoiridoid glycosides from the leaves of Ligustrum purpurascens[J].Phytochemistry Letters,2015,13: 177-181.DOI:10.1016/j.phytol.2015.06.011.
[14]高浩祥,薛凡,何强,等.鼠曲草提取物对食用油脂贮藏过程中氧化酸败的抑制及机理研究[J].食品工业科技,2017,38(4): 148-151.DOI:10.13386/j.issn1002-0306.2017.04.020.
[15]GAO H X,YU Z L,HE Q,et al.A potentially functional yogurt cofermentation with Gnaphalium affine[J].LWT-Food Science and Technology,2018,91: 423-430.DOI:10.1016/j.lwt.2018.01.085.
[16]TAI K D,RAPPOLT M,MAO L K,et al.Stability and release performance of curcumin-loaded liposomes with varying content of hydrogenated phospholipids[J].Food Chemistry,2020,326: 126973.DOI:10.1016/j.foodchem.2020.126973.
[17]HARMAN D.Aging: a theory based on free radical and radiation chemistry[J].Journals of Gerontology,1956,11(3): 298-300.DOI:10.1093/geronj/11.3.298.
[18] BRAND W W,CUVELIER M E,BERSET C.Use of a free radical method to evaluate antioxidant activity[J].Food Science and Technology-Lebensmittel-Wissenschaft and Technologie,1995,28(1):25-30.DOI:10.1016/S0023-6438(95)80008-5.
[19] LUCHSINGER W W,CORNESKY R A.Reducing power by the dinitrosalicylic acid method[J].Analytical Biochemistry,1962,4(4):346-347.DOI:10.1016/0003-2697(62)90098-2.
[20] BENZIE I F F,STRAIN J J.The ferric reducing ability of plasma (FRAP)as a measure of “antioxidant power”: the FRAP assay[J].Analytical Biochemistry,1996,239(1): 70-76.DOI:10.1006/abio.1996.0292.
[21]LIU X,CHAO C,YU J L,et al.Mechanistic studies of starch retrogradation and its effects on starch gel properties[J].Food Hydrocolloids,2021,120: 106914.DOI:10.1016/j.foodhyd.2021.106914.
[22] HARBOWY M E,BALENTINE D A.Tea chemistry[J].Critical Reviews in Plant Sciences,1997,16(5): 415-480.DOI:10.1080/713608154.
[23]LI Y,LV H,XUE C Y,et al.Plant polyphenols: potential antidotes for lead exposure[J].Biological Trace Element Research,2020,199(10):3960-3976.DOI:10.1007/s12011-020-02498-w.
[24]SANG S M,LAMBERT J D,HO C T,et al.The chemistry and biotransformation of tea constituents[J].Pharmacological Research,2011,64(2): 87-99.DOI:10.1016/j.phrs.2011.02.007.
[25] PANZELLA L.Natural phenolic compounds for health,food and cosmetic applications[J].Antioxidants,2020,9(5): 427.DOI:10.3390/antiox9050427.
[26]ZHU F.Interactions between starch and phenolic compound[J].Trends in Food Science and Technology,2015,43(2): 129-143.DOI:10.1016/j.tifs.2015.02.003.
[27]PEREZ M N,SAHA S,PHILO M,et al.Comparative bio-accessibility,bioavailability and bioequivalence of quercetin,apigenin,glucoraphanin and carotenoids from freeze-dried vegetables incorporated into a baked snack versus minimally processed vegetables: evidence from in vitro models and a human bioavailability study[J].Journal of Functional Foods,2018,48: 410-419.DOI:10.1016/j.jff.2018.07.035.
[28] VIUDA M M,LUCAS G R,BALLESTER C C,et al.Evaluation of protective effect of different dietary fibers on polyphenolic profile stability of maqui berry (Aristotelia chilensis (Molina) Stuntz) during in vitro gastrointestinal digestion[J].Food &Function,2018,9(1):573-584.DOI:10.1039/c7fo01671a.
[29]STROCCHI A,LEVITT M D.Measurement of starch absorption in humans[J].Canadian Journal of Physiology and Pharmacology,1991,69(1): 108-110.DOI:10.1139/y91-015.