杂豆是除大豆外各种小宗豆类的通称。我国杂豆品种繁多,主要有芸豆、鹰嘴豆、豌豆、黑豆、绿豆、蚕豆等。杂豆具有高碳水化合物(24%~68%,其中淀粉占40%~60%)、高蛋白(20%~50%)、低脂肪(<1%)、B族维生素和矿物质丰富等特点,是一种优质的食物来源[1]。此外,杂豆还具有降血脂[2]、抗肿瘤[3]等生理功能。
淀粉是杂豆的主要成分之一,例如豌豆中淀粉含量约为53%,扁豆中淀粉含量约为50%[4],鹰嘴豆中的淀粉含量为40%~80%[5]。杂豆淀粉具有直链淀粉含量高(40%)、凝胶特性较好、抗剪切能力强等特点,是食用淀粉和工业淀粉的潜在来源,但其具体的应用取决于淀粉来源及其特性。目前关于杂豆淀粉结构特征和理化性质如凝胶特性、糊化特性等方面的研究已有相关报道。例如,大多数杂豆淀粉为C-型晶体类型[6]。杨丹红等[7]发现豇豆淀粉、小扁豆淀粉、小黑芸豆淀粉颗粒多为卵圆形,少数呈圆形,具有热稳定性较好、抗剪切、易回生的特性。汪丽萍等[8]提取了绿豆淀粉、花芸豆淀粉、红小豆淀粉、豌豆淀粉、红芸豆淀粉、小扁豆淀粉,发现6 种杂豆淀粉具有相似的颗粒形貌,糊化特性差异显著。绿豆淀粉、蚕豆淀粉、鹰嘴豆淀粉等在工业上也有较为广泛的应用[9]。
不同杂豆淀粉间的结构特征存在差异,使其具有不同的理化特性,影响淀粉在食品加工工业中的应用。然而杂豆种类繁多,对不同杂豆淀粉之间结构特征与其理化特性之间的关系的研究报道较少或缺乏全面认识。因此本研究选取豇豆、扁豆、豌豆、红芸豆4 种杂豆为原料,采用湿磨法制备淀粉,对杂豆淀粉的特性开展系统研究,明晰不同杂豆淀粉的基本结构特征和理化特性,为杂豆淀粉的开发利用提供理论依据。
1 材料与方法
1.1 材料与试剂
豇豆、扁豆购、豌豆、红芸豆分别购于陕西榆林、江西南昌、重庆、山西朔州。
总淀粉试剂盒、直支链淀粉试剂盒 爱尔兰Megazyme公司;冰醋酸、无水乙酸钠、氯化钠、二水合氯化钙、六水合氯化镁、四水合氯化锰、氢氧化钾、硫酸铜、硫酸钾、无水乙醇、浓盐酸、氢氧化钠(均为分析纯)西陇科学股份有限公司;溴化锂、二甲基亚砜(均为色谱级)德国Merck公司;GPC/SEC混合柱(使用分子质量342~2.35×106 Da的普鲁兰标准品校准SEC)德国PSS公司。
1.2 仪器与设备
1100超高效液相色谱 安捷伦科技有限公司;RID-10A折射率检测器 日本京都岛津公司;D8 Advance X-射线衍射仪 德国Bruker公司;Nicolet 5700傅里叶红外光谱仪、Varioskan Flash全波长多功能酶标仪 美国Thermo公司;B-383POL偏光显微镜 意大利Optika公司;JSM6701F场发射扫描电镜带能谱仪 日本电子株式会社;RVA-Tec Maste快速黏度分析仪 瑞典Perten公司;TGA4000热重分析仪 美国PerkinElmer公司;DL-5V台式离心机 上海安亭科学仪器厂;GZX-9420 MBE电热恒温鼓风干燥箱 上海博讯实业有限公司医疗设备厂;T-9双光束紫外-可见分光光度计 北京普析通用仪器公司;VOSHIN-COS-100B数显恒温摇床 无锡沃信仪器有限公司;FE-28精密pH计、XS205电子分析天平 梅特勒-托利多仪器公司;JYL-C020E家用多功能榨汁机 中国九阳股份有限公司。
1.3 方法
1.3.1 淀粉提取
参考Malumba等[10]的方法,采用的湿磨法并进行修改提取淀粉。称取200 g豆粒,用1000 mL蒸馏水在室温下浸泡后去除种皮和胚芽,再加入1000 mL蒸馏水后使用打浆机磨碎打浆,过滤打浆后的混合物,此步骤重复3~4 次,弃去滤渣。将滤液在4 ℃静置8~10 h,弃去上清液,将沉淀按料液比1∶5与0.2%氢氧化钠溶液混合均匀,过夜静置,分层后的上清液倒出,沉淀中加入蒸馏水并搅拌均匀,静置后弃去上清液,重复上述加水搅拌、静置等步骤3~4 次,直至淀粉沉淀颜色洁白无杂质为止。将淀粉置于50 ℃鼓风干燥箱中,干燥后即得淀粉成品。
所得豇豆淀粉、扁豆淀粉、豌豆淀粉、红芸豆淀粉分别命名为CS、LS、PS、RKBS。
1.3.2 基本组成
总淀粉含量、直链淀粉含量分别使用总淀粉试剂盒和直链淀粉试剂盒测定,利用二者差值得到支链淀粉含量。
1.3.3 分子尺寸分布
使用RID-10A折射率检测器的LC-20AD Shimadzu体积排阻色谱系统对淀粉进行分子尺寸测定,具体步骤如下:准确称取5 mg淀粉,溶于5 mL二甲基亚砜溶液(0.5% LiBr),80 ℃水浴12 h后进样。
测试条件:流动相为二甲基亚砜溶液(0.5%LiBr),进样质量浓度为1 mg/mL,凝胶色谱柱:GRAM预制柱,GRAM 30和GRAM 3000分析柱,分离范围分别为100~3×104 Da和103~1.6×106 Da;柱温80 ℃,流速0.3 mL/min,dn/dc值为0.0717 mL/g[11]。
1.3.4 结晶特性
杂豆淀粉过100 目筛后采用X射线衍射仪进行测定,参数设定为管压40 kV,电流100 mA,在2θ为4°~40°范围内进行连续扫描,数据采集步宽0.02°。使用MDI Jade 6.0计算相对结晶度,即衍射曲线下的峰面积与总衍射图面积之比[12]。
1.3.5 红外光谱
称取约2 mg的样品,与干燥的溴化钾粉末混合,置于玛瑙研钵中研磨。采用压片法置于红外光谱仪上扫描,扫描范围为4000~500 cm-1,绘制红外光谱图。用Omnic软件对1200~800 cm-1进行傅里叶自去卷积处理,设置半峰宽和增强因子分别为40 cm-1和2.4,计算1045 cm-1/1022 cm-1的峰强度比值。
1.3.6 偏光十字显微镜观察
取少量淀粉样品均匀涂于载玻片上,滴1~2 滴蒸馏水使之均匀分散,盖上盖玻片后,置于带有偏光片的光学显微镜下进行观察。
1.3.7 颗粒形貌
取少量干燥后的淀粉样品在导电双面胶上涂抹均匀,喷金处理后将载物台放入扫描电子显微镜中观察,电子枪加速电压为3 kV,500 倍放大倍数下观察淀粉的颗粒形态。
1.3.8 糊化特性
称取3.0 g杂豆淀粉样品,加入25 mL蒸馏水,配制成8%的淀粉乳,混合于快速黏度计专用铝盒内。具体测定条件:50 ℃保持1 min;以5 ℃/min上升到95 ℃(9 min);95 ℃保持7 min;以6 ℃/min下降到50 ℃(7.5 min);50 ℃保持4.5 min;搅拌器在起始10 s内转动速率为960 r/min,之后保持在160 r/min。测得淀粉糊黏度曲线,并通过快速黏度分析仪专用测试软件TCW分析获得杂豆淀粉的糊化黏度特征参数。
1.3.9 热稳定性分析
采用热重分析法测定淀粉的热稳定性。称取淀粉量约10 mg,反应气氛为高纯氮气,流量为20 mL/min,以10 ℃/min速率从30 ℃匀速升温至600 ℃。
1.3.10 凝沉特性和沉降积
配制质量分数为1%的淀粉乳,于沸水中搅拌20 min[13],冷却至25 ℃。用量筒取100 mL后在室温下静置,记录0、2、4、6、8、10 h时淀粉糊中上清液的体积,绘制淀粉糊的凝沉曲线。24 h后淀粉糊所占体积为沉降积。
1.4 数据处理
采用IBM SPSS 24.0软件进行单因素方差和Duncan检验,P<0.05认为样品间差异具有统计学意义。
2 结果与分析
2.1 基本组成
采用湿磨法提取CS、LS、PS、RKBS,得率分别为18.8%、28.8%、12.8%、15.5%。Hoover等[14]报道大多数杂豆淀粉的提取率为18%~54%,本实验淀粉得率在此范围内,但与部分文献报道不同的原因可能与品种、脱壳方法、种皮硬度、浸泡方法等有关[15]。对所提取的淀粉基本组成进行分析(表1),4 种杂豆淀粉中的总淀粉质量分数为77.9%~88.7%。CS的直链淀粉质量分数为26.3%,显著低于其他样品(P<0.05),而RKBS的支链淀粉质量分数最高(57.2%)。
表1 不同来源杂豆淀粉样品基本组成(n=3)
Table 1 Basic composition of legume starch from different sources (n=3)
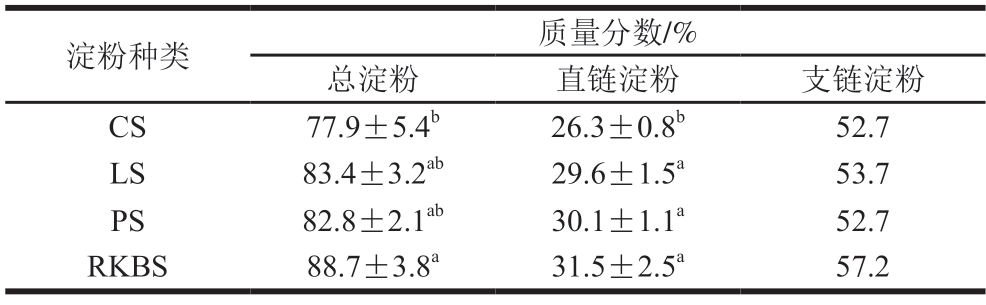
注:数据以![]() 表示;同列不同字母表示差异显著(P<0.05);表4同。
表示;同列不同字母表示差异显著(P<0.05);表4同。
2.2 分子尺寸分布
如图1所示,样品的峰形较为相似,从左到右出现2 个峰,分别归属为直链淀粉(AM)分子和支链淀粉(AP)分子。使用凝胶渗透色谱法测定其平均流体力学半径(即![]() ),结果见表2,CS、LS、PS、RKBS的
),结果见表2,CS、LS、PS、RKBS的![]() 分别为116.5、113.6、115.7、99.4 nm,RKBS的平均分子半径最小。样品中支链淀粉分子的平均半径(
分别为116.5、113.6、115.7、99.4 nm,RKBS的平均分子半径最小。样品中支链淀粉分子的平均半径(![]() >29)分布范围为138.6~159.4 nm。由表1可知,不同样品间的直链淀粉含量呈现显著性差异(P<0.05),但4 种杂豆淀粉中的直链淀粉平均分子半径大小相近,均为17.9~20.8 nm。
>29)分布范围为138.6~159.4 nm。由表1可知,不同样品间的直链淀粉含量呈现显著性差异(P<0.05),但4 种杂豆淀粉中的直链淀粉平均分子半径大小相近,均为17.9~20.8 nm。
表2 不同来源杂豆淀粉的分子尺寸比较
Table 2 Comparison of molecular size of legume starch from different sources
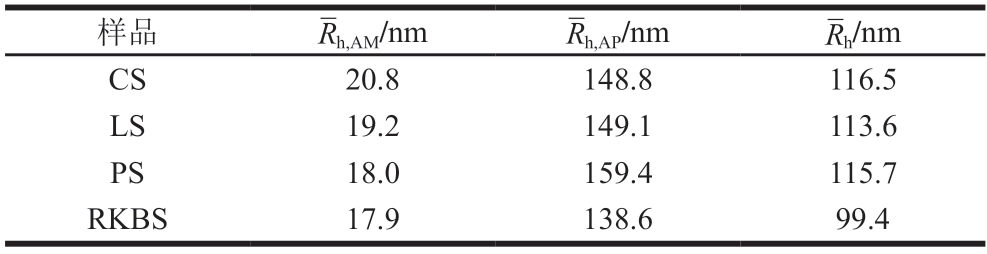
注: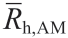 为直链淀粉分子的平均流体力学半径;
为直链淀粉分子的平均流体力学半径;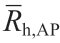 为支链淀粉分子的平均流体力学半径。
为支链淀粉分子的平均流体力学半径。
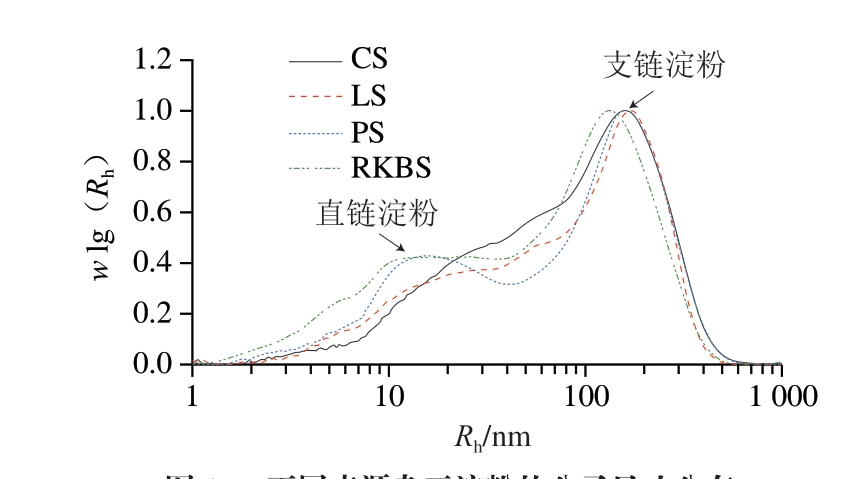
图1 不同来源杂豆淀粉的分子尺寸分布
Fig.1 Molecular size distribution of legume starch from different sources
2.3 结晶特性
淀粉颗粒具有独特的半结晶体系,它是由结晶区和无定形区交替组成,两者之间并没有明确的界线[16]。结晶区主要由支链淀粉侧链形成的双螺旋结构有序排列构成,还包含少量的直链淀粉-脂质单螺旋有序结构,在X射线衍射图谱上表现为尖锐衍射峰。无定形区则是由分子链无序排列构成,其X射线衍射图谱上表现为弥散峰[17]。
由图2可以看出,PS在15°、17°、23°(2θ)处出现了强衍射峰,呈现典型的CC-型淀粉结晶特征。CS、LS、RKBS均在18°出现较弱衍射峰,为CA-型晶体。4 种杂豆淀粉的相对结晶度如表3所示,顺序为PS>CS>LS>RKBS。结晶度越高表明淀粉结构的稳定性越好,可能是由于双螺旋间的相互作用程度较强、晶粒取向较好以及“束簇”状(聚合度为45~63)的支链淀粉含量高[18]。RKBS的相对结晶度(27.6%)最低,可能与其较高的直链淀粉含量(31.5%)有关[19]。
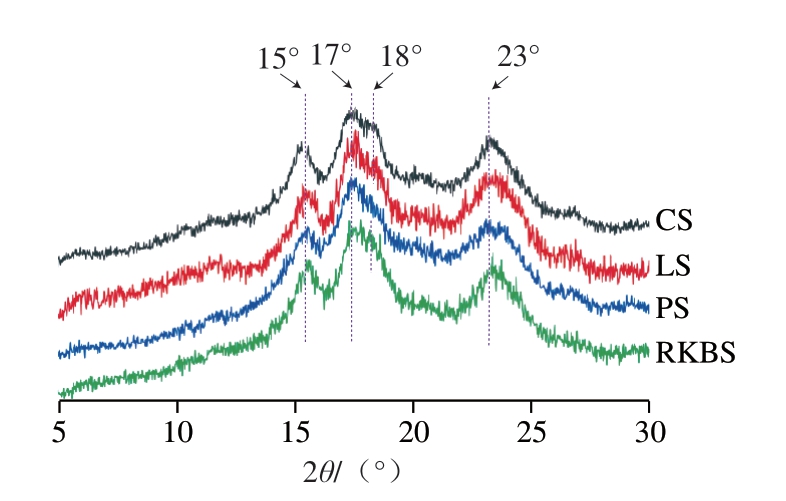
图2 不同来源杂豆淀粉的X射线衍射
Fig.2 X-ray diffractogram of legume starch from different sources
表3 不同来源杂豆淀粉相对结晶度与短程有序程度
Table 3 Relative crystallinity and short-range order degree of legume starch from different sources
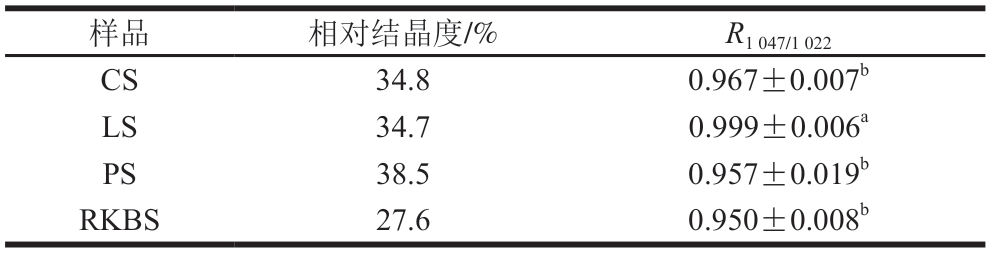
注:R1047/1022表示红外光谱中1047 cm-1与1022 cm-1峰强度比值。
2.4 短程有序性分析
淀粉特征条带主要分为3 个区域:O—H 拉伸区域(3000~3600 c m-1)、C—H 拉伸区域(2800~3000 cm-1)和指纹区域(800 cm-1以下,800~1500 cm-1)[4]。如图3所示,样品均在3411、2928、1463、1163、1086、986、928、763 cm-1处出现吸收峰,呈现典型的淀粉类多糖特征。其中,3411 cm-1处的宽峰对应O—H的伸缩振动;2928 cm-1处对应C—H拉伸区域;1463 cm-1处归属为C—H的弯曲振动;1163、1086、986 cm-1处归属为葡萄糖C—O—C键的伸缩振动[20];928 cm-1处被认为是α-1,4糖苷键的特征峰;763 cm-1附近吸收峰为C—C键的伸缩振动。淀粉中的短程有序性结构是指双螺旋间短距离内有序堆积形成的结构,通常使用红外光谱中1047 cm-1/1022 cm-1处的吸光度比值表征(R1047/1022),1047 cm-1处对应淀粉分子中的有序结构,1022 cm-1处对应无规则线团结构[21],结果如表3所示。LS的R1047/1022显著高于CS、PS、RKBS(P<0.05),有序化程度最高。CS、PS、RKBS的R1047/1022无显著性差异,表明三者的短程分子有序性相似。
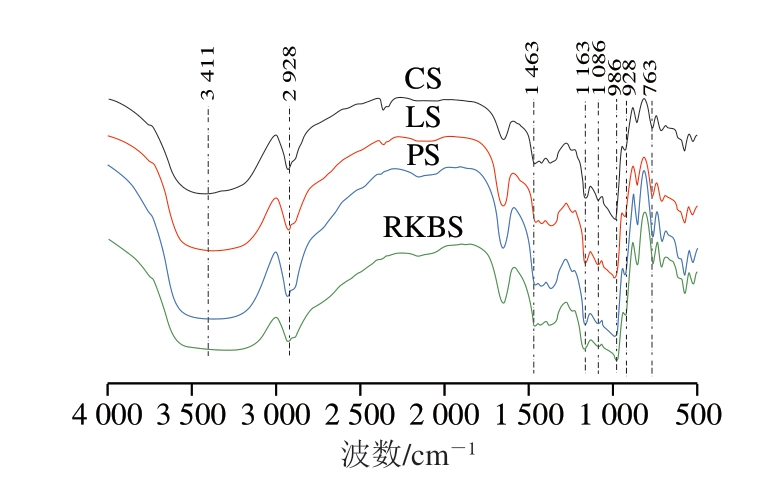
图3 不同来源杂豆淀粉的红外光谱扫描
Fig.3 Infrared spectra of legume starch from different sources
2.5 偏光十字
淀粉颗粒存在结晶区和非结晶区,由于这2 个区域中淀粉分子的排列有序程度存在差异,导致折射率不同而产生各向异性,所以淀粉颗粒可形成偏光十字[22]。淀粉颗粒偏光十字的变化可反映其结晶结构变化,若颗粒内部分子链径向有序排列的结晶结构受到破坏,则偏光十字现象消失[23]。由图4可以看出,4 种杂豆淀粉的偏光十字均比较明显,交叉点都接近于颗粒中心位置,LS、PS、RKBS中存在“X”形和斜十字形两种,CS主要呈现“X”形。
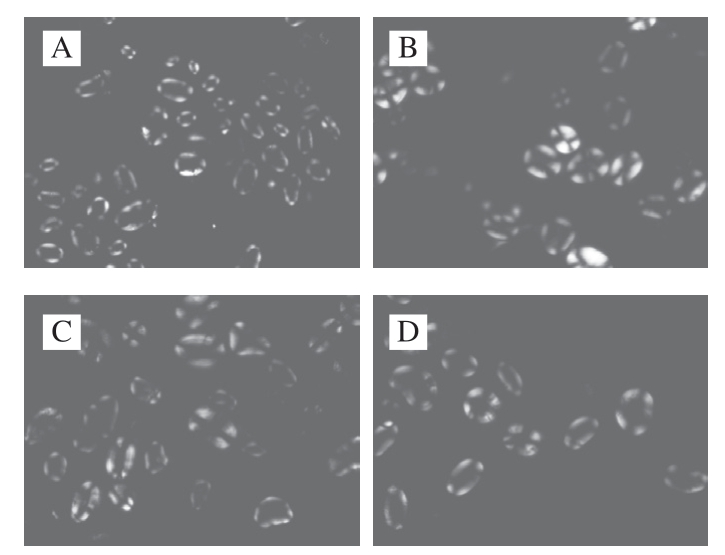
图4 不同来源杂豆淀粉的偏光十字图谱
Fig.4 Polarized cross spectra of legume starch from different sources
A.CS;B.LS;C.PS;D.RKBS。图5同。
2.6 颗粒形貌
如图5所示,4 种杂豆淀粉颗粒形貌相似,大部分颗粒呈肾型、椭圆形,少数呈球形和不规则形态。多数颗粒表面光滑,表明湿磨法提取基本保留了淀粉颗粒的完整结构[24]。

图5 不同来源杂豆淀粉的扫描电镜图(×500)
Fig.5 SEM images of legume starch from different sources (× 500)
2.7 糊化特性
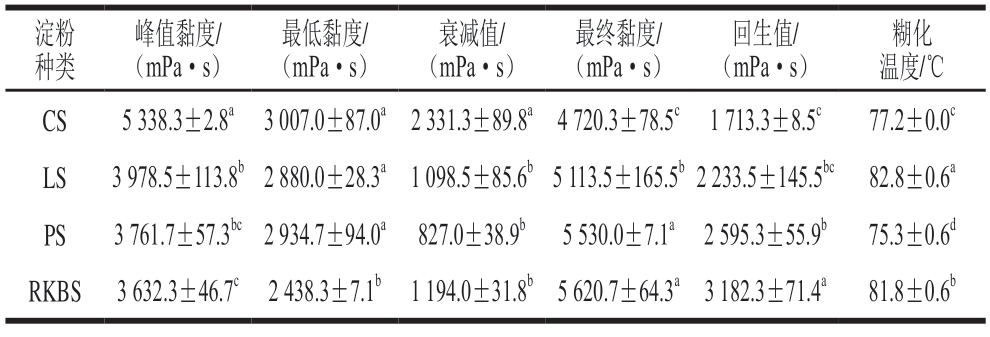
如表4 所示,4 种杂豆淀粉中,C S 的峰值黏度(5338.3 mPa·s)显著高于LS、PS、RKBS(P<0.05),表明其与水结合能力更强,吸水膨胀后淀粉糊更黏稠,具有作为食品增稠剂的潜力[8]。回生值反映淀粉的冷糊稳定性,回生值越小则淀粉的冷糊稳定性越佳,越不易老化。样品的回生值大小为RKBS>PS>LS>CS,与直链淀粉含量高低顺序一致,推测样品的易老化程度主要是受到直链淀粉含量的影响。衰减值反映了淀粉的热糊稳定性,衰减值越大则热糊稳定性越差。CS的衰减值最高,表明其热糊稳定性最差,溶胀后的淀粉颗粒易破裂,PS的衰减值低于CS、LS、RKBS,表明溶胀后的PS颗粒强度较大,不易破裂。高温环境下有更强的耐热性和抗剪切性,这可能是由于其结晶度(38.5%)较高。样品的糊化温度均较高(75.3~82.8 ℃),均不易糊化,其中LS的糊化温度显著高于其他样品,表明LS中的淀粉颗粒结构更加紧密,具有较强的抵抗溶胀和破裂的能力,最不易糊化。
表4 不同来源杂豆淀粉的糊化特性参数(n=3)
Table 4 Gelatinization parameters of legume starch from different sources (n=3)
2.8 热稳定性分析
如图6所示,根据热重曲线可看出,4 种杂豆淀粉的降解主要有2 个过程,第1阶段质量损失发生在30~130 ℃之间,样品的质量损失了10%左右,这一阶段主要与水分的蒸发有关[25]。第1阶段脱水过程结束后,杂豆淀粉在250 ℃以下处于稳定状态,超过250 ℃后,可以明显观察到样品在250~400 ℃之间发生降解,这一失重阶段主要由于淀粉在高温下发生分解,淀粉结构被破坏。导数热重曲线是由热重曲线一阶求导所得,其表示降解过程的质量损失速率。导数热重曲线分别在98~118 ℃和303~320 ℃出现2 个峰,分别与淀粉脱水和结构分解有关,这与热重曲线图相对应。303~320 ℃内,CS、LS、PS、RKBS的出峰温度分别为320、317、318、303 ℃,与部分玉米淀粉相比,杂豆淀粉均具有良好的热稳定性[26],顺序为CS>PS>LS>RKBS,这与样品的平均分子半径为CS>PS>LS>RKBS相对应,推测分解温度主要是受到分子尺寸的影响,分子尺寸越大则热稳定性越佳。Chen Pei等[27]研究发现酸解后淀粉第2阶段的热分解温度低于原淀粉,与显示酸解后分子质量降低的尺寸排阻色谱结果一致。
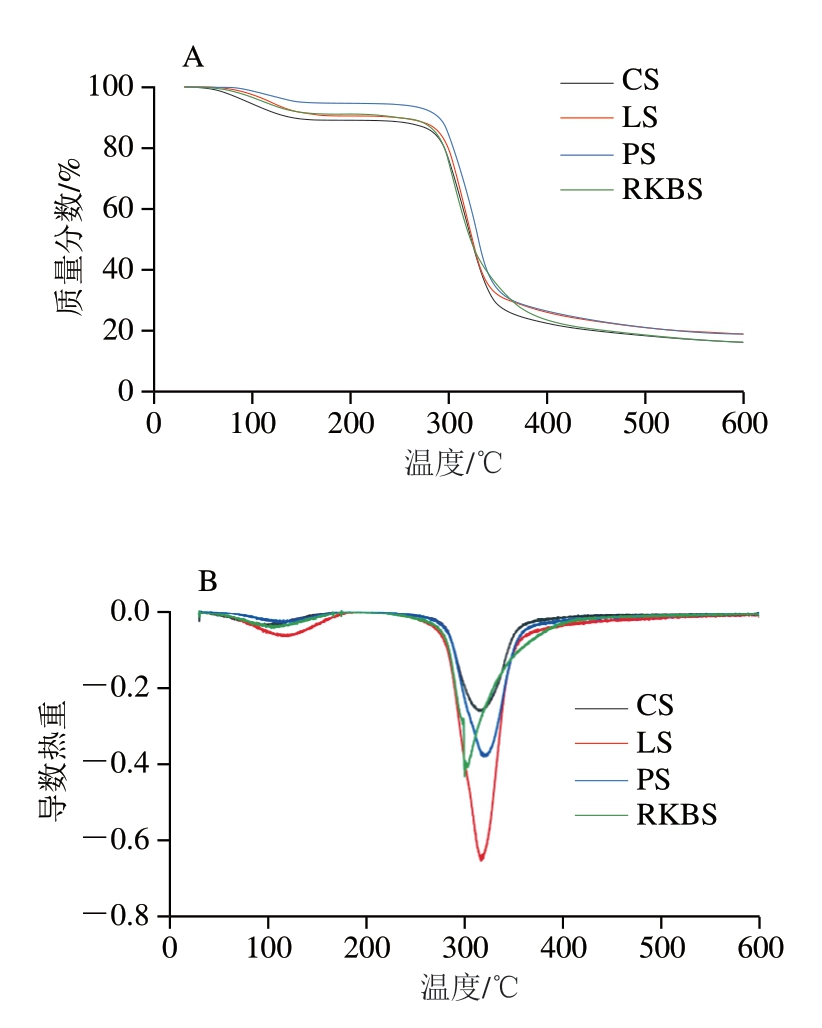
图6 不同来源杂豆淀粉的热重(A)和导数热重(B)曲线图
Fig.6 TGA (A) and DTG (B) curves of legume starch from different sources
2.9 凝沉特性
淀粉的凝沉特性主要与直链淀粉含量及其聚合度、分子尺寸、脂质含量等有关[28],是评价淀粉糊化特性的重要指标之一。如图7所示,随着放置时间的延长,4 种杂豆淀粉糊都产生了不同程度的凝沉。CS、LS、PS、RKBS在2 h内大幅度上升,2 h时,PS、RKBS的上清液体积分别达到82.7%、83.3%,随后趋于平缓,10 h后PS的上清液体积保持在82.7%,RKBS则缓慢增加至84.5%。LS和CS的上清液体积在4 h内大幅度上升,在4 h时分别上升至76.8%和40.0%,4 h后上升程度平缓,10 h时缓慢增加到80.3%和53.7%。放置时间为10 h时,这4 种杂豆淀粉的易老化趋势为RKBS>PS>LS>CS,与糊化特性结果一致。24 h时,CS、LS、PS、RKBS的沉降积分别为37.3、18.5、16.3 mL和14.8 mL,CS沉降积最大,最不易老化,可能是由于其直链淀粉含量最低(26.3%)。
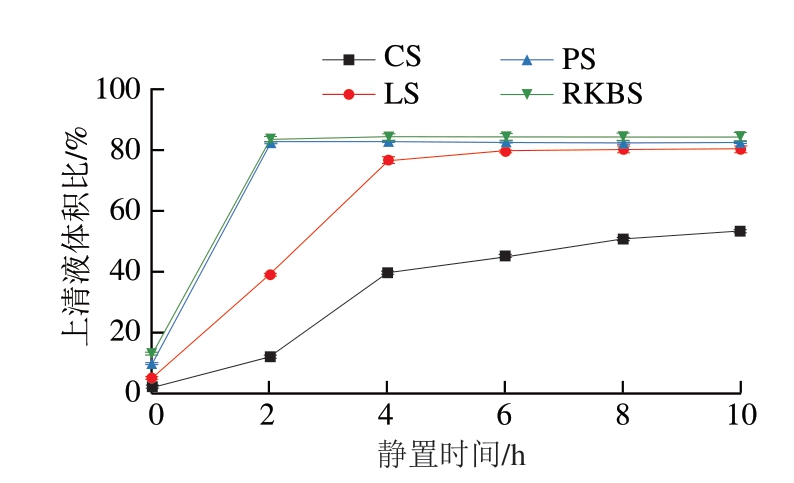
图7 不同来源杂豆淀粉的凝沉特性
Fig.7 Retrogradation characteristics of legume starch from different sources
3 结论
4 种杂豆淀粉的组成、分子结构以及晶型方面均存在一定差异。总淀粉含量、直链淀粉含量、支链淀粉含量范围分别为77.9%~88.7%、26.3%~31.5%、52.7%~57.2%。4 种杂豆淀粉颗粒完整,平均流体力学半径大小顺序为CS>PS>LS>RKBS;均具有典型的双折射现象,CS主要呈现“X”形,PS、LS、RKBS存在“X”形和斜十字形2 种;此外,4 种杂豆淀粉均为C-型淀粉,其中PS为CC-型晶体,其余为CA-型晶体。4 种杂豆淀粉因组成、结构不同,其理化特性存在较大差异:受高直链淀粉含量的影响,RKBS的回生值高、凝沉性差,最易发生老化行为。CS的直链淀粉含量最低,沉降积最大,最不易老化,并且因其平均分子半径较大而具有良好的热稳定性。糊化性质方面,样品中PS较易糊化,LS最不易糊化。
[1]JEONG D,HAN J A,LIU Q,et al.Effect of processing,storage,and modification on in vitro starch digestion characteristics of food legumes: a review[J].Food Hydrocolloids,2019,90: 367-376.DOI:10.1016/j.foodhyd.2018.12.039.
[2]JING C L,WEN Z,ZOU P,et al.Consumption of black legumes glycine soja and glycine max lowers serum lipids and alters the gut microbiome profile in mice fed a high-fat diet[J].Journal of Agricultural and Food Chemistry,2018,66(28): 7367-7375.DOI:10.1021/acs.jafc.8b02016.
[3]LACERDA R R E,NASCIMENTO E S D,LACERDA JT JG D,et al.Lectin from seeds of a Brazilian lima bean variety (Phaseolus lunatus L.var.cascavel) presents antioxidant,antitumour and gastroprotective activities[J].International Journal of Biological Macromolecules,2017,95: 1072-1081.DOI:10.1016/j.ijbiomac.2016.10.097.
[4]PRAZERES KGMD,ANDRADE I H P,CAMILLOTO G P,et al.Physicochemical and functional properties of mangalô bean (Lablab purpureus L.) starch[J].Colloids and Surfaces A: Physicochemical and Engineering Aspects,2021,610: 125706.DOI:10.1016/j.colsurfa.2020.125706.
[5]缪铭,江波,张涛,等.不同品种鹰嘴豆淀粉的理化性质研究[J].食品科学,2008,29(6): 79-82.DOI:10.3321/j.issn:1002-6630.2008.06.011.
[6]NWOKOCHA L M,SOETAN K O,WILLIAMS P A.A study of the properties of starch isolated from three varieties of Lablab purpureus seeds[J].Carbohydrate Polymers,2010,79(3): 685-693.DOI:10.1016/j.carbpol.2009.09.024.
[7]杨红丹,杜双奎,周丽卿,等.3 种杂豆淀粉理化特性的比较[J].食品科学,2010,31(21): 186-190.DOI:CNKI:SUN:SPKX.0.2010-21-043.
[8]汪丽萍,刘艳香,田晓红.六种杂豆淀粉的理化性质研究[J].粮油食品科技,2014,22(4): 1-5.DOI:10.3969/j.issn.1007-7561.2014.04.001.
[9]REN Y,YUAN T Z,CHIGWEDERE C M,et al.A current review of structure,functional properties,and industrial applications of pulse starches for value-added utilization[J].Comprehensive Reviews in Food Science and Food Safety,2021,20(3): 3061-3092.DOI:10.1111/1541-4337.12735.
[10] MALUMBA P,BUNGU M D,KATANGA K J,et al.Structural and physicochemical characterization of Sphenostylis stenocarpa (Hochst.ex A.Rich.) Harms tuber starch[J].Food Chemistry,2016,212: 305-312.DOI:10.1016/j.foodchem.2016.05.181.
[11]LI E,YANG C,WANG J,et al.Leached starch content and molecular size during sorghum steaming for baijiu production is not determined by starch fine molecular structures[J].International Journal of Biological Macromolecules,2021,184: 50-56.DOI:10.1016/j.ijbiomac.2021.06.031.
[12] KOMIYA T,NARA S.Changes in crystallinity and gelatinization phenomena of potato starch by acid treatment[J].Starch-Starke,1986,38(1): 9-13.DOI:10.1002/star.19860380104.
[13]许鑫.杂豆类淀粉提取及性质比较研究[D].哈尔滨: 哈尔滨商业大学,2011.
[14]HOOVER R,HUGHES T,CHUNG H J,et al.Composition,molecular structure,properties,and modification of pulse starches: a review[J].Food Research International,2010,43(2): 399-413.
[15] ASHOGBON A O,AKINTAYO E T,OLADEBEYE A O,et al.Developments in the isolation,composition,and physicochemical properties of legume starches[J].Critical Reviews in Food Science and Nutrition,2021,61(17): 2938-2959.DOI:10.1080/10408398.2020.1791048.
[16] ZHANG G Y,VENKATACHALAM M,HAMAKER B R.Impact of heatmoisture treatment and annealing in starches: a review[J].Carbohydrate Polymers,2011,83(2): 317-328.DOI:10.1016/j.carbpol.2010.08.064.
[17]GENYI Z,MAHESH V,R H B.Structural basis for the slow digestion property of native cereal starches[J].Biomacromolecules,2006,7(11):3259-3266.DOI:10.1021/bm060343a.
[18]WANG W T,GE J L,XU K,et al.Differences in starch structure,thermal properties,and texture characteristics of rice from main stem and tiller panicles[J].Food Hydrocolloids,2020,99: 105341.DOI:10.1016/j.foodhyd.2019.105341.
[19]韩文芳,林亲录,赵思明,等.淀粉中间级分的研究进展[J].食品科学,2019,40(23): 277-282.DOI:10.7506/spkx1002-6630-20181105-060.
[20] LOPEZ-SILVA M,BELLO-PEREZ L A,AGAMA-ACEVEDO E,et al.Effect of amylose content in morphological,functional and emulsification properties of OSA modified corn starch[J].Food Hydrocolloids,2019,97: 105212.DOI:10.1016/j.foodhyd.2019.105212.
[21] 王怡杰,洪雁,顾正彪,等.储藏时间对大米淀粉精细结构的影响[J].食品与生物技术学报,2021,40(5): 45-52.DOI:10.3969/j.issn.1673-1689.2021.05.006.
[22] ATROUS H,BENBETTAIEB N,HOSNI F,et al.Effect of gamma-radiation on free radicals formation,structural changes and functional properties of wheat starch[J].International Journal of Biological Macromolecules,2015,80: 64-76.DOI:10.1016/j.ijbiomac.2015.06.014.
[23]LI Q,WU Q Y,JIANG W,et al.Effect of pulsed electric field on structural properties and digestibility of starches with different crystalline type in solid state[J].Carbohydrate Polymers,2019,207:362-370.DOI:10.1016/j.carbpol.2018.12.001.
[24] KAPTSO G K,NJINTANG N Y,NGUEMTCHOUIN M G M,et al.Characterization of morphology and structural and thermal properties of legume flours: cowpea (Vigna unguiculata L.Walp) and bambara groundnut (Vigna subterranea L.Verdc.) varieties[J].International Journal of Food Engineering,2016,12(2): 139-152.DOI:10.1515/ijfe-2014-0146.
[25] 孟广宇,曾世通,刘珊,等.β-紫罗兰醇-β-D-葡糖苷的合成及热解性质[J].食品科学,2012,33(20): 21-26.DOI:CNKI:SUN:SP KX.0.2012-20-004.
[26]董宇晴.挤压对几种淀粉多尺度结构和理化性质影响的研究[D].济南: 齐鲁工业大学,2021.
[27]CHEN P,XIE F W,ZHAO L,et al.Effect of acid hydrolysis on the multi-scale structure change of starch with different amylose content[J].Food Hydrocolloids,2017,69: 359-368.DOI:10.1016/j.foodhyd.2017.03.003.
[28]宋一诺,谢新华,艾志录,等.月桂酸对不同直链淀粉含量小麦淀粉黏滞性和质构特性的影响[J].中国粮油学报,2016,31(9): 52-56;63.