近年来,海洋生物活性肽成为研究热点,其抗氧化、抗高血压和抗动脉粥样硬化等生物学特性以及溶解性、起泡性和乳化性等功能特性被广泛关注,这些特性缘于其化学组成和物理结构[1-3]。目前生物活性肽最常用的制备方法是酶解法[4],其中应用较多的酶是胃肠酶[5]。海洋资源是新型功能性成分的良好来源,如多糖、矿物质、维生素、抗氧化剂和多肽等[6]。海洋生物活性肽可被应用于功能食品、药品或化妆品领域[7]。
海洋活性肽主要从软体动物、甲壳动物、鱼类、藻类和一些海洋副产品(贝类、鱼皮、内脏和肌肉)中提取(图1)。藻类含有丰富的蛋白质,因此它是生物活性肽的良好来源,在食品、制药和化妆品行业有潜在的应用[2]。甲壳纲动物和软体动物也含有7%~23%的蛋白质,根据《世界海洋物种名录》,海洋软体动物在世界各地分布广泛,据估计,海洋软体动物约有48584 种。其中贻贝具有较高的观赏价值和食用价值,在捕捞过程中较小的或破碎的贻贝常常被直接丢弃,对废弃贻贝进行加工有助于工业的可持续发展,也有利于促进循环经济的发展[8]。近年来,有关海洋生物活性化合物的研究多关于海洋生物活性肽的抑菌活性、抗高血压活性和抗氧化活性,同时介绍多限于特定来源,如鱼类、贻贝和藻类的生物活性肽。本综述旨在收集从不同海洋来源(藻类、软体动物、鱼类和甲壳类动物)生物活性肽的生物活性和功能特性,总结其已开发的不同工业应用,对促进生物活性肽功能食品开发与产业应用方面具有重要意义。
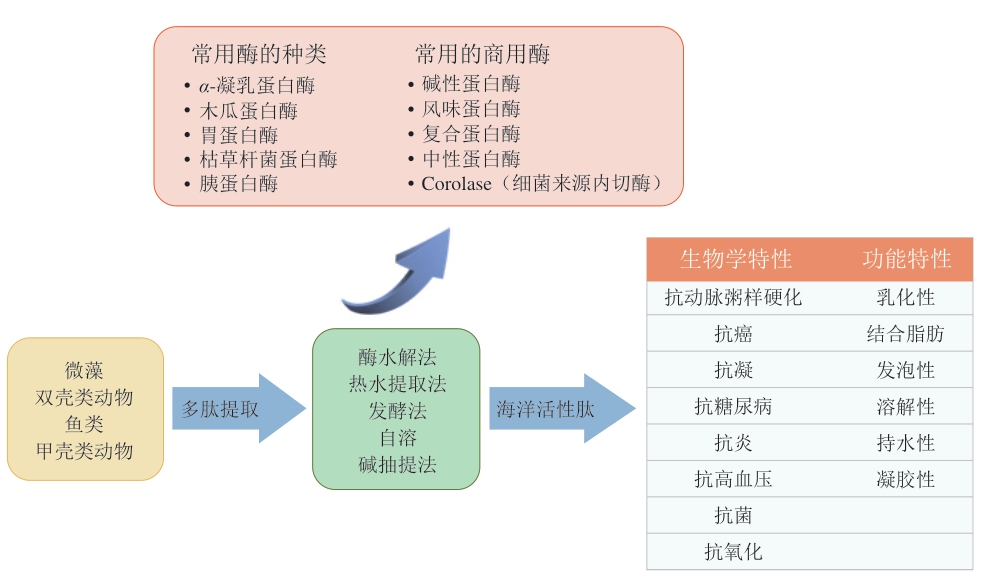
图1 海洋生物活性肽的常用生产方法及性质
Fig.1 Common production methods and properties of marine bioactive peptides
1 多肽的生物利用度
多肽在体外的活性可能与在体内不同,经口摄入多肽时,人体的消化系统可能会降低其生物活性[9],因此常通过体内和体外实验分析多肽的生物利用度。体外实验通常需要模拟胃肠道环境,首先可将多肽暴露在α-淀粉酶中,控制pH值在5.6~6.9之间,模拟口腔消化;然后通过模拟胃液(含胃蛋白酶,pH 2.0)、模拟肠液(含胰酶和胆盐,pH 6.0)模拟胃、肠消化;随后采用分子截留尺寸为3 kDa的半透膜进行透析,分析多肽能否被小肠吸收[10];最后,还需要对细胞膜内、外溶液中的多肽进行生物活性测试。为探究多肽在目标靶点的作用机理,多肽的体内活性研究(动物实验和临床研究)也是必要的,体内活性实验主要验证多肽的胃肠道消化率和溶解度、吸收、分布、利用率及最佳剂量等[2,11]。多肽的体内研究可采用不同的受试动物建立模型,如无脊椎动物(秀丽隐杆线虫和果蝇)、脊椎动物(大鼠和小鼠)等[11-12]。
为提高多肽的生物利用度,通常可制备多肽微胶囊和多肽纳米胶囊,降低胃肠消化系统对多肽的消化作用。一些常见的多肽包埋运载系统有微乳剂(水包油(oil in water,O/W)、油包水乳剂(water in oil,W/O))、乳化微乳剂(水包油包水(water-in-oil-inwater,W/O/W))、乳剂(O/W或W/O)、纳米乳剂(O/W或W/O)[13]、固体脂质纳米粒、脂质体和生物聚合微凝胶[14-15](图2)。在抗肿瘤研究中,多肽的包埋不会使其丧失抗肿瘤活性[16]。此外,微胶囊包埋还可以被应用于疫苗生产[17],这些研究结果为活性肽生物利用度的研究指明了方向。多肽的包埋可以防止多肽摄入后被消化降解,或防止其他因素(如氧化)导致的降解,还可以控制肽的释放(速率及环境条件)、增强肽的稳定性、降低多肽的毒性[3,18]。对于多肽的包埋,需要研究多肽的运载系统和终产品特性。对于活性肽本身,除分析其分子质量、电学性质、极性、溶解度、表面活性和稳定性外,还需要研究包埋后多肽颗粒的组成、大小和形状、界面属性和聚集状态等特性[14]。
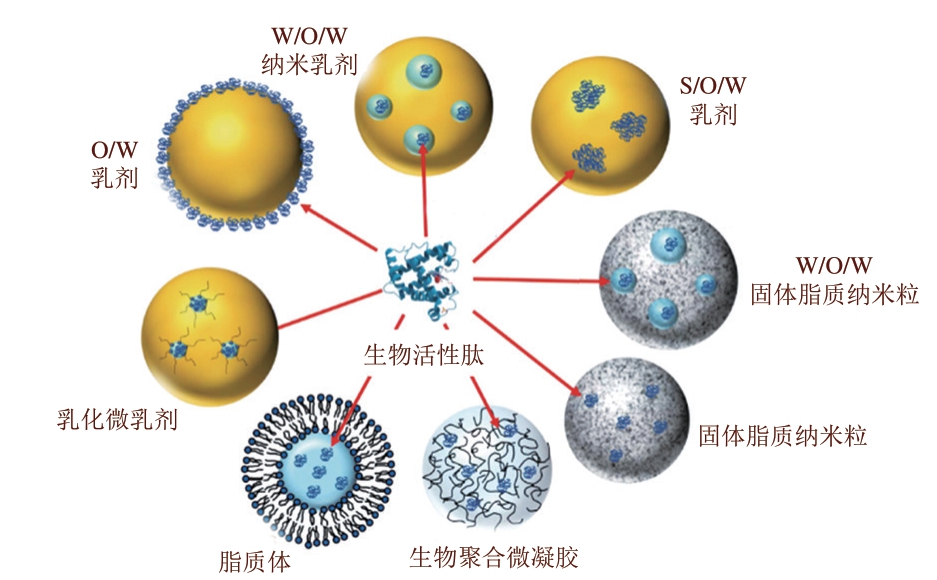
图2 亲水性生物活性肽胶体包埋运载系统的示意图
Fig.2 Schematic diagram of some common types of colloidal delivery systems for the encapsulation of hydrophilic bioactive peptides
S/O/W.水包油包固体物质(solid-in-oil-in-water)。
2 海洋生物活性肽的生物学特性
海洋生物活性肽的来源主要有藻类、软体动物、鱼类和甲壳类动物,近5 年有关这些来源活性肽的制备方法及产物特点的研究分别如表1~3所示。提取方法有酶法水解、发酵法、酸碱抽提法、热水提取法或不同技术的组合,其中最常用的方法是酶法水解,胃蛋白酶、木瓜蛋白酶、胰蛋白酶和碱性蛋白酶等是常用酶。部分研究已经确定了多肽的序列、分子质量以及生物学特性,Cunha等[5]整理了不同来源海洋生物活性肽的分子质量范围,发现多数生物活性肽的分子质量低于3 kDa,如27 种藻类多肽中,仅有2 种活性肽分子质量在3 kDa以上,11 种活性肽分子质量在1~3 kDa之间,14 种活性肽分子质量在1 kDa以下;28 种软体动物活性肽中,10 种活性肽分子质量在4 kDa以上,8 种活性肽的分子质量在1~4 kDa,6 种活性肽分子质量低于1 kDa;20 种鱼类、甲壳类活性肽中,13 种活性肽分子质量低于1 kDa,3 种活性肽分子质量为1~3 kDa,7 种活性肽分子质量大于3 kDa。此外,贻贝多肽往往比藻类和其他物种的多肽具有更高的分子质量[5]。
表1 近5 年从藻类中提取的生物活性肽研究
Table 1 Bioactive peptides derived from alga in the last five years
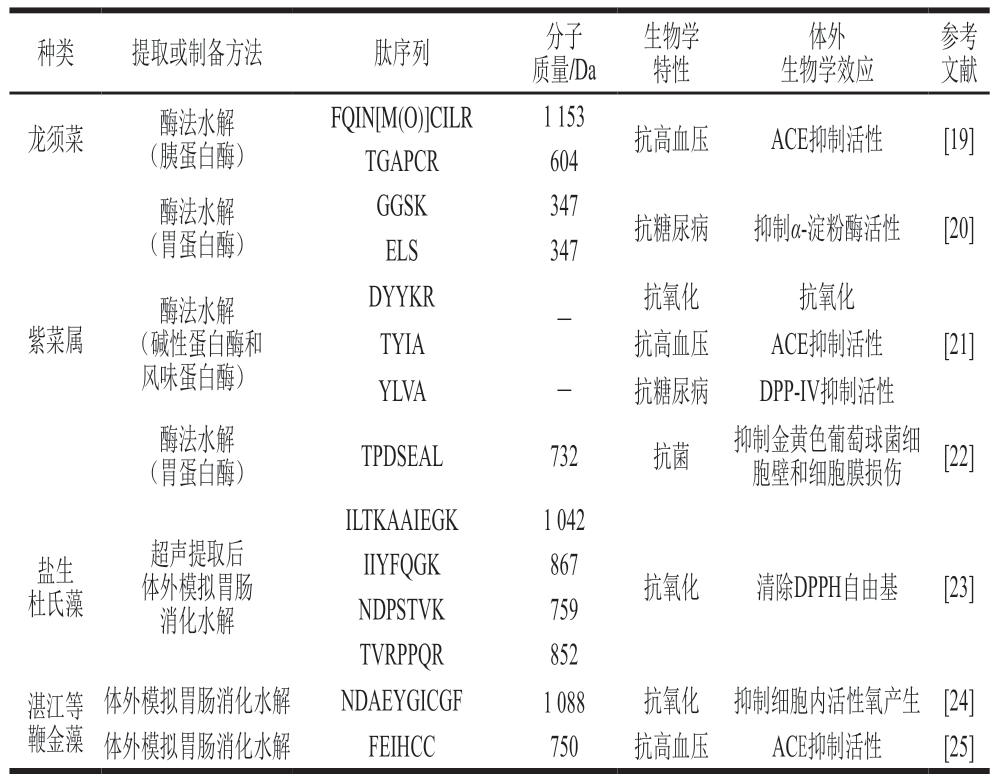
注:ACE.血管紧张素转化酶(angiotensin converting enzyme);DPP-IV.二肽基肽酶抑制剂(dipeptidyl peptidase IV);DPPH.1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl);-.未报道;下同。
表2 近5 年软体动物源的生物活性肽研究
Table 2 Bioactive peptides derived from mollusks in the last five years
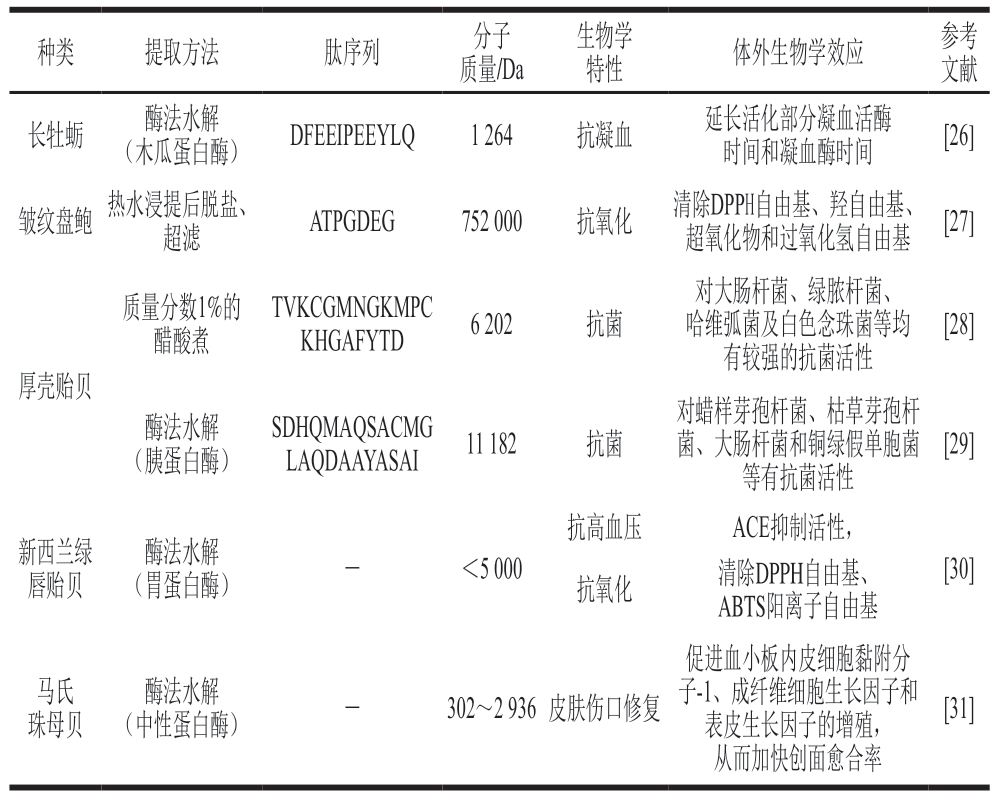
注:ABTS.2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(2,2’-azinobis-(3-ethylbenzthiazoline-6-sulphonate))。
表3 近5 年来自鱼类、甲壳纲动物和其他海洋物种的生物活性肽研究
Table 3 Bioactive peptides derived from fish,crustaceans and other marine species in the last five years
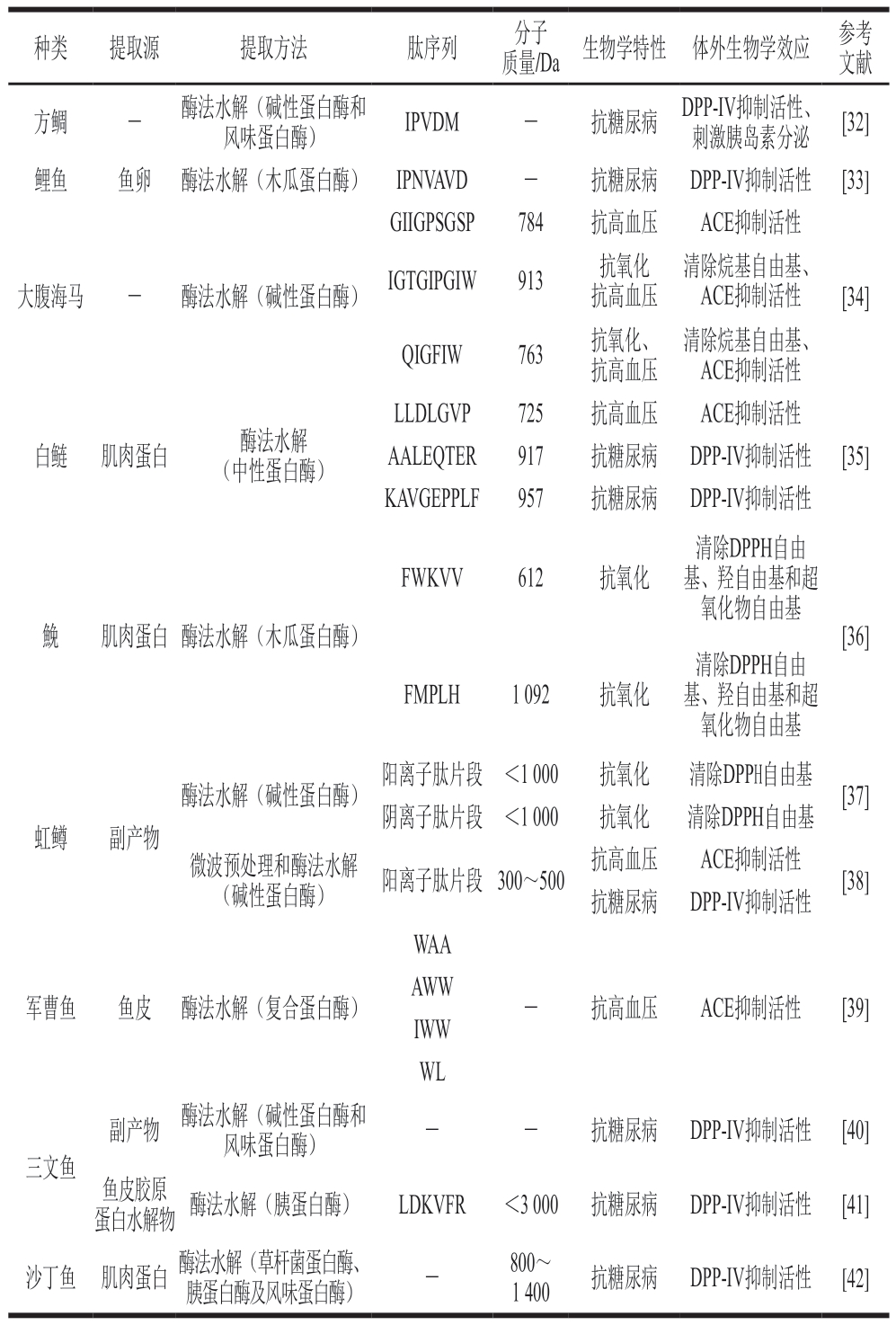
海洋活性肽具有抗动脉粥样硬化、抗癌、抗凝血、抗糖尿病、抗炎、抗高血压、抗菌和抗氧化的活性,其中抗高血压和抗氧化活性被广泛研究。从藻类中分离得到的抗癌和抗菌肽(antimicrobial peptides,AMPs)较少,抗菌和抗炎肽常源于软体动物。此外,一些研究结果显示了多肽往往同时具有多种生物活性,如常同时具备抗氧化和抗高血压作用。
2.1 抗动脉粥样硬化活性
心血管疾病(cardiovascular disease,CVD)是世界范围内导致死亡的主要疾病。动脉粥样硬化是一种多因素的慢性疾病,发病机制复杂,可导致心肌梗死、缺血性心肌病、中风和外周动脉疾病,是CVD的主要病因。在动脉粥样硬化中,动脉阻塞是由减少血流的病变或斑块的形成引起的。这些斑块主要由胆固醇等脂质在动脉膜空间中大量积累导致[43-45]。
关于海洋肽抗动脉粥样硬化活性的近期研究很少,2013 年Vo 等[46]发现极大螺旋藻提取的多肽可以下调组胺诱导的内皮细胞激活,具有潜在的抗动脉粥样硬化活性。Shih等[47]从小球藻中提取的多肽(VGCTGPAAPGP)显示出体外活性,降低了内皮细胞选择素的产生,这种选择素是参与动脉粥样硬化的最重要的血管黏附分子;同时还降低了细胞间细胞黏附分子和血管细胞黏附分子的产生。Fitzgerald等[48]利用木瓜蛋白酶水解红海藻,制备并分离了一种四肽,其显示出体外抑制乙酰水解酶的能力,此外,其良好的水溶性有利于应用于食品和制药产品中。
尽管已经发现一些藻类衍生多肽具有抗动脉粥样硬化活性,而近些年却鲜有报道。作为一个潜力领域,在其他藻类中寻找可抑制乙酰水解酶或血管黏附分子的活性肽是可行的。
2.2 抗癌活性
癌症是全球常见的主要死亡原因之一,是严重影响人类福祉的慢性疾病。癌症病例数量和死亡率不断增加,2020年,全球新发癌症1810万 例,导致989万 人死亡,预计在未来20 年癌症病例将增加约50%[49]。多年来,一些天然化合物已被证明具有抗癌作用,如类黄酮、类胡萝卜素、酚酸、异硫氰酸酯、姜黄素、白藜芦醇[50]。抗癌肽(anticancer peptides,ACPs)和蛋白质数据库(CancerPPD)(http://crdd.osdd.net/raghava/cancerppd/)中约有3491 种多肽具有抗癌活性,这些多肽通过与癌细胞特定位点结合,抑制癌细胞分裂或诱导癌细胞凋亡来发挥作用[51]。
ACPs的功效和作用机制已被广泛研究,天然的宿主防御肽具有抗菌或抗真菌活性,已在不同的生物体中发现。与单克隆抗体和检查点抑制剂相比,ACPs体积更小,溶解度更高,具有更好的药代动力学和更高的细胞吸收率,可以增强其效力和疗效[52]。许多天然多肽,如普立肽(plitidepsin)、微管蛋白聚合抑制剂、地地霉素B和海洋环脂肽都已被用于临床试验,用于治疗各种癌症。弄清这些肽的构效关系有助于肽基药物的设计和开发。
近些年,来自于陆地植物和动物多肽在抗癌活性方面研究的较为深入,例如Karami等[53]发现小麦胚芽蛋白水解物生物活性肽具有抗氧化、抗癌和ACE抑制活性;Ayisigi等[54]研究发现壳聚糖包埋的稻壳水解多肽具有抗癌活性;Taghizadeh等[55]发现穿山甲新型生物活性肽具有抗癌和抗氧化活性。人们已对海洋药物的生产进行了广泛的研究,第一个源自海洋的抗癌药物阿糖胞苷从加勒比海海绵中提取,于1959年获批。目前共有8 种天然产物衍生的抗癌药物被美国食品和药物管理局(Food and Drug Administration,FDA)或欧洲医学机构(European Medical Agency,EMA)批准,其中两种抗癌药物是属于海洋肽[56]。齐考诺肽是从僧袍芋螺毒液中纯化出的一种可用于减轻癌症晚期病人疼痛的海洋肽药物,2004年获FDA批准,2005年获EMA批准,标记名称为Prialt®,齐考诺肽可阻断N型钙通道,抑制痛觉传入神经递质向突触空间的释放,从而抑制疼痛向大脑的传递[56-57]。第二种标记的海洋肽衍生药物是本妥昔单抗(ADCETRIS®),源于微管蛋白聚合抑制剂一甲基澳瑞他汀E(monomethyl auristatin E,MMAE),是一种源于软体动物海兔的活性肽。本妥昔单抗与白细胞抗原分化簇30抗体结合后,与溶酶体融合,经蛋白酶水解,MMAE进入细胞并与细胞质微管蛋白结合,破坏细胞内微管网络,诱导G2/M期细胞周期阻滞和凋亡[56]。
海洋多肽可能是一种很有前途的癌症药物的天然替代品,需要在动物模型和人体中进行体内研究来证实多肽对癌细胞的作用。
2.3 抗凝血活性
凝血因子可以止血和修复受损的血管,抗凝剂作为一种治疗药物,通过延长凝血时间或阻止凝血来干扰凝血机制。目前主要的商业抗凝剂是肝素,然而其副作用较多,如血小板计数低和出血效应,会引起严重的并发症,限制了其长期应用[26]。阿司匹林和氯吡格雷也具有抗凝血效果,但同样存在出血风险[58],而海洋活性肽无细胞毒性,具有替代这些药物的潜力。
活化部分凝血活酶时间、凝血酶原时间和凝血酶时间是常见的抗凝血活性分析指标。现有研究中海洋抗凝剂化合物主要是多糖和蛋白聚糖。目前海洋来源的有抗凝血活性多肽的主要源自藻类(条斑紫菜)、贻贝(长牡蛎、紫贻贝)、螠虫(单环刺螠)[26,59-60]。所有多肽经过体外测试均显示出延长活化部分凝血活酶时间,且呈剂量-效应关系。紫贻贝活性肽的作用是抑制酶复合物中X因子的激活和将凝血酶原酶复合物中的II因子转化为IIa因子。类似的,单环刺螠中提取的活性肽可抑制凝血因子FXIa,木瓜蛋白酶水解获得的长牡蛎活性肽(DFEEIPEEYLQ)通过与纤维蛋白原竞争来抑制凝血酶活性,延长活化部分凝血活酶时间和凝血酶时间。
海洋源活性肽可能是良好的肝素替代品,通常具有抗凝血活性的多肽分子质量均小于3.5 kDa,大部分低于2.5 kDa[5]。因此,考虑到已识别的抗凝肽的低分子质量,可以过滤筛选分子质量低于3 kDa的抗凝血活性肽。然后需要进一步的研究,以评估它们是否显示出类似肝素的副作用。
2.4 抗糖尿病活性
活性肽具有抑制葡萄糖苷酶、α-淀粉酶或DPP-IV的能力,为糖尿病治疗开辟了新的途径。抗糖尿病多肽最早是从牛奶和大豆蛋白中提取的,但是海洋来源抗糖尿病多肽的研究一直在增加,特别是在鱼类中[11]。方鲷水解多肽(IPVDM和IPV)显示出体外抑制DPP-IV能力,常规体外试验中,IPVDM肽对DPP-IV半抑制浓度(half maximal inhibitory concentration,IC50)为(21.72±1.08)µmol/L,在Caco-2细胞为基础的DPP-IV抑制试验中,IC50达到(44.26±0.65)µmol/L,并且这两种活性肽均可刺激胰岛素分泌[32]。在木瓜蛋白酶鲤鱼卵水解物中,分离出的多肽(IPNVAVD)具有DPP-IV抑制活性,通过Caco-2细胞和HepG2细胞模型的研究结果显示,IC50达到(777.35±5.50)μmol/L[33]。三文鱼副产物胰蛋白酶水解物中,多肽LDKVFR具有DPP-IV抑制活性,IC50达到(0.10±0.03)mg/mL,分子对接发现LDKVFR与DPP-IV之间的6 个氢键和8 个疏水作用有助于抑制DPP-IV活性[40]。
鲜有关于贻贝多肽抗糖尿病活性的研究。在紫菜中分离的抗糖尿病活性肽(GGSK和ELS)可抑制α-淀粉酶活性,从而控制血液中的葡萄糖水平[20]。几乎所有抗糖尿病肽的分子质量都很小,一般小于1000 Da。这些肽大部分具有体外DPP-IV抑制作用,部分抗糖尿病多肽通过抑制α-淀粉酶活力从而控制血糖水平。
2.5 抗炎活性
炎症是免疫系统对有害刺激的反应,如毒物或病原体,它是身体防御机制的一部分[61]。多种途径与炎症相关,但它们都涉及细胞表面模式受体对有害刺激的识别、炎症途径的激活、炎症标志物的释放和炎症细胞的募集[62]。巨噬细胞在免疫反应中起着重要作用,免疫系统经刺激后,巨噬细胞可以分泌多种炎症介质,如一氧化氮(NO)、前列腺素E2(prostaglandin E2,PGE2)、肿瘤坏死因子(tumour necrosis factor,TNF)-α、白介素(interleukin,IL)-6和IL-1。此外,干扰素γ、促炎细胞因子(TNF-α、IL-6和IL-1b)和革兰氏阴性细菌脂多糖(lipopolysaccharide,LPS)可激活巨噬细胞。
大多数抗炎活性肽是从软体动物中提取的。从藻类、鱼类和甲壳类动物中分离出多肽的文献很少。从菲律宾蛤仔碱性蛋白酶水解获得抗炎活性肽(QCQQAVQSAV),体外试验中,该多肽可以抑制LPS诱导炎症RAW264.7小鼠单核巨噬细胞NO的产生,另外,从厚壳贻贝和长牡蛎中也分离到类似的抗炎活性肽[63-65]。鲑鱼的胸鳍经胃蛋白酶水解得到抗炎肽,该肽在LPS诱导的RAW264.7小鼠单核巨噬细胞中显示出多种抗炎作用,如抑制诱导型NO合成酶和环氧合酶-2的蛋白表达,减少促炎细胞因子(TNF-α、IL-6和IL-1b)的产生[66]。
2.6 抗过敏活性
过敏反应是免疫系统对正常无害的环境物质的一种反应,过敏反应的严重程度无法预测,从轻微的瘙痒和呕吐到危及生命的全身过敏反应,每年导致数千人死亡。肥大细胞、嗜碱性粒细胞和嗜酸性粒细胞在过敏反应的起始和传播中起关键作用[67]。肥大细胞在过敏性疾病的发病机制中起着至关重要的作用[68],它们被免疫球蛋白E介导的过敏原引起的过敏反应激活。组胺是一种与急性炎症反应相关的重要媒介,与多种过敏反应有关,如血管水肿、血管高通透性、血管舒张、支气管收缩、黏液产生和体温过低。因此,抗过敏药物的主要靶点是抑制肥大细胞的降解和组胺的产生。
从巨大螺旋藻中提取的海洋肽的抗过敏活性已有相关体外试验研究,多肽LDAVNR(P1肽)和MMMLDF(P2肽)均表现出剂量依赖的抗过敏活性。因为它们能够减少组胺释放和细胞内Ca2+水平的升高,从而抑制肥大细胞脱颗粒(经形态学研究证实)。P1肽在依赖钙和微管的信号通路中起作用,而P2肽可抑制磷脂酶的激活和活性氧的形成[69]。海洋肽的抗过敏特性还没有被充分挖掘,有待进一步研究。
2.7 抗高血压活性
高血压是一种非常常见的疾病,与心血管风险直接相关。尽管可以利用健康的生活方式和抗高血压药物控制病情,一些患者的血压控制仍然很差。肾素-血管紧张素系统参与机体水、电解质和血液的调节,在高血压的发生发展中具有重要作用。ACE-I参与调节血压、催化血管紧张素II(一种强血管升压剂)的形成[70]。因此,抑制肾素-血管紧张素系统中两种限速酶(ACE-I或肾素酶)的活性可以控制高血压。现有合成降压药具有许多副作用,如慢性咳嗽、味觉丧失、肾损害、血管神经性水肿。因此,通过抑制ACE-I或肾素酶活性,找到具有抗高血压活性但又没有不良的副作用的天然化合物变得很重要。
牛乳清、蘑菇、核桃等来源的ACE抑制肽已被广泛研究。在海洋资源中,抗高血压肽已在鱼类、贻贝和藻类中进行了研究。大多数发现的抗高血压肽分子质量低于1.5 kDa,ACE抑制活性具有剂量-效应关系[5]。此外,通过木瓜蛋白酶的酶解作用从大型海藻-红海藻中分离获得一种具有体外肾素抑制活性的肽;从微藻类-小球藻中获得肽VECYGPNRPQF;从龙须菜中获得肽FQIN [M(O)]CILR和TGAPCR;从裙带菜中获得YH、KY、FY、IY、YNKL、IY、IW;这些海洋活性肽都显示了很好的体外ACE抑制活性。YH、KY、FY、IY采用热水提取制备,其余均由胃蛋白酶或胰蛋白酶酶解后制得[5,25,71]。在军曹鱼和鲣鱼的研究中也展示了潜在的活性,其衍生肽AWW、IWW、WL、VRP、IKP、LRP和IRP具有体外ACE抑制活性[39]。
2.8 抗菌活性
AMPs是先天免疫防御的主要成分之一,广泛存在于植物、哺乳动物以及微生物中。作为抵御病原微生物的第一道防线,抗菌因子具有重要的功能。通常AMPs是由12~50 个氨基酸组成阳离子多肽,具有两亲性结构特征[19,72-73]。AMPs的阳离子特性是其具有活性的主要原因,其可通过静电引力特异性地结合微生物细胞膜中带负电荷的LPS。阳离子AMPs的作用取决于它们的二级结构、总体净电荷、亲水性、疏水性、大小以及疏水区和极性区之间的平衡[74]。自AMPs被发现以来,其作用机制一直受到广泛的研究。了解AMPs的作用机制对其未来的治疗发展至关重要。AMPs主要通过两种不同的途径发挥抗菌作用:直接杀死微生物和调节免疫系统。根据作用靶点位置,直接杀死微生物通过两种不同的机制实现:非膜靶向机制和膜靶向机制。膜靶向肽破坏细胞膜,而非膜靶向肽阻碍细胞内关键代谢过程,如核酸和蛋白质的合成。如图3所示,AMPs可根据生物来源、理化性质、生物功能、共价键合模式、生物合成、分子靶标和二级结构进行分类[75]。
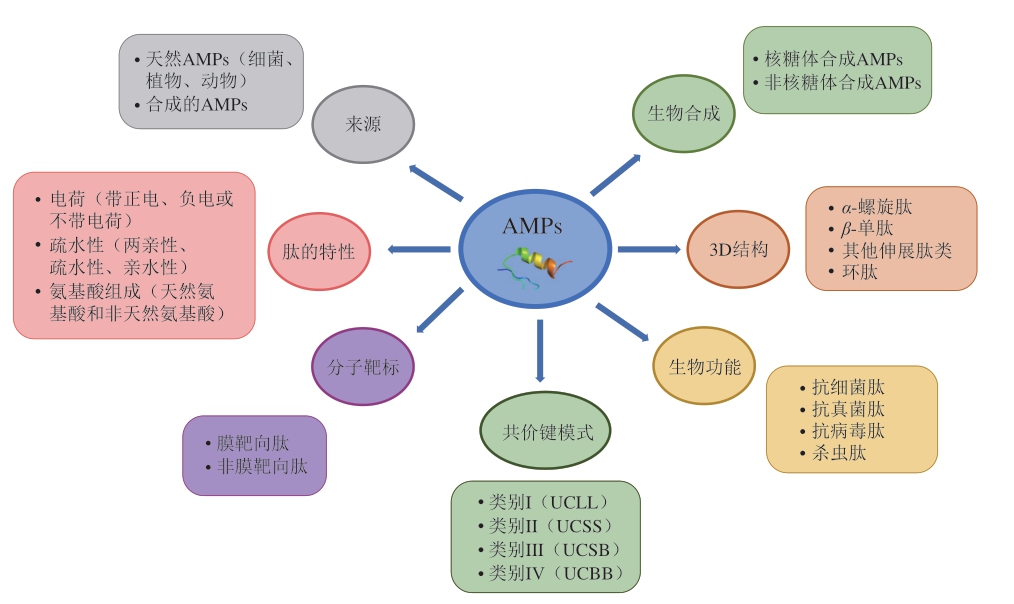
图3 基于来源、理化性质、分子靶点、共价键模式、生物功能、结构和生物合成的AMPs分类
Fig.3 Classification of antimicrobial peptides based on sources,physicochemical properties,molecular targets,covalent bonding pattern,biological function,structure and biosynthesis
海洋无脊椎动物不像脊椎动物那样具有适应性免疫,例如双壳类动物只有先天免疫,因此它们需要发展防御系统来适应其生活的环境,这些环境通常富含致病性微生物和病毒。它们的过滤活性也增加了它们与病原体的接触几率,无脊椎动物体内防御机制中之一是具有抗菌活性多肽。海洋贻贝AMPs的研究被分为8 类:Defensin、Mytilin、Myticin、Mytimycin、Mytimacin、Bigdefensin、Mytichitin-CBD和Myticusin-1[29]。从海洋贻贝中已经纯化和鉴定了几种AMPs,例如,紫贻贝(Mytilus galloprovincialis)胃蛋白酶水解得到贻贝肽Myticin C,其具有抗病毒活性,可抵抗人类单纯性疱疹病毒1和2。Oh等[28]2018年从双壳类的厚壳贻贝(Mytilus coruscus)中用热水提取出AMPs,该肽对革兰氏阳性和革兰氏阴性细菌以及真菌具有很强的抗菌活性。随后该团队利用厚壳贻贝(Mytilus coruscus)制备了AMPs Myticusin-beta,该活性肽总分子质量约为11 kDa,对大肠杆菌和金黄色葡萄球菌等多种病原微生物显示了抗菌活性[29]。在藻类AMPs的研究中,Guzmán等[76]从水腹圆藻中通过酸浸提获得的多肽混合物具有很强的革兰氏阳性菌和革兰氏阴性菌的活性;Jiao Kui等[22]利用胃蛋白酶水解紫菜制备了分子质量732 Da的活性肽TPDSEAL,该活性肽可损伤金黄色葡萄球菌细胞壁和细胞膜。
2.9 抗氧化活性
活性氧和自由基参与了大量的代谢过程,可引起细胞损伤,从而导致癌症、CVD、神经疾病、肺病、类风湿性关节炎、肾病、眼部疾病和产前医学问题[77]。大型藻类被认为是天然生物活性化合物的重要来源,特别是那些具有抗氧化活性的化合物。在藻类中鉴定出的具有抗氧化活性的化合物主要有叶绿素和衍生物、类胡萝卜素、VE和VC、藻黄质、酶、椰孢素类氨基酸、多糖和多酚[78]。尽管抗氧化肽的确切作用机制仍未完全揭示,但目前研究最多的机制有:抑制脂质过氧化、清除自由基和金属络合能力。
海洋来源的抗氧化肽分子质量较低,一般低于3 kDa,除了太平洋无须鳕(Merluccius productus)的自解产物和巴夫藻(Pavlova lutheri)的酵母发酵产物外,几乎都是通过酶水解产生的,胃蛋白酶是生产海洋抗氧化肽常用酶[5]。研究结果主要集中在清除羟自由基、过氧自由基、DPPH自由基和ABTS阳离子自由基的能力上。此外,只有少数研究评估了多肽对DNA和细胞的保护作用及氧自由基吸收能力。
2.10 其他活性
其余的海洋活性肽活性研究中,从鱼或副产物中提取的胶原蛋白水解物是一种有前途的功能食品的成分,通过提高皮肤胶原蛋白含量,来促进皮肤改善可以预防皮肤衰老,此外,研究表明海洋AMPs可以通过调节成骨合成途径而发挥抗骨质疏松作用[79]。
3 海洋活性肽的功能性质
蛋白质或蛋白质水解物的功能特性受其分子质量、物理结构、氨基酸组成和序列、电荷、疏水性/亲水性比以及与其他成分相互作用的影响。尽管关于特定海洋肽功能特性的研究不多,然而,一些研究显示了蛋白质水解物对功能性质的影响,如乳化能力和溶解度。海洋蛋白质的酶解已被用于改善蛋白质的功能性质,特别是鱼的副产物[5]。食品配方中最重要的性质是乳化能力和稳定性、溶解度和脂肪结合能力,蛋白质水解可以增强这些特性[80]。
3.1 溶解性
溶解度是食品中最重要的功能特性之一,高可溶性蛋白更适合食品工业,溶解度影响其他性质,如乳化和起泡,多肽的溶解性提高,乳化和起泡性增强。蛋白酶水解度越高,溶解度越好。pH值为6或7可增加鲑鱼副产物水解物的溶解度[80]。沙丁鱼副产品水解物也显示了类似的结果,蛋白质水解物比未消化的水解物更容易溶解。水解度较高的水解产物在pH 6~10的条件下具有较好的溶解性[5]。通过碱性蛋白酶和风味蛋白酶水解金带细鲹鱼制备的蛋白水解物在pH 2~12条件下蛋白溶解度可达85%以上。此外,通过美拉德反应提高蛋白水解物溶解性是其功能改性的有效途径,探索精准控制食源蛋白水解物与糖类物质美拉德反应进程,对提高其溶解性也具有重要意义[1]。
3.2 乳化性质和发泡性能
用乳化活性指数(emulsifying activity index,EAI)来测定乳化能力,并通过乳液稳定性指数(emulsion stability index,ESI)衡量乳剂抗分解的能力,因此ESI越高,乳液越稳定。多肽的长度和乳化能力相关,因为较小的多肽具有较低的乳化性能,另一方面,更大的肽或疏水性更强的肽ESI更高。从鱼的肌肉、皮肤和副产物(头部、内脏、鳍等)中提取的鱼蛋白水解物(fish protein hydrolysate,FPH),表现出良好的溶解性、起泡和乳化性能[81]。乳化能力和乳化稳定性并没有因水解程度而提高。水解度越高,肽段越小,乳化性能越弱。蛋白水解物的乳化性质受溶解度、肽的分子质量和氨基酸序列、水解程度、肽的乙酰化程度、使用的酶种类、提取溶剂、环境pH值等因素的影响。
Taheri等[81]从咸味鲱鱼卤水中分离得到的分子质量大于50 kDa的多肽具有良好的EAI和较高的发泡能力,而短肽段的多肽则没有这种能力,且分子质量大于50 kDa的多肽在pH 10时发泡能力最强,在pH 4时发泡能力最弱,这可能与其等电点有关。在沙丁鱼水解物中,随着水解程度的增加和pH值的升高,泡沫形成量减少[5]。与鳕鱼皮胶原蛋白肽相比,鳕鱼皮胶原蛋白肽-木糖共价复合物起泡性和泡沫稳定性明显增强[1]。
3.3 保水性和脂肪结合能力
保水性在食品工业中是重要的加工性质,一旦蛋白质水解物或多肽赋予食物保持水分的能力,通常会改善食品质地。在FPH中,高溶解度会降低保水能力。具有较低分子质量肽的FPH表现出较高的持水能力[82]。多肽或蛋白质水解物的脂肪结合能力是某些食品(肉类和糖果)所需要的特性,它也会影响食品的味道。蛋白质的容重、水解度和酶-底物特异性都可能影响酶的活性。对两种FPH的研究结果表明,随着肽分子尺寸的增大,脂肪结合能力下降[83]。
4 海洋活性肽的工业应用
4.1 当前工业应用
生物活性肽可用于不同的工业领域,如食品、化妆品或制药行业。在食品工业中,几种含有生物活性多肽的乳制品已经商业化。微藻在化妆品中的应用越来越受到人们的关注,特别是节旋藻和小球藻。Dermochlorella®是由小球藻制备的寡肽,其有助于紧致皮肤、增强眼部轮廓效果以并能够促进胶原蛋白合成,已被用于化妆品配方[69]。
抗氧化肽在食品包装中的应用也很有意义,因为脂质氧化是食品变质的主要原因之一,如在坚果、鱼、肉类和酱汁中,脂质氧化导致酸败,形成有毒的醛和营养质量的损失。为了防止这种变质,抗氧化剂被用作食品添加剂或在受控气氛中包装以限制氧气的存在[84]。
一些含有FPH和多肽的产品已经在日本作为功能食品出售,如饮料和汤粉或膳食补充剂。在美国和加拿大功能食品市场,通过酶水解深海白鱼蛋白制备的多肽作为膳食补充剂有助于调节肠道功能,自溶法制备的大西洋鲑鱼鱼蛋白水解多肽,可用于运动营养补充剂。在英国功能食品市场,由酶水解鱼蛋白获得的多肽作为膳食补充剂,调节情绪性压力症状[5]。
超过60 种多肽已经被FDA批准在医学上应用,大量的临床前研究正在进行中[11]。一些基于海洋多肽的药物已经获得了FDA的批准,其他药物正在进行临床试验。例如,一种从僧袍芋螺分离的肽唑可肽,可用于治疗严重的慢性疼痛;从阿斯普伦狸藻(Utricularia asplundii)中提取的普利肽和阿普利定可用于治疗癌症;从海兔中提取的本妥昔单抗和格伦巴图单抗维多汀可用于癌症治疗。然而,大多数来自海洋物种的肽或水解物只在体外进行了测试,少有研究进行了人体实验[11]。
4.2 未来工业应用
与常见农作物(小麦和大豆)相比,海洋藻类储量丰富、易于生产、生物量高、富含蛋白质、更易获取,因此从藻类中分离出的有益活性肽极具工业应用潜力。螺旋藻是一种蓝藻,其蛋白质含量(干质量的53%~62%)高于其他藻类,含有所有必需氨基酸,且作为生物活性肽的优质来源,螺旋藻活性肽具有多种生物活性,例如抗菌、抗过敏和抗高血压等,极具应用前景。近年来,相关学者研究了很多海洋多肽,并表征了一些重要的生物活性,但目前研究仍有很多不足,如藻类蛋白质含量随季节、温度和捕捞地点的变化而改变。因此,蛋白质含量是影响藻类活性肽制备的一个关键因素[2]。
4.2.1 在制药和营养中的应用
具有抗高血压、抗凝血、抗菌和抗氧化作用的多肽可能对疾病的预防或治疗有作用。一些来自海洋的多肽已经进行了临床试验,但大多数研究都是基于体外实验,为了进一步将多肽用作营养药品和药物,则必须进行体内实验以了解其具体效果。例如,海洋来源抗高血压活性多肽药物的开发,必须进行更多的体内实验和药代动力学研究[25];海洋来源抗糖尿病活性多肽有助于促进2型糖尿病的治疗,而备受关注[38]。
4.2.2 在食品工业中的应用
AMPs对一些细菌和真菌菌株具有抑制作用,有助于食物的保存,具有很高的作为食品防腐剂的潜力。微藻细胞壁往往由于其纤维素性质难以消化,导致食用蛋白质效率低。然而,从微藻中制备的蛋白质水解物显示出更高的消化率和更高的肽和氨基酸生物有效性,增加了它们的食品应用价值。未来开发和研究应突出海洋生物肽在人类营养中的几个优势,以增加其在食品中的应用[5],例如:它们比完整的蛋白质或游离氨基酸更容易被胃肠道吸收;它们有多种生物活性,可增强食物对人类健康的益处;可以作为防腐剂使用;可以为可持续发展作出贡献,因为可以利用海洋副产品。
4.2.3 在化妆品工业中的应用
抗氧化多肽的开发对化妆品行业的发展具有重要意义,一方面,抗氧化多肽可清除体内自由基,具有防止皮肤老化和皮肤紊乱的功能;另一方面,抗氧化多肽可防止脂质氧化,进而延长商品的保质期[85]。从一些藻类中提取的多肽可用于皮肤和头发护理的化妆品配方中,如身体乳液、洗发水、头发修复剂、染发剂、肥皂等。
4.3 涉及多肽应用的问题
尽管生物活性肽的应用有很大的可能性,但在人类健康和最终产品特性方面仍应考虑一些问题。一些海洋物种,尤其是贝类,在很大程度上被描述为过敏原。食物过敏原具有蛋白质性质,可被免疫球蛋白E表面抗体识别,从而产生一种防御机制,其特征为皮疹、湿疹、鼻炎、发烧。蛋白质分解成多肽可能保留原蛋白质的过敏原性质,因此,生物活性多肽在应用前必须测试其过敏原性[69]。为了了解多肽的潜在致敏性,应该了解原始基质是否与致敏性有关,应进行体外研究、免疫学方法和动物研究等试验,在最后阶段,应进行临床试验,如皮肤试验和其他临床试验,以确定这些化合物是否适合用于食品或化妆品。由于来自动植物的多种蛋白和多肽被证实具有细胞毒性作用,可能导致癌症和其他并发症,因此要对这些多肽进行细胞毒性分析。此外,人类摄入的蛋白质和多肽的类型可能对人类肠道菌群是有利的也可能是不利的。有些肽可以维持或促进肠道益生菌的生长,然而,不可消化蛋白质是一个值得关注的问题,因为它们会增加患炎症性肠病、CVD、癌症或糖尿病的风险[82]。
蛋白质水解物与苦味有关,这是食品工业中存在的一个问题。为了去除这种苦味,研究人员采用了溶剂选择性萃取、微孔树脂和活性炭吸附、外肽酶酶解、美拉德反应、“质体反应”和包封等方法。另一方面,为了掩盖最终产品中的苦味,肽可以与食品添加剂、甜味剂和香料混合[83]。此外,多肽的生物活性可能随着食品加工或与其他成分的相互作用而降低或改变。例如,食品加工方法(热处理、非热处理、储存条件、干燥和分离方法)、消化都可能使多肽发生化学或物理变化,从而影响多肽的生物活性。氨基酸的组成可能受到食品加工的影响,导致对人类有害的化合物的形成,如D-氨基酸和生物胺[11]。因此,需要进一步研究更好的方法或基质,以避免在食品中添加多肽时产生的异味或相互作用,防止多肽降解和生物活性的降低。
5 结语
海洋物种作为生物活性化合物的来源,具有多种生物活性与功能,在制药、食品、营养和化妆品行业具有潜在应用价值。此外,为了更深入地了解肽的应用,本文列举了生物利用度等问题。海洋生物活性肽是一个很有发展前景的领域,但目前在海洋生物活性肽领域的应用还很匮乏。因此,有必要进一步研究生物活性肽在最终产品中的应用,以更好地了解它们的性能、潜力和消费者接受度。海洋的生物多样性高,相关产品存在大量高蛋白含量的废弃物,因此,利用海洋物种生产活性肽可促进社会可持续发展,有助于促进其未来在功能食品、医药产品和化妆品中的开发与应用。
[1]沈圆圆,于福田,赵笑颍,等.食源性抗炎活性肽对肠道炎症的作用研究进展[J].食品科学,2022,43(7): 305-316.DOI:10.7506/spkx1002-6630-20210319-244.
[2]BLEAKLEY S,HAYES M.Algal proteins: extraction,application,and challenges concerning production[J].Foods,2017,6(5): 33.DOI:10.3390/foods6050033.
[3]LEMES A C,SALA L,ORES J D C,et al.A review of the latest advances in encrypted bioactive peptides from protein-rich waste[J].International Journal of Molecular Sciences,2016,17(6): 950.DOI:10.3390/ijms17060950.
[4]PIMENTEL F B,ALVES R C,HARNEDY P,et al.Macroalgalderived protein hydrolysates and bioactive peptides: enzymatic release and potential health enhancing properties[J].Trends in Food Science &Technology,2019,93: 106-124.DOI:10.1016/j.tifs.2019.09.006.
[5]CUNHA S A,PINTADO M E.Bioactive peptides derived from marine sources: biological and functional properties[J].Trends in Food Science &Technology,2022,119: 348-370.DOI:10.1016/j.tifs.2021.08.017.
[6]AGRAWAL S,ACHARYA D,ADHOLEYA A,et al.Nonribosomal peptides from marine microbes and their antimicrobial and anticancer potential[J].Frontiers in Pharmacology,2017,21(8): 828.DOI:10.3389/fphar.2017.00828.
[7]GOGINENI V,HAMANN M T.Marine natural product peptides with therapeutic potential: chemistry,biosynthesis,and pharmacology[J].Biochimica et Biophysica Acta,2017,1862(1): 181-196.DOI:10.1016/j.bbagen.2017.08.014.
[8]NAIK A S,HAYES M.Bioprocessing of mussel by-products for value added ingredients[J].Trends in Food Science &Technology,2019,92:111-121.DOI:10.1016/j.tifs.2019.08.013.
[9]BHANDARI D,RAFIQ S,GAT Y,et al.A review on bioactive peptides: physiological functions,bioavailability and safety[J].International Journal of Peptide Research and Therapeutics,2020,26:139-150.DOI:10.1007/s10989-019-09823-5.
[10]CAMPOS D A,COSCUETA E R,VILAS-BOAS A A,et al.Impact of functional flours from pineapple by-products on human intestinal microbiota[J].Journal of Functional Foods,2020,67: 103830.DOI:10.1016/j.jff.2020.103830.
[11]RIVERO-PINO F,ESPEJO-CARPIO F J,GUADIX E M.Antidiabetic food-derived peptides for functional feeding: production,functionality and in vivo evidences[J].Foods,2020,9(8): 983.DOI:10.3390/foods9080983.
[12]NOVA P,MARTINS A P,TEIXEIRA C,et al.Foods with microalgae and seaweeds fostering consumers health: a review on scientific and market innovations[J].Journal of Applied Phycology,2020,32(2):1789-1802.DOI:10.1007/s10811-020-02129-w.
[13]MCCLEMENTS D J.Nanoemulsions versus microemulsions:terminology,differences,and similarities[J].Soft Matter,2012,8(6):1719-1729.DOI:10.1039/C2SM06903B.
[14]MCCLEMENTS D J.Encapsulation,protection,and delivery of bioactive proteins and peptides using nanoparticle and microparticle systems: a review[J].Advances in Colloid &Interface Science,2018,253: 1-22.DOI:10.1016/j.cis.2018.02.002.
[15]LI Q,SHI J L,LIU L,et al.Encapsulation of fruit peel proanthocyanidins in biopolymer microgels: relationship between structural characteristics and encapsulation/release properties[J].Food Hydrocolloids,2021,117: 106693.DOI:10.1016/j.foodhyd.2021.106693.
[16]ZHANG B C,ZHANG X W.Separation and nanoencapsulation of antitumor polypeptide from Spirulina platensis[J].Biotechnology Progress,2013,29(5): 1230-1238.DOI:10.1002/btpr.1769.
[17]XI X B,YE T,WANG S,et al.Self-healing microcapsules synergetically modulate immunization microenvironments for potent cancer vaccination[J].Science Advances,2020,6(21): 7735.DOI:10.1126/sciadv.aay7735.
[18]COSTA J R,SILVA N C,SARMENTO B,et al.Delivery Systems for antimicrobial peptides and proteins: towards optimization of bioavailability and targeting[J].Current Pharmaceutical Biotechnology,2017,18(2): 108-120.DOI:10.2174/1389201017666161207112244.
[19]DENG Z,LIU Y,WANG J,et al.Antihypertensive effects of two novel angiotensin iconverting enzyme (ACE) inhibitory peptides from Gracilariopsis lemaneiformis (Rhodophyta) in spontaneously hypertensive rats (SHRs)[J].Mar Drugs,2018,16(9): 299.DOI:10.3390/md16090299.
[20]ADMASSU H,GASMALLA M A A,YANG Ruijin,et al.Identification of bioactive peptides with α-amylase inhibitory potential from enzymatic protein hydrolysates of red seaweed (Porphyra spp)[J].Journal of Agricultural and Food Chemistry,2018,66(19): 4872-4882.DOI:10.1021/acs.jafc.8b00960.
[21]CERMENO M,STACK J,TOBIN P R.Peptide identification from a Porphyra dioica protein hydrolysate with antioxidant,angiotensin converting enzyme and dipeptidyl peptidase IV inhibitory activities[J].Food &Function,2019,10(6): 3421-3429.DOI:10.1039/C9FO00680J.
[22]JIAO Kui,GAO Jie,ZHOU Tao,et al.Isolation and purification of a novel antimicrobial peptide from Porphyra yezoensis[J].Journal of Food Biochemistry,2019,43(7): e12864.DOI:10.1111/jfbc.12864.
[23]XIA E Q,ZHAI L,HUANG Z G,et al.Optimization and identification of antioxidant peptide from underutilized Dunaliella salina protein: extraction, in vitro gastrointestinal digestion,and fractionation[J].BioMed Research International,2019,2019: 642465.DOI:10.1155/2019/6424651.
[24]CHEN M F,ZHANG Y Y,HE M D,et al.Antioxidant peptide purified from enzymatic hydrolysates of Isochrysis zhanjiangensis and its protective effect against ethanol induced oxidative stress of HepG2 cells[J].Biotechnology and Bioprocess Engineering,2019,24: 308-317.DOI:10.1007/s12257-018-0391-5.
[25]CHEN J L,TAN L,LI C Y,et al.Mechanism analysis of a novel angiotensin-I-converting enzyme inhibitory peptide from Isochrysis zhanjiangensis microalgae for suppressing vascular injury in human umbilical vein endothelial cells[J].Journal of Agricultural and Food Chemistry,2020,68(15): 4411-4423.DOI:10.1021/acs.jafc.0c00925.
[26]CHENG S Z,TU M L,CHEN H,et al.Identification and inhibitory activity against α-thrombin of a novel anticoagulant peptide derived from oyster (Crassostrea gigas) protein[J].Food &Function,2018,9(12): 6391-6400.DOI:10.1039/c8fo01635f.
[27]QIAN Z J,ZHANG Y Y,OH G W,et al.Antioxidant and angiotensin I converting enzyme inhibition effects and antihypertensive effect in spontaneously hyertensive rats of peptide isolated from boiled abalone by-products, Hallotis discus hannai[J].Journal of Aquatic Food Product Technology,2018,27(9): 946-960.DOI:10.1080/10498850.
[28]OH R,LEE M J,KIM Y O,et al.Purification and characterization of an antimicrobial peptide mytichitin-chitin binding domain from the hard-shelled mussel,Mytilus coruscus[J].Fish &Shellfish Immunology,2018,83: 425-435.DOI:10.1016/j.fsi.2018.09.009.
[29]OH R,MIN J L,KIM Y O,et al.Myticusin-beta,antimicrobial peptide from the marine bivalve,Mytilus coruscus[J].Fish &Shellfish Immunology,2020,99: 342-352.DOI:10.1016/j.fsi.2020.02.020.
[30]JAYAPRAKASH R,PERERA C O.Partial purification and characterization of bioactive peptides from cooked New Zealand green-lipped mussel (Perna canaliculus) protein hydrolyzates[J].Foods,2020,9(7): 879.DOI:10.3390/foods9070879.
[31]YANG F M,QIN X M,ZHANG T,et al.Effect of oral administration of active peptides of Pinctada martensii on the repair of skin wounds[J].Marine Drugs,2019,17(12): 697.DOI:10.3390/md17120697.
[32]HARNEDY-ROTHWELL P A,MCLAUGHLIN C M,O’KEEFFE M B,et al.Identification and characterisation of peptides from a boarfish(Capros aper) protein hydrolysate displaying in vitro dipeptidyl peptidase-IV (DPP-IV) inhibitory and insulinotropic activity[J].Food Research International,2020,131: 108989.DOI:10.1016/j.foodres.2020.108989.
[33]ZHANG C Y,GAO S,ZHANG C,et al.Evaluating in vitro dipeptidyl peptidase IV inhibition by peptides from common carp (Cyprinus carpio) roe in cell culture models[J].European Food Research and Technology,2020,246(1): 179-191.DOI:10.1007/s00217-019-03399-6.
[34]KIM H S,JE J G,RYU B,et al.Antioxidant and angiotensin-I converting enzyme inhibitory peptides from Hippocampus abdominalis[J].European Food Research and Technology,2019,245:479-487.DOI:10.1007/s00217-018-3179-0.
[35]ZHANG Y Q,LIU H G,HONG H,et al.Purification and identification of dipeptidyl peptidase IV and angiotensin-converting enzyme inhibitory peptides from silver carp (Hypophthalmichthys molitrix)muscle hydrolysate[J].European Food Research and Technology,2019,245(1): 243-255.DOI:10.1007/s00217-018-3157-6.
[36]HE Y,PAN X,CHI C F,et al.Ten new pentapeptides from protein hydrolysate of miiuy croaker (Miichthys miiuy) muscle:preparation,identification,and antioxidant activity evaluation[J].LWT-Food Science and Technology,2019,105: 1-8.DOI:10.1016/j.lwt.2019.01.054.
[37]SUWAL S,KETNAWA S,LICEAGA A M,et al.Electro-membrane fractionation of antioxidant peptides from protein hydrolysates of rainbow trout (Oncorhynchus mykiss) byproducts[J].Innovative Food Science &Emerging Technologies,2018,45: 122-131.DOI:10.1016/j.ifset.2017.08.016.
[38]KETNAWA S,SUWAL S,HUANG J Y,et al.Selective separation and characterisation of dual ACE and DPP-IV inhibitory peptides from rainbow trout (Oncorhynchus mykiss) protein hydrolysates[J].International Journal of Food Science and Technology,2019,54(4):1062-1073.DOI:10.1111/ijfs.13939.
[39]LIN Y H,CHEN C A,TSAI J S,et al.Preparation and identification of novel antihypertensive peptides from the in vitro gastrointestinal digestion of marine cobia skin hydrolysates[J].Nutrients,2019,11(6):1351.DOI:10.3390/nu11061351.
[40]HARNEDY P A,PARTHSARATHY V,MCLAUGHLIN C M,et al.Atlantic salmon (Salmo salar) co-product-derived protein hydrolysates:a source of antidiabetic peptides[J].Food Research International,2018,106: 598-606.DOI:10.1016/j.foodres.2018.01.025.
[41]JIN R T,TENG X Y,SHANG J Q,et al.Identification of novel DPP-IV inhibitory peptides from Atlantic salmon (Salmo salar) skin[J].Food Research International,2020,133: 109161.DOI:10.1016/j.foodres.2020.109161.
[42]RIVERO-PINO F,ESPEJO-CARPIO F J,GUADIX E M.Production and identification of dipeptidyl peptidase IV (DPP-IV) inhibitory peptides from discarded Sardine pilchardus protein[J].Food Chemistry,2020,328: 127096.DOI:10.1016/j.foodchem.2020.127096.
[43]CAI P Y,ZHENG Y L,ZHOU Y F,et al.Research progress on the role of exosomes in obstructive sleep apnea-hypopnea syndromerelated atherosclerosis[J].Sleep Medicine Reviews,2022,66: 101696.DOI:10.1016/j.smrv.2022.101696.
[44]WOLF D,LEY K.Immunity and inflammation in atherosclerosis[J].Circulation Research,2019,124(2): 315-327.DOI:10.1161/CIRCRESAHA.118.313591.
[45]HETHERINGTON I,JAIN H T.Anti-atherosclerotic therapies:milestones,challenges,and emerging innovations[J].Molecular Therapy,2022,30(10): 3106-3117.DOI:10.1016/j.ymthe.2022.08.024.
[46]VO T S,KIM S K.Down-regulation of histamine-induced endothelial cell activation as potential anti-atherosclerotic activity of peptides from Spirulina maxima[J].European Journal of Pharmaceutical Sciences,2013,50(2): 198-207.DOI:10.1016/j.ejps.2013.07.001.
[47]SHIH M.F,CHEN L C,CHERNG J Y.Chlorella 11-peptide inhibits the production of macrophage-induced adhesion molecules and reduces endothelin-1 expression and endothelial permeability[J].Marine Drugs,2013,11(10): 3861-3874.DOI:10.3390/md11103861.
[48]FITZGERALD C,GALLAGHER E,O’CONNOR P,et al.Development of a seaweed derived platelet activating factor acetylhydrolase (PAF-AH) inhibitory hydrolysate,synthesis of inhibitory peptides and assessment of their toxicity using the Zebrafish larvae assay[J].Peptides,2013,50: 119-124.DOI:10.1016/j.peptides.2013.10.006.
[49]PINGAEW R,PRACHAYASITTIKUL V,WORACHARTCHEEWAN A,et al.Anticancer activity and QSAR study of sulfur-containing thiourea and sulfonamide derivatives[J].Heliyon,2022,8(8): e10067.DOI:10.1016/j.heliyon.2022.e10067.
[50]CHALAMAIAH M,YU W,WU J.Immunomodulatory and anticancer protein hydrolysates (peptides) from food proteins: a review[J].Food Chemistry,2018,245: 205-222.DOI:10.1016/j.foodchem.2017.10.087.
[51]SAADAOUI I,RASHEED R,ABDULRAHMAN N,et al.Algaederived bioactive compounds with anti-lung cancer potential[J].Marine drugs,2020,18(4): 197.DOI:10.3390/md18040197.
[52]HADIANAMREIA R,TOMEH M A,BROWN S,et al.Correlation between the secondary structure and surface activity of β-sheet forming cationic amphiphilic peptides and their anticancer activity[J].Colloids and Surfaces B: Biointerfaces,2022,209: 112165.DOI:10.1016/j.colsurfb.2021.112165.
[53]KARAMI Z,PEIGHAMBARDOUST S H,HESARI J,et al.Antioxidant,anticancer and ACE-inhibitory activities of bioactive peptides from wheat germ protein hydrolysates[J].Food Bioscience,2019,32: 100450.DOI:10.1016/j.fbio.2019.100450.
[54]AYISIGI E,BUDAK G,CELIKTAS M S,et al.Anticancer activities of bioactive peptides derived from rice husk both in free and encapsulated form in chitosan[J].Journal of Industrial and Engineering Chemistry,2021,103: 381-391.DOI:10.1016/j.jiec.2021.08.006.
[55]TAGHIZADEH M S,NIAZI A,MOGHADAM A,et al.Novel bioactive peptides of Achillea eriophora show anticancer and antioxidant activities[J].Bioorganic Chemistry,2021,110: 104777.DOI:10.1016/j.bioorg.2021.104777.
[56]JIMENEZ P C,WILKE D V,BRANCO P C,et al.Enriching cancer pharmacology with drugs of marine origin[J].British Journal of Pharmacology,2019,177(1): 3-27.DOI:10.1111/bph.14876.
[57]SAFAVI-HEMAMI H,BROGAN S E,OLIVERA B M.Pain therapeutics from cone snail venoms: from ziconotide to novel non-opioid pathways[J].Journal of Proteomics,2019,190: 12-20.DOI:10.1016/j.jprot.2018.05.009.
[58]WANG H Y,XU B,DOU K F.Clopidogrel monotherapy versus aspirin monotherapy for chronic maintenance beyond 12 months after PCI among patients with high risk of ischemic or bleeding events[J].Journal of the Society for Cardiovascular Angiography &Interventions,2022,1(3): 100325.DOI:10.1016/j.jscai.2022.100325.
[59]INDUMATHI P,MEHTA A.A novel anticoagulant peptide from the nori hydrolysate[J].Journal of Functional Foods,2016,20: 606-617.DOI:10.1016/j.jff.2015.11.016.
[60]JUNG W K,KIM S K.Isolation and characterisation of an anticoagulant oligopeptide from blue mussel,Mytilus edulis[J].Food Chemistry,2009,117(4): 687-692.DOI:10.1016/j.foodchem.2009.04.077.
[61]SUBBARAO S A.Cancer vs.SARS-CoV-2 induced inflammation,overlapping functions,and pharmacological targeting[J].Inflammopharmacology,2021,29(2): 343-366.DOI:10.1007/S10787-021-00796-W.
[62]CHEN L L,DENG H D,CUI H M,et al.Inflammatory responses and inflammation-associated diseases in organs[J].Oncotarget,2018,9(6):7204.DOI:10.18632/ONCOTARGET.23208.
[63]LEE S J,KIM,E K,KIM Y S,et al.Purification and characterization of a nitric oxide inhibitory peptide from Ruditapes philippinarum[J].Food and Chemical Toxicology,2012,50(5): 1660-1666.DOI:10.1016/j.fct.2012.02.021.
[64]KIM E K,OH H J,KIM Y S,et al.Purification of a novel peptide derived from Mytilus coruscus and in vitro/in vivo evaluation of its bioactive properties[J].Fish &Shellfish Immunology,2013,34(5):1078-1084.DOI:10.1016/j.fsi.2013.01.013.
[65]HWANG J W,LEE S J,KIM Y S,et al.Purification and characterization of a novel peptide with inhibitory effects on colitis induced mice by dextran sulfate sodium from enzymatic hydrolysates of Crassostrea gigas[J].Fish &Shellfish Immunology,2012,33(4):993-999.DOI:10.1016/j.fsi.2012.08.017.
[66]AHN C B,CHO Y S,JE J Y.Purification and anti-inflammatory action of tripeptide from salmon pectoral fin byproduct protein hydrolysate[J].Food Chemistry,2015,168: 151-156.DOI:10.1016/j.foodchem.2014.05.112.
[67]NGUYEN T M N,LOMUNOVA M,VU T P D,et al.Antiallergic effects of the ethanol extract of Syzygium formosum(Wall.) Masam leaves and its immunoregulatory mechanisms[J].Journal of Ethnopharmacology,2018,211: 171-179.DOI:10.1016/j.jep.2017.09.026.
[68]KO S C,LEE D S,PARK W S,et al.Anti-allergic effects of a nonameric peptide isolated from the intestine gastrointestinal digests of abalone (Haliotis discus hannai) in activated HMC-1 human mast cells[J].International Journal of Molecular Medicine,2016,37(1):243-250.DOI:10.3892/ijmm.2015.2420.
[69]CHEUNG R C F,NG T B,WONG J H.Marine peptides: bioactivities and applications[J].Marine Drugs,2015,13(7): 4006-4043.DOI:10.3390/md13074006.
[70]CAO D,LV X,XU X,et al.Purification and identification of a novel ACE inhibitory peptide from marine alga Gracilariopsis lemaneiformis protein hydrolysate[J].European Food Research and Technology,2017,243(10): 1829-1837.DOI:10.1007/s00217-017-2886-2.
[71]NEVES A C,HARNEDY P A,FITZGERALD R J.Angiotensin converting enzyme and dipeptidyl peptidase-IV inhibitory,and antioxidant activities of a blue mussel (Mytilus edulis) meat protein extract and its hydrolysates[J].Journal of Aquatic Food Product Technology,2016,25(8): 1221-1233.DOI:10.1080/10498850.2015.1051259.
[72]SEMREEN M H,EL-GAMAL M I,ABDIN S,et al.Recent updates of marine antimicrobial peptides[J].Saudi Pharmaceutical Journal,2018,26(3): 396-409.DOI:10.1016/j.jsps.2018.01.001.
[73]ANBUCHEZIAN R,RAVICHANDRAN S,RAJAN D K,et al.Identification and functional characterization of antimicrobial peptide from the marine crab Dromia dehaani[J].Microbial Pathogenesis,2018,125: 60-65.DOI:10.1016/j.micpath.2018.08.056.
[74]TEIXEIRA V,FEIO M J,BASTOS M.Role of lipids in the interaction of antimicrobial peptides with membranes[J].Progress in Lipid Research,2012,51(2): 149-177.DOI:10.1016/j.plipres.2011.12.005.
[75]THAKUR A,SHARMA A,ALAJANGI H K,et al.In pursuit of next-generation therapeutics: antimicrobial peptides against superbugs,their sources,mechanism of action,nanotechnologybased delivery,and clinical applications[J].International Journal of Biological Macromolecules,2022,218: 135-156.DOI:10.1016/j.ijbiomac.2022.07.103.
[76]GUZMÁN F,WONG G,ROMAN T,et al.Identification of antimicrobial peptides from the microalgae Tetraselmis suecica (kylin)butcher and bactericidal activity improvement[J].Marine Drugs,2019,17(8): 453.DOI:10.3390/md17080453.
[77]ZHANG X Q,CAO D Q,SUN X,et al.Preparation and identification of antioxidant peptides from protein hydrolysate of marine alga Gracilariopsis lemaneiformis[J].Journal of Applied Phycology,2019,31(4): 2585-2596.DOI:10.1007/s10811-019-1746-9.
[78]VEGA J,ÁLVAREZ-GÓMEZ F,GÜENAGA L,et al.Antioxidant activity of extracts from marine macroalgae,wild-collected and cultivated,in an integrated multi-trophic aquaculture system[J].Aquaculture,2020,522: 735088.DOI:10.1016/j.aquaculture.2020.735088.
[79]LEE Y,FENG C,PENG M,et al.Antiosteoporosis effects of a marine antimicrobial peptide pardaxin via regulation of the osteogenesis pathway[J].Peptides,2022,148: 170686.DOI:10.1016/j.peptides.2021.170686.
[80]ATEF M,OJAGH S M.Health benefits and food applications of bioactive compounds from fish byproducts: a review[J].Journal of Functional Foods,2017,35: 673-681.DOI:10.1016/j.jff.2017.06.034.
[81]TAHERI A,FARVIN K H S,JACOBSEN C,et al.Antioxidant activities and functional properties of protein and peptide fractions isolated from salted herring brine[J].Food Chemistry,2014,142: 318-326.DOI:10.1016/j.foodchem.2013.06.113.
[82]HALIM N R A,YUSOF H M,SARBON N M.Functional and bioactive properties of fish protein hydolysates and peptides: a comprehensive review[J].Trends in Food Science &Technology,2016,51: 24-33.DOI:10.1016/j.tifs.2016.02.007.
[83]MBATIA B,OGONDA L A,MUGE E K,et al.Antioxidative and functional properties of Rastrineobola argentea (Dagaa) fish protein hydrolysate[J].Discourse Journal of Agriculture and Food Sciences,2014,2(6): 180-189.
[84]GÓMEZ-ESTACA J,LÓPEZ-DE-DICASTILLO C,HERNÁNDEZMUÑOZ P,et al.Advances in antioxidant active food packaging[J].Trends in Food Science&Technology,2014,35(1): 42-51.DOI:10.1016/j.tifs.2013.10.008.
[85]WANG L,JIANG Y,WANG X X,et al.Effect of oral administration of collagen hydrolysates from Nile tilapia on the chronologically aged skin[J].Journal of Functional Foods,2018,44: 112-117.DOI:10.1016/j.jff.2018.03.005.

