大部分新鲜肌肉中水分活度在0.98以上[1],且含有脂肪、蛋白质、碳水化合物等丰富的营养成分,很容易受到微生物污染而发生腐败变质。在这一过程中,肉的营养成分和感官性状发生变化,不仅会造成产品腐败、货架期缩短,甚至会严重威胁人体健康。在我国肉类食品生产供应链中,12%以上的损失和浪费是由腐败变质造成的[2],如何有效控制肉与肉制品中微生物的生长、延长货架期和提高贮存品质,已成为肉类行业和学术界的共同目标之一。食品防腐剂能够延缓微生物生长或抑制化学变化引起的食品腐败,但出于对健康的考虑,人们更期望使用天然物质来代替人工合成防腐剂。
天然酚类化合物是从植物中提取的次生代谢产物,具有抗氧化性和抗菌活性,能够有效控制肉类氧化和腐败[3]。同时部分酚类化合物已列入GB 2760ü2019《食品安全国家标准 食品添加剂使用标准》(以下简称GB 2760),可作为肉类工业中化学防腐剂的替代物。本文从天然酚类化合物自身的抑菌活性出发,总结其分类、生物活性及影响其抗菌活性的因素,并着重对天然酚类化合物抑菌机制进行系统概述,以期为研究天然酚类化合物的抑菌机理以及天然酚类化合物在肉制品加工中的应用提供理论参考。
1 肉的腐败
健康动物的肌肉通常是无菌的,肉类腐败一般由屠宰、加工、运输过程中微生物的污染和内源酶共同作用所致[4]。导致肉类制品腐败的微生物种类繁多、来源广泛,包括假单胞菌属(Pseudomonas)、希瓦氏菌属(Shewanella)、不动杆菌属(Acinetobacter)等革兰氏阴性菌及乳酸杆菌属(Lactobacillus)、明串珠菌属(Leuconstoc)、环丝菌属(Brochothrix)等革兰氏阳性菌[5]。在肉品腐败初期,这些腐败微生物分解葡萄糖等低分子质量物质为各种有机酸、醇和CO2气体;当肉中葡萄糖不能满足微生物的生长需求时,它们就开始降解氨基酸,并产生带有恶臭味的副产物;同时,腐败微生物分泌的蛋白酶和脂肪酶分解肉中的蛋白质和脂肪,产生胺硫化氢、粪臭素、脂肪酸、醛、酮等物质[6]。上述变化不仅破坏了肉与肉制品的营养成分,使肉的颜色、弹性、气味等发生严重劣变,还可能形成肉毒杆菌毒素等有毒代谢产物从而引起食物中毒[7]。酚类化合物或富含酚类物质的植物提取物已被公认为具有良好的抗菌活性,能够抑制存在于肉及肉制品中的金黄色葡萄球菌、大肠杆菌、乳酸菌等致病和腐败微生物的生长,有效延长货架期和提高产品品质[8]。
2 酚类化合物及抗菌活性
2.1 酚类化合物的合成及分类
天然酚类化合物是植物组织的次生代谢产物,广泛存在于植物的茎、果实、叶、花等部位[3],虽然属于非营养部分,但其能在食品工业中发挥抑菌、抗氧化等作用。影响植物代谢酚类化合物的因素有很多,除植物种类、生长发育阶段、组织部位和植物酚类物质的含量、种类外,紫外线是影响植物种酚类化合物合成最关键的因素[9]。紫外线辐射暴露会对植物蛋白质结构以及DNA造成损伤,引起内源性酚类物质在植物细胞中的积累,进而通过形成屏蔽以及修复损伤来保护细胞成分[10]。酚类化合物通常通过溶剂提取法、超声波辅助提取法、微波辅助提取法等方法进行提取,通过柱层析法、色谱法、膜分离法、萃取分离法等方法进行分离纯化,通过福林-酚比色法、高效液相色谱法、红外吸收光谱法、超高效液相色谱-串联质谱联用法等进行鉴定[11]。
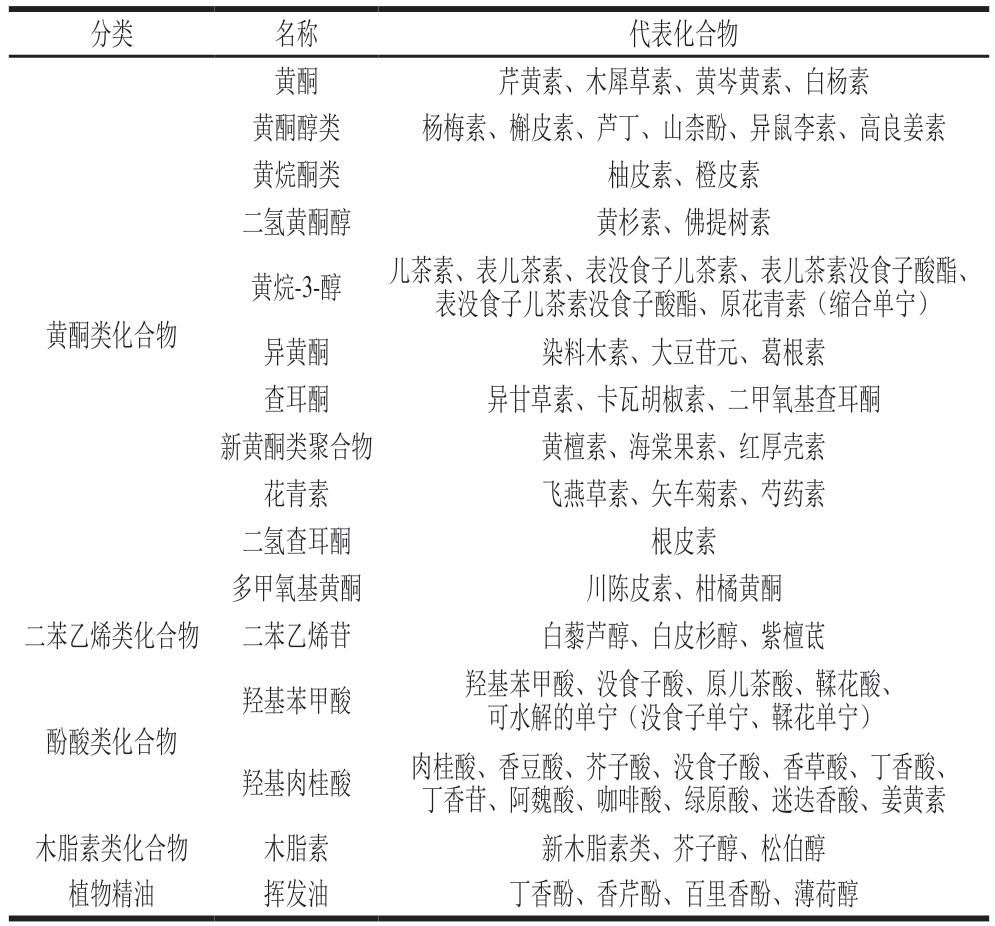
酚类化合物的种类复杂,由至少一个芳香环与羟基取代基连接,可以根据化合物分子结构和苯酚亚基数量对其进行区分。根据化合物分子结构差异可以将酚类化合物分为4 个大类:酚酸类、黄酮类、二苯乙烯类和木脂素类[8];根据苯酚亚基的数量将酚类化合物分为简单酚和多酚:酚酸类物质属于简单酚,黄酮类、二苯乙烯类、木脂素类化合物属于多酚类物质。此外,植物精油中也含有部分酚类化合物如丁香酚、香芹酚、百里香酚和薄荷醇[12]。表1总结了酚类化合物的分类及代表化合物。
表1 酚类化合物的分类及代表物
Table 1 Classification and representatives of phenolic compounds
分类 名称 代表化合物黄酮 芹黄素、木犀草素、黄岑黄素、白杨素黄酮醇类 杨梅素、槲皮素、芦丁、山柰酚、异鼠李素、高良姜素黄烷酮类 柚皮素、橙皮素二氢黄酮醇 黄杉素、佛提树素黄烷-3-醇 儿茶素、表儿茶素、表没食子儿茶素、表儿茶素没食子酸酯、表没食子儿茶素没食子酸酯、原花青素(缩合单宁)异黄酮 染料木素、大豆苷元、葛根素查耳酮 异甘草素、卡瓦胡椒素、二甲氧基查耳酮新黄酮类聚合物 黄檀素、海棠果素、红厚壳素花青素 飞燕草素、矢车菊素、芍药素二氢查耳酮 根皮素多甲氧基黄酮 川陈皮素、柑橘黄酮二苯乙烯类化合物 二苯乙烯苷 白藜芦醇、白皮杉醇、紫檀茋黄酮类化合物羟基肉桂酸 肉桂酸、香豆酸、芥子酸、没食子酸、香草酸、丁香酸、丁香苷、阿魏酸、咖啡酸、绿原酸、迷迭香酸、姜黄素木脂素类化合物 木脂素 新木脂素类、芥子醇、松伯醇植物精油 挥发油 丁香酚、香芹酚、百里香酚、薄荷醇酚酸类化合物羟基苯甲酸 羟基苯甲酸、没食子酸、原儿茶酸、鞣花酸、可水解的单宁(没食子单宁、鞣花单宁)
2.2 影响酚类化合物抗菌活性的因素
影响酚类化合物抗菌活性的因素有很多,除了浓度、外界环境、植物的提取部位和提取方式等因素外,分子结构(尤其是与芳香环相连羟基的位置和数量)、分子极性以及酚类化合物之间的协同和拮抗现象都会对酚类化合物的抑菌活性产生影响[13]。
2.2.1 酚类化合物羟基位置和数量
如表2所示,酚羟基对酚类化合物的抗菌活性至关重要,它们可以通过氢键与细胞膜发生相互作用,破坏膜结构,导致细胞成分泄漏;同时羟基可以促进电子的离域效应,使细胞跨膜pH值梯度和ATP池的能量水平降低,最终导致细胞死亡[14]。酚羟基的数量会影响酚类化合物抗菌活性的强度。Stojkovic等[13]探究了咖啡酸、对香豆酸和芦丁的抗菌作用,结果显示,3 种酚类化合物中咖啡酸对金黄色葡萄球菌(Staphylococcus aureus)的抑制效果最好,其原因可能是咖啡酸芳香环上具有一个额外的羟基基团。同时,芳香环上羟基的位置也会影响酚类化合物的抗菌效果。百里香酚和香芹酚是同分异构体,其差别是酚羟基在苯环上的位置不同。Gyawali等[15]对比分析了百里香酚和香芹酚的抗菌活性,发现百里香酚和香芹酚的抑菌效果具有一定差异;吴克刚等[16]的研究也表明香芹酚对大肠杆菌(Escherichia coli)的抗菌能力高于百里香酚。
表2 影响酚类化合物抗菌活性的因素及抑菌机制
Table 2 Factors affecting antibacterial activity of phenolic compounds and their action mechanisms

因素 抑菌机制酚羟基位置及数量1)通过酚羟基中氢键与细胞膜发生相互作用,破坏膜结构2)促进电子的离域,使细胞跨膜pH值梯度和ATP池的能量水平降低酚类化合物的疏水性1)通过疏水性作用与微生物细胞膜磷脂双分子层结合,破坏细胞膜结构2)通过疏水性嵌入磷脂双分子层后破坏酶的活性3)疏水性增加提高酚类化合物在脂肪中积累,提高抗菌能力酚类化合物的协同作用1)与抗生素发挥协同作用时,酚类化合物通过破坏微生物的细胞壁和细胞膜使抗生素更快进入细胞2)多种酚类化合物联合使用发挥抑菌协同作用的具体机制仍需进一步研究
2.2.2 酚类化合物的疏水性
酚类化合物的抗菌活性随着疏水性的增加而有一定提升,这可能和疏水性酚类化合物与细胞膜的相互作用有关[17]。疏水性酚类化合物可以与微生物细胞膜磷脂双分子层结合,破坏细胞膜结构;同时酚类化合物嵌入磷脂双分子层后还可能导致蛋白质(如Na+/K+-ATP酶泵)功能失调和细胞膜孔隙生成[17-18]。Hashimoto等[19]发现表儿茶素没食子酸酯和表没食子儿茶素没食子酸酯可以增强儿茶素对膜结构的扰动性,并认为儿茶素中没食子酰基对细胞膜磷脂双分子层的高亲和力增强了酚类化合物的抗菌活性;同时酚类化合物的疏水性有利于提高其在脂肪中的积累,从而增强酚类化合物在肉类制品中的抗菌活性。
2.2.3 酚类化合物间的协同作用
有研究表明,当多种酚类化合物联合使用或植物提取物中含有两种及以上的酚类化合物时,其抑菌作用比单一化合物效果更好[20]。王帆等[21]通过实验探究了肉桂醛、单宁酸、丁香酚、麝香草酚对5 种微生物(金黄色葡萄球菌、铜绿假单胞菌、大肠杆菌、肠炎沙门氏菌、单核细胞增生李斯特菌(以下简称单增李斯特菌)的协同抑制作用,结果显示肉桂醛、单宁酸、丁香酚麝香草酚两两复配后各组分的最小抑菌浓度都有所降低;葡萄中含有丰富的酚类化合物,如原花青素、没食子酸、白黎芦醇、儿茶素、单宁等,Serra等[22]发现,20 mg/L的槲皮素与葡萄提取物混合物对蜡样芽孢杆菌的抑制作用比同等质量浓度的纯槲皮素更有效,并指出其原因可能是葡萄提取物中其他活性物质与槲皮素发生了积极的协同作用,从而产生了较强的抗菌活性。目前,酚类化合物的协同作用更多是与抗生素联合使用,酚类化合物通过破坏微生物的细胞壁和细胞膜使抗生素更快进入细胞,从而加快抑菌进程[23]。但有关多种酚类化合物联合使用增强抑菌效果的研究相对较少,需要大量实验验证其协同作用效果及机制。研究酚类化合物的协同、拮抗关系,获得有效的植物多酚复配物,也有利于更好地发挥天然酚类化合物的生物活性。
3 酚类化合物的抑菌机理
酚类化合物发挥抗菌作用的机制主要包括以下5 个方面:1)与细胞壁相互作用,导致细胞壁的破坏和细胞内容物的释放;2)干扰细胞膜的功能,影响细胞膜的流动性和稳定性;3)影响细菌生物膜的合成;4)抑制蛋白质、核酸的合成;5)螯合金属离子[24]。然而目前酚类化合物抗菌活性的确切分子机制尚不完全明确,不同酚类化合物或抑菌活性分子也会发挥协同或拮抗作用,这意味着酚类化合物会同时以多种方式影响微生物。图1总结了目前已知酚类化合物的主要抑菌机制。
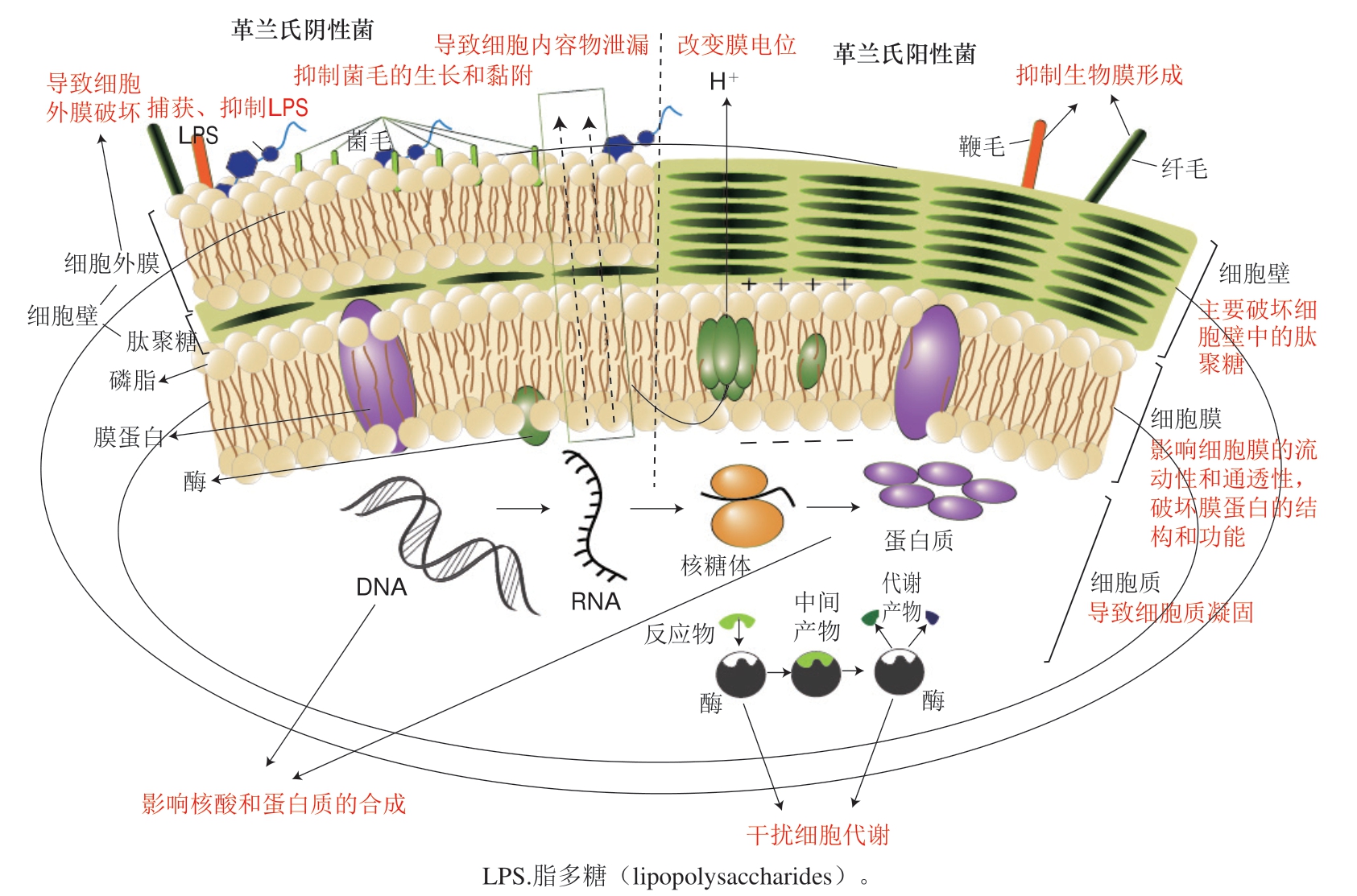
图1 酚类化合物抑制微生物的机制示意图
Fig. 1 Schematic diagram of the mechanism by which phenolic compounds inhibit microorganisms
3.1 酚类化合物通过影响细胞壁抑制微生物
细胞壁能够保护细胞免受渗透压变化的破坏,细胞壁的损伤会降低细胞对高离子强度和低渗透压的耐受性。酚类化合物能够通过影响细胞壁起到抑菌作用,且革兰氏阳性菌和革兰氏阴性菌对酚类化合物的敏感性不同[25]。
3.1.1 酚类化合物直接与肽聚糖连接抑制微生物
肽聚糖是细菌细胞壁的必需结构,也是抑菌剂的重点攻击对象。酚类化合物可以通过与细胞壁中肽聚糖连接来破坏细胞壁结构,进而导致细菌死亡[24]。如图1所示,革兰氏阳性菌和革兰氏阴性菌的细胞壁结构不同。革兰氏阴性菌的细胞壁由一层较薄的肽聚糖和外膜组成,外膜的存在可以阻碍多酚与肽聚糖连接[26],而革兰氏阳性菌的细胞壁中没有外膜,因此更易受到酚类物质的攻击[27]。Yoda等[28]研究了没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)对多种葡萄球菌(革兰氏阳性菌)和革兰氏阴性菌的抑制效果,结果显示EGCG对革兰氏阳性菌的最小抑菌质量浓度(50~100 µg/mL)显著低于对革兰氏阴性菌的最小抑菌质量浓度(800 µg/mL);在培养基中加入肽聚糖后可以阻断EGCG对金黄色葡萄球菌的抑菌作用,这说明EGCG可以直接与革兰氏阳性菌细胞壁中的肽聚糖结合而破坏细胞壁。
3.1.2 酚类化合物通过使革兰氏阴性菌细胞壁的外膜解体抑制微生物
如图1所示,革兰氏阴性菌细胞壁的外膜由磷脂双分子层和蛋白质组成,其外层小叶上含有LPS,外膜的存在一定程度上可以降低抑菌物质对微生物的影响。有研究发现链霉素类抗生素与没食子酸、阿魏酸、绿原酸混合使用时对革兰氏阴性菌具有更好的抑制效果,这种协同作用可能是由于羟基肉桂酸及其衍生物破坏了微生物外膜,使抗生素能够更快进入细胞内部,提高其抑菌效果[29]。
LPS是革兰氏阴性菌细胞壁中的一种特有成分,当细菌死亡溶解或细胞结构被破坏时才会释放出来,由于其对宿主细胞具有毒性作用,也被称为内毒素[30]。LPS的存在有利于维持细菌细胞壁或细胞外膜结构的稳定性,避免其结构改变导致细菌死亡,并保护细菌免受亲脂类抗生素的破坏[31]。Nohynek等[32]发现含有山柰酚、香草酸等酚类化合物的云莓和覆盆子提取物可以使沙门氏菌的外膜解体,并指出这一现象是酚类化合物通过释放LPS、螯合外膜上的二价阳离子或以稳定阳离子的方式插入外膜而导致,外膜结构破坏后,革兰氏阴性菌的肽聚糖层暴露出来,使革兰氏阴性菌对抗菌物质的敏感性升高。LPS由3 个部分组成,由内到外分别是类脂A、核心多糖和O-抗原,其中类脂A是脂多糖的毒性部分及主要成分,可以单独体现其生理作用。Delehanty等[33]发现,原花青素能够捕获并中和细菌LPS,抑制LPS与哺乳动物细胞表面结合;还有研究证实,原花青素捕获细菌LPS是酚类物质与类脂A结合所致[34]。综上,酚类化合物能够捕获细菌LPS,破坏细胞壁外膜导致微生物死亡。
3.1.3 酚类物质通过抑制菌毛的生长和黏附抑制微生物
在很多革兰氏阴性菌及少数革兰氏阳性菌的细胞表面存在着一些细短而直硬的丝状物,称为菌毛(图1)。菌毛可以和细胞膜上的特异性受体结合,使细菌紧密地黏附在宿主组织上。Hisano等[35]发现,多酚类物质尤其是原花青素,可以抑制菌毛与细胞特异性受体结合,并提出两种通过菌毛抑制微生物的机制:1)原花青素作为受体类似物,与细胞特异性受体竞争,减少了菌毛与宿主组织的黏附结合;2)影响菌毛的长度和密度,降低细菌的黏附能力。
3.2 酚类化合物通过影响细胞膜抑制微生物
细胞膜主要由磷脂双分子层和镶嵌在其中的蛋白质分子构成,其渗透性屏障作用对于保证细胞的正常生命活动具有重要意义。酚类化合物通过对细胞膜中磷脂双分子层和蛋白质作用,使细胞膜的流动性和渗透性发生改变;许多酚类化合物的抗菌活性随着亲脂性的提高而增加,亲脂性的提高会使酚类化合物更易与细胞膜磷脂双分子层结合,导致细胞膜发生不可逆损伤,影响细胞膜和胞内物质的正常生理活性。
3.2.1 酚类化合物通过影响细胞膜磷脂双分子层抑制微生物
酚类化合物尤其是疏水性多酚可以和磷脂双分子层结合,影响细胞膜中不饱和脂肪酸的比例并导致细胞膜的结构破坏和功能性丧失。当作用在微生物上的酚类化合物达到最小抑菌浓度时,细菌细胞膜的组成成分会发生一定变化,包括细胞膜不饱和脂肪酸比例上升、细胞膜流动性增加;当疏水性物质进入细胞膜后会引起细胞膜渗透性改变,细胞内容物泄漏出来,最终导致细菌死亡(图1)。黄酮类化合物可以与磷脂双分子层相互作用而显著降低细胞膜的流动性:黄酮类化合物分子中含有多个酚羟基,酚羟基可以与磷脂分子的磷酸基团、羰基相互作用形成氢键,氢键限制了分子的自由运动,从而导致膜的胶态化[36-37]。Yi Shumin等[38]使用透射电子显微镜研究茶多酚的抗菌作用,结果发现经茶多酚处理后,细菌的细胞膜发生一定损伤,导致外膜和内膜通透性的增加和胞内小分子的释放。Borges等[23]研究了没食子酸和阿魏酸对大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌和单增李斯特菌细胞膜的作用,发现没食子酸和阿魏酸使细胞膜的疏水性发生改变,导致细胞膜表面负电荷减少、细胞膜局部破裂、膜孔洞形成、细胞内成分泄漏,最终使细胞发生不可逆变化,导致细胞死亡。
3.2.2 酚类化合物通过影响细胞膜蛋白抑制微生物
如图1所示,疏水性酚类化合物嵌入细菌磷脂双分子层后与蛋白质结合,不仅导致细菌细胞膜的破坏、细胞膜化学渗透控制的丧失,还会影响膜蛋白的正常表达[3]。Yi Shumin等[39]研究了茶多酚处理铜绿假单胞菌前后细胞膜蛋白的差异,在处理组和对照组中共观察到27 个差异表达蛋白,其中大部分是参与细胞代谢过程如三羧酸循环、脂肪酸生物合成、蛋白质生物合成、甘氨酸代谢、DNA代谢的酶。Ulrey等[40]研究发现,使用蔓越莓原花青素处理铜绿假单胞菌后,其细胞膜中参与阳离子转运的蛋白质、铁载体和应激激活蛋白表达上调,而ATP合酶、细胞色素c、参与DNA和RNA合成等蛋白质的表达下调。这些蛋白表达变化使细胞代谢发生紊乱,进而导致细胞死亡。
3.3 酚类化合物通过抑制生物膜的形成抑制微生物
生物膜是一种或多种细菌不可逆地附着在接触表面形成的具有三维结构的微生物菌落,是微生物抵抗外界不良环境的一种生长方式,假单胞菌属、梭状芽孢杆菌属、乳杆菌属、沙门氏菌属、单增李斯特菌和大肠杆菌等肉制品中常见的微生物会附着在肉类接触面形成生物膜,危胁屠宰和肉类加工过程中的食品安全[41]。有研究表明,高浓度的酚类化合物可通过影响群体感应机制、细菌集群运动或改变生物膜结构影响生物膜的形成[3-42]。Borges等[43]探究了没食子酸和阿魏酸对大肠杆菌、金黄色葡萄球菌、单增李斯特菌运动和黏附作用的影响,结果表明这两种酚酸均能抑制细菌的运动和黏附能力,并对生物膜的形成产生抑制作用。群体感应是细菌通过释放自诱导信号分子在种内或种间进行信息交流的信号传导机制,在生物膜形成中发挥着重要作用[44]。有研究报道酚类化合物姜黄素能够抑制群体感应介导的微生物生物膜形成;还有学者建议将具有抗群体感应和抑制生物膜活性的天然分子和提取物应用于新的食品安全控制体系中[45-46]。
不同浓度的酚类化合物对生物膜的影响不同,较高浓度的酚类化合物对生物膜的形成具有抑制作用,而较低浓度时可能会促进生物膜的形成。Plyuta等[47]研究发现4-羟基苯甲酸、香草醛、没食子酸、阿魏酸、芥子酸、肉桂酸和绿原酸的存在可以使铜绿假单胞菌生物膜形成增加,其中香草醛和表儿茶素(750 μg/mL)对生物膜的影响最大,可使生物膜的形成量增加5~7 倍,4-羟基苯甲酸、没食子酸和肉桂酚酸(25~100 μg/mL)、芥子酸(200~400 μg/mL)、阿魏酸(400 μg/mL)、绿原酸(100~400 μg/mL)可使生物膜的形成量增加2~3 倍;而酚类化合物到达一定质量浓度后(香草醛(1 500 μg/mL)、表儿茶素(3 000 μg/mL)、芥子酸(800 μg/mL)、绿原酸(800 μg/mL)、阿魏酸(400 μg/mL)、肉桂酚酸(200 μg/mL)、4-羟基苯甲酸(200 μg/mL)、没食子酸(100 μg/mL))会抑制生物膜的形成。
3.4 酚类化合物通过影响细胞内蛋白质、核酸的生物合成抑制微生物
蛋白质和核酸是微生物生命活动的重要物质基础,对微生物的呼吸代谢和生长繁殖起重要作用。影响蛋白质的合成是酚类化合物主要的抑菌机制之一,除了与细胞膜蛋白结合影响其正常表达外,酚类化合物还能够通过细胞膜进入细胞内部,抑制细胞蛋白酶的活性,甚至影响胞内蛋白质的合成。
茶多酚可以使大肠杆菌细胞内蛋白质合成发生显著变化,其中热休克蛋白(heat shock protein,HSP)和参与细胞防御的8 种蛋白质表达上调,参与大肠杆菌细胞内能量代谢和氨基酸生物合成有关的蛋白质表达下调[48]。ATP合酶是微生物细胞产生能量的关键酶,可以在跨膜质子动力的推动下合成ATP,维持细胞正常的能量供应,而白藜芦醇、白皮杉醇、槲皮素等酚类化合物可以通过影响大肠杆菌ATP合酶的活性降低能量供应,其中白藜芦醇能够完全抑制大肠杆菌ATP合酶的合成[49](图2)。酚类化合物还可以通过影响依赖于NADPH的3-酮脂酰ACP还原酶(FabG)和依赖于NADH的烯脂酰-ACP还原酶(FabI)抑制脂肪酸的伸长。Zhang Yimin等[50]研究表明,EGCG和相关植物多酚能够有效抑制参与II型脂肪酸链延伸循环的FabG和FabI两种还原酶活性,从而抑制细胞脂肪酸的合成(图3)。
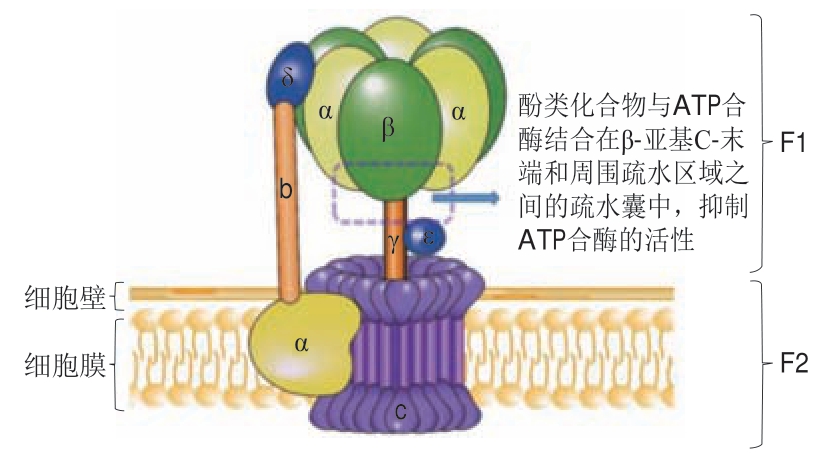
图2 大肠杆菌ATP合酶结构[51]
Fig. 2 Structure of Escherichia coli ATP synthase[51]
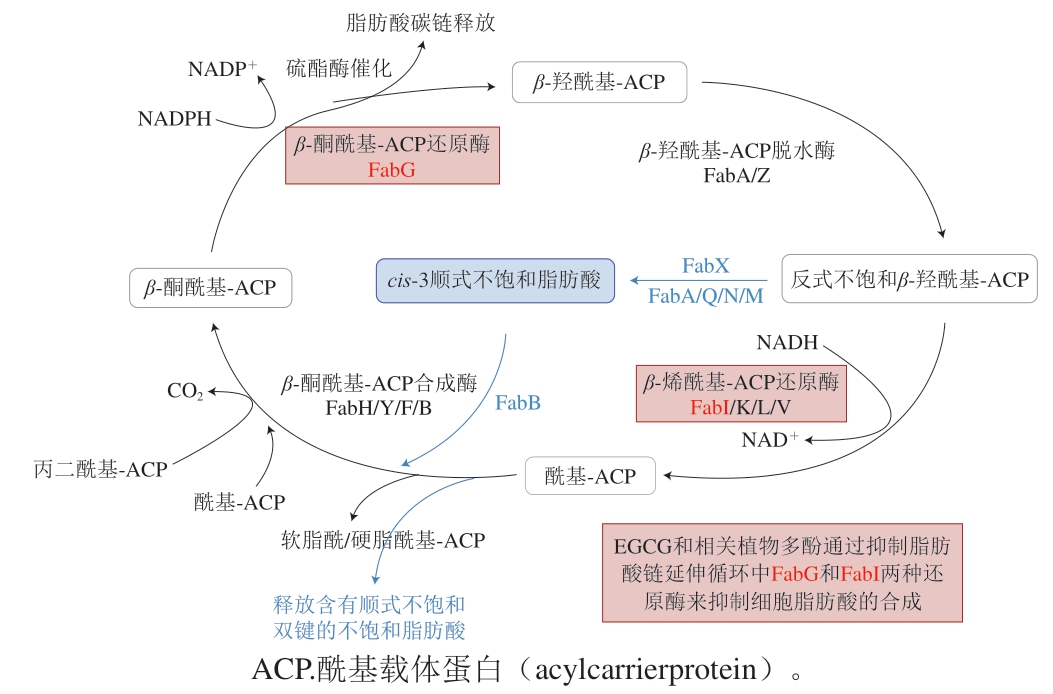
图3 II型脂肪酸生物合成途径碳链延长阶段示意图[52]
Fig. 3 Schematic diagram of the carbon chain elongation stage of type-Ⅱfatty acid biosynthesis pathway[52]
DNA是微生物细胞遗传和细胞物质合成中重要的遗传信息载体,DNA的损伤会影响微生物遗传物质的正常复制和生长繁殖[53]。DNA拓扑异构酶参与DNA复制、转录和重组,许多抗菌药物的作用都与DNA拓扑异构酶有关,有研究显示酚类化合物可以通过抑制拓扑异构酶中的DNA旋转酶活性来控制DNA合成[37]。DNA旋转酶由两个A亚基和两个B亚基组成,A亚基催化DNA断裂,B亚基催化ATP水解,酚类化合物能够通过与B亚基(ATP结合位点)结合来抑制酶的活性[54]。Wu Ting等[55]研究发现,黄酮类化合物具有抑制大肠杆菌DNA旋转酶活性的能力;Haraguchi等[56]通过研究也推测黄酮类化合物可能通过抑制能量代谢和DNA合成抑制微生物,并在一定程度上影响蛋白质和RNA的合成。此外,酚类化合物进入细胞后可以与DNA等细胞内成分相互作用,使细胞功能受到抑制;细胞膜的破坏也会导致自由基的释放,进而导致DNA损伤和脂质氧化。
3.5 酚类化合物通过螯合金属离子抑制微生物生长
铁是绝大多腐败菌和食源性微生物生长的基本元素。肉中的血红素蛋白(肌红蛋白、血红蛋白等)和非血红素蛋白(转铁蛋白、铁蛋白等)为细菌提供了丰富的铁源,更有利于细菌在肉类制品中生长繁殖,因此控制肉中有效铁离子的浓度可以抑制微生物的生长[57-58]。Engels等[59]在芒果中提取到的3 种水解单宁能够对革兰氏阳性食品腐败菌和大肠杆菌产生抑菌作用,而在培养基中加入铁元素后细菌恢复生长,因此认为单宁的抗菌活性与其螯合铁离子的能力有关。
4 酚类化合物在肉类中的应用
目前,酚类化合物在肉与肉制品生产中常见的使用方式有3 类:直接添加在肉类制品中、添加在动物日粮中和与活性包装结合使用。下面对肉与肉制品中应用的植物多酚种类、有效成分、使用的肉制品产品进行介绍,并从微生物和食用品质方面明确其应用效果。
4.1 酚类化合物在肉制品中的应用
迄今为止,GB 2760已批准了部分酚类化合物(如丁香酚、百里香酚、单宁酸等)、含有酚类物质的植物提取物(迷迭香提取物、柠檬提取物、芹菜籽提取物等)或天然植物精油(生姜油、百里香油、肉桂皮油等)作为抗氧化剂和防腐剂直接添加在肉类制品中。添加方式主要有以下3 种:1)以粉末、汁液或精油的方式混合到肉糜中;2)配制一定浓度的溶液或腌料均匀喷洒或涂抹、或浸渍到肉类产品表面;3)利用注射器将溶液注射进大块肉内部[57]。表3展示了一些酚类化合物在肉制品中应用的研究及其效果。
表3 酚类化合物直接添加在肉制品中的应用
Table 3 Application of phenolic compounds directly for addition to meat products
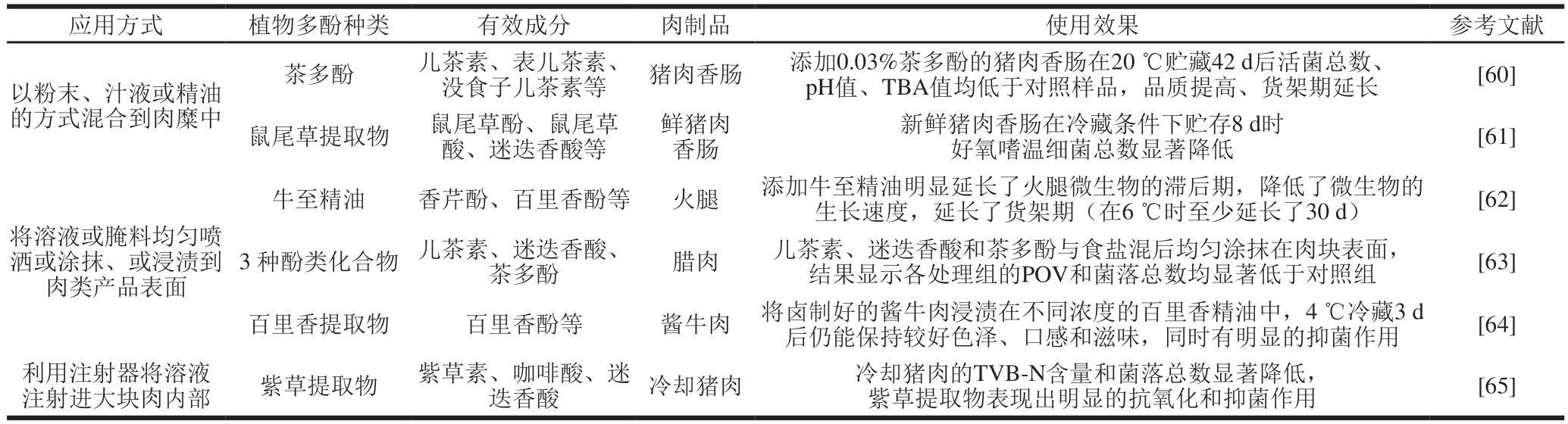
注:TBA.硫代巴比妥酸(thiobarbituric acid);POV.过氧化值(peroxide value);TVB-N.总挥发性盐基氮(total volatile basic nitrogen)。
应用方式 植物多酚种类 有效成分 肉制品 使用效果 参考文献以粉末、汁液或精油的方式混合到肉糜中没食子儿茶素等猪肉香肠添加0.03%茶多酚的猪肉香肠在20 ℃贮藏42 d后活菌总数、pH值、TBA值均低于对照样品,品质提高、货架期延长[60]鼠尾草提取物 鼠尾草酚、鼠尾草酸、迷迭香酸等茶多酚 儿茶素、表儿茶素、鲜猪肉香肠新鲜猪肉香肠在冷藏条件下贮存8 d时好氧嗜温细菌总数显著降低 [61]牛至精油 香芹酚、百里香酚等 火腿 添加牛至精油明显延长了火腿微生物的滞后期,降低了微生物的生长速度,延长了货架期(在6 ℃时至少延长了30 d) [62]将溶液或腌料均匀喷洒或涂抹、或浸渍到肉类产品表面 茶多酚 腊肉 儿茶素、迷迭香酸和茶多酚与食盐混后均匀涂抹在肉块表面,结果显示各处理组的POV和菌落总数均显著低于对照组[63]百里香提取物 百里香酚等 酱牛肉 将卤制好的酱牛肉浸渍在不同浓度的百里香精油中,4 ℃冷藏3 d后仍能保持较好色泽、口感和滋味,同时有明显的抑菌作用 [64]利用注射器将溶液3 种酚类化合物 儿茶素、迷迭香酸、注射进大块肉内部紫草提取物紫草素、咖啡酸、迷迭香酸冷却猪肉冷却猪肉的TVB-N含量和菌落总数显著降低,紫草提取物表现出明显的抗氧化和抑菌作用[65]
4.2 酚类化合物添加在动物日粮中的应用
根据《饲料添加剂品种目录(2013)》规定,人类食品添加剂中允许的食用香料(如黑胡椒提取物、茶多酚)和植物精油(如迷迭香精油)可以作为膳食补充剂添加到动物日粮中,在动物日粮中添加酚类物质是一种有效延缓肉与肉制品脂质过氧化、提高贮藏过程中氧化稳定性的方法[66]。将部分含有酚类化合物的天然提取物添加到日粮中可能对畜禽生长性能、免疫功能、抗氧化能力等造成一定影响。表4展示了部分酚类化合物以动物日粮形式应用的研究及其效果。
表4 酚类化合物添加在动物日粮中的应用
Table 4 Application of phenolic compounds for addition to animal feed

注:DPPH. 1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl)。
添加物质 有效成分 饲喂畜禽种类 使用效果 参考文献没食子酸、亚油酸 没食子酸 肉鸡饲料中添加1.0%没食子酸和亚油酸,能显著提高鸡肉中DPPH自由基清除活性,TBA值降低,并具有一定的抗菌活性[67]坚木单宁 单宁酸等 育肥猪饲粮中添加1 000 mg/kg的坚木单宁,饲喂期35 d,能显著提高猪肉的感官品质,降低微生物数量[68]葡萄残渣白藜芦醇、花青素、儿茶素等兔 400 mg/kg葡萄残渣可显著降低兔背最长肌的粗脂肪含量、失水率、剪切力和滴水损失 [69]
4.3 酚类化合物与活性包装结合的应用
活性包装是一种新型的、具有附加功能的食品包装方式,通过与不同的活性物质共同作用,可有效减少食品微生物生长和产品的氧化变质,提高产品品质,延长产品货架期[70]。将活性包装与酚类化合物结合,可以在抵御外界环境对肉类制品影响的同时,通过可控的方式将其释放到肉类表面或内部,从而发挥抗氧化和抑菌作用[57]。目前酚类化合物和活性包装的结合方式主要包括:1)制成可以逐渐释放酚类化合物的小袋;2)制成含有酚类化合物并与产品直接接触的衬垫;3)制成涂有精油的可食用或聚乙烯生物活性薄膜等[71-72]。表5展示了部分酚类化合物与活性包装结合应用在肉与肉制品加工中的代表性研究成果。
表5 酚类化合物与活性包装结合的应用
Table 5 Application of phenolic compounds in combination with active packaging
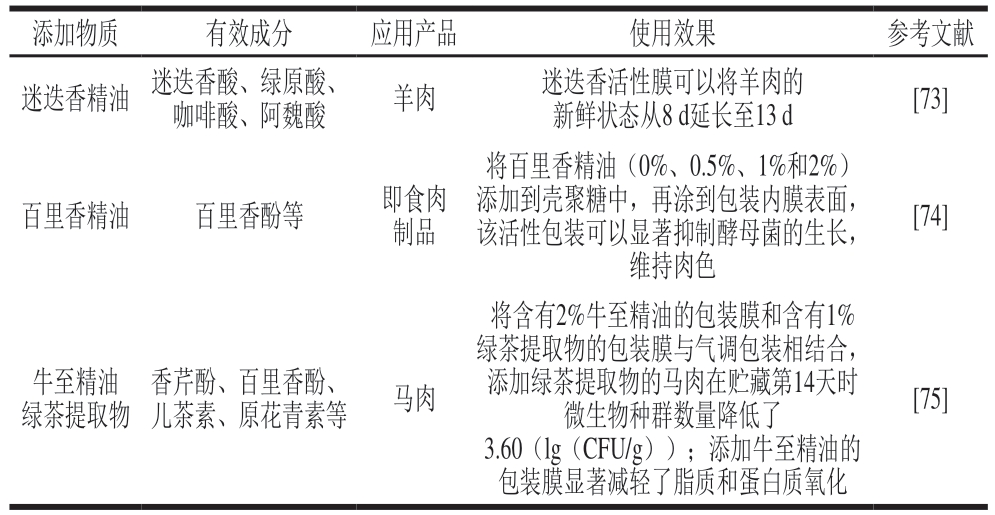
添加物质 有效成分 应用产品 使用效果 参考文献迷迭香精油 迷迭香酸、绿原酸、咖啡酸、阿魏酸 羊肉 迷迭香活性膜可以将羊肉的新鲜状态从8 d延长至13 d [73]百里香精油 百里香酚等 即食肉制品将百里香精油(0%、0.5%、1%和2%)添加到壳聚糖中,再涂到包装内膜表面,该活性包装可以显著抑制酵母菌的生长,维持肉色[74]牛至精油绿茶提取物香芹酚、百里香酚、儿茶素、原花青素等 马肉将含有2%牛至精油的包装膜和含有1%绿茶提取物的包装膜与气调包装相结合,添加绿茶提取物的马肉在贮藏第14天时微生物种群数量降低了3.60(lg(CFU/g));添加牛至精油的包装膜显著减轻了脂质和蛋白质氧化[75]
5 结 语
微生物腐败、脂肪和蛋白质氧化是影响肉与肉类制品货架期的主要原因,开发并应用健康的天然物质来延长肉与肉制品的货架期是产业的发展方向。酚类化合物具有很强的生物活性,可以替代防腐剂抑制腐败微生物和食源性病原体的生长,其抑菌活性与其结构中芳香环上羟基数量和位置有关,部分酚类化合物的疏水性和协同作用可以使其更好地发挥抑菌活性。酚类化合物主要通过与细胞壁相互作用、干扰细胞膜的功能、影响细菌生物膜的合成、抑制蛋白质合成和螯合金属离子等方式发挥抑菌作用。当酚类化合物直接应用于肉类或肉制品时,不仅能抑制微生物的生长,还可以抑制脂肪和蛋白质的氧化,改善肉色或防止变色。
尽管天然酚类化合物对抑制肉类氧化、腐败和食源性病原体的生长具有显著作用,但其在肉类行业的广泛使用和商业化仍存在很多问题。首先,酚类化合物抗菌活性的确切机制尚不完全明确,对肉与肉制品中优势菌群的抑菌效果也需要进一步研究。其次,天然酚类化合物可以通过直接添加在肉与肉制品中或与活性包装结合来发挥作用,但肉类加工过程中的一些工艺操作可能会使性质不稳定的酚类化合物遭到破坏,降低其抑菌和抗氧化活性。同时,一些天然提取物如牛至精油等具有较强的刺激气味,消费者接受度较低。
综上,系统总结酚类化合物的抑菌效果和机制、利用协同作用开发高效植物多酚复配物、确定酚类物质最佳添加浓度和使用条件、减少其给肉制品带来的不良风味,对酚类化合物在肉类工业中的商业化应用具有重要意义。
[1]翁航萍, 徐雄新. 肉类保藏技术(十六) 肉与肉制品的水分活度[J]. 肉类研究, 2009(5): 67-70; 83. DOI:10.3969/j.issn.1001-8123.2009.05.019.
[2]何贝贝. 乳源抗菌肽磁性微球分离纯化及其在酱牛肉中的应用研究[D]. 杨凌: 西北农林科技大学, 2018: 15-20.
[3]EFENBERGER-SZMECHTYK M, NOWAK A, CZYZOWSKA A.Plant extracts rich in polyphenols: antibacterial agents and natural preservatives for meat and meat products[J]. Critical Reviews in Food Science and Nutrition, 2021, 61(1): 149-178. DOI:10.1080/10408398.2020.1722060.
[4]戴金岳, 曾宪文, 方利敏, 等. 特定致腐菌对冷却猪肉的致腐作用机制[J]. 肉类研究, 2019, 33(12): 50-55. DOI:10.7506/rlyj1001-8123-20190926-231.
[5]PENNACCHIA C, ERCOLINI D, VILLANI F. Spoilage-related microbiota associated with chilled beef stored in air or vacuum pack[J]. Food Microbiology, 2011, 28(1): 84-93. DOI:10.1016/j.fm.2010.08.010.
[6]张若煜, 董鹏程, 朱立贤, 等. 生鲜肉中假单胞菌致腐机制的研究进展[J]. 食品科学, 2020, 41(17): 291-297. DOI:10.7506/spkx1002-6630-20190828-309.
[7]贾芳宇. 肉品快速诊断试验[J]. 动物检疫, 1988(2): 18-19.
[8]BEYA M M, NETZEL M E, SULTANBAWA Y, et al. Plantbased phenolic molecules as natural preservatives in comminuted meats: a review[J]. Antioxidants, 2021, 10(2): 263. DOI:10.3390/antiox10020263.
[9]黄小丹, 陈梦雨, 黄文洁, 等. 基于代谢组学的植物多酚及其肠道健康效应研究进展[J]. 生物技术通报, 2021, 37(1): 123-136.DOI:10.13560/j.cnki.biotech.bull.1985.2020-1409.
[10]SHARMA A, SHAHZAD B, REHMAN A, et al. Response of phenylpropanoid pathway and the role of polyphenols in plants under abiotic stress[J]. Molecules, 2019, 24(13): 2452. DOI:10.3390/molecules24132452.
[11]徐赫, 李荣华, 夏岩石, 等. 黄酮类化合物提取、分离纯化方法研究现状及展望[J]. 应用化工, 2021, 50(6): 1677-1682. DOI:10.16581/j.cnki.issn1671-3206.2021.06.010.
[12]耿文静, 王改琴, 邬本成, 等. 植物精油在畜牧养殖中的应用及机理研究进展[J]. 黑龙江畜牧兽医, 2017(2): 178-181. DOI:10.13881/j.cnki.hljxmsy.2017.0072.
[13]STOJKOVIC D, PETROVIC J, SOKOVIC M, et al. In situ antioxidant and antimicrobial activities of naturally occurring caffeic acid, p-coumaric acid and rutin, using food systems[J]. Journal of the Science of Food and Agriculture, 2013, 93(13): 3205-3208.DOI:10.1002/jsfa.6156.
[14]CHIBANE L B, DEGRAEVE P, FERHOUT H, et al. Plant antimicrobial polyphenols as potential natural food preservatives[J].Journal of the Science of Food and Agriculture, 2019, 99(4): 1457-1474. DOI:10.1002/jsfa.9357.
[15]GYAWALI R, IBRAHIM S A. Natural products as antimicrobial agents[J]. Food Control, 2014, 46: 412-429. DOI:10.1016/j.foodcont.2014.05.047.
[16]吴克刚, 赵欣欣, 段雪娟, 等. 芳樟醇气相抗菌活性与作用机制[J].食品科学, 2020, 41(1): 61-67. DOI:10.7506/spkx1002-6630-20181130-365.
[17]DEVI K P, NISHA S A, SAKTHIVEL R, et al. Eugenol (an essential oil of clove) acts as an antibacterial agent against Salmonella typhi by disrupting the cellular membrane[J]. Journal of Ethnopharmacology,2010, 130(1): 107-115. DOI:10.1016/j.jep.2010.04.025.
[18]BURT S. Essential oils: their antibacterial properties and potential applications in foods: a review[J]. International Journal of Food Microbiology, 2004, 94(3): 223-253. DOI:10.1016/j.ijfoodmicro.2004.03.022.
[19]HASHIMOTO T, KUMAZAWA S, NANJO F, et al. Interaction of tea catechins with lipid bilayers investigated with liposome systems[J].Bioscience Biotechnology and Biochemistry, 1999, 63(12): 2252-2255. DOI:10.1271/bbb.63.2252.
[20]HYLDGAARD M, MYGIND T, MEYER R L. Essential oils in food preservation: mode of action, synergies, and interactions with food matrix components[J]. Frontiers in Microbiology, 2012, 3: 12.DOI:10.3389/fmicb.2012.00012.
[21]王帆, 杨静东, 王春梅, 等. 复配植物源杀菌剂的开发研究[J].江西农业学报, 2010, 22(2): 87-89. DOI:10.19386/j.cnki.jxnyxb.2010.02.028.
[22]SERRA A T, MATIAS A A, NUNES A V M, et al. In vitro evaluation of olive- and grape-based natural extracts as potential preservatives for food[J]. Innovative Food Science and Emerging Technologies, 2008,9(3): 311-319. DOI:10.1016/j.ifset.2007.07.011.
[23]BORGES A, FERREIRA C, SAAVEDRA M J, et al. Antibacterial activity and mode of action of ferulic and gallic acids against pathogenic bacteria[J]. Microbial Drug Resistance, 2013, 19(4): 256-265. DOI:10.1089/mdr.2012.0244.
[24]PAPUC C, GORAN G V, PREDESCU C N, et al. Plant polyphenols as antioxidant and antibacterial agents for shelf-life extension of meat and meat products: classification, structures, sources, and action mechanisms[J]. Comprehensive Reviews in Food Science and Food Safety, 2017, 16(6): 1243-1268. DOI:10.1111/1541-4337.12298.
[25]NAZZARO F, FRATIANNI F, DE MARTINO L, et al. Effect of essential oils on pathogenic bacteria[J]. Pharmaceuticals, 2013, 6(12):1451-1474. DOI:10.3390/ph6121451.
[26]CUI Y, OH Y J, LIM J, et al. AFM study of the differential inhibitory effects of the green tea polyphenol (-)-epigallocatechin-3-gallate(EGCG) against Gram-positive and Gram-negative bacteria[J]. Food Microbiology, 2012, 29(1): 80-87. DOI:10.1016/j.fm.2011.08.019.
[27]BROWN L, WOLF J M, PRADOS-ROSALES R, et al. Through the wall: extracellular vesicles in Gram-positive bacteria, mycobacteria and fungi[J]. Nature Reviews Microbiology, 2015, 13(10): 620-630.DOI:10.1038/nrmicro3480.
[28]YODA Y, HU Z Q, ZHAO W H, et al. Different susceptibilities of Staphylococcus and Gram-negative rods to epigallocatechin gallate[J]. Journal of Infection and Chemotherapy, 2004, 10(1): 55-58.DOI:10.1007/s10156-003-0284-0.
[29]SSAAVEDRA M J, BORGES A, DIAS C, et al. Antimicrobial activity of phenolics and glucosinolate hydrolysis products and their synergy with streptomycin against pathogenic bacteria[J]. Journal of Medicinal Chemistry, 2010, 6(3): 174-183. DOI:10.2174/1573406411006030174.
[30]黄凤春. 河弧菌脂多糖单域重链抗体的生物淘选并运用于河弧菌血清分型[D]. 南昌: 南昌大学, 2016: 1-20.
[31]任格. 大肠杆菌脂多糖结构对胞外多糖克拉酸合成的影响机制[D].无锡: 江南大学, 2016: 3-10.
[32]NOHYNEK L J, ALAKOMI H L, KAHKONEN M P, et al. Berry phenolics: antimicrobial properties and mechanisms of action against severe human pathogens[J]. Nutrition and Cancer, 2006, 54(1): 18-32.DOI:10.1207/s15327914nc5401_4.
[33]DELEHANTY J B, JOHNSON B J, HICKEY T E, et al. Binding and neutralization of lipopolysaccharides by plant proanthocyanidins[J].Journal of Natural Products, 2007, 70(11): 1718-1724. DOI:10.1021/np0703601.
[34]JOHNSON B J, DELEHANTY J B, LIN B, et al. Immobilized proanthocyanidins for the capture of bacterial lipopolysaccharides[J].Analytical Chemistry, 2008, 80(6): 2113-2117. DOI:10.1021/ac7024128.
[35]HISANO M, BRUSCHINI H, NICODEMO A C, et al. Cranberries and lower urinary tract infection prevention[J]. Clinic Definition &Meaning, 2012, 67(6): 661-667. DOI:10.6061/clinics/2012(06)18.
[36]徐绚绚, 巩继贤, 张健飞, 等. 罗布麻抑菌物质及其作用机制的研究进展[J]. 纺织学报, 2020, 41(9): 149-154. DOI:10.13475/j.fzxb.20191000506.
[37]WU T, HE M, ZANG X, et al. A structure-activity relationship study of flavonoids as inhibitors of E. coli by membrane interaction effect[J]. Biochimica et Biophysica Acta, 2013, 1828(11): 2751-2756.DOI:10.1016/j.bbamem.2013.07.029.
[38]YI Shumin, WANG Wei, BAI Fengling, et al. Antimicrobial effect and membrane-active mechanism of tea polyphenols against serratia marcescens[J]. World Journal of Microbiology and Biotechnology,2014, 30(2): 451-460. DOI:10.1007/s11274-013-1464-4.
[39]YI Shumi, ZHU Junli, FU Linglin, et al. Tea polyphenols inhibit pseudomonas aeruginosa through damage to the cell membrane[J].International Journal of Food Microbiology, 2010, 144(1): 111-117.DOI:10.1016/j.ijfoodmicro.2010.09.005.
[40]ULREY R K, BARKSDALE S M, ZHOU W, et al. Cranberry proanthocyanidins have anti-biofilm properties against pseudomonas aeruginosa[J]. BMC Complementary and Alternative Medicine, 2014,14: 499. DOI:10.1186/1472-6882-14-499.
[41]孙孟娇, 王稳航. 肉类食品生物膜的形成机制及预防措施[J].中国食品学报, 2021, 21(4): 375-383. DOI:10.16429/j.1009-7848.2021.04.044.
[42]GIAOURIS E, HEIR E, HEBRAUD M, et al. Attachment and biofilm formation by foodborne bacteria in meat processing environments:causes, implications, role of bacterial interactions and control by alternative novel methods[J]. Meat Science, 2014, 97(3): 298-309.DOI:10.1016/j.meatsci.2013.05.023.
[43]BORGES A, SAAVEDRA M J, SIMOES M. The activity of ferulic and gallic acids in biofilm prevention and control of pathogenic bacteria[J]. Biofouling, 2012, 28(7): 755-767. DOI:10.1080/08927014.2012.706751.
[44]张炼辉. 微生物群体感应系统的研究进展[J]. 华南农业大学学报,2019, 40(5): 50-58. DOI:10.7671/j.issn.1001-411X.201905061 .
[45]ZHANG J, RUI X, WANG L, et al. Polyphenolic extract from rosa rugosa tea inhibits bacterial quorum sensing and biofilm formation[J]. Food Control, 2014, 42: 125-131. DOI:10.1016/j.foodcont.2014.02.001.
[46]PACKIAVATHY I A, SASIKUMAR P, PANDIAN S K, et al.Prevention of quorum-sensing-mediated biofilm development and virulence factors production in Vibrio spp. by curcumin[J]. Applied Microbiology and Biotechnology, 2013, 97(23): 10177-10187.DOI:10.1007/s00253-013-4704-5.
[47]PLYUTA V, ZAITSEVA J, LOBAKOVA E, et al. Effect of plant phenolic compounds on biofilm formation by Pseudomonas aeruginosa[J]. APMIS, 2013, 121(11): 1073-1081. DOI:10.1111/apm.12083.
[48]CHO Y S, SCHILLER N L, KAHNG H Y, et al. Cellular responses and proteomic analysis of Escherichia coli exposed to green tea polyphenols[J]. Current Microbiology, 2007, 55(6): 501-506.DOI:10.1007/s00284-007-9021-8.
[49]DADI P K, AHMAD M, AHMAD Z. Inhibition of atpase activity of Escherichia coli ATP synthase by polyphenols[J]. International Journal of Biological Macromolecules, 2009, 45(1): 72-79. DOI:10.1016/j.ijbiomac.2009.04.004.
[50]ZHANG Yimin, ROCK C O. Evaluation of epigallocatechin gallate and related plant polyphenols as inhibitors of the FabG and FabI reductases of bacterial type II fatty-acid synthase[J]. Journal of Biological Chemistry, 2004, 279(30): 30994-31001. DOI:10.1074/jbc.M403697200.
[51]袁李佳龙, 秦旭平. ATP合酶β亚基功能与疾病[J]. 中国临床药理学与治疗学, 2018, 23(4): 464-470. DOI:10.12092/j.issn.1009-2501.2018.04.017.
[52]周甲申, 张琳, 张良. II型脂肪酸生物合成途径机制和药物发现研究进展[J]. 化学学报, 2020, 78(12): 1383-1398. DOI:10.6023/A20070299.
[53]萨仁高娃, 胡文忠, 冯可, 等. 植物精油及其成分对病原微生物抗菌机理的研究进展[J]. 食品科学, 2020, 41(11): 285-294. DOI:10.7506/spkx1002-6630-20190603-018.
[54]PLAPER A, GOLOB M, HAFNER I, et al. Characterization of quercetin binding site on DNA gyrase[J]. Biochemical and Biophysical Research Communications, 2003, 306(2): 530-536. DOI:10.1016/s0006-291x(03)01006-4.
[55]WU Ting, ZANG Xixi, HE Mengying, et al. Structure-activity relationship of flavonoids on their anti-Escherichia coli activity and inhibition of DNA gyrase[J]. Journal of Agricultural and Food Chemistry, 2013, 61(34): 8185-8190. DOI:10.1021/jf402222v.
[56]HARAGUCHI H, TANIMOTO K, TAMURA Y, et al. Mode of antibacterial action of retrochalcones from Glycyrrhiza inflata[J].Phytochemistry, 1998, 48(1): 125-129. DOI:10.1016/s0031-9422(97)01105-9.
[57]类红梅, 罗欣, 毛衍伟, 等. 天然抗氧化剂的功能及其在肉与肉制品中的应用研究进展[J]. 食品科学, 2020, 41(21): 267-277.DOI:10.7506/spkx1002-6630-20191025-286.
[58]MOON J H, KIM C, LEE H S, et al. Antibacterial and antibiofilm effects of iron chelators against Prevotella intermedia[J]. Journal of Medical Microbiology, 2013, 62: 1307-1316. DOI:10.1099/jmm.0.053553-0.
[59]ENGELS C, KNODLER M, ZHAO Y Y, et al. Antimicrobial activity of gallotannins isolated from mango (Mangifera indica L.) kernels[J].Journal of Agricultural and Food Chemistry, 2009, 57(17): 7712-7718.DOI:10.1021/jf901621m.
[60]FAN W J, CHEN Y C, SUN J X, et al. Effects of tea polyphenol on quality and shelf life of pork sausages[J]. Journal of Food Science and Technology, 2014, 51(1): 191-195. DOI:10.1007/s13197-013-1076-x.
[61]ŠOJIĆ B, PAVLIĆ B, ZEKOVIĆ Z, et al. The effect of essential oil and extract from sage (Salvia officinalis L.) herbal dust (food industry by-product) on the oxidative and microbiological stability of fresh pork sausages[J]. LWT-Food Science and Technology, 2018, 89: 749-755. DOI:10.1016/j.lwt.2017.11.055.
[62]MENEZES N M C, MARTINS W F, LONGHI D A, et al. Modeling the effect of oregano essential oil on shelf-life extension of vacuumpacked cooked sliced ham[J]. Meat Science, 2018, 139: 113-119.DOI:10.1016/j.meatsci.2018.01.017.
[63]刘光宪, 王丽, 李雪, 等. 3 种天然抗氧化剂对腊肉理化性质的影响[J]. 食品安全质量检测学报, 2021, 12(15): 6177-6184.DOI:10.19812/j.cnki.jfsq11-5956/ts.2021.15.039.
[64]李玉邯, 杨柳, 张一, 等. 百里香精油对酱牛肉品质和抑菌抗氧化性能的研究[J]. 中国调味品, 2017, 42(9): 36-39. DOI:10.3969/j.issn.1000-9973.2017.09.008.
[65]闫文杰, 徐宝才, 韩衍青. 紫草提取物对冷却猪肉贮藏品质的影响[J]. 食品研究与开发, 2016, 37(6): 190-192. DOI:10.3969/j.issn.1005-6521.2016.06.045.
[66]ARSHAD M S, IMRAN A, NADEEM M T, et al. Enhancing the quality and lipid stability of chicken nuggets using natural antioxidants[J]. Lipid Droplets in Health and Disease, 2017, 16(1):108. DOI:10.1186/s12944-017-0496-4.
[67]JUNG S, CHOE J H, KIM B, et al. Effect of dietary mixture of gallic acid and linoleic acid on antioxidative potential and quality of breast meat from broilers[J]. Meat Science, 2010, 86(2): 520-526.DOI:10.1016/j.meatsci.2010.06.007.
[68]苏成文, 宋之波, 徐相亭, 等. 坚木单宁对育肥猪生长性能和猪肉货架期的影响[J]. 动物营养学报, 2019, 31(10): 4834-4842.DOI:10.3969 /j.issn.1006-267x.2019.10.049 .
[69]党文庆, 何敏敏, 曹亮亮, 等. 葡萄残渣及提取物在兔日粮中的应用研究进展[J]. 中国养兔杂志, 2021(3): 18-23.
[70]李墨琳, 罗欣, 刘国星, 等. 活性包装对肉制品品质及货架期影响的研究进展[J]. 食品科学, 2019, 40(11): 313-320. DOI:10.7506/spkx1002-6630-20180627-497.
[71]COMA V. Bioactive packaging technologies for extended shelf life of meat-based products[J]. Meat Science, 2008, 78(1/2): 90-103.DOI:10.1016/j.meatsci.2007.07.035.
[72]BARBOSA-PEREIRA L, ANGULO I, LAGARÓN J M, et al.Development of new active packaging films containing bioactive nanocomposites[J]. Innovative Food Science and Emerging Technologies, 2014, 26: 310-318. DOI:10.1016/j.ifset.2014.06.002.
[73]CAMO J, BELTRAN J A, RONCALES P. Extension of the display life of lamb with an antioxidant active packaging[J]. Meat Science,2008, 80(4): 1086-1091. DOI:10.1016/j.meatsci.2008.04.031.
[74]QUESADA J, SENDRA E, NAVARRO C, et al. Antimicrobial active packaging including chitosan films with Thymus vulgaris L. essential oil for ready-to-eat meat[J]. Foods, 2016, 5(3): 57. DOI:10.3390/foods5030057.
[75]LORENZO J M, BATLLE R, GÓMEZ M. Extension of the shelf-life of foal meat with two antioxidant active packaging systems[J]. LWTFood Science and Technology, 2014, 59(1): 181-188. DOI:10.1016/j.lwt.2014.04.061.