食物的味道主要是挥发性香气物质和非挥发性呈味物质共同作用的结果,是影响消费者购买决策的主要因素[1]。其中,非挥发性呈味物质使不同种类水果具有不同的口感滋味,包括酸、甜、苦、涩、鲜等。此外,氨基酸组成和丰度也会影响果实滋味[2]。多年来,甜味一直是多数消费者购买水果的决定性因素,但随着人们生活水平的提高,营养过剩引发的糖尿病、高血压、高血脂等慢性疾病越来越多,人们的保健意识越来越强,对健康饮食的要求也日益提高。传统中药理论认为苦味成分是苦味中药发挥药效的重要物质基础[3]。日常生活中,具有苦味的食物如苦瓜、苦菜等均具有清热解毒的食疗保健功效。植物性来源的苦味物质种类繁多、分布广泛。其中,多酚类化合物是枣、柑橘、茶叶、啤酒花等植物的主要苦味物质[4-7];生物碱中的咖啡因是咖啡的主要苦味来源[8];氨基酸中具有滋味特性的多为L-氨基酸,疏水氨基酸与苦味受体结合会产生苦味[9];皂苷是藜麦种皮的主要苦味物质[10];杏仁中的苦味取决于苦杏仁苷含量[11];苦瓜特有的苦味归因于高含量的葫芦烷型三萜类化合物[12]。这些苦味成分也是苦味食物发挥保健作用的关键物质。
柑橘属(Citrus L.)植物包括酸橙(Citrus aurantifolia)、甜橙(Citrus sinensis)、香橼(Citrus medica)、柚(Citrus maxima)、柠檬(Citrus limon)等约20 个种[13],是一类典型的果实带有苦味特征的果树,其中不同种或品种果实由于苦味物质种类与含量差异而表现出的苦味程度不尽相同。香橼和酸橙因苦味与酸味重而难以直接食用,通常只作为中药材使用;而葡萄柚(Citrus paradisi)、瓯柑、狮头柑等品种具有一定程度的苦味,具有抗氧化、抑制癌细胞生长和抑菌等生物活性[14-15],属于传统的药食同源水果。然而,柑橘因具有明显的苦味特征而难以为部分消费者接受。因此在柑橘育种中常采用基因编辑技术、低苦品种育种等减少果实苦味成分积累,或在柑橘产品加工过程中采用脱苦技术去除苦味物质以减轻苦味。近年来,越来越多消费者开始关注药食同源物质,有关柑橘苦味物质种类、形成及功能活性方面的研究不断增加,为系统评述柑橘果实中苦味物质的形成、结构与功能,本文总结柑橘果实苦味物质的结构特征、合成机制、功能活性和加工过程中主要脱苦技术,为有关柑橘果实中苦味物质的进一步深入研究提供思路,也为培育兼具风味和保健功能成分的柑橘品种提供理论支持。
1 柑橘果实苦味物质的种类、结构及特征
柑橘果实中存在多种具有特定功能的活性物质[16],包括黄烷酮类、异黄酮类、黄酮类、黄酮醇类、三萜类和柠檬苦素类等,而糖苷链的类型是这些化合物是否呈苦味的关键[17]。使柑橘果实呈现苦味的物质主要分为2 类:一类是黄烷酮类化合物,包括柚皮苷、新橙皮苷和枸橘苷,其中柚皮苷为主要的苦味物质,其次为新橙皮苷[18]。另一类是高度氧化的三萜类化合物的衍生物,主要以柠檬苦素和诺米林为代表。柚皮苷苦味阈值较高,水溶液中阈值为20 mg/L,柠檬苦素苦味阈值较低,苦味强烈,在水溶液中达到1.0 mg/L便能呈现明显的苦味,其在果汁中的苦味阈值为3.4 mg/L[17]。诺米林苦味弱于柠檬苦素,宜昌根辛和诺米林酸在柑橘果实中含量较低,因此苦味不强。不同柑橘产品苦味来源物质不同,柑橘果汁苦味主要来源于柠檬苦素,而柑橘类果实苦味主要由柚皮苷引起。由于柚皮苷、柠檬苦素和诺米林为柑橘果实中的代表性苦味物质,本文将主要总结这3 种物质呈现苦味的结构特征、合成代谢途径与功能活性。
1.1 柚皮苷和新橙皮苷
柑橘黄酮是一组具有共同C6—C3—C6结构的酚类化合物,由2 个苯环(A环和B环)和1 个作为连接基的杂环吡喃环(C环)组成(图1)。其中黄烷酮类含量最为丰富,为代表性物质,主要以糖苷形式存在于柑橘果实中[19],约占其总黄酮类化合物的95%。柚皮苷和新橙皮苷是黄烷酮类化合物中2 种主要苦味物质。葡萄柚、苦橙(Citrus aurantium)和柚果实因富含柚皮苷而具有明显的苦味性状[20]。柚皮苷化学结构在1928年由Asahina和Inubuse阐明,美国罗格斯大学的Natarajan于1976年从酸橙成熟果皮中成功提取新橙皮苷,得率2.8%[21]。随着检测技术的突破,研究者发现柚皮苷和新橙皮苷分别是柚皮素和橙皮素的糖苷衍生物,分别由柚皮素和橙皮素骨架的C7位置加一个鼠李糖-α-1,2-葡萄糖苷形成[22],新橙皮苷骨架B-3’处缺失一个羟基形成枸橘苷。柚皮苷、新橙皮苷和枸橘苷呈现苦味特征正是由于C7位置上存在鼠李糖-α-1,2-葡萄糖基[23]。黄酮类化合物结构与苦味具有定量构象关系,氢键供体及基团与黄酮类化合物的苦味密切相关,增加黄酮类骨架A-5或B-3’处的氢键供体、A-8处的大基团或B-4’处的吸电子基团均可增强黄酮类化合物的苦味[5]。
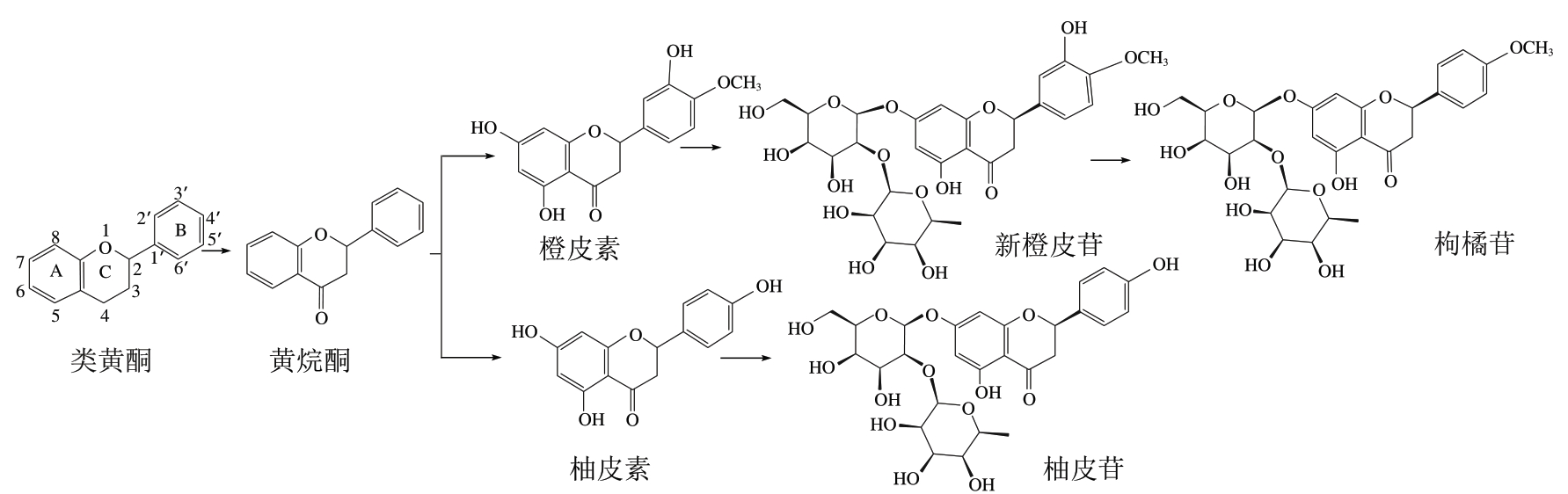
图1 植物类黄酮结构式[24]
Fig. 1 Structural formula of plant flavonoids[24]
柑橘品种、果实组织、发育期、生长环境均会影响黄烷酮化合物含量[25]。徐贵华等[26]对市场上15 个柑橘品种进行比较发现,不同品种柑橘及其不同组织均含有丰富的黄酮类化合物并呈现显著的多样性。例如,塔罗科血橙(C. sinensis (L.) Osbeck cv. Taroco)橙皮苷含量最高但未检出柚皮苷,四季柚(C. grandis (L.) Osbeck cv.Sijiyou)含有大量柚皮苷但橙皮苷和新橙皮苷未检出。柚果类柚皮苷含量呈现内皮层>外皮层>果肉的规律。在琯溪蜜柚(C. maxima (Burm.) Merr.)幼果期,随着果实发育,白衣层与绿色表皮中柚皮苷含量不断下降,且两组织间柚皮苷含量差异不断缩小[27];在果实成熟期,柚皮苷在果肉中的含量呈下降趋势,而在外皮层和内皮层中呈现先升高后下降的趋势[28]。研究[29]表明,不同生长季节和气候条件下的光照和温度差异均会影响柚皮苷的代谢速率。另外,外部损伤也会影响柚皮苷含量,轻度外伤可促进果实体内柚皮苷的生物合成,而重度损伤则会减少柚皮苷的生物合成[30]。
1.2 柠檬苦素和诺米林
在芸香科植物中,类柠檬苦素化合物主要分为苷元型柠檬苦素类、糖苷型柠檬苦素类和降解型柠檬苦素类。目前,已经从不同科属的植物中分离出数百种类柠檬苦素化合物,在植物界其主要存在于芸香科植物的种子中,如枳实(脐橙、柑桔、香橙)种子、柚种子等[31]。类柠檬苦素化合物是一类具有呋喃环并且高度氧化的四环三萜类化合物,具有4,4,8-三甲基-17-呋喃基类固醇的骨架结构,含有相对较多的氧原子。所有天然存在的柑橘类柠檬苦素化合物在C17处均有与D环相连的呋喃环,在C3、C4、C7、C16和C17处均具有含氧官能团[32-33](图2)。类柠檬苦素化合物以中性(非羧基化/苷元)和酸性(羧基化/糖苷)形式存在,前者不溶于水且具有苦味,后者可溶于水且无味,导致柑橘产品呈苦味的重要物质柠檬苦素和诺米林,两者均具有苦味且水溶性低。
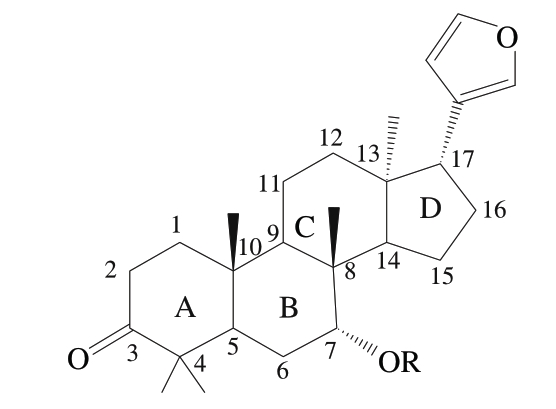
图2 类柠檬苦素化合物基本结构[32-33]
Fig. 2 Basic structure of limonoids[32-33]
类柠檬苦素化合物主要集中在柑橘种子(果核)中,其次为囊衣[34-35],而汁胞、白皮层、黄皮层中含量较少[36]。如柚(C. grandis (L.) Osbeck)种子中包含相对高水平的柠檬苦素苷元,苷元与糖苷的比例约为2∶1[37],呈现出较强的苦味。就分布而言,囊衣中柠檬苦素和诺米林含量较高,而黄皮层中只含有较低水平的柚皮苷,可能是一个弱库,这表明这些化合物的生物合成或积累可能存在组织偏向模式。多项研究表明柠檬苦素的积累很大程度上受遗传背景、生长发育和环境影响。秦芸桦等[38]比较不同品种柑橘果实中类柠檬苦素化合物含量发现,柚类、柑类、橙类、橘类果实中3 种类柠檬苦素化合物(柠檬苦素、诺米林、黄柏酮)含量依次降低。柚子被认为是柑橘类中最苦的水果,其柠檬苦素的积累主要由基因型决定[34]。红美人(Citrus reticulata ‘Hong Mei Ren’)幼果中柠檬苦素和诺米林含量随其生长呈现先上升后下降的趋势[39]。在琯溪蜜柚不同组织中,柠檬苦素和诺米林含量均随果实成熟度的增加而下降,尤其是成熟期间下降幅度更大[27]。在不同的生长季节,柠檬苦素和诺米林含量存在差异,对3 个生长季节不同发育阶段“国庆一号”温州蜜柑(Citrus unshiu Marc.)果实组织中的柠檬苦素和诺米林含量进行连续检测发现,柠檬苦素和诺米林含量大多呈现下降趋势,但由于温度和降水变化,每个季节含量并不一致[35]。同时,一些外部环境也会影响柠檬苦素和诺米林积累,如低温生物胁迫会提高柠檬苦素和诺米林积累[40];感染黄龙病会导致柑橘类水果和果汁中柠檬苦素和诺米林含量升高[41]等。
2 柑橘果实苦味物质的合成机制
黄烷酮糖苷和类柠檬苦素化合物的合成分别始于苯丙氨酸和乙酰辅酶A。乙酰辅酶A是生物体能源物质代谢过程中产生的一种重要的中间代谢产物,可由苯丙氨酸经过一系列酶分解得到。两类苦味物质的合成共享前体物质,在合成前期存在共同的生物化学基础,后续经不同的合成途径生成各自特有的苦味物质。
2.1 黄烷酮合成途径及关键基因
黄烷酮的生物合成属于苯丙烷代谢途径的一个分支。苯丙烷途径始于苯丙氨酸,苯丙氨酸经一系列酶促反应通过酰化、甲基化、糖基化和羟基化对其基本骨架进行化学修饰合成多样的苯丙烷代谢物[42](图3)。苯丙烷代谢物对植物的发育和生存尤为重要。苯丙烷途径的前3 个步骤构成了所谓的公共苯丙烷途径,为所有下游代谢产物提供前体[43]。首先,苯丙氨酸解氨酶(phenylalanine ammonia-lyase,PAL)催化是公共苯丙烷途径中的第1个关键步骤,将苯丙氨酸脱氨基为反式肉桂酸[44]。第2步,肉桂酸4-羟化酶(cinnamate 4-hydroxylase,C4H)催化反式肉桂酸生成对香豆酸,这也是类黄酮合成途径中的第1个氧化反应[45]。在公共苯丙烷途径的第3步中,对香豆酸的羧基被激活,4-香豆酸辅酶A连接酶(4-coumarate:coenzyme A ligase,4CL)通过向对香豆酸添加辅酶A单元与对香豆酸的羧基形成硫酯键,从而形成对香豆酰辅酶A,至此,类黄酮生物合成途径开始。一般苯丙烷途径的下游是苯丙烷代谢的不同分支,其中黄酮类途径是本文主要讨论的分支。
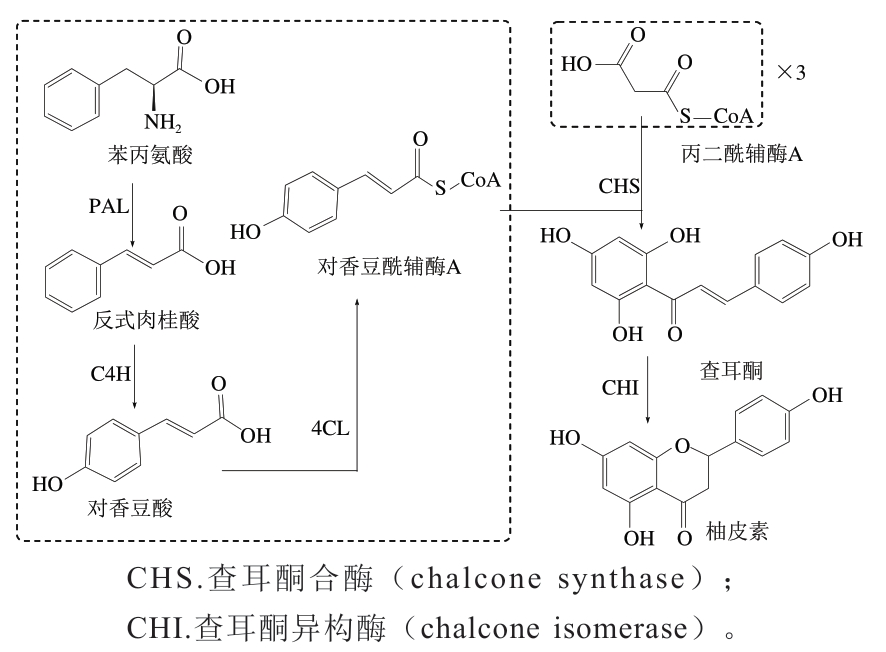
图3 苯丙烷代谢上游途径
Fig. 3 Upstream pathways of phenylpropane metabolism
CHS属于III型聚酮化合物合酶家族,是类黄酮生物合成途径中的第1个关键限速酶[46]。对香豆酰辅酶A与CHS活性位点的半胱氨酸残基结合,经过脱羧缩合反应,添加3 分子丙二酰辅酶A形成柚皮苷配基查耳酮[47]。查耳酮是类黄酮代谢途径中第1个关键中间产物,为下游类黄酮合成提供基本骨架。查耳酮在CHI的催化下内环化生成柚皮素,导致类黄酮途径中杂环C的形成。CHI是类黄酮生物合成途径中的第2个关键限速酶[48]。至此,黄烷酮合成途径开始,黄烷酮(柚皮素、甘草素、五羟基黄烷酮和圣草酚)是类黄酮生物合成途径的中心分支点。
柚皮素作为柚皮苷、新橙皮苷、枸橘苷和新圣草次苷的共同底物,可通过2 条独立的代谢途径合成黄烷酮糖苷(图4)。首先柚皮素先经羟基化或甲基化反应生成异樱野素、橙皮素和圣草酚等化合物,随后3 种化合物在7-O-葡萄糖苷转移酶(7-O-glucosyltransferase,7-GlcT)的催化下,在C7位置上通过O连接添加葡萄糖苷分别形成异樱野素-7-O-葡萄糖苷、橙皮素-7-O-葡萄糖苷、圣草酚-7-O-葡萄糖苷[49]。紧接着在3 种黄烷酮糖苷作为底物的情况下,经由不同酶作用同时生成多种不同的化合物。经1,2-鼠李糖转移酶(1,2-rhamnosyltransferase,1,2-RhaT)催化,葡萄糖部分C2位置上的羟基连接鼠李糖分别生成有苦味的新橙皮苷、枸橘苷、新圣草次苷,而在1,6-鼠李糖转移酶(1,6-rhamnosyltransferase,1,6-RhaT)催化下,鼠李糖与葡萄糖部分C6位置上的羟基连接生成无苦味的橙皮苷、香风草苷、圣草次苷[50]。另一条代谢支路是7-GlcT直接催化柚皮素生成柚皮素-7-O-葡萄糖苷,然后在1,2-RhaT的催化下生成有苦味的柚皮苷,在1,6-RhaT催化下生成无苦味的芸香柚皮苷[30]。1,2-RhaT和1,6-RhaT催化合成苦味和无苦味化合物的根本区别在于鼠李糖的连接位置。因此,鼠李糖附着位置是化合物是否具有苦味的决定因素。另外,新橙皮苷还能够通过加氢反应生成具有甜味的新橙皮苷二氢查耳酮,其甜度是蔗糖的1 500 倍,因其低热量、高甜度被作为甜味剂广泛应用于饮料和医药领域[51]。
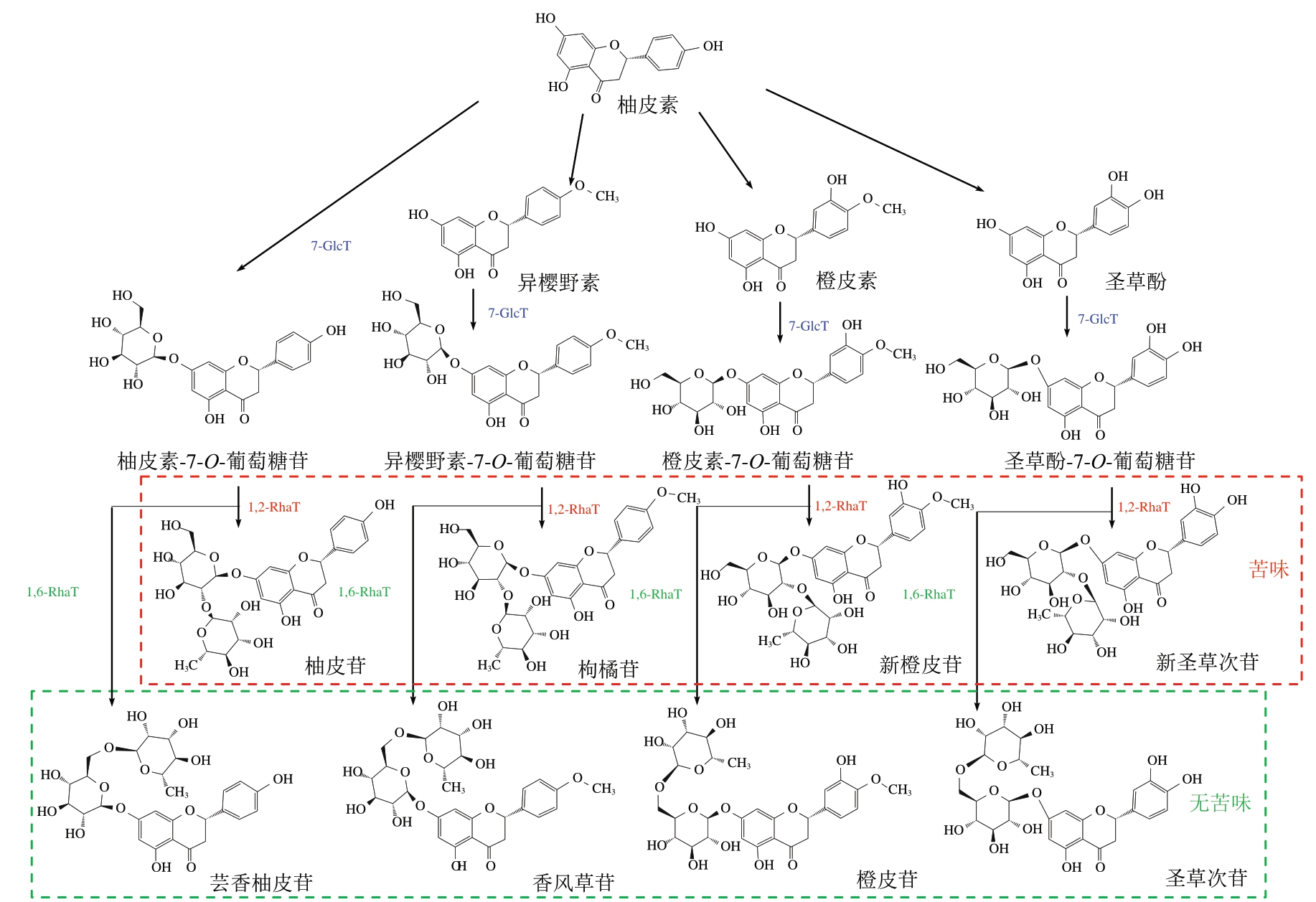
图4 柚皮素代谢途径
Fig. 4 Metabolic pathways of naringenin
1,2-RhaT基因Cm1,2-RhaT为调节柚皮苷和新橙皮苷合成的关键基因,对Cm1,2-RhaT的研究最早始于Bar-Peled等[52],其从葡萄柚中分离得到该基因。随后Frydman等[53]对从葡萄柚中分离出的Cm1,2-RhaT基因进行功能验证,发现该基因编码柑橘中苦味化合物生物合成的关键酶1,2-RhaT。除Cm1,2-RhaT基因外,各柑橘基因组中还存在2 种与Cm1,2RhaT高度同源的1,2RhaT-like基因。但是,1,2RhaT-like基因编码的酶不具备催化合成新橙皮苷的功能,仅能够催化合成非苦味类黄酮-7-O-葡萄糖苷[54]。编码类黄酮生物合成酶的基因表达受到MYB、bHLH和WD40等转录因子共同调节,这些转录因子已被发现在苹果、桃、葡萄、梨和柑橘等多种水果作物中参与调节类黄酮的生物合成,特别是花青素相关化合物[50]。
2.2 类柠檬苦素化合物合成途径及关键基因
柠檬苦素是从柑橘苦味成分中获得的第1个四环三萜类化合物,由异戊烯基焦磷酸盐(isopentenyl pyrophosphate,IPP)和二甲基烯丙基二磷酸盐(dimethylallyl diphosphate,DMAPP)分别通过甲羟戊酸盐(mevalonate,MVA)途径和甲基赤藓糖醇磷酸盐(methylerythritol 4-phosphate,MEP)途径合成[55]。在法呢基二磷酸合酶(farnesyl diphosphate synthase,FPPS)催化下,由2 个C5单元的IPP和1 个C5单元的DMAPP缩合形成C15法呢基二磷酸盐(farnesyl diphosphate,FPP),在角鲨烯合酶(squalene synthase,SQS)的催化下,通过头对头缩合反应进一步转化为直链C30三萜前体角鲨烯(图5)。随后,角鲨烯环氧化酶(squalene epoxidase,SQE)将角鲨烯氧化形成2,3-氧化角鲨烯,其在特定的氧化角鲨烯环化酶(oxidosqualene cyclase,OSC)介导下进行环化,形成多种三萜类骨架。角鲨烯是柠檬苦素类、甾醇和油菜素类固醇等三萜类化合物的第1个前体物质。由于位于关键的分支点充当开关,SQS在三萜生物合成中发挥着重要的调节作用[56]。SQE和OSC是三萜生物合成中关键的限速酶,分别催化第1个氧化和环化步骤[57]。根据产物的不同可将代谢途径分为4 类,分别为卡拉途径、柠檬苦素途径、宜昌根辛途径和醋酸酯途径。
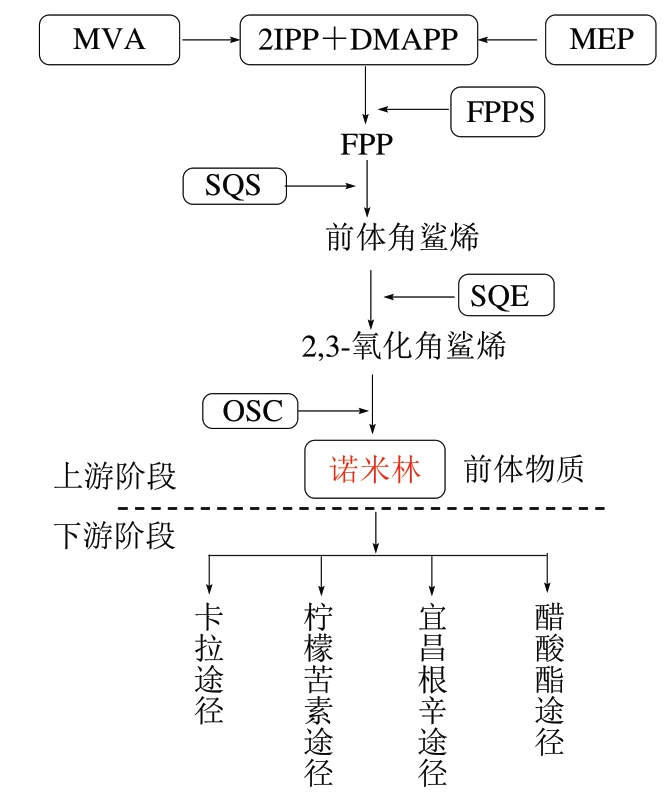
图5 类柠檬苦素合成途径[58]
Fig. 5 Synthesis pathways of limonoids[58]
柑橘属大多数品种中的类柠檬苦素主要通过柠檬苦素途径合成(图6),前体物质诺米林在茎部组织中合成并转移至果实组织,经过一系列生化反应转化为黄柏酮,再转化为黄柏酮酸、宜昌素,最终合成柠檬苦素。同时还会伴随生成含量较低的类柠檬苦素,包括柠檬苦醇、脱氧柠檬苦素等。在柠檬苦素的生物合成途径中,诺米林在非结果期会达到更高的水平,表明果蔬可能在开花期之前已准备生成高水平苦味物质以保护自体免受害虫和病毒的侵害[59]。而在果实收获后,诺米林在果实组织中的积累停止,果实组织中积累的诺米林将继续用于柠檬苦素苷元的生物合成。非苦味柠檬苦素酸A-环内酯(limonoate A-ring lactone,LARL)是合成柠檬苦素的前体物质,由柠檬苦素酸D-环内酯水解酶(limonin D-ring lactone hydrolase,LDRLase)在生理酸性下催化合成具有苦味的柠檬苦素。该反应可逆,在强酸或强碱环境中无酶参与也可加速反应,该反应是柑橘果实出现延迟苦味的主要原因。成熟未加工的柑橘果实中柠檬苦素含量极低,而加工果汁中含量较高,主要是由于柠檬苦素的前体物质LARL存在于中性至微碱性环境的膜中,而柑橘果实在榨汁过程经过物理挤压,汁胞中的酸性果汁将LARL转化为柠檬苦素[17],导致果汁中柠檬苦素含量增加。LARL还可以接受从尿苷二磷酸葡萄糖(uridine diphosphate-glucose,UDP-Glu)转移的葡萄糖,以产生由柠檬苦素糖基转移酶(limonin glucosyltransferase,LGT)催化的非苦味柠檬苦素17-β-D-吡喃葡萄糖苷(糖基柠檬苦素)[45]。这种天然存在的生物合成途径为柑橘产品脱苦提供一种新思路。
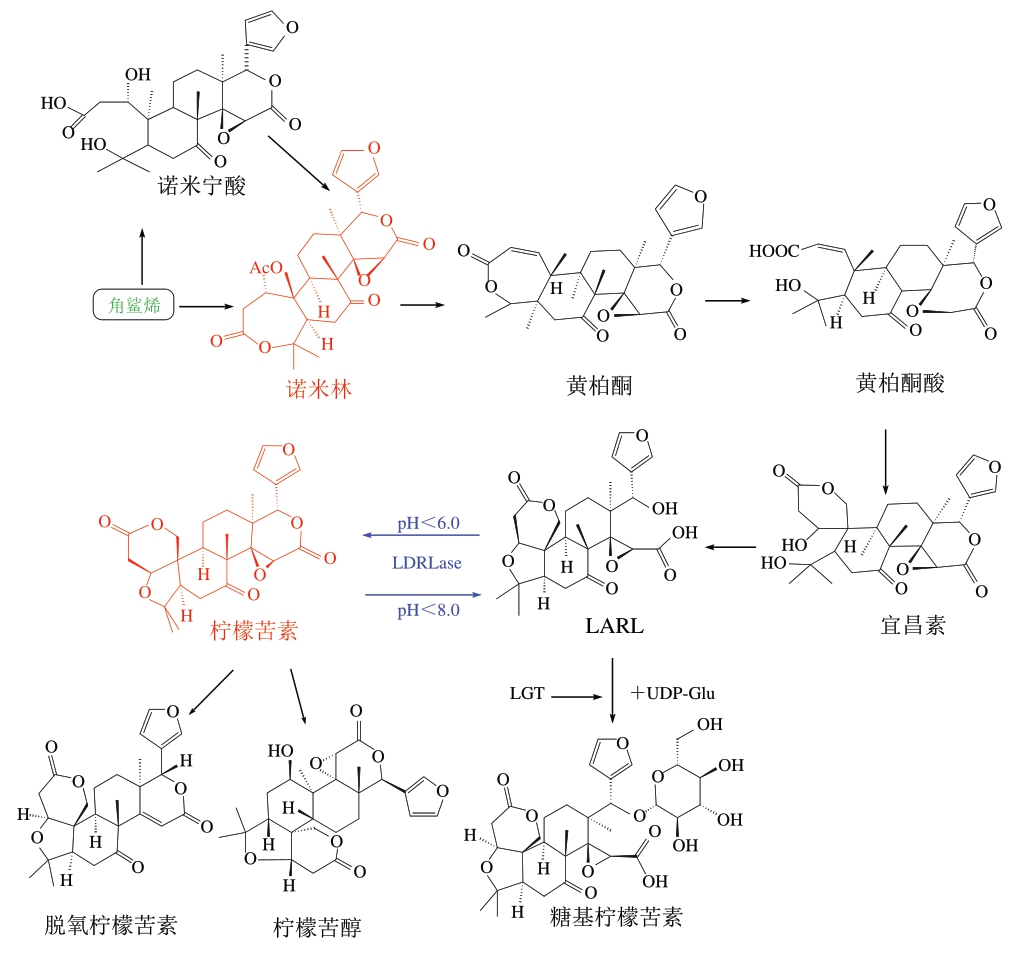
图6 柠檬苦素生物合成途径
Fig. 6 Biosynthetic pathway of limonin
有研究[60]对类柠檬苦素生物合成相关基因进行鉴定,发现CiSQS和CiOSC基因能调控类柠檬苦素的生物合成,可能是位于类柠檬苦素生物合成途径上游的重要基因。同时,CiMYB42是柠檬苦素代谢网络中的转录激活剂,CiMYB42通过与CiOSC启动子中的II型MYB核心(TNGTTG/A)序列结合参与柠檬苦素生物合成途径[61]。还有研究[62]表明,CclSAUR49基因与类柠檬苦素的积累呈显著负相关,可在植物中抑制类柠檬苦素的合成或积累。
3 柑橘果实苦味物质的功能活性
柑橘苦味化合物因其营养和药用价值成为制药学和营养学中一个新兴且重要的研究领域[63]。越来越多的证据表明柑橘苦味化合物可通过调节细胞代谢和增殖改善慢性疾病,苦味柑橘可作为具有保健功效的水果进行推广。
3.1 抗炎与抑菌
细菌作为病原体感染机体会引起炎症,而炎症是身体对潜在有害刺激的保护性反应,不受控制的炎症反应可导致癌症、心血管功能障碍和自身免疫性疾病等[64]。研究[65]表明,柑橘中柚皮苷可以抑制股骨中金黄色葡萄球菌诱导的细菌生长和炎症。同样,新橙皮苷可以调节1-甲基-4-苯基-1,2,3,6-四氢吡啶诱导的帕金森氏病小鼠模型肠道微生物失衡,减少有害细菌丰度,进而减轻神经炎症[66]。Silva等[67]发现柠檬苦素能够显著改善慢性炎症模型中的鼠爪水肿,Liu Shijia等[68]在葡聚糖硫酸钠诱导的溃疡性结肠炎体内治疗中发现,柠檬苦素可显著降低疾病活动指数、肠道损伤及促炎细胞因子(如肿瘤坏死因子α和白细胞介素6)水平,具有抗炎作用。此外,诺米林可通过抑制促炎细胞因子白细胞介素6基因表达发挥抗炎能力,进而缓解小鼠非酒精性脂肪性肝炎和肝纤维化[69]。大量研究表明柑橘苦味化合物具有抗炎与抑菌效果,而大多数的炎症性疾病由病原体感染和组织损伤造成,因此,利用柑橘苦味化合物控制早期异常免疫反应的发展是治疗炎症性疾病的一种非常有效的手段。但柑橘中苦味化合物对炎症性疾病治疗效果的通路机制还缺少系统、全面的理论分析。
3.2 降血糖与降脂
黄酮类化合物和类柠檬苦素化合物可以干预多糖分解及葡萄糖吸收,通过调节血糖、血脂水平发挥预防与治疗糖尿病和控制脂肪积累作用。例如,柑橘中的柚皮苷可通过降低氧化应激、减少链脲佐菌素诱导的糖尿病大鼠促炎细胞因子产生改善其血糖状态,从而发挥心肌保护作用[70]。采用以新橙皮苷和柚皮苷为主要物质的佛手柑果实提取物处理HepG2肝癌细胞,结果表明,新橙皮苷可能通过下调3-羟基-3-甲基戊二酰辅酶A还原酶基因的表达抑制胆固醇的合成和吸收,进而降低胆固醇水平[71]。Wu Wangling等[72]发现补充柠檬苦素可显著降低高脂饮食诱导血脂异常小鼠的血脂水平,显著抑制高脂饮食引起的体质量增加和附睾脂肪积累。
3.3 抗癌与抗心血管疾病
柚皮苷和新橙皮苷在体外和体内可通过几种细胞信号通路抑制多种癌细胞生长[73-74]。此外,更有研究[75]表明,柚皮苷和柚皮素与其他药物联合治疗可协同增强其抗癌活性,同时减少其他化疗药物因剂量依赖性引起的毒副作用,证明柚皮苷和柚皮素糖苷配体与其他药物联合疗法比单一疗法效果更佳,因此化合物间的协同作用可作为促进人类健康的研究重点。血管内皮是血液循环和机体组织之间的主要连接桥梁,与心血管健康密切相关。柑橘提取物中的柚皮苷通过调节血管内皮细胞分泌NO信号,抑制血管平滑肌细胞增殖,促进动脉血管扩张和血管内血流顺畅,发挥心脏保护作用[76]。喂食柠檬苦素可降低Nω-硝基-L-精氨酸甲酯诱导高血压大鼠的血压,降低高血压大鼠组织和循环中血管紧张素II水平,提高血管紧张素转化酶2活性,证明柠檬苦素具有抗高血压作用,可作为治疗心血管疾病的潜在药物[77]。
3.4 其他功能活性
除上述功能活性外,柑橘提取物中的苦味物质还具有缓解过敏、保护肝脏、保护神经系统、抗病毒等作用[78]。通过明暗箱、高架十字迷宫等实验研究发现,富含柚皮苷(200 mg/kg)的葡萄柚果皮提取物口服给药对小鼠表现出显著的抗焦虑和抗抑郁作用,葡萄柚提取物中柚皮苷可能是抗焦虑和抗抑郁的潜在药物[79]。最近有研究[71]表明,柚皮素和柚皮苷对多种新型冠状病毒肺炎后遗症具有缓解作用,具有作为新冠肺炎治疗药物的潜力。
4 柑橘加工过程中的脱苦技术
果汁是柑橘主流加工产品,其脱苦加工技术分为热处理和非热处理。热处理法因其低成本、易操作的优点在工厂生产环节中应用最多。热处理能同时实现杀菌和灭酶,但会破坏鲜榨柑橘汁中囊泡、质粒体小球和淀粉粒,加速柑橘汁中延迟苦味的出现,降低柚子汁的营养价值,因此柑橘果汁加热处理脱苦效果差。非热处理方法对果汁营养成分的影响相对较小,且能够针对性地分离和去除苦味物质,因此成为当前研究热点。目前研究较多的非热处理方法有苦味掩盖、吸附分离、改变苦味物质结构等。
4.1 苦味抑制剂掩盖
苦味是由苦味受体介导的,苦味抑制剂与苦味受体结合引起苦味受体结构改变,中止苦味信号传递,苦味被降低或消除[44]。添加苦味抑制剂可以通过掩盖苦味化合物后苦味的方式,提高苦味阈值,从而淡化苦味。常见的苦味抑制剂有β-环糊精、新地奥明和阿魏酸等。阿魏酸能够有效抑制甜菊糖苷、咖啡、糖精钠等多种物质的苦味,同时不影响物质的基本口味。但阿魏酸苦味抑制效果有限,浓度较高时会出现酸涩味和苦味。但目前发现的苦味抑制剂种类较少,限制了苦味抑制剂在食品加工中的广泛应用[80]。
4.2 苦味物质吸附分离
利用吸附剂吸附苦味物质脱苦是目前食品行业中使用最多的方法,具有成本低、设备简单、操作简单的优点。其原理是吸附剂通过离子交换或借助范德华力吸附部分或全部苦味物质。目前常用的吸附剂包括活性炭、离子交换树脂、硅胶等[81]。赵洋溢[82]采用5 种树脂对黄果柑酒进行脱苦处理,发现在树脂用量3.2%(m/m)、脱苦时间29 min、脱苦温度20 ℃时,黄果柑酒的脱苦效果和口感最佳。树脂用量越大,比表面积越大,脱苦效果越好;但随着树脂用量的增加,营养物质和风味物质也会被吸附,使得产品品质下降。通过树脂洗脱去除苦味化合物在需要保留苦味化合物时表现出局限性。另外,由于吸附材料需符合食品安全规范,吸附技术的使用范围也较为有限。
4.3 改变苦味化合物结构
苦味化合物结构改变会引起其味觉特征和阈值变化。例如,橙皮苷与新橙皮苷为同分异构体,但是前者无味,后者具有苦味[9]。基于此,酶法脱苦利用特定的酶作用于相应的苦味物质,使之转化为无苦味化合物[81]。脱苦酶按作用对象不同可分为黄烷酮糖苷类化合物脱苦酶和柠檬苦素类化合物脱苦酶,前者主要是柚皮苷酶,可以将柚皮苷水解成无苦味的柚皮素、葡萄糖、鼠李糖和普鲁宁;后者主要包括柠檬苦素环氧酶、柠檬苦素醇脱氢酶、反式消除酶等。柠檬苦素降解酶在果汁酸性条件下易失活,限制了其在生产中的应用,将生产柠檬苦素降解酶细胞进行固定化能够解决这一问题。酶法脱苦具有专一性强、效果好、不干扰其他成分、操作简单等优点,是目前较为理想的脱苦方法。刘伟[83]使用酶法和大孔吸附树脂对柑橘果汁进行脱苦,结果表明,酶法脱苦对柚皮苷的脱除率高于树脂吸附法。但酶法脱苦需要提取、纯化脱苦酶,步骤复杂且成本较高,同时脱苦酶及产脱苦酶菌种研究还停留在实验室阶段。
以上脱苦方法中,苦味抑制剂掩盖最简便、应用最多,但对人体健康有影响;吸附分离法和酶法脱苦效果好,具有专一性,但均有一定的操作难度,缺少安全性研究,工厂应用少,可以进一步深入研究。除上述脱苦技术外,还有一些新型的脱苦技术,如代谢法脱苦、膜分离脱苦、超临界CO2脱苦、基因工程脱苦等。多种脱苦技术联合应用可以弥补单一技术缺陷。Fayoux等[84]对比不同薄膜的脱苦效果发现,增塑聚氯乙烯是去除柠檬苦素效果最好的材料,然而塑料材料的安全性及回收再利用可能性还有待研究。此外,这些新型脱苦技术大多仍停留在实验室阶段,运用到工业化生产还需考虑成本、技术难度和安全性问题。随着研究的深入,新型技术和材料不断被开发,脱苦技术还有很大的发展前景。
5 结 语
苦味作为味觉的一种,在生活中存在“良药苦口”的说法,更是中药药性理论的特征之一,被中药学认为“能泄、能燥、能坚”,具有清热泻火、降气平喘、降逆止呕、通泄大便、清热燥湿、泻火存阴等功效。柑橘中的苦味物质主要分为黄烷酮和类柠檬苦素化合物2 类,具有抗菌、抗炎、抗癌、降血糖、降脂等保健作用。对柑橘苦味物质的结构特征、合成机制、功能活性及其加工产品主要脱苦技术进行研究,有助于柑橘新品种的培育和相关保健食品开发,为柑橘产业高质量发展提供理论支撑。
近年来对柑橘果实苦味物质的研究取得了一定的成果,但总体而言,柑橘果实苦味物质的保留利用研究还不够深入,还有一些方面需要进一步深入研究:1)除苦味物质外,柑橘果实中含有的其他苦味成分,如儿茶素、精氨酸、没食子酸、异甘草素等对柑橘苦味的贡献如何;2)柑橘果实中苦味物质结构与苦味程度、生物活性之间的关系,不同官能团对应的作用机制等需要进一步阐明;3)柑橘果实中主要苦味物质均已被证明具有一系列生物活性,进而在一些疾病治疗中发挥积极作用。然而,在生物活性发挥中,这些苦味物质与其他主要成分之间是否存在协同或拮抗作用,其量效关系还有待揭示;4)从柑橘果实中提取苦味物质生产药剂,是减轻化学合成途径药物毒副作用的有效手段,因此,一方面需要针对柑橘苦味成分如柚皮苷、新橙皮苷等开展提取、分离纯化技术研究,另一方面,可通过基因调控代谢物合成途径中相关酶的活性,有效增加苦味物质在果实成熟过程中的积累,拓宽苦味物质的有效来源;5)当下人们更加重视膳食平衡,如何在最大程度保留柑橘营养和功能的同时降低产品苦味是柑橘加工产品脱苦研究的中心问题。苦味抑制剂掩盖、苦味物质吸附分离、改变苦味物质结构等技术各有其优缺点。非热处理加工技术是目前主要的研究方向,针对特定苦味成分的靶向定点包埋缓释技术有望成为研究热点;6)柑橘育种目标与大多数水果一样,主要朝着色泽艳丽、无核、高糖、风味浓郁方向发展,但如今,更多人群倾向于选择风味独特、具备保健作用的食品,尤其是糖尿病患者等特殊人群对低糖、适度苦味兼具保健功效的水果消费需求更高。因此,不能一味追求去除柑橘果实苦味物质,应合理、适度保留天然苦味物质,不断提高消费者对柑橘苦味的认知度和接受度。
[1] CHRISTOFIDES S R, SETAREHNEJAD A, FAIRCHILD R, et al.Cross-cultural differences between Italian and UK consumer preferences for ‘Big Top’ nectarines in relation to cold storage[J].Foods, 2022, 11(16): 2424. DOI:10.3390/foods11162424.
[2] ZOU S C, WU J C, SHAHID M Q, et al. Identification of key taste components in loquat using widely targeted metabolomics[J]. Food Chemistry, 2020, 323: 126822. DOI:10.1016/j.fitote.2020.104543.
[3] SUN Q R, HU S Y, LOU Z H, et al. The macrophage polarization in inflammatory dermatosis and its potential drug candidates[J].Biomedicine & Pharmacotherapy, 2023, 161: 114469. DOI:10.1016/j.biopha.2023.114469.
[4] SHI Q Q, LI X, DU J T, et al. Association of bitter metabolites and flavonoid synthesis pathway in jujube fruit[J]. Frontiers in Nutrition,2022, 9: 901756. DOI:10.3389/fnut.2022.901756.
[5] CHEN L F, LIN Y L, YAN X, et al. 3D-QSAR studies on the structurebitterness analysis of citrus flavonoids[J]. Food & Function, 2023,14(10): 4921-4930. DOI:10.1039/d3fo00601h.
[6] ZHU J Y, XU Q S, ZHAO S Q, et al. Comprehensive co-expression analysis provides novel insights into temporal variation of flavonoids in fresh leaves of the tea plant (Camellia sinensis)[J]. Plant Science,2020, 290: 110306. DOI:10.1016/j.plantsci.2019.110306.
[7] OLADOKUN O, TARREGA A, JAMES S, et al. The impact of hop bitter acid and polyphenol profiles on the perceived bitterness of beer[J]. Food Chemistry, 2016, 205: 212-220. DOI:10.1016/j.foodchem.2016.03.023.
[8] GAO C Y, TELLO E, PETERSON D G. Identification of compounds that enhance bitterness of coffee brew[J]. Food Chemistry, 2023, 415:135674. DOI:10.1016/j.foodchem.2023.135674.
[9] 黄岩, 史伊格, 梁莉, 等. 食品中苦味物质的感知与调控研究进展[J].食品科学, 2023, 44(11): 185-195. DOI:10.7506/spkx1002-6630-20220624-275.
[10] FIALLOS-JURADO J, POLLIER J, MOSES T, et al. Saponin determination, expression analysis and functional characterization of saponin biosynthetic genes in Chenopodium quinoa leaves[J]. Plant Science, 2016, 250: 188-197. DOI:10.1016/j.plantsci.2016.05.015.
[11] SÁNCHEZ-PÉREZ R, JØRGENSEN K, OLSEN C E, et al.Bitterness in almonds[J]. Plant Physiology, 2008, 146(3): 1040-1052.DOI:10.1104/pp.107.112979.
[12] DENG Y Y, MA Y X, LIU H J, et al. Structure determination,bitterness evaluation and hepatic gluconeogenesis inhibitory activity of triterpenoids from the Momordica charantia fruit[J]. Food Chemistry,2022, 372: 131224. DOI:10.1016/j.foodchem.2021.131224.
[13] 中国科学院中国植物志编辑委员会. 中国植物志[M]. 北京: 科学出版社, 1993.
[14] CHEN J B, LIU Y, WANG H X, et al. Polymethoxyflavone-enriched fraction from Ougan (Citrus reticulata cv. Suavissima) attenuated diabetes and modulatedgut microbiota in diabetic KK-Ay mice[J].Journal of Agricultural and Food Chemistry, 2023, 71(18): 6944-6955.DOI:10.1021/acs.jafc.2c08607.
[15] 宋雪, 王增斌, 包俊文, 等. 基于水蒸气蒸馏法的狮头柑精油提取工艺优化及成分分析[J]. 食品工业科技, 2022, 43(14): 233-242.DOI:10.13386/j.issn1002-0306.2021100182.
[16] SHAN Y. Comprehensive utilization of citrus by-products[M]. London:Academic Press, 2017.
[17] 张娜威, 潘思轶, 范刚, 等. 柑橘果汁中的苦味物质及脱苦技术研究进展[J]. 华中农业大学学报, 2021, 40(1): 40-48. DOI:10.13300/j.cnki.hnlkxb.2021.01.005.
[18] 毕静莹, 李华, 王华. 柑橘中苦味物质对HeLa细胞增殖与凋亡的作用机制[J]. 食品科学, 2019, 40(19): 224-230. DOI:10.7506/spkx1002-6630-20181008-027.
[19] JIANG B T, WANG Z K, SHI X J, et al. Stereoselective separation,configuration determination, and quantification of flavanone glycosides in citrus using chiral HPLC-UV in combination with CD spectra[J].Analytical Methods, 2023, 15(46): 6444-6450. DOI:10.1039/d3ay01654d.
[20] CSUTI A, SIK B, AJTONY Z. Measurement of naringin from citrus fruits by high-performance liquid chromatography: a review[J].Critical Reviews in Analytical Chemistry, 2024, 54(3): 473-486. DOI:10.1080/10408347.2022.2082241.
[21] NATARAJAN S, EVELEIGH D E, DAWSON R H. A nature source for neohesperidin[J]. Economic Botany, 1976, 30(1): 38. DOI:10.1007/BF02866782
[22] 周心悦, 周逸辰, 陈晋, 等. 胡柚及其苦味黄烷酮对糖脂代谢相关疾病的调节功能研究进展[J]. 中国食品添加剂, 2022, 33(12): 41-49.DOI:10.19804/j.issn1006-2513.2022.12.006.
[23] TRIPOLI E, LA GUARDIA M, GIAMMANCO S, et al. Citrus flavonoids: molecular structure, biological activity and nutritional properties: a review[J]. Food Chemistry, 2007, 104(2): 466-479.DOI:10.1016/j.foodchem.2006.11.054.
[24] LI L J, YAN X, CHEN F Y, et al. A comprehensive review of the metabolism of citrus flavonoids and their binding to bitter taste receptors[J]. Comprehensive Reviews in Food Science and Food Safety, 2023, 22(3): 1763-1793. DOI:10.1111/1541-4337.13129.
[25] ZHU C Q, CHEN J B, ZHAO C N, et al. Advances in extraction and purification of citrus flavonoids[J]. Food Frontiers, 2023, 4(2): 750-781. DOI:10.1002/fft2.236.
[26] 徐贵华, 刘东红, 李波, 等. 柑橘果皮中类黄酮组成与抗氧化能力研究[J]. 食品工业科技, 2015, 36(16): 114-117. DOI:10.13386/j.issn1002-0306.2015.16.015.
[27] 胡阳, 晏幸, 伍菱, 等. 琯溪蜜柚幼果中柚皮苷含量变化规律[J].食品科学, 2021, 42(12): 159-165. DOI:10.7506/spkx1002-6630-20200423-307.
[28] 张念, 彭怡霖, 陈细羽, 等. 不同成熟期琯溪蜜柚果实功能成分的差异分析[J]. 果树学报, 2022, 39(6): 1042-1053. DOI:10.13925/j.cnki.gsxb.20210627.
[29] GUPTA A K, DHUA S, SAHU P P, et al. Variation in phytochemical,antioxidant and volatile composition of pomelo fruit (Citrus grandis(L.) Osbeck) during seasonal growth and development[J]. Plants, 2021,10(9): 1941. DOI:10.3390/plants10091941.
[30] LIU H F, LIANG C R, MA L K, et al. Analysis of antioxidant response in pomelo fruitlets subjected to external injury stress: significance of naringin biosynthesis[J]. LWT-Food Science and Technology, 2021,150: 111908. DOI:10.1016/j.lwt.2021.111908.
[31] DURAN-PENA M J, BOTUBOL-ARES J M, COLLADO I G, et al.Degraded limonoids: biologically active limonoid fragments re-enhancing interest in Meliaceae and Rutaceae sources[J]. Phytochemistry Reviews,2023, 22(3): 695-741. DOI:10.1007/s11101-023-09856-1.
[32] FU S M, LIU B. Recent progress in the synthesis of limonoids and limonoid-like natural products[J]. Organic Chemistry Frontiers, 2020,7(14): 1903-1947. DOI:10.1039/d0qo00203h.
[33] ROY A, SARAF S. Limonoids: overview of significant bioactive triterpenes distributed in plants kingdom[J]. Biological & Pharmaceutical Bulletin, 2006, 29(2): 191-201. DOI:10.1248/bpb.29.191.
[34] WANG F S, YU X H, LIU X N, et al. Temporal and spatial variations on accumulation of nomilin and limonin in the pummelos[J]. Plant Physiology and Biochemistry, 2016, 106: 23-29. DOI:10.1016/j.plaphy.2016.04.039.
[35] LI S J, WANG Z, DING F, et al. Content changes of bitter compounds in ‘Guoqing No.1’ satsuma mandarin (Citrus unshiu Marc.) during fruit development of consecutive 3 seasons[J]. Food Chemistry, 2014,145: 963-969. DOI:10.1016/j.foodchem.2013.09.040.
[36] ZHAO X N, WANG Y, WANG Y R, et al. Investigation the differences in key taste-contributing substances between Shitougan (Citrus reticulata Blanco cv. Manau Gan) and other citrus varieties[J]. Journal of Food Measurement and Characterization, 2024, 18: 6074-6086.DOI:10.1007/s11694-024-02630-7.
[37] OHTA H, HASEGAWA S. Limonoids in pummelos [Citrus grandis(L.) Osbeck][J]. Journal of Food Science, 1995, 60(6): 1284-1285.DOI:10.1111/j.1365-2621.1995.tb04574.x.
[38] 秦芸桦, 钟世欢, 陈青俊, 等. 分散固相萃取-液相色谱-串联质谱法测定不同品种柑橘果实不同部位中3 种柠檬苦素类似物的含量[J].理化检验-化学分册, 2024, 60(2): 171-179. DOI:10.11973/lhjyhx202402007.
[39] 宣晓婷, 朱麟, 沈波涛, 等. 红美人柑橘幼果生长期营养物质及苦味物质变化规律[J]. 食品安全质量检测学报, 2022, 13(11): 3557-3565.DOI:10.19812/j.cnki.jfsq11-5956/ts.2022.11.014.
[40] CHEBROLU K K, JAYAPRAKASHA G K, JIFON J, et al. Production system and storage temperature influence grapefruit vitamin C,limonoids, and carotenoids[J]. Journal of Agricultural and Food Chemistry, 2012, 60(29): 7096-7103. DOI:10.1021/jf301681p.
[41] BALDWIN E, PLOTTO A, MANTHEY J, et al. Effect of liberibacter infection (Huanglongbing disease) of citrus on orange fruit physiology and fruit/fruit juice quality: chemical and physical analyses[J].Journal of Agricultural and Food Chemistry, 2010, 58(2): 1247-1262.DOI:10.1021/jf9031958.
[42] WANG Q B, WANG Y P, SUN H H, et al. Transposon-induced methylation of the RsMYB1 promoter disturbs anthocyanin accumulation in red-fleshed radish[J]. Journal of Experimental Botany,2020, 71(9): 2537-2550. DOI:10.1093/jxb/eraa010.
[43] DONG N Q, LIN H X. Contribution of phenylpropanoid metabolism to plant development and plant-environment interactions[J]. Journal of Integrative Plant Biology, 2021, 63(1): 180-209. DOI:10.1111/jipb.13054.
[44] 蒲明慧, 吴昊, 文李, 等. 苦味肽的苦味机制及脱苦策略研究进展[J].食品科学, 2024, 45(21): 344-356. DOI:10.7506/spkx1002-6630-20240306-041.
[45] WOHL J, PETERSEN M. Functional expression and characterization of cinnamic acid 4-hydroxylase from the hornwort Anthoceros agrestis in Physcomitrella patens[J]. Plant Cell Reports, 2020, 39(5): 597-607.DOI:10.1007/s00299-020-02517-z.
[46] ZHANG X B, ABRAHAN C, COLQUHOUN T A, et al. A proteolytic regulator controlling chalcone synthase stability and flavonoid biosynthesis in Arabidopsis[J]. The Plant Cell, 2017, 29(5): 1157-1174. DOI:10.1105/tpc.16.00855.
[47] LIU W X, FENG Y, YU S H, et al. The flavonoid biosynthesis network in plants[J]. International Journal of Molecular Sciences, 2021, 22(23):12824. DOI:10.3390/ijms222312824.
[48] YIN Y C, ZHANG X D, GAO Z Q, et al. The research progress of chalcone isomerase (CHI) in plants[J]. Molecular Biotechnology,2019, 61(1): 32-52. DOI:10.1007/s12033-018-0130-3.
[49] FRYDMAN A, WEISSHAUS O, HUHMAN D V, et al. Metabolic engineering of plant cells for biotransformation of hesperedin into neohesperidin, a substrate for production of the low-calorie sweetener and flavor enhancer NHDC[J]. Journal of Agricultural and Food Chemistry, 2005, 53(25): 9708-9712. DOI:10.1021/jf051509m.
[50] CHEN J J, LI G, ZHANG H P, et al. Primary bitter taste of citrus is linked to a functional allele of the 1,2-rhamnosyltransferase gene originating from citrus grandis[J]. Journal of Agricultural and Food Chemistry, 2021, 69(34): 9869-9882. DOI:10.1021/acs.jafc.1c01211.
[51] 王刚, 蔡才, 王亚珍, 等. 新橙皮苷二氢查耳酮的合成工艺及应用进展[J]. 江汉大学学报(自然科学版), 2020, 48(1): 37-44.DOI:10.16389/j.cnki.cn42-1737/n.2020.01.005.
[52] BAR-PELED M, LEWINSOHN E, FLUHR R, et al. UDP-rhamnose:flavanone-7-O-glucoside-2”-O-rhamnosyltransferase.Purification and characterization of an enzyme catalyzing the production of bitter compounds in citrus[J]. Journal of Biological Chemistry, 1991,266(31): 20953-20959. DOI:10.1016/S0021-9258(18)54803-1.
[53] FRYDMAN A, WEISSHAUS O, BAR-PELED M, et al. Citrus fruit bitter flavors: isolation and functional characterization of the gene Cm1,2RhaT encoding a 1,2 rhamnosyltransferase, a key enzyme in the biosynthesis of the bitter flavonoids of citrus[J]. The Plant Journal,2004, 40(1): 88-100. DOI:10.1111/j.1365-313X.2004.02193.x.
[54] CHEN J J, YUAN Z Y, ZHANG H P, et al. Cit1,2RhaT and two novel CitdGlcTs participate in flavor-related flavonoid metabolism during citrus fruit development[J]. Journal of Experimental Botany, 2019,70(10): 2759-2771. DOI:10.1093/jxb/erz081.
[55] VRANOVA E, COMAN D, GRUISSEM W. Network analysis of the MVA and MEP pathways for isoprenoid synthesis[J]. Annual Review of Plant Biology, 2013, 64(1): 665-700. DOI:10.1146/annurevarplant-050312-120116.
[56] FU J Y, LIU G H, YANG M, et al. Isolation and functional analysis of squalene synthase gene in tea plant Camellia sinensis[J]. Plant Physiology and Biochemistry, 2019, 142: 53-58. DOI:10.1016/j.plaphy.2019.06.030.
[57] WANG F S, WANG M, LIU X N, et al. Identification of putative genes involved in limonoids biosynthesis in citrus by comparative transcriptomic analysis[J]. Frontiers in Plant Science, 2017, 8: 782.DOI:10.3389/fpls.2017.00782.
[58] 张盼. CiMYB42对柑橘类柠檬苦素生物合成的调控机制[D]. 重庆:西南大学, 2020. DOI:10.27684/d.cnki.gxndx.2020.000072.
[59] CERAOLO C R, VAZQUEZ V, MIGUES I, et al. Flavonoids and limonoids profiles variation in leaves from mandarin cultivars and its relationship with alternate bearing[J]. Agronomy, 2022, 12(1): 121.DOI:10.3390/agronomy12010121.
[60] 王福生, 刘晓纳, 徐媛媛, 等. 柑橘SQS基因的克隆及功能分析[J].园艺学报, 2021, 48(9): 1641-1652. DOI:10.16420/j.issn.0513-353x.2021-0580.
[61] ZHANG P, LIU X F, YU X, et al. The MYB transcription factor CiMYB42 regulates limonoids biosynthesis in citrus[J]. BMC Plant Biology, 2020, 20(1): 254. DOI:10.1186/s12870-020-02475-4.
[62] 余洪, 易倩, 张曼曼, 等. CclSAUR49基因的表达特征及对类柠檬苦素生物合成的影响[J]. 果树学报, 2021, 38(8): 1240-1251.DOI:10.13925/j.cnki.gsxb.20210126.
[63] SHAN Y. Peeling back the science of citrus fruits[EB/OL]. (2023-06-15) [2024-08-12]. https://www.nature.com/articles/d42473-023-00172-y.
[64] HILMAYANTI E, NURLELASARI, SUPRATMAN U, et al. Limonoids with anti-inflammatory activity: a review[J]. Phytochemistry, 2022, 204:113469. DOI:10.1016/j.phytochem.2022.113469.
[65] WANG R, WU N X, ZHAN D A, et al. Naringin exerts antibacterial and anti-inflammatory effects on mice with Staphylococcus aureusinduced osteomyelitis[J]. Journal of Biochemical and Molecular Toxicology, 2024, 38(7): e23753. DOI:10.1002/jbt.23753.
[66] HE D W, GAO X Y, WEN J R, et al. Orally administered neohesperidin attenuates MPTP-induced neurodegeneration by inhibiting inflammatory responses and regulating intestinal flora in mice[J]. Food &Function, 2024, 15(3): 1460-1475. DOI:10.1039/d3fo04714h.
[67] SILVA S A V D, CLEMENTE A, ROCHA J, et al. Anti-inflammatory effect of limonin from cyclodextrin (un)processed orange juices in in vivo acute inflammation and chronic rheumatoid arthritis models[J].Journal of Functional Foods, 2018, 49: 146-153. DOI:10.1016/j.jff.2018.08.024.
[68] LIU S J, ZHANG S F, LÜ X Y, et al. Limonin ameliorates ulcerative colitis by regulating STAT3/miR-214 signaling pathway[J].International Immunopharmacology, 2019, 75: 105768. DOI:10.1016/j.intimp.2019.105768.
[69] HAN Y L, LUO L L, LI H L, et al. Nomilin and its analogue obacunone alleviate NASH and hepatic fibrosis in mice via enhancing antioxidant and anti-inflammation capacity[J]. Biofactors, 2023, 49(6):1189-1204. DOI:10.1002/biof.1987.
[70] 杨丽, 张侃迪, 张俊峰. 柚皮苷对糖尿病大鼠心肌缺血再灌注损伤的保护作用[J]. 中西医结合心脑血管病杂志, 2023, 21(22): 4106-4111. DOI:10.12102/j.issn.1672-1349.2023.22.008.
[71] HUANG Y, TOCMO R, NAUMAN M C, et al. Defining the cholesterol lowering mechanism of bergamot (Citrus bergamia) extract in HepG2 and Caco-2 cells[J]. Nutrients, 2021, 13(9): 3156. DOI:10.3390/nu13093156.
[72] WU W L, PAN Y Y, ZHENG T Y, et al. Limonin alleviates high-fat diet-induced dyslipidemia by regulating the intestinal barrier via the microbiota-related ILC3-IL22-IL22R pathway[J]. Food & Function,2024, 15(5): 2679-2692. DOI:10.1039/d3fo04530g.
[73] 王树斌. 新橙皮苷通过ROS/JNK信号通路诱导人骨肉瘤细胞周期停滞、凋亡和自噬[D]. 厦门: 厦门大学, 2021. DOI:10.27424/d.cnki.gxmdu.2021.003450.
[74] MEMARIANI Z, ABBAS S Q, HASSAN S S U, et al. Naringin and naringenin as anticancer agents and adjuvants in cancer combination therapy: efficacy and molecular mechanisms of action, a comprehensive narrative review[J]. Pharmacological Research, 2021,171: 105264. DOI:10.1016/j.phrs.2020.105264.
[75] RAEISI S, CHAVOSHI H, MOHAMMADI M, et al. Naringeninloaded nano-structured lipid carrier fortifies oxaliplatin-dependent apoptosis in HT-29 cell line[J]. Process Biochemistry, 2019, 83: 168-175. DOI:10.1016/j.procbio.2019.05.013.
[76] PENG Y, QU R Y, XU S Q, et al. Regulatory mechanism and therapeutic potentials of naringin against inflammatory disorders[J].Heliyon, 2024, 10(3): e26419. DOI:10.1016/j.heliyon.2024.e24619.
[77] IAMPANICHAKUL M, POTUE P, RATTANAKANOKCHAI S, et al.Limonin ameliorates cardiovascular dysfunction and remodeling in hypertensive rats[J]. Life Sciences, 2023, 327: 121834. DOI:10.1016/j.lfs.2023.121834.
[78] YANG W L, LIANG Y Y, LIU Y J, et al. Enhancement of hepatoprotective activity of limonin from citrus seeds against acetaminophen-induced liver injury by HSCCC purification and liposomal encapsulation[J]. Fitoterapia, 2024, 175: 105899.DOI:10.1016/j.fitote.2024.105899.
[79] HERNÁNDEZ-VÁZQUEZ L, CASSANI J, HEYERDAHL-VIAU I,et al. Recovery of naringin-rich flavonoid extracts from agroresidues with anxiolytic- and antidepressant-like effects in mice[J]. Molecules,2022, 27(23): 8507. DOI:10.3390/molecules27238507.
[80] 方子超, 周隽涵, 郑建仙. 苦味抑制剂阿魏酸的构效关系[J]. 食品科学, 2024, 45(14): 14-22. DOI:10.7506/spkx1002-6630-20231123-179.
[81] 刘永安, 刘欣, 魏法山, 等. 柑橘类果汁脱苦技术研究进展[J]. 食品安全导刊, 2015(27): 137-138. DOI:10.16043/j.cnki.cfs.2015.27.086.
[82] 赵洋溢. 酵母菌株对黄果柑酒品质的影响及黄果柑酒吸附脱苦工艺优化研究[D]. 雅安: 四川农业大学, 2022. DOI:10.27345/d.cnki.gsnyu.2022.000491.
[83] 刘伟. 生物酶法脱除柑橘汁苦味的研究[D]. 长沙: 中南大学, 2009.DOI:10.7666/d.y1537044.
[84] FAYOUX S C, HERNANDEZ R J, HOLLAND R V. The debittering of navel orange juice using polymeric films[J]. Journal of Food Science,2007, 72(4): E143-E154. DOI:10.1111/j.1750-3841.2007.00283.x.