病原菌可通过食物、水、空气等多种方式进行传播,畜禽感染病原菌后多出现消化系统、呼吸系统、生殖系统等疾病,导致畜禽生长缓慢、肉质下降、生产性能降低甚至死亡,给养殖业造成了巨大的经济损失。目前对于畜禽细菌病多采用抗生素进行治疗,但近些年,抗生素的不规范使用造成了细菌普遍耐药,以及肉、蛋、奶等食品中抗生素严重残留[1]。因此,亟需筛选或研发抑菌效果明显、不易产生耐药性的兽用中药或饲料添加剂。藤茶作为一种绿色安全的药用植物,具有广泛的生物学活性[2-3]。藤茶中含有黄酮类、多酚、多糖类、萜类等多种活性成分,其中黄酮类化合物是藤茶的主要活性成分。藤茶中黄酮类化合物包括二氢杨梅素、槲皮素、杨梅素、杨梅苷等[4-5]。近年来研究表明,黄酮类化合物具有较为显著的生物学活性,如抑菌、抗炎、抗氧化、抗肿瘤等[6-7]。研究发现,藤茶提取物及活性成分对金黄色葡萄球菌、大肠杆菌、沙门氏菌等细菌有较强的体内外抑菌效果[8-9]。如Liang Haiyun等[10]研究发现,藤茶提取物可改变金黄色葡萄球菌的形态、抑制总蛋白的表达及降低能量代谢相关酶的活性。同时研究表明,二氢杨梅素对耐甲氧西林金黄色葡萄球菌的耐药性具有消减作用[11],并可通过下调生存素诱导细胞凋亡,进而逆转对卵巢癌症细胞的多药耐药性[12]。此外,藤茶及其活性成分还可通过调节机体肠道菌群的多样性和丰度进而调节机体机能[13]。
目前对于藤茶中黄酮类化合物的研究主要集中于抗肿瘤和抗肝损伤方面[14-17],对于其抑菌的作用及机制研究鲜有报道。本研究通过网络药理学、分子对接技术及体外实验筛选和分析藤茶中黄酮类化合物抑菌的活性物质、相关靶点及可能的机制,旨在为藤茶黄酮类物质在畜禽抗生素替代方面提供理论基础。
1 材料与方法
1.1 材料与试剂
大肠杆菌、沙门氏菌各5 株,由铜仁职业技术学院鸡场分离纯化所得。
营养琼脂培养基、二氢杨梅素、二甲基亚砜(dimethyl sulfoxide,DMSO)、磷酸盐缓冲液(phosphate buffered saline,PBS) 上海麦克林生化科技股份有限公司。
1.2 仪器与设备
BN-200高精密电子天平 中国台湾巨林樱花企业;BA210Digital生物显微镜 厦门市麦克奥迪实业集团有限公司;JSM-IT700HR扫描电镜、JEM-1400 FLASH透射电镜 日本电子公司。
1.3 方法
1.3.1 网络药理学与分子对接分析
1.3.1.1 藤茶黄酮类化合物成分及靶点筛选
以“藤茶”“藤茶黄酮”“藤茶成分”“显齿蛇葡萄黄酮”“Ampelopsis flavone”为关键词,在中国知网、万方、PubMed等数据库检索汇总藤茶黄酮得有效成分,通过TCMSP数据库,以类药性(druglike properties,DL)≥0.1、口服生物利用度(oral bioavailability,OB)≥30%的条件进行筛选,以得到藤茶黄酮类化合物的药效成分。
1.3.1.2 藤茶黄酮类化合物抑菌靶点及疾病靶点筛选
将1.3.1.1节所得有效成分的CAS号转化为相应的SMILES字符,在TCMSP、DrugBank、SwissTargetPrediction等数据库中进行检索,得到藤茶黄酮类化合物的有效成分潜在靶点。以bacteriostat为关键词,在GeneGards中检测相关疾病靶点。利用在线Venny 2.1.0平台分别导入藤茶黄酮类化合物和抑菌的靶点,取交集,获得共同靶点,绘制Venn图。交集部分即为藤茶黄酮类化合物抑菌可能的靶点。
1.3.1.3 藤茶黄酮类化合物药物-活性成分-靶点网络构建
将药物、活性成分、潜在靶点导入Cytoscape 3.9.1软件,构建药物-活性成分-靶点网络,寻找重要的候选成分。选取排名靠前活性成分,这些活性成分可能就是藤茶黄酮类化合物核心活性成分。
1.3.1.4 藤茶黄酮类化合物蛋白质-蛋白质相互作用网络构建
将交集靶点导入String(https://string-db.org/)数据库,选择种属“Homo saoiens”,置信区间>0.4。将文件导入Cytoscape 3.9.1软件中,构建蛋白相互作用网络,用“Analyze Network”功能进行网络分析,计算网络中所有节点的度值(degree),筛选出排名靠前的靶点。度值大的靶点很可能是藤茶黄酮类化合物的核心靶点。
1.3.1.5 藤茶黄酮类化合物抑菌靶点基因本体论(Gene Ontology,GO)富集分析和京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)通路富集分析
通过DAVID网站(https://david.ncifcrf.gov/)对得到的潜在作用靶点进行GO富集分析和KEGG信号通路富集分析,得到的分析结果GO以P<0.05为标准进行筛选,KEGG以P<0.05为标准进行筛选,并按照富集基因数目进行排序,分别选取前100 个条目,绘制柱状图和气泡图,找出涉及的主要生物过程(biological process,BP)、主要细胞组成(cellular component,CC)、主要分子功能(molecular function,MF)以及主要信号通路。
1.3.1.6 藤茶黄酮类化合物核心活性成分-靶点分子对接验证
从PubChem数据库中获取藤茶黄酮类化合物核心成分2D结构,利用Chem3D 19.0.0.22软件转换格式为mol2。在RCSB PDB数据库(https://www.rcsb.org/)中进行蛋白构象筛选并下载PDB格式的3D结构,筛选条件应满足蛋白结构;蛋白结构通过X-晶体衍射得到;蛋白质晶体分辨率小于3 Å。导入PyMol软件进行去除水和小分子配体等处理,同时在Autodock Tools 1.5.7软件中进行加氢、加电荷、合并非极性氢等操作。最后通过AutoDock Vina 1.1.2软件进行分子对接。根据结合自由能将受体-配体对进行排序、筛选。当结合能小于—5 kcal/mol时可认为两者结合效果良好,当结合能小于—7 kcal/mol时则表明两者具有强烈的结合活性。最后,利用PyMol软件进行可视化处理。
1.3.2 二氢杨梅素体外抑菌性能表征
1.3.2.1 试剂及菌悬液的制备
二氢杨梅素溶液的制备:将40 mg二氢杨梅素溶于5 mL DMSO中,取2.4 mL原液加2.4 mL PBS进行二倍稀释;取2 倍稀释液2.4 mL加2.4 mL PBS,依次稀释至8 倍。溶剂对照按照上述方法进行稀释处理。以聚乙二醇为溶剂的制备方法同上。
菌悬液的制备:活化后的不同菌种通过平板划线法接种于固体培养基上,37 ℃培养12 h后,再挑取单菌落接种TSB液体培养基,37 ℃、240 r/min振荡培养12 h,采用0.5号麦氏比浊管将细菌浓度调整为1.5×108 CFU/mL,再用灭菌PBS稀释为1.0×108 CFU/mL。
1.3.2.2 抑菌圈直径的测定
取供试菌均匀涂布于固体培养基上,再采用牛津杯法分析不同药物的抑菌效果,每个牛津杯添加二氢杨梅素(200 μL/孔),并设溶剂对照,37 ℃培养24 h,测定抑菌圈直径。
1.3.2.3 最小抑菌浓度(minimal inhibit concentration,MIC)和最小杀菌浓度(minimum bactericidal concentration,MBC)测定
将二氢杨梅素用聚乙二醇溶解后,使用PBS在无菌96 孔培养板上进行倍比稀释,随后于第1~10孔和第12孔分别加入灭菌肉汤培养基和菌悬液各100 μL,样品及对照各设3 个重复。37 ℃培养24 h,同时设不加药物的阳性对照孔和不加菌的阴性对照孔,采用微量肉汤稀释法测定MIC,以肉眼观察无细菌生长沉淀形成的最低药物浓度判定为该药物的MIC。将MIC以上不同浓度的药液和菌液100 μL均匀涂布于营养琼脂培养基上,置于恒温培养箱中,37 ℃培养24 h,以平板上菌落数少于5 CFU为药物的MBC。
1.3.2.4 扫描电镜和透射电镜方法观察细菌形态
依据1.3.2.2节结果,筛选出二氢杨梅素抑菌效果明显的2 株菌,设置药物组和对照组,药物组为含1 MIC二氢杨梅素的菌液,对照组为等体积PBS的菌液,菌液浓度约5×106 CFU/mL,37 ℃、280 r/min振荡10 h培养至对数生长末期。将各组细菌3 000 r/min离心5 min收集细菌,PBS洗涤3 次,沉淀用PBS稀释至合适浓度,离心收集细菌至肉眼可见细菌沉淀为芝麻至绿豆大小,弃培养基后用PBS轻轻漂洗后,以体积分数2.5%戊二醛溶液预固定,质量分数1%四氧化锇溶液再固定,丙酮逐级脱水,脱水剂和包埋剂按照3∶1、1∶1、1∶3体积比依次渗透后用Epon-812纯包埋剂包埋,用超薄切片机制备60~90 nm超薄切片并捞至铜网上,然后先用醋酸铀染色10~15 min,再用柠檬酸铅染色1~2 min,采用JSMIT700HR扫描电镜、JEM-1400 FLASH透射电子显微镜对铜网进行图像采集,每张铜网先于低倍下观察全部组织,选择要观察的区域采集图片,观察具体病变。
2 结果与分析
2.1 藤茶黄酮类化合物成分筛选
通过TCMSP数据库,根据OB≥30%、DL≥0.1进行筛选,获得5 种主要活性成分,分别为杨梅素、山柰酚、槲皮素、橙皮素、芦丁。同时通过文献检索,发现二氢杨梅素和芹菜素亦为藤茶黄酮类主要活性成分[16,18-20],因此共获得7 种主要黄酮类化合物,分别为二氢杨梅素、杨梅素、山柰酚、槲皮素、芹菜素、橙皮素、芦丁(表1)。
表1 藤茶黄酮类化合物主要活性成分
Table 1 Major bioactive flavonoids in Ampelopsis
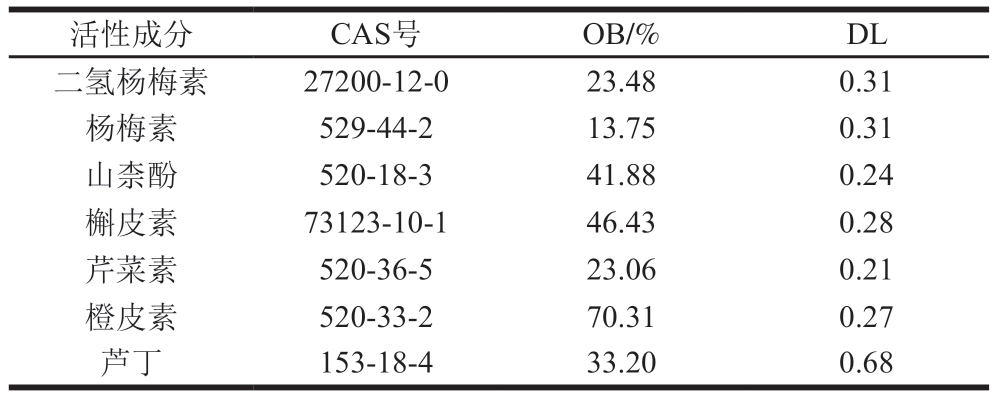
活性成分CAS号OB/%DL二氢杨梅素27200-12-023.480.31杨梅素529-44-213.750.31山柰酚520-18-341.880.24槲皮素73123-10-146.430.28芹菜素520-36-523.060.21橙皮素520-33-270.310.27芦丁153-18-433.200.68
2.2 藤茶黄酮类化合物抑菌靶点及疾病靶点筛选
通过SwissTargetPrediction数据库对上述成分进行作用靶点检索,并删除重复靶点,共计得到藤茶黄酮类化合物靶点208 个,以“bacteriostat”为关键词,在GeneGards数据库中检测相关疾病靶点,得到靶点147 个。藤茶黄酮类化合物靶点和抑菌靶点的共同靶点19 个(图1)。
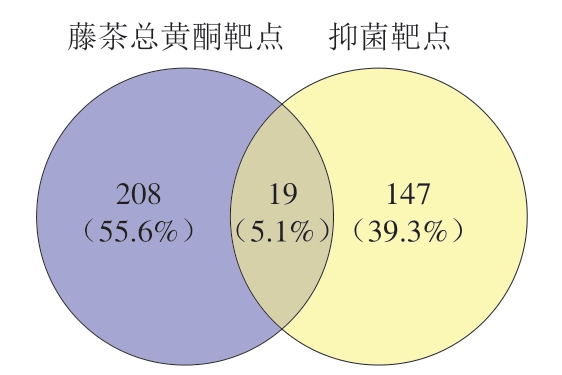
图1 藤茶黄酮类化合物-抑菌靶点Venn图
Fig. 1 Venn diagram showing the intersection between flavonoids from Ampelopsis and antibacterial targets
2.3 藤茶黄酮类化合物药物-活性成分-靶点网络构建
成分-疾病-靶点网络如图2所示,其中度值排名靠前的分别为二氢杨梅素、山柰酚、槲皮素、杨梅素、芹菜素等。结合文献报道,推测其可能为藤茶黄酮类化合物抑菌的关键成分。
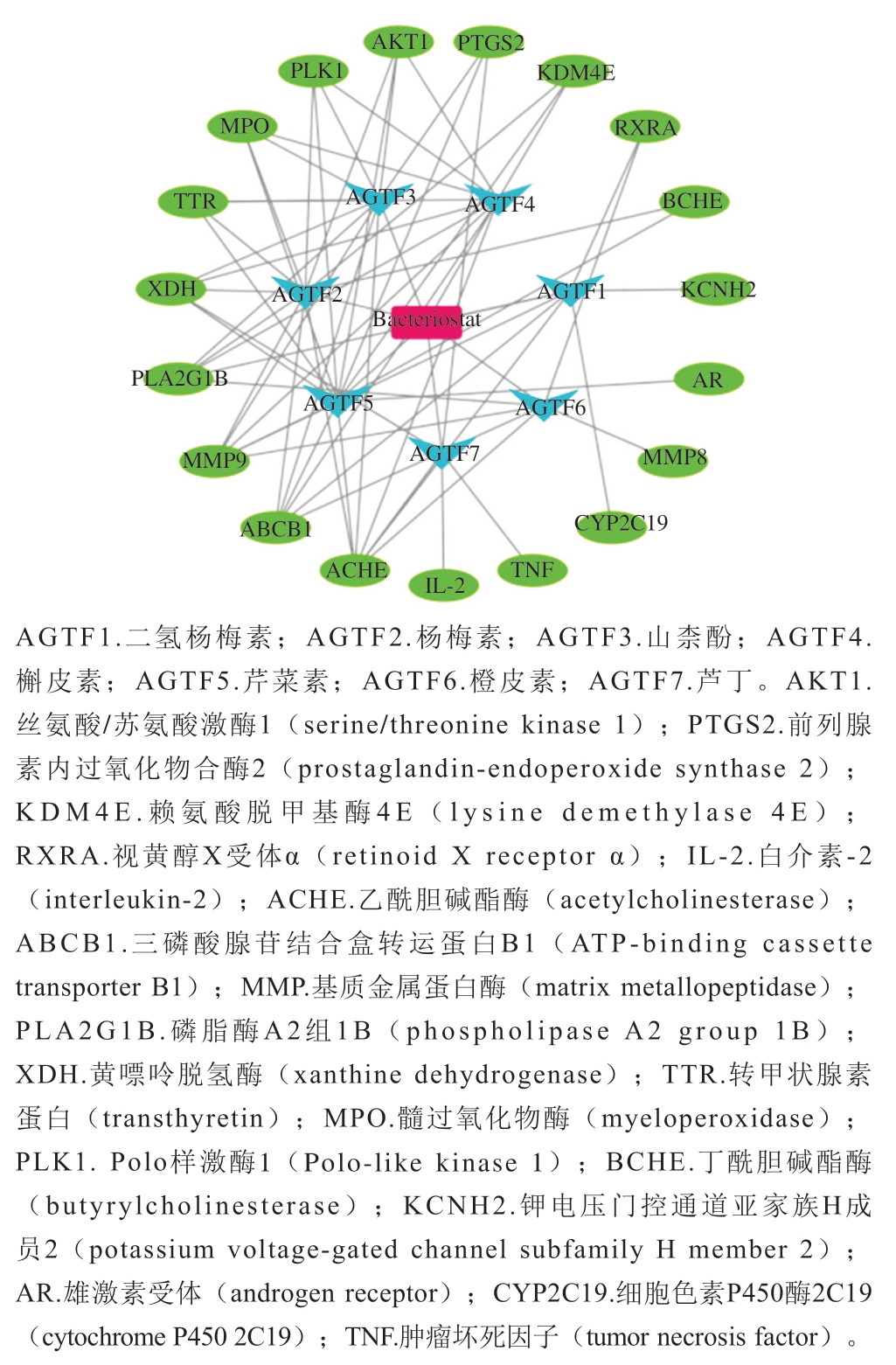
图2 藤茶黄酮类化合物抑菌作用成分和靶点网络
Fig. 2 Network diagram of antibacterial flavonoids in Ampelopsis and targets
2.4 藤茶黄酮类化合物蛋白质-蛋白质相互作用网络构建
如图3所示,构建蛋白互作网络,其中度值排名靠前的5 位分别为PTGS2、TNF、AKT1、MMP9、MPO等,其中度值大于2 倍中位数的靶点有两个,分别为PTGS2、TNF,其可能是藤茶黄酮类化合物抑菌的核心靶点。
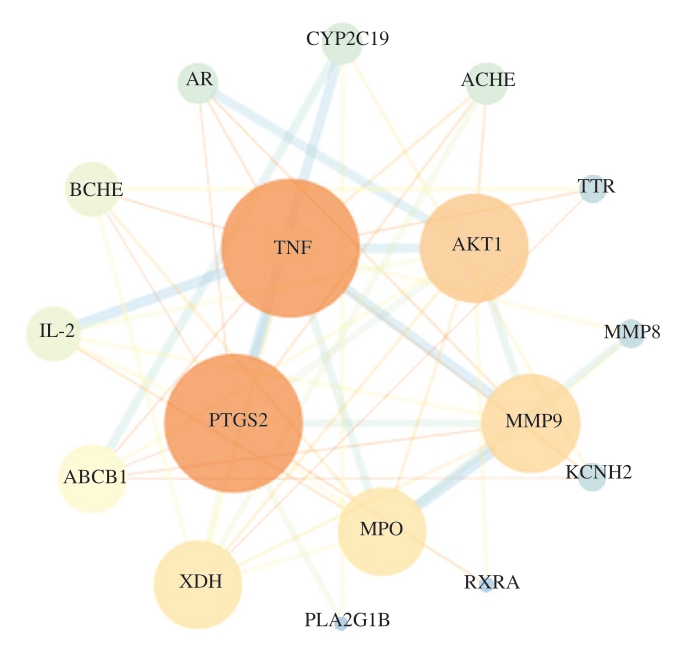
图3 藤茶黄酮类化合物抑菌的核心靶点
Fig. 3 Core antibacterial targets of flavonoids in Ampelopsis
2.5 藤茶黄酮类化合物抑菌靶点GO富集分析和KEGG通路富集分析
对藤茶黄酮类化合物和抑菌的交集靶点进行GO分析,得到P<0.05的BP条目有42 条,CC条目有4 条,MF条目有10 条。排名靠前的条目如图4所示,其中BP主要涉及凋亡过程的负调控、一氧化氮生物合成过程的正向调控、对糖皮质激素的应答等,CC主要涉及细胞外间隙、胞外区、细胞表面等;MF主要涉及酶结合、相同蛋白结合、转录顺式调控结合等。对对藤茶黄酮类化合物和抑菌的交集靶点进行KEGG分析,得到P<0.05的信号通路23 条,其中前10 条如图5所示,主要为癌症的发病途径、TNF信号通路、C型凝集素受体信号通路等,与藤茶黄酮类化合物的抑菌功效相关性较高。
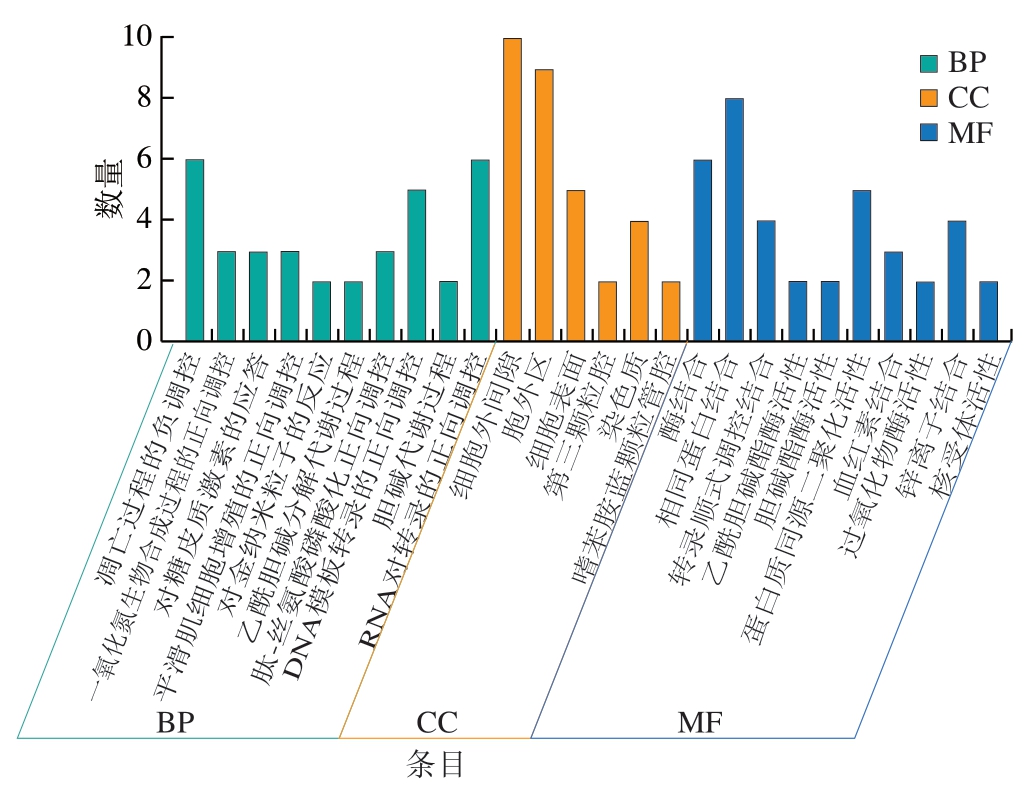
图4 藤茶黄酮类化合物成分-抑菌交集靶点的GO功能富集分析
Fig. 4 GO functional enrichment analysis of intersection targets between flavonoid components in Ampelopsis and antibacterial action
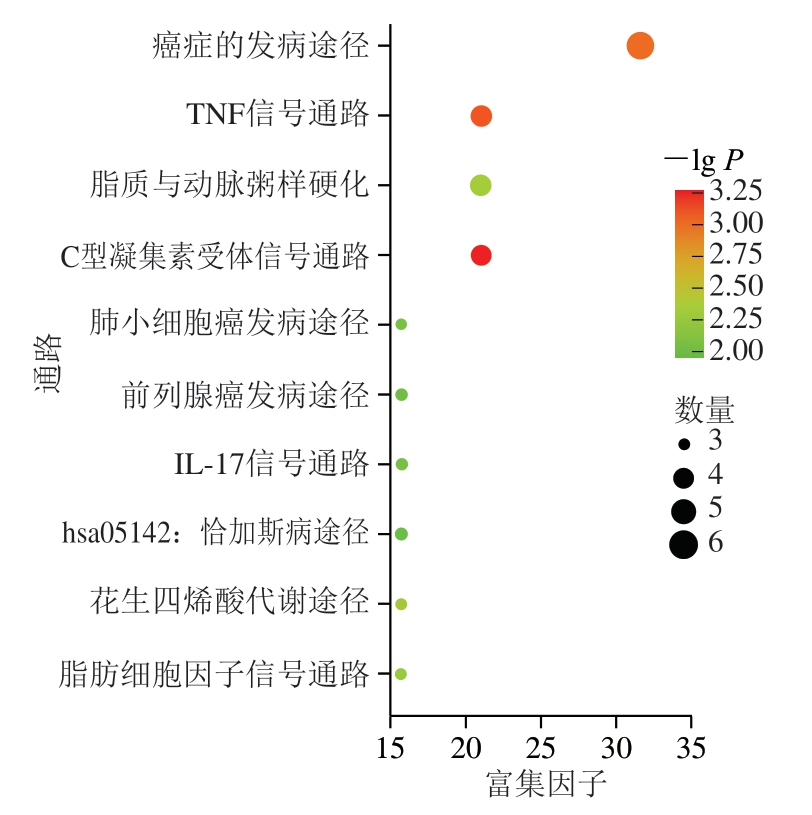
图5 藤茶黄酮类化合物成分-抑菌交集靶点的KEGG通路富集分析
Fig. 5 KEGG pathway enrichment analysis of intersection targets between flavonoid components in Ampelopsis and antibacterial action
2.6 藤茶黄酮类化合物核心活性成分-靶点分子对接验证
基于网络药理学和参考文献结果,对藤茶黄酮类化合物核心活性成分二氢杨梅素、槲皮素、山柰酚和抑菌靶点TNF、AKT1、PTG2S进行分子对接,结果见表2,各成分与各个靶点的结合能均低于—7 kcal/mol,根据分子对接理论,结合自由能为负值表明配体与受体可自发结合,且绝对值越大,复合物稳定性越高[21]。因此,表明核心活性成分和靶点间具有较强的结合活性。由图6可知,藤茶黄酮类化合物核心活性成分和抑菌靶点主要通过氢键进行结合,形成稳定的结构。
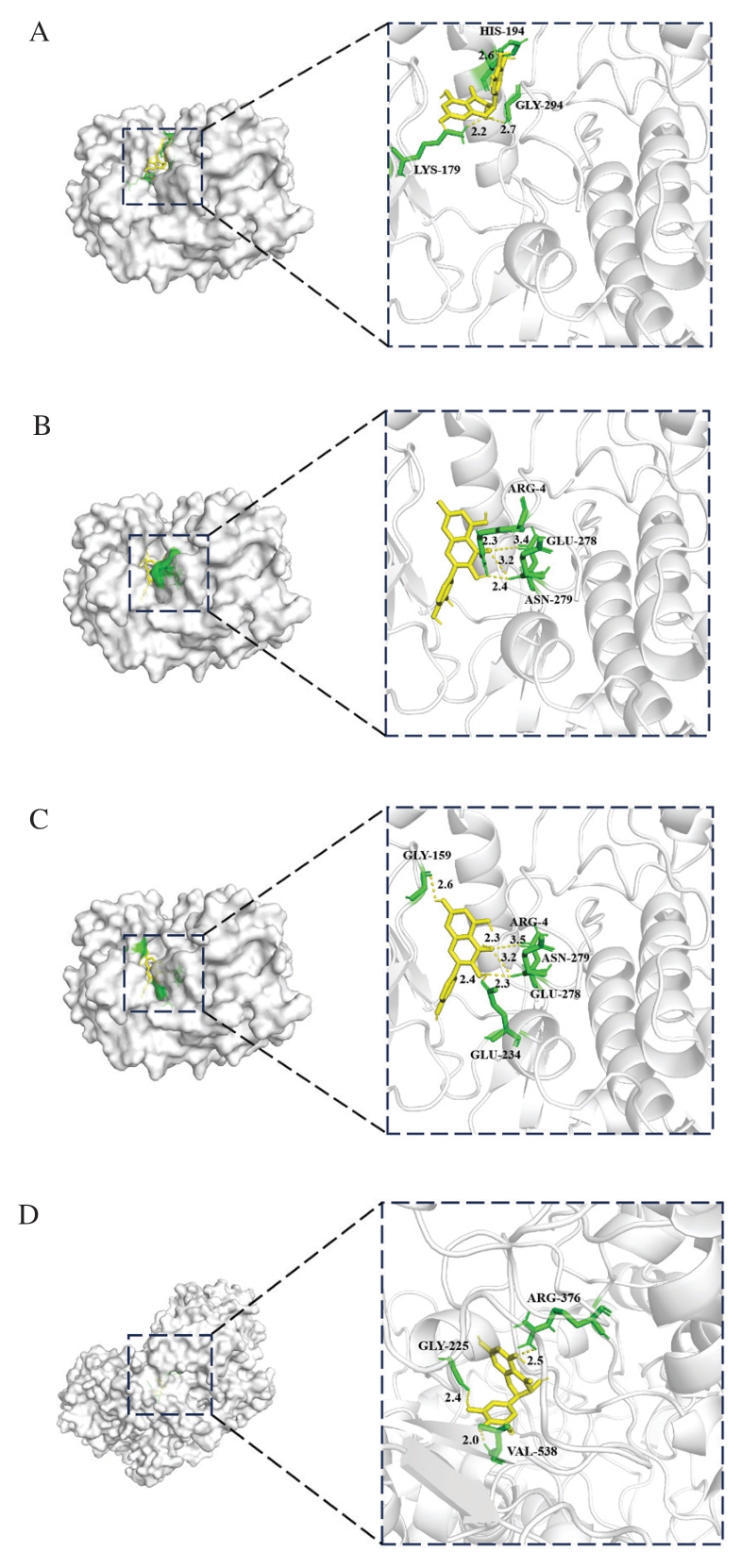
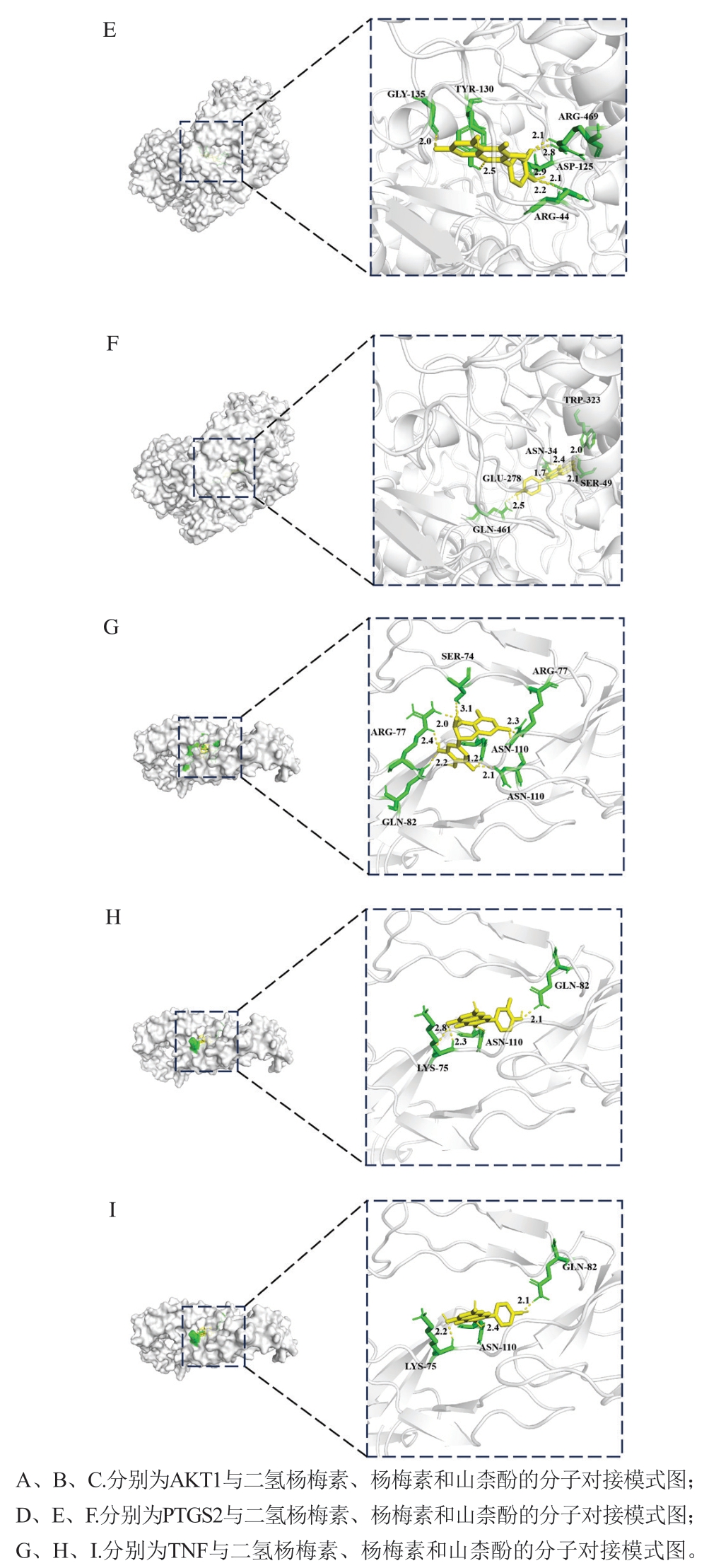
图6 藤茶黄酮类化合物与抑菌相关靶点分子对接模式图
Fig. 6 Molecular docking patterns of flavonoids from Ampelopsis to antibacterial targets
表2 藤茶黄酮类化合物核心成分与抑菌相关靶点分子对接结合能
Table 2 Docking binding energy between core flavonoid components in Ampelopsis and antibacterial targets
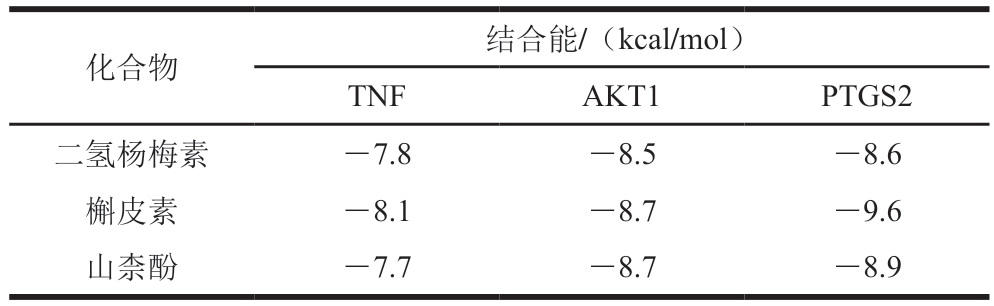
化合物结合能/(kcal/mol)TNFAKT1PTGS2二氢杨梅素—7.8—8.5—8.6槲皮素—8.1—8.7—9.6山柰酚—7.7—8.7—8.9
2.7 二氢杨梅素抑菌效果
由表3可知,二氢杨梅素和DMSO溶剂对临床筛选的大肠杆菌和沙门氏菌有一定的抑菌效果,对鸡场分离的金黄色葡萄球菌无抑菌效果。以DMSO为溶剂,如表3所示,二氢杨梅素对5 株大肠杆菌的抑菌效果不明显,对沙门氏菌3和沙门氏菌5的抑菌效果相对明显(抑菌圈直径分别为15.94 mm和14.94 mm)。
表3 以DMSO为溶剂的二氢杨梅素抑菌效果
Table 3 Antibacterial effect of dihydromyricetin in DMSO mm
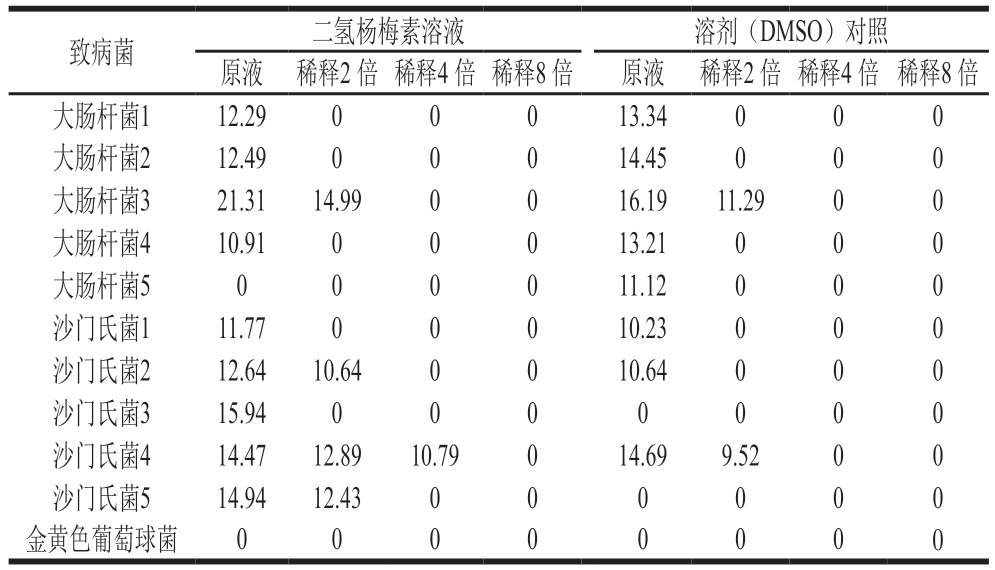
致病菌二氢杨梅素溶液溶剂(DMSO)对照原液稀释2 倍稀释4 倍稀释8 倍原液稀释2 倍稀释4 倍稀释8 倍大肠杆菌112.2900013.34000大肠杆菌212.4900014.45000大肠杆菌321.3114.990016.1911.2900大肠杆菌410.9100013.21000大肠杆菌5000011.12000沙门氏菌111.7700010.23000沙门氏菌212.6410.640010.64000沙门氏菌315.940000000沙门氏菌414.4712.8910.79014.699.5200沙门氏菌514.9412.43000000金黄色葡萄球菌00000000
由表4可知,二氢杨梅素和聚乙二醇溶剂对临床筛选的大肠杆菌和沙门氏菌有一定的抑菌效果,对金黄色葡萄球菌无抑菌效果,排除原液中聚乙二醇抑菌效果进行分析发现,二氢杨梅素对5 株大肠杆菌的抑菌效果不明显,对沙门氏菌3和沙门氏菌5的抑菌效果相对明显(抑菌圈直径分别为17.88 mm和16.63 mm)。
表4 以聚乙二醇为溶剂的二氢杨梅素抑菌效果测定
Table 4 Antibacterial effect of dihydromyricetin in polyethylene glycol mm
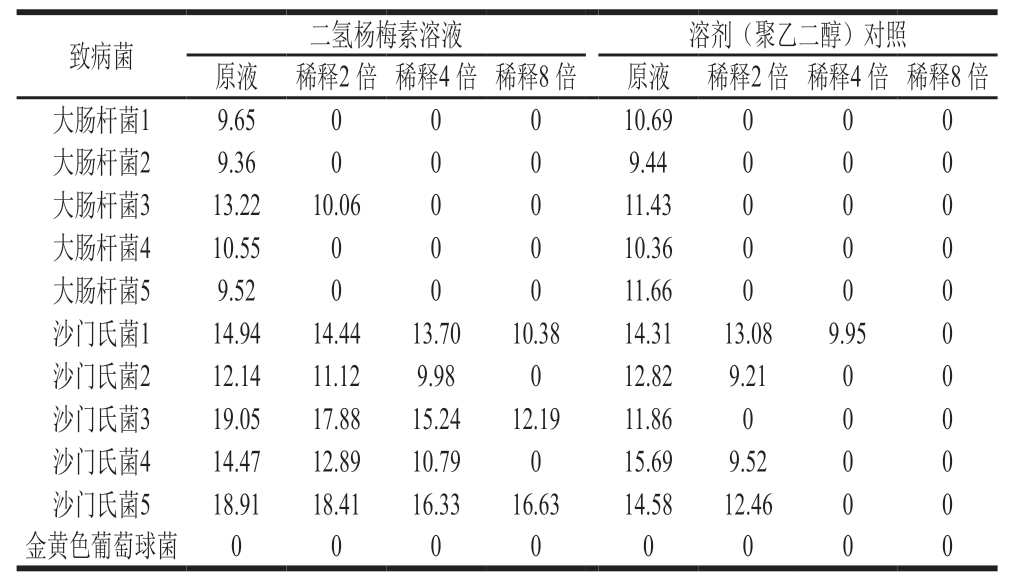
致病菌二氢杨梅素溶液溶剂(聚乙二醇)对照原液稀释2 倍稀释4 倍稀释8 倍原液稀释2 倍稀释4 倍稀释8 倍大肠杆菌19.6500010.69000大肠杆菌29.360009.44000大肠杆菌313.2210.060011.43000大肠杆菌410.5500010.36000大肠杆菌59.5200011.66000沙门氏菌114.9414.4413.7010.3814.3113.089.950沙门氏菌212.1411.129.98012.829.2100沙门氏菌319.0517.8815.2412.1911.86000沙门氏菌414.4712.8910.79015.699.5200沙门氏菌518.9118.4116.3316.6314.5812.4600金黄色葡萄球菌00000000
2.8 二氢杨梅素的MIC和MBC分析结果
基于2.7节筛选出二氢杨梅素抑菌效果较明显的沙门氏菌3和5作为目标菌,以聚乙二醇为溶剂,以稀释不同倍数的二氢杨梅素对沙门氏菌3和沙门氏菌5进行MIC和MBC的测定。由表5、7可知,二氢杨梅素对沙门氏菌3、5的MIC浓度对应为稀释8 倍,即5 mg/mL。由表6、8可知,二氢杨梅素对沙门氏菌3和沙门氏菌5的MBC均对应为稀释2 倍,即10 mg/mL。
表5 二氢杨梅素对沙门氏菌3的MIC测定
Table 5 MIC determination of dihydromyricetin against Salmonella 3
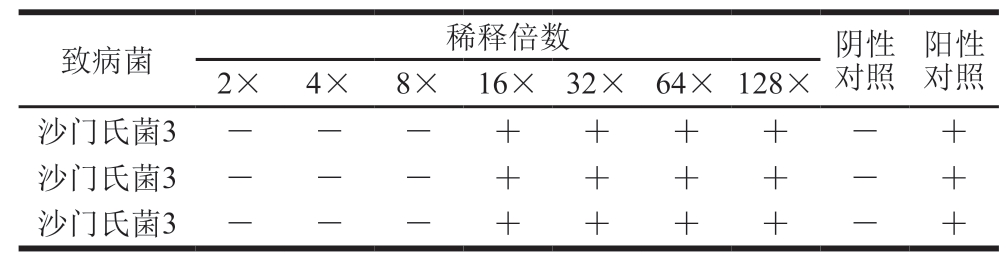
注:+.有细菌沉淀形成;—.无细菌沉淀形成。下同。
致病菌稀释倍数阴性对照阳性对照2×4×8×16×32×64×128×沙门氏菌3——++++—+沙门氏菌3——++++—+沙门氏菌3——++++—+
表6 二氢杨梅素对沙门氏菌3的MBC测定
Table 6 MBC determination of dihydromyricetin against Salmonella 3
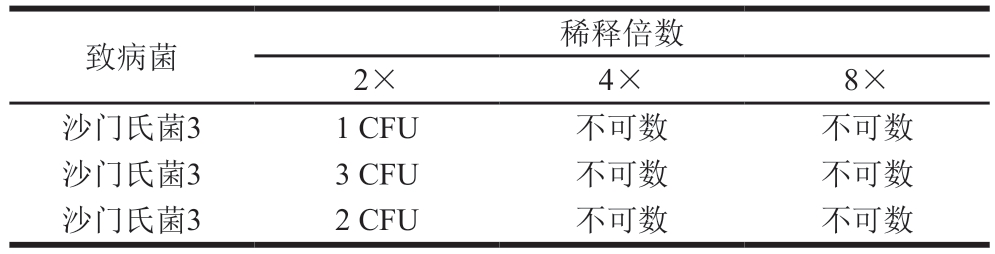
注:不可数为平皿上菌落铺满整个平皿且距离较近,下同。
致病菌稀释倍数2×4×8×沙门氏菌31 CFU不可数不可数沙门氏菌33 CFU不可数不可数沙门氏菌32 CFU不可数不可数
表7 二氢杨梅素对沙门氏菌5的MIC测定
Table 7 MIC determination of dihydromyricetin against Salmonella 5
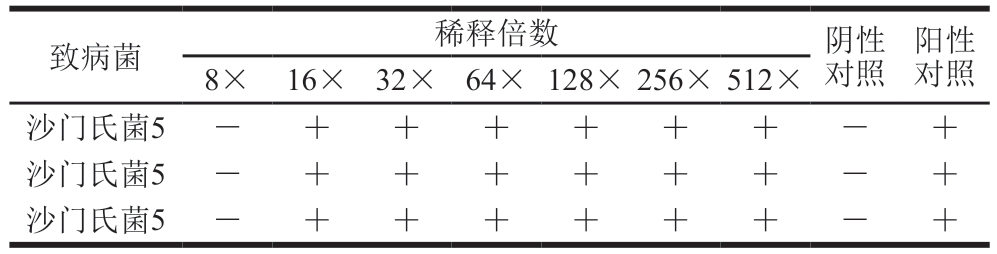
致病菌稀释倍数阴性对照阳性对照8×16×32×64×128×256×512×沙门氏菌5—++++++—+沙门氏菌5—++++++—+沙门氏菌5—++++++—+
表8 二氢杨梅素对沙门氏菌5的MBC测定
Table 8 MBC determination of dihydromyricetin against Salmonella 3
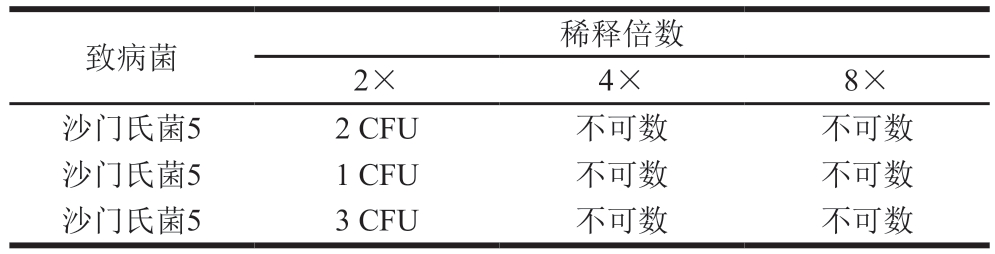
致病菌稀释倍数2×4×8×沙门氏菌52 CFU不可数不可数沙门氏菌51 CFU不可数不可数沙门氏菌53 CFU不可数不可数
2.9 二氢杨梅素对沙门氏菌细菌形态的影响
扫描电镜观察结果显示,与空白组(图7A)相比,经1 MIC二氢杨梅素处理后,细菌结构被破坏,大部分细胞破碎,形态结构不完整,伴随大量内容物流出,部分细菌皱缩(图7B)。
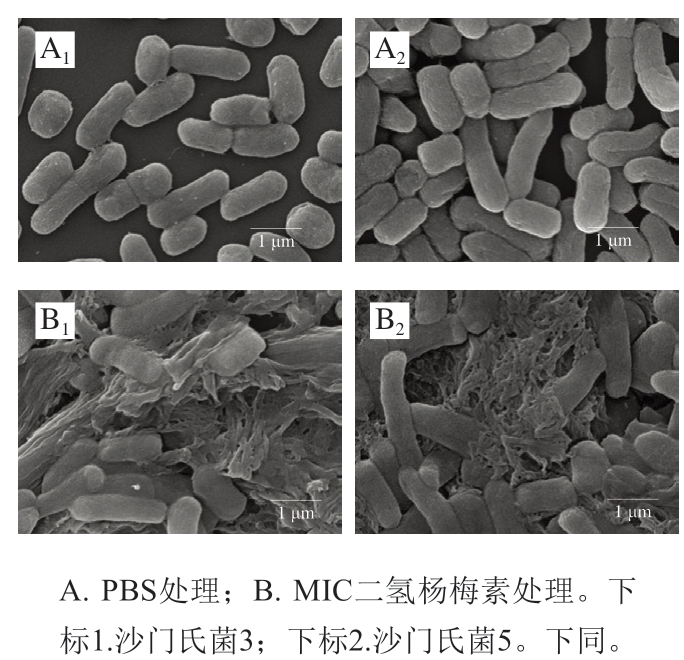
图7 扫描电镜观察二氢杨梅素对2 株沙门氏菌形态的影响(×20 000)
Fig. 7 Effects of dihydromyricetin on the morphology of two Salmonella strains observed by scanning electron microscopy (× 20 000)
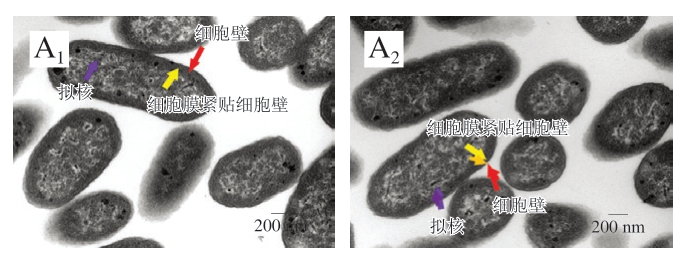
透射电镜观察结果显示,与空白组(图8A)相比,经二氢杨梅素处理后,细菌出现质壁分离、细胞壁溶解模糊、细胞膜溶解模糊、内容物溶解、细胞空化(图8B)。
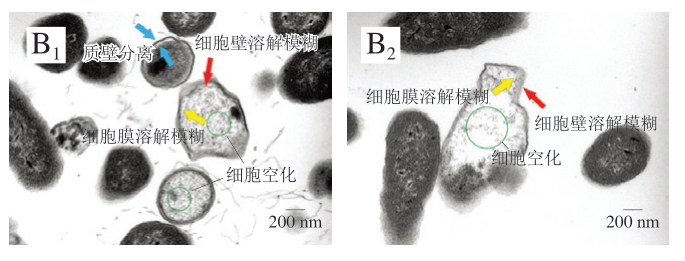
图8 透射电镜观察二氢杨梅素对2 株沙门氏菌形态的影响(×40 000)
Fig. 8 Effects of dihydromyricetin on the morphology of two Salmonella strains observed by transmission electron microscopy (× 40 000)
3 讨 论
大肠杆菌、沙门氏菌、金黄色葡萄球菌为GB 29921—2021明确规定的食源性致病菌,且均被世界卫生组织列为重要的耐药菌监测对象[22-24],可造成食品污染、食品腐败变质、引发食物中毒、影响食品安全及增加食品企业的经济负担等,其广泛的感染范围和多样的感染途径对人类和动物的健康构成严重威胁[25]。藤茶作为一种传统的中药饮品,不仅口感独特,还具有丰富的食用价值和药用功效,其主要活性成分黄酮类化合物具有抗氧化、抗炎、抑菌等多种生物活性,且大量的研究表明其安全较高[26]。
网络药理学以“多成分-多靶点-复杂疾病”的整体研究模式为中草药研究提供了全新的思路和切实可行的探索途径,在揭示中兽药药效成分、靶点及作用信号通路方面应用广泛。本研究网络药理学结果表明:藤茶黄酮类化合物抑菌的关键成分为二氢杨梅素、杨梅素、山柰酚等,此结果与前期多项研究结果[27-29]一致,二氢杨梅素可能通过破坏大肠杆菌、副伤寒沙门氏菌和铜绿假单胞菌等细胞壁,促使细胞内成分泄漏和及影响细菌三羧酸循环途径,进而引起细菌死亡[30]。山柰酚可通过破坏细菌细胞膜、促进细胞凋亡、抑制DNA解旋酶等方式抑制细菌增殖[31]。藤茶黄酮类化合物抑菌的核心靶点为PTGS2、TNF、AKT1。研究发现,PTGS2通过调节前列腺素的合成在抗炎反应方面发挥重要作用[32-33]。TNF是由活化的巨噬细胞和T淋巴细胞分泌的细胞因子,具有抗感染、抗肿瘤、促进细胞活化及白细胞向炎症部位迁移等重要作用。在细菌感染过程中,其可刺激其他炎症因子的产生,促进白细胞的黏附和向炎症部位的迁移,从而加强机体对感染的抵御能力[34]。AKT1是PI3K/AKT/mTOR信号通路中的关键蛋白,在调节细胞生长、分裂以及细胞凋亡抑制等多种过程中发挥着关键作用。在抑菌过程中主要通过PI3K/Akt通路参与细胞凋亡调控和抑制过度的炎症反应,进而影响病原体的感染和存活[35]。KEGG分析结果也证实藤茶黄酮类化合物可通过对TNF信号通路和C型凝集素受体信号通路的激活,调节TNF和AKT1等的释放,进而参与炎症、免疫调节等生理和病理过程[36-38]。此外通过分子对接技术发现,藤茶黄酮类化合物抑菌核心靶点能与关键活性成分较好地结合。因此,推测藤茶黄酮类化合物的抑菌作用具有多靶点、多成分和多途径的特点,其可通过调节机体免疫功能,促进相关细胞因子的释放,同时减少因细菌造成的炎症反应,进而起到抑菌效果。
黄酮类化合物是具有较高抗菌活性的植物次级代谢产物,在一定范围内其抗菌活性与含量呈正相关[39-40]。二氢杨梅素是藤茶中含量最高的黄酮类活性成分,是其发挥多种药理作用的关键物质基础[41],其对铜绿假单胞菌、副伤寒沙门氏菌、白色念珠菌等均有较好的抑菌效果[14,42],同时根据网络药理学分析结果,选择藤茶黄酮类化合物抑菌关键成分二氢杨梅素对临床分离易造成食品污染的常见致病菌进行体外实验验证,结果发现二氢杨梅素对临床分离的大肠杆菌和沙门氏菌有一定的抑菌效果,其中对沙门氏菌的效果更为明显,其MIC和MBC分别为5 mg/mL和10 mg/mL,并可通过造成细胞壁或细胞膜溶解模糊、细胞空化等破坏细菌的结构,表明二氢杨梅素可直接作用沙门氏菌从而起到抑菌作用。
综上所述,藤茶黄酮类化合物可能通过二氢杨梅素等活性成分、TNF等靶点及TNF信号通路等间接发挥抑菌作用,同时可通过破坏细菌细胞壁和细胞膜,进而起到直接抑菌作用。
[1] 孙傲楠, 林圣华, 赵涛, 等. 动物源性食品中抗生素多残留检测的研究进展[J]. 食品研究与开发, 2022, 43(23): 217-224.
[2] 张桐, 丁桂清, 乔曦, 等. 藤茶及其活性成分二氢杨梅素的药理作用[J]. 辽宁中医药大学学报, 2024, 26(7): 107-113. DOI:10.13194/j.issn.1673-842x.2024.07.020.
[3] 杨冰慧, 李兵, 马金龙, 等. 药用植物藤茶的研究进展[J]. 大连民族大学学报, 2023, 25(3): 199-203. DOI:10.13744/j.cnki.cn21-1431/g4.2023.03.001.
[4] 冯涵, 李娜, 王华林, 等. 藤茶中黄酮类成分的功效研究进展[J].公共卫生与预防医学, 2018, 29(1): 82-86. DOI:10.3969/j.issn.1006-2483.2018.01.022.
[5] 黄权锋, 陈泽豪, 彭琳, 等. 藤茶中黄酮类物质抗流感病毒作用机制的分子对接研究[J]. 时珍国医国药, 2020, 31(9): 2053-2055.DOI:10.3969/j.issn.1008-0805.2020.09.002.
[6] 李宁, 杨媛媛, 曲彤, 等. 异戊烯基黄酮类化合物药理作用研究进展[J].中成药, 2024, 46(4): 1255-1262. DOI:10.3969/j.issn.1001-1528.2024.04.029.
[7] 刘雪艳, 查代君. 黄酮类活性成分的代谢研究进展[J]. 福建医科大学学报, 2021, 55(4): 358-366.
[8] 邓浩健, 曾春晖, 陈益清, 等. 基于网络药理学的双氢杨梅树皮素抗金黄色葡萄球菌活性和作用机制研究[J]. 食品工业科技, 2022,43(10): 23-31. DOI:10.13386/j.issn1002-0306.2021080240.
[9] 周茜雅, 陈婧, 方建国, 等. 藤茶抑菌作用研究进展[J]. 中草药, 2017,48(22): 4819-4825.
[10] LIANG H Y, HE K K, LI T, et al. Mechanism and antibacterial activity of vine tea extract and dihydromyricetin against Staphylococcus aureus[J]. Scientific Reports, 2020, 10(1): 21416. DOI:10.1038/s41598-020-78379-y.
[11] 康秋月. 二氢杨梅素对耐甲氧西林金黄色葡萄球菌(MRSA)的耐药消减作用研究[D]. 乌鲁木齐: 新疆农业大学, 2022. DOI:10.27431/d.cnki.gxnyu.2022.000056.
[12] XU Y Q, WANG S P, CHAN H F, et al. Dihydromyricetin induces apoptosis and reverses drug resistance in ovarian cancer cells by p53-mediated downregulation of survivin[J]. Scientific Reports, 2017, 7:46060. DOI:10.1038/srep46060.
[13] 王楚婷, 孙懿, 陈志伟, 等. 藤茶总黄酮对非酒精性脂肪性肝病模型小鼠肠道菌群的影响[J]. 医药导报, 2024, 43(6): 867-873.
[14] 罗非君, 丁锦屏. 藤茶及二氢杨梅素的生物学功能研究进展[J]. 食品与生物技术学报, 2022, 41(2): 8-21. DOI:10.3969/j.issn.1673-1689.2022.02.002.
[15] GONG H, XU H M, LI M Y, et al. Molecular mechanism and therapeutic significance of dihydromyricetin in nonalcoholic fatty liver disease[J]. European Journal of Pharmacology, 2022, 935: 175325.DOI:10.1016/j.ejphar.2022.175325.
[16] ZHANG Q L, ZHAO Y F, ZHANG M Y, et al. Recent advances in research on vine tea, a potential and functional herbal tea with dihydromyricetin and myricetin as major bioactive compounds[J]. Journal of Pharmaceutical Analysis, 2021, 11(5): 555-563. DOI:10.1016/j.jpha.2020.10.002.
[17] 吕浩. 藤茶总黄酮的提取分离工艺及体外抗肿瘤活性研究[D]. 哈尔滨:哈尔滨商业大学, 2021. DOI:10.27787/d.cnki.ghrbs.2021.000639.
[18] 戚舜尧. 藤茶及其主要活性成分二氢杨梅素的开发与应用研究[D]. 北京: 北京协和医学院, 2024. DOI:10.27648/d.cnki.gzxhu.2024.000797.
[19] 张朝阳, 陈娥, 马世龙, 等. HPLC法测定藤茶中5 种黄酮类物质的含量[J]. 湖南农业大学学报(自然科学版), 2024, 50(6): 54-61.DOI:10.13331/j.cnki.jhau.2024.06.007.
[20] 叶诚, 王东鹏, 黄岭岭. HPLC-MS/MS法同时测定藤茶中5 个黄酮类成分含量[J]. 药物分析杂志, 2022, 42(12): 2195-2201.DOI:10.16155/j.0254-1793.2022.12.17.
[21] 韩贺龙, 曾卫军, 李静, 等. 基于网络药理学和分子对接技术分析樱桃李多酚抗糖尿病的作用机制[J/OL]. 食品研究与开发, 1-10.
[22] 刘婷宇, 董庆利, 李嘉铭, 等. 食品中食源性致病菌活菌检测方法研究进展[J]. 食品工业科技, 2025, 46(13): 395-403. DOI:10.13386/j.issn1002-0306.2024070120.
[23] 张明娟. 食品中沙门氏菌、大肠杆菌等致病菌的传播途径及防治研究[J]. 中国食品工业, 2024(18): 89-91.
[24] 朱诗语, 许云飞. 某市动物性食品中食源性致病菌的分离鉴定和致病性分析[J]. 食品安全导刊, 2024(21): 81-83; 88. DOI:10.16043/j.cnki.cfs.2024.21.046.
[25] 卢亮平, 万康林, 徐建国. 人兽共患细菌性疾病防控现状及特征分析[J]. 中国人兽共患病学报, 2018, 34(11): 967-970; 976.DOI:10.3969/j.issn.1002-2694.2018.00.192.
[26] 张典典, 高家东, 戴彰言, 等. 藤茶的食用历史及安全性[J]. 现代食品科技, 2024, 40(7): 363-368. DOI:10.13982/j.mfst.1673-9078.2024.7.0289.
[27] 祁子麟, 陈咏琪, 蔡延渠, 等. 藤茶提取物及活性成分对创伤弧菌的体外抑菌活性及作用机制[J]. 广东药科大学学报, 2023, 39(1): 95-99. DOI:10.16809/j.cnki.2096-3653.2022081101.
[28] REHMAN T. 山奈酚抗鸡肠炎沙门菌感染的作用及机制研究[D].雅安: 四川农业大学, 2023.
[29] RAN W Y, YUE Y X, LONG F W, et al. Antibacterial mechanism of 2R,3R-dihydromyricetin against Staphylococcus aureus: deciphering inhibitory effect on biofilm and virulence based on transcriptomic and proteomic analyses[J]. Foodborne Pathogens and Disease, 2023, 20(3):90-99. DOI:10.1089/fpd.2022.0075.
[30] XIAO X N, WANG F, YUAN Y T, et al. Antibacterial activity and mode of action of dihydromyricetin from Ampelopsis grossedentata leaves against food-borne bacteria[J]. Molecules, 2019, 24(15): 2831.DOI:10.3390/molecules24152831.
[31] PERIFERAKIS A, PERIFERAKIS K, BADARAU I A, et al.Kaempferol: antimicrobial properties, sources, clinical, and traditional applications[J]. International Journal of Molecular Sciences, 2022,23(23): 15054. DOI:10.3390/ijms232315054.
[32] 贺旸知歌, 姜旭, 张志文, 等. PTGS2调控细胞增殖及抗氧化能力影响结肠癌患者预后[J]. 基础医学与临床, 2024, 44(11): 1522-1529.DOI:10.16352/j.issn.1001-6325.2024.11.1522.
[33] 高貂艳, 訾和平, 张静雯, 等. 血清PTGS2、IL-21水平对儿童难治性肺炎支原体肺炎的预测效能[J]. 山东医药, 2024, 64(29): 74-77.
[34] CROFT M, SALEK-ARDAKANI S, WARE C F. Targeting the TNF and TNFR superfamilies in autoimmune disease and cancer[J]. Nature Reviews Drug Discovery, 2024, 23(12): 939-961. DOI:10.1038/s41573-024-01053-9.
[35] TIAN G R, CHEN Z, SHI K Q, et al. The evolution of smallmolecule Akt inhibitors from hit to clinical candidate[J]. European Journal of Medicinal Chemistry, 2024, 279: 116906. DOI:10.1016/j.ejmech.2024.116906.
[36] 张琴, 史伟峰. C型凝集素受体介导的抗真菌感染机制研究进展[J].临床检验杂志, 2018, 36(10): 763-766. DOI:10.13602/j.cnki.jcls.2018.10.11.
[37] LI D, KORTEKAAS R K, DOUGLAS K B I, et al. TNF signaling mediates lipopolysaccharide-induced lung epithelial progenitor cell responses in mouse lung organoids[J]. Biomedicine & Pharmacotherapy,2024, 181: 117704. DOI:10.1016/j.biopha.2024.117704.
[38] PARK J, KIM D, SIM J, et al. The inflammatory characteristics of symptomatic glioma associated with poor prognosis and chemoresistance via tumor necrosis factor signaling pathway[J]. Brain Tumor Research and Treatment, 2024, 12(4): 237-244. DOI:10.14791/btrt.2024.0035.
[39] 刘璐, 付嘉阳, 邓红霞. 超声波辅助提取泡桐花总黄酮工艺及抑菌活性研究[J]. 东北农业大学学报, 2022, 53(7): 57-66. DOI:10.19720/j.cnki.issn.1005-9369.2022.07.007.
[40] 韩秀枝, 曹源, 詹跃勇, 等. Design-Expert软件设计优化万寿菊黄酮提取工艺及抗氧化活性、抑菌活性测定[J]. 食品研究与开发, 2023,44(14): 163-168. DOI:10.12161/j.issn.1005-6521.2023.14.024.
[41] ZENG T X, SONG Y J, QI S Y, et al. A comprehensive review of vine tea: origin, research on Materia Medica, phytochemistry and pharmacology[J]. Journal of Ethnopharmacology, 2023, 317: 116788.DOI:10.1016/j.jep.2023.116788.
[42] LI H H, BAO Y H, HE J, et al. Chitosan-based dihydromyricetin composite hydrogel demonstrating sustained release and exceptional antibacterial activity[J]. International Journal of Biological Macromolecules, 2025, 291: 139128. DOI:10.1016/j.ijbiomac.2024.139128.