骨桥蛋白(osteopontin,OPN)是一种存在于所有脊椎动物体内的多功能磷酸化糖蛋白[1],最早于1985年在成骨细胞中发现[2],目前已证实在人体骨细胞、上皮细胞、神经细胞、淋巴细胞、巨噬细胞等不同类型的细胞中均有表达,并广泛分布于骨、脑、肾脏、乳腺等组织以及血液、尿液和人乳等体液中。在研究母乳主要功能性蛋白及其对新生儿健康贡献的过程中,科学家于20世纪90年代初通过质谱分析及免疫印迹等技术,首次确认了人乳中存在OPN,由乳腺上皮细胞分泌,以可溶性蛋白存在于乳清蛋白中,并发现其浓度在母乳的不同阶段呈现显著差异,初乳中的含量尤为丰富[3-5]。1993年,Sørensen等[6]首次从牛乳中分离得到牛乳OPN并对其进行了表征。
OPN是一种高度糖基化和磷酸化的酸性分泌蛋白,具有与多种细胞表面受体结合的功能性区域,这些结构特征使OPN能够和细胞表面受体结合,激活细胞信号通路而发挥生物学功能[7-8]。在消化吸收方面,OPN在胃肠道中具有抗消化特性,磷酸化、糖基化位点对其消化稳定性和功能活性具有调节作用。其完整蛋白、水解片段及活性肽可通过肠上皮细胞表面受体或进入血液循环,发挥调节免疫调节,促进大脑发育、肠道健康、骨健康等生物功能[9]。随着欧盟批准牛乳OPN作为新型食品原料,OPN已成为婴幼儿配方奶粉的“新星”营养素。目前,欧洲Arla食品公司由纯度大于95%的牛乳源OPN组成的Lacprodan® OPN-10产品已被欧洲食品安全局(European Food Safety Authority,EFSA)推荐用作婴儿配方奶粉中的新型食品添加剂[10]。尽管如此,OPN的相关提取技术及功能性研究尚处于起步阶段,未来需进一步加强其结构-消化吸收和营养功能及跨物种适用性与安全性的系统研究,以推动其在婴幼儿配方乳粉等特殊人群食品中的科学应用。基于此,本文综述乳源OPN结构特征、消化吸收以及营养功能的研究进展。
1 乳中OPN含量
虽然动物体内多种组织都可以表达OPN,但乳中含量最高,这也进一步说明乳OPN在婴儿发育过程中起到重要的作用。不同物种乳汁中的OPN含量存在显著差异(图1)。母乳中的OPN平均质量浓度约为138 mg/L,相当于母乳中总蛋白的2.1%,而牛乳中的OPN质量浓度显著低于人母乳中OPN含量,一般在18~23.0 mg/L之间,约占总乳清蛋白的0.01%~0.05%[4,11],而常见婴儿配方奶粉中的OPN质量浓度约为9 mg/L[4],这也是开发OPN作为婴配粉添加剂的目的。Hu Bei等[12]利用超高效液相色谱-串联质谱(ultra-high performance liquid chromatographytandem mass spectrometry,UPLC-MS/MS)测定了奶牛(53.9 mg/L)、水牛(60.15 mg/L)、牦牛(77.7 mg/L)、绵羊(35.43 mg/L)和山羊(28.5 mg/L)的OPN质量浓度。可以看出奶牛中OPN含量高于山羊和绵羊乳,但低于水牛和牦牛乳,更是显著低于人乳(138~217 mg/L)。
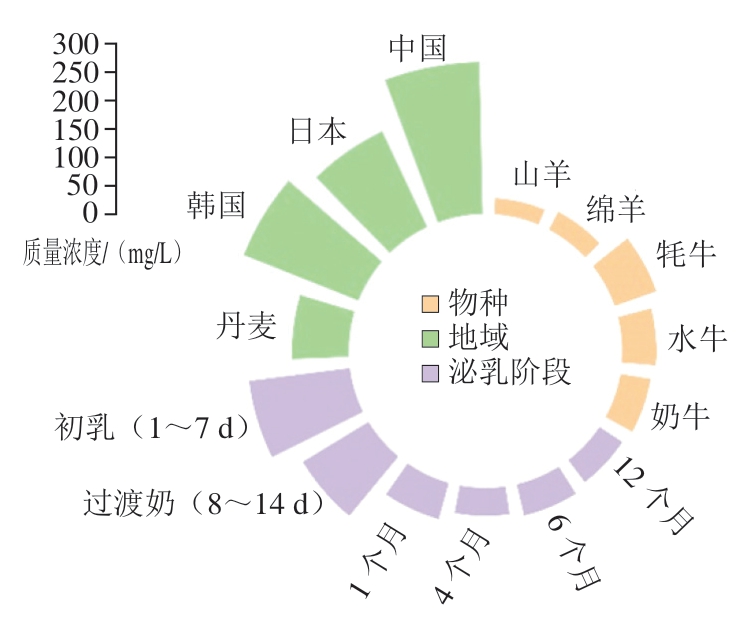
图1 不同乳中OPN含量
Fig. 1 OPN contents in milks from different species
除了物种间的含量差异,其含量可能会因地理差异、饮食差异、泌乳期、胎次以及个体而不同(图1)[11,13-15]。有研究显示,能量摄入不足(<1 800 kcal/d)的哺乳期女性,其母乳OPN质量浓度显著低于正常摄入组(P<0.05);高蛋白质摄入(>15%总能量)与OPN水平正相关(r=0.32,P=0.02),可能与氨基酸代谢影响乳腺合成相关[5,16]。一项针对中国、日本、韩国和丹麦母亲的大型多中心队列研究发现,平均母乳OPN水平存在较大的地理差异,丹麦母亲(平均产后17.4 周)为99.7 mg/L,日本母亲为185.0 mg/L(平均产后9.1 周),韩国母亲为216.2 mg/L(平均产后3.9 周),中国母亲(平均产后3.9 周)为266.2 mg/L[17],可能与东亚传统高钙饮食(如豆制品、鱼类)促进乳腺OPN分泌有关。最近研究也证明了这种地理差异以及哺乳期导致的OPN含量下降,通过酶联免疫吸附试验(enzymelinked immunosorbent assay,ELISA)和UPLC-MS/MS确定中国母亲的乳汁OPN水平为300~350 mg/L(产后1~2 周)和137.1 mg/L(泌乳的第3个月),土耳其和美国母亲为178 mg/L(产后1 周)[5,16]。母乳OPN质量浓度随哺乳期延长呈下降趋势。产后72 h至7 d的初乳OPN质量浓度可高达1 493.4 mg/L,而产后11~14 个月降至412.7 mg/L[9]。此外,研究表明,OPN水平随胎次而降低,OPN含量随泌乳时间的延长而显著增加。Dudemaine等[18]研究也发现在哺乳期第25周后观察到牛乳OPN水平显著增加。Christensen等[11]研究发现丹麦荷斯坦奶牛之间的OPN含量存在相当大的个体差异,水平从0.4 mg/L到67.8 mg/L不等。
2 结构特征
2.1 OPN结构特性
乳中的OPN主要由乳腺上皮细胞分泌,是一种重要的磷酸化糖蛋白[1],分子质量通常在44~66 kDa之间,具体取决于蛋白的糖基化和磷酸化程度[4,19-20]。其结构中包含多个关键功能域,如整合素结合位点、转谷氨酰胺酶作用位点、聚组氨酸位点以及肝素结合位点等。这些功能域赋予了OPN多种生物学活性,包括促进细胞黏附、调节免疫反应、参与炎症反应以及影响细胞增殖和分化等。
OPN的序列在不同物种间具有一定的保守性,但也存在显著差异,包括一级结构、翻译后修饰(posttranslational modification,PTM)等差异。不同物种的成熟OPN在氨基酸序列长度上存在显著差异,这种长度差异主要源于N端信号肽区域和C端延伸区的变异(图2)。成熟的人OPN包含298 个氨基酸,成熟的牛乳OPN蛋白包含262 个氨基酸,与人相比,最主要缺失了对应于人OPN中的188~209位置的22 个残基[21]。人乳和牛乳OPN序列具有约50%~60%的序列同源性,特别是在磷酸化位点和RGD(Arg-Gly-Asp)序列附近,在182 个位点上具有相同的氨基酸,另外44 个残基是结构保守的替换。山羊和绵羊乳OPN的氨基酸序列与牛乳OPN有较高的相似性,其序列同源性约为85%~90%,整合素序列、RGD序列和隐蔽基序完全一致,内源酶切位点存在高度一致性,磷酸化修饰位点基本一致,仅在相同位点的修饰覆盖率上存在细微差异。山羊乳OPN未鉴定到O-糖基化修饰,而牛乳OPN可鉴定到1 个O-糖基化修饰[22]。这表明两种乳OPN的主要功能序列和大多数磷酸化修饰具有高度相似性,可能具有相似的生物学功能。与牛乳OPN相比,水牛乳OPN的主要差异为蛋白质序列中第95位(N95)和第227位(N227)出现天冬酰胺残基插入。总之,不同物种OPN的非保守区域差异不影响核心功能域,保留了基础生物学功能,同时具有物种特异性的调控特征。

图2 不同乳源OPN序列对比图
Fig. 2 Alignment of OPN sequences from various milk sources
作为一种强磷酸化的蛋白,其富含丝氨酸、苏氨酸和天冬氨酸,这些氨基酸的磷酸化是其与钙离子结合、矿化调控以及参与细胞信号传导的重要基础[23]。OPN的糖基化修饰对其稳定性和功能具有重要影响。乳OPN含有多个糖基化位点,主要是N-和O-糖基化位点,这些修饰不仅影响其空间结构,也有助于维持其在胃肠道中的稳定性和生物活性。由于其富含天冬氨酸、谷氨酸以及大量的磷酸化残基,OPN在中性pH值条件下为酸性蛋白,等电点在3~4之间使OPN成为牛奶中酸性最强的蛋白质[9]。由于其带负电的特性,OPN能够与阳离子(尤其是钙离子)强烈结合,从而参与多种矿化过程[24]。OPN的二级结构主要由无规卷曲和少量的α-螺旋与β-折叠组成,其柔性结构有助于与细胞外基质和受体相互作用,增强其在组织修复、细胞迁移中的作用[25]。
目前关于人乳和牛乳OPN的磷酸化位点已经研究的比较清楚,其中人乳平均含有25 个磷酸盐分布在34 个磷酸丝氨酸和2 个磷酸苏氨酸上[20,26]。牛乳平均含有22 个磷酸化残基,分布在28 个不同的位点[1,27]。这些磷酸化氨基酸以3~5 个磷酸残基簇的形式聚集在一起[1,20]。OPN中唯一不含磷酸化的部分是位于整合素结合基序的N端的苏氨酸-脯氨酸富集区域。在该区域,OPN包含几个保守的苏氨酸残基,其中3~5 个在牛和人乳OPN中被O连接糖基化修饰[1,20]。而且人乳OPN和牛乳OPN的聚糖结构不同,人乳中由岩藻糖基化的N-乙酰乳糖胺单元组成[26],牛乳中由二唾液酸化的N-乙酰半乳糖胺-β-1,3-半乳糖组成[28]。
乳OPN主要通过和整合素结合发挥生理作用,最经典的结合序列为N端的RGD序列,该序列在目前发现的所有物种中高度保守[29]。该序列下游还有一个整合素结合位点隐蔽SVVYGLR序列(牛乳OPN为SVAYGLK)。除此之外还包括多聚天冬氨酸序列(结合钙)、凝血酶切割位点GLRS(Gly-Leu-Arg-Ser)序列以及C端的肝素结合位点等[29]。靠近整合素结合区域附近包含许多蛋白酶位点(纤溶酶、凝血酶和组织蛋白酶D),水解后释放包含有整合素结合基序的片段,能够和整合素特异性结合。其中乳中纤溶酶与凝血酶水解相同的肽键,二者水解OPN增加了由αVβ3-或α5β1-整合素介导的细胞黏附[30-32]。有研究表明,在人乳和牛乳中,OPN既以全长蛋白的形式存在,也以乳中内源性蛋白水解活性产生的不同N末端衍生大片段的形式存在[3,31-33]。如牛乳中的OPN主要存在60 kDa全长和40 kDa水解大片段两种形式[33]。在人乳中发现的N末端衍生片段是通过内源性蛋白酶组织蛋白酶D,特别是纤溶酶在Leu151-Arg159处多个位点裂解OPN形成的[32],切割产生的所有N端片段都包含整合素结合的143RGD145序列,并且大多数还包含146SVVYGLR152序列。这些全长OPN和N端大肽段可能在新生儿的免疫调节、抗炎反应和肠道健康中发挥不同的生物学功能。对天然存在的全长片段和N端片段的牛奶混合物的分析表明,OPN的N端片段能更有效地结合肠细胞,并且片段通过胞吞途径穿过肠膜屏障运输[34],这表明OPN的蛋白水解处理增加了其摄入后的生物活性。
OPN和乳铁蛋白(lactoferrin,LF)都是多功能乳清蛋白,在人乳中含量很高。这两种蛋白质由于电荷相反,可通过静电作用形成物质的量比为3∶1(LF∶OPN)的复合物[35-37],LF-OPN复合物已被证明比单独的单个蛋白质更能抵抗胃肠道消化[37-39],复合物的形成会增加人类肠道细胞的结合和摄取[40],复合物都通过刺激白细胞介素(interleukin,IL)-18的表达促进人肠道细胞的增殖和分化[38,40],且增强肠道免疫力抗炎效果也比单独使用一种蛋白更强[37,41-43]。
2.2 OPN结构表征方法
OPN作为高度PTM的内在无序蛋白(intrinsically disordered protein,IDP),其结构表征依赖于多技术的联合应用。质谱分析通过对乳源OPN中的关键肽段及其化学修饰状态进行验证。利用UPLC-高分辨率质谱(high resolution mass spectrometry,HRMS)法对牛乳样品中经预二甲基化和完全二甲基化处理后的OPN特征肽段GDSVAYGLK和YPDAVATWLKPDPSQK进行了比对,成功通过总离子流图表征OPN关键结构[44]。基质辅助激光解吸电离-飞行时间质谱(matrix-assisted laser desorption/ionization time-of-flight mass spectrometry,MALDI-TIF MS)可定位人乳OPN的36 个磷酸化位点和5 个O-糖基化位点,揭示了修饰簇状分布特征[20]。核磁共振(nuclear magnetic resonance,NMR)技术通过多维实验解析动态构象,磷酸化增强了OPN的局部灵活性,高度磷酸化诱导OPN发生构象延伸,进一步影响了OPN的功能活性(如整合素的结合能力)[45]。结合分子动力学(molecular dynamics,MD)分析和圆二色光谱(circular dichroism spectroscopy,CD)技术揭示了OPN在生物矿物富钙晶面的吸附作用受静电相互作用调控,且多肽链的构象灵活性可促进该过程[46]。另有研究采用生物信息学工具SOPMA对牦牛乳OPN的二级结构组成进行预测,结果显示该蛋白由86 个α-螺旋(占30.94%)、28 个β-折叠(10.07%)、3 个β-转角(1.08%)以及161 个无规卷曲(57.91%)构成,这种高比例的无序结构赋予了OPN高度的柔性和功能可塑性[47]。OPN是一类典型的IDP,其天然状态下缺乏稳定的三维构象,导致其在结构生物学研究中难以结晶。因此,迄今通过X射线衍射(X-ray diffraction,XRD)技术解析获得的OPN晶体结构仍较为有限。结构生物信息学研究协作组织(Research Collaboratory for Structural Bioinformatics,RCSB)蛋白质结构数据库(Protein Data Bank,PDB)已解析的OPN功能性短肽片段晶体结构表现为两个串联的β-转角[48-49]。为研究OPN在加工状态下的物理结构特征,采用扫描电子显微镜(scanning electron microscopy,SEM)对OPN粉末进行微观形貌观察,喷雾干燥处理后的OPN呈规则球形颗粒,表面光滑均匀[50]。
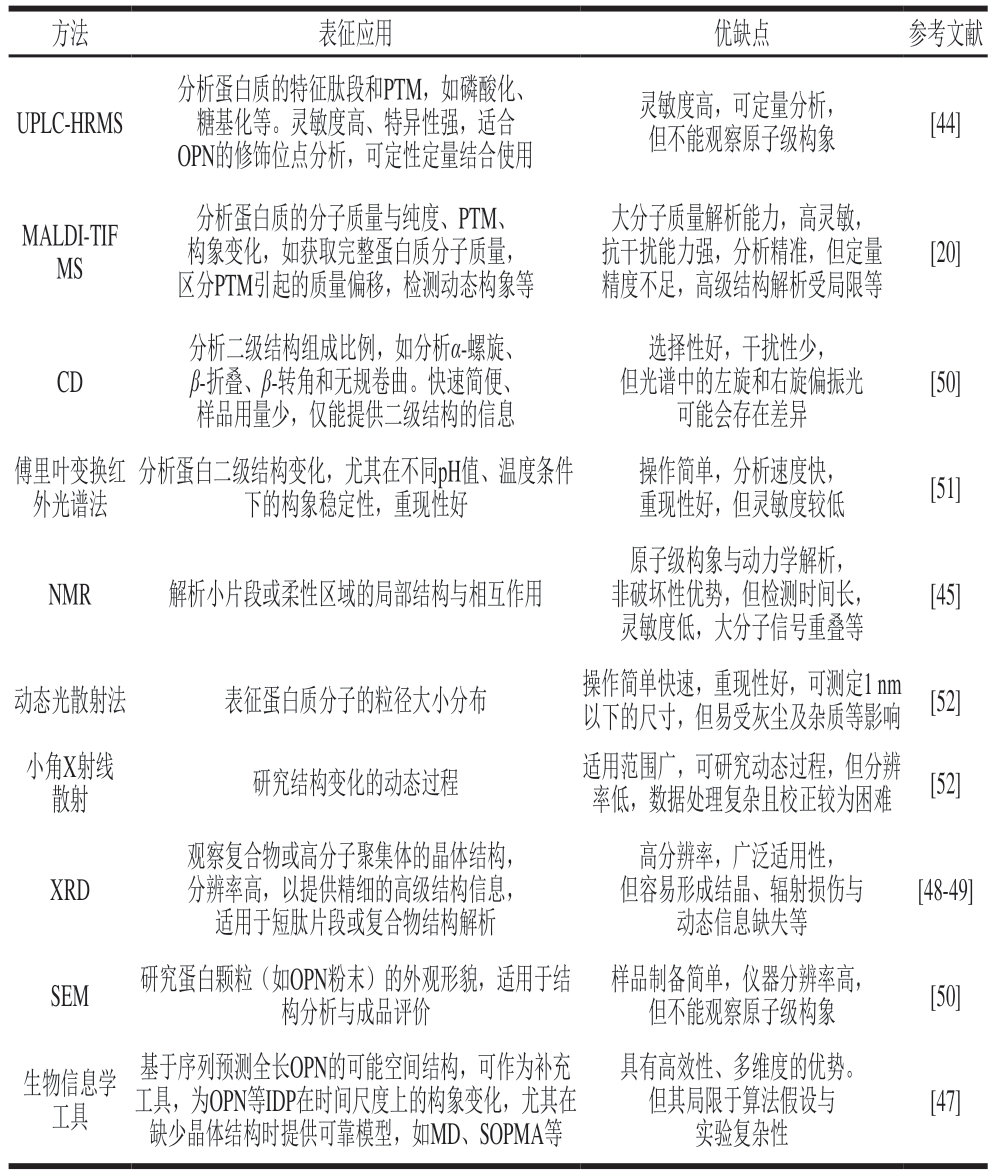
综上所述,从氨基酸序列、PTM到分子结构构象,再到干燥颗粒的宏观形态,乳源OPN在多层级结构上均展现出典型的功能性蛋白特征。通过多技术手段综合表征,为进一步挖掘乳OPN的生物功能与应用潜力提供了重要的结构基础与理论支持(表1)。
表1 OPN结构表征方法
Table 1 Methods for structural characterization of OPN
方法表征应用优缺点参考文献UPLC-HRMS分析蛋白质的特征肽段和PTM,如磷酸化、糖基化等。灵敏度高、特异性强,适合OPN的修饰位点分析,可定性定量结合使用灵敏度高,可定量分析,但不能观察原子级构象[44]MALDI-TIF MS分析蛋白质的分子质量与纯度、PTM、构象变化,如获取完整蛋白质分子质量,区分PTM引起的质量偏移,检测动态构象等大分子质量解析能力,高灵敏,抗干扰能力强,分析精准,但定量精度不足,高级结构解析受局限等[20]CD分析二级结构组成比例,如分析α-螺旋、β-折叠、β-转角和无规卷曲。快速简便、样品用量少,仅能提供二级结构的信息选择性好,干扰性少,但光谱中的左旋和右旋偏振光可能会存在差异[50]傅里叶变换红外光谱法分析蛋白二级结构变化,尤其在不同pH值、温度条件下的构象稳定性,重现性好操作简单,分析速度快,重现性好,但灵敏度较低[51]NMR解析小片段或柔性区域的局部结构与相互作用原子级构象与动力学解析,非破坏性优势,但检测时间长,灵敏度低,大分子信号重叠等[45]动态光散射法表征蛋白质分子的粒径大小分布操作简单快速,重现性好,可测定1 nm以下的尺寸,但易受灰尘及杂质等影响[52]小角X射线散射研究结构变化的动态过程适用范围广,可研究动态过程,但分辨率低,数据处理复杂且校正较为困难[52]XRD观察复合物或高分子聚集体的晶体结构,分辨率高,以提供精细的高级结构信息,适用于短肽片段或复合物结构解析高分辨率,广泛适用性,但容易形成结晶、辐射损伤与动态信息缺失等[48-49]SEM研究蛋白颗粒(如OPN粉末)的外观形貌,适用于结构分析与成品评价样品制备简单,仪器分辨率高,但不能观察原子级构象[50]生物信息学工具基于序列预测全长OPN的可能空间结构,可作为补充工具,为OPN等IDP在时间尺度上的构象变化,尤其在缺少晶体结构时提供可靠模型,如MD、SOPMA等具有高效性、多维度的优势。但其局限于算法假设与实验复杂性[47]
3 消化吸收特性
近年来,科研工作者们对乳源OPN的消化吸收特性进行了深入探讨,取得了一定的进展。其中磷酸化修饰和糖基化修饰的影响机制显得尤为重要。本节旨在系统分析乳源OPN的消化吸收特性,概述其在机体内的稳定性、消化、吸收机制和生物利用度等相关研究的现状,以期为后续研究提供参考和启示。
3.1 消化特性
OPN在胃肠道中表现出一定的抗消化酶特性,了解机体内OPN的稳定性对于其在胃肠道的吸收和生物活性至关重要。虽然OPN是一种本质上无序的蛋白质,包含很少的三级结构[53],容易被蛋白水解酶攻击和消化,但将人乳和牛乳OPN在pH值为3的条件下与新生儿胃抽吸物孵育1 h后OPN仍保持完整[54],表明牛乳OPN具有很强的抗胃酸和胃蛋白酶水解能力。OPN不仅能够抵抗胃酸和胃蛋白酶消化,在肠道内也有一定的抗消化能力(图3)。在一项人体干预研究中,通过夹心ELISA在喂养富含牛奶OPN的婴儿配方奶粉的婴儿血浆中鉴定出全长或片段的牛奶OPN[5],这些研究表明,OPN或大的OPN片段可以通过肠道屏障。口服饲喂小鼠OPN后可以在小鼠的血浆、肝脏和结肠中检出OPN或OPN片段[13,55-56]。Christensen等[57]研究发现含有整合素结合136RGD138和139SVAYGLK145基序的糖基化牛乳OPN片段Trp27-Phe151能够抵抗胃蛋白酶的消化,这种抗性依赖于人乳和牛乳OPN中靠近整合素结合序列的苏氨酸残基的糖基化。这说明OPN的磷酸化糖基化修饰在抗消化水解中起着重要的作用。抗消化降解不等于不水解,如前面提到靠近整合素结合区域附近包含许多蛋白酶位点(纤溶酶、凝血酶和组织蛋白酶D),在乳中就可能会降解生成包含有整合素结合序列的N端大片段[31-32]。
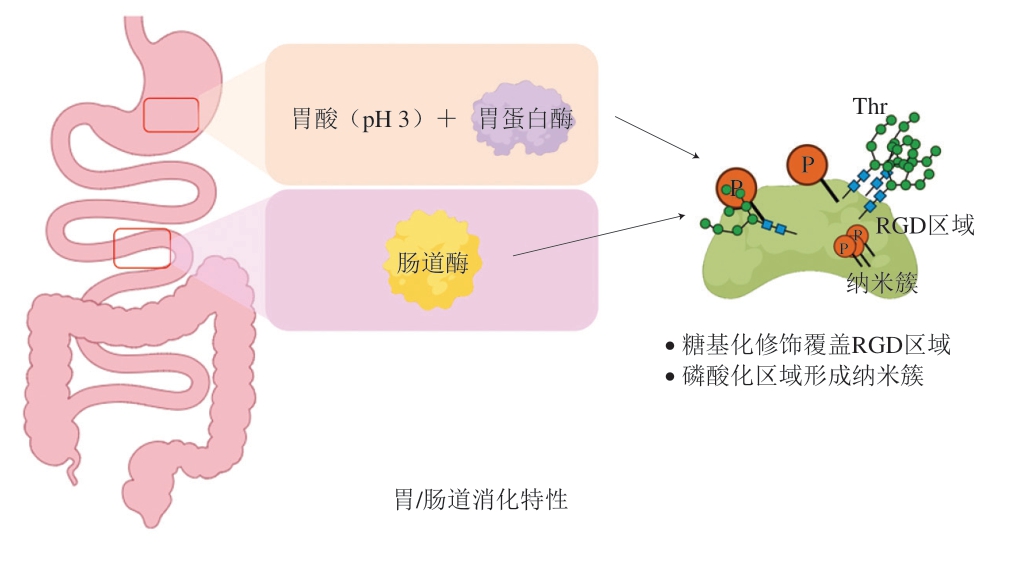
图3 胃/肠道消化特性
Fig. 3 Gastrointestinal digestion properties of OPN
3.2 吸收机制
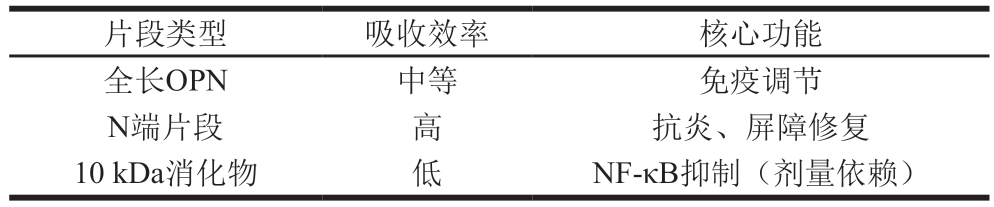
OPN的吸收主要发生在肠道上皮细胞,尤其是在胞吞作用和跨细胞转运的过程中。OPN及其消化产物是发挥其生物学活性的关键效应分子(表2)。研究表明,胃蛋白酶裂解产生的牛乳OPN片段Trp27-Phe151保留了OPN的功能性结构域,例如整合素结合区(RGD序列),能够以RGD依赖性方式结合αVβ3整合素[57],然后通过转胞吞作用穿过肠道屏障模型[34,42]。与全长OPN相比,天然存在的含有整合素结合序列RND(Arg-Asn-Asp)的N末端OPN片段更有效地结合肠道细胞,并且更有效地跨膜模型运输,在肠道中发挥免疫调节、抗炎和促进细胞黏附的功能[34]。例如适量其10 kDa消化物通过抑制核因子κB(nuclear factor kappa B,NF-κB)信号通路的激活减轻肠上皮细胞的炎症,增强肠上皮的屏障功能,但过高剂量的OPN可能具有一定的促炎作用[42]。除了整合素结合位点,OPN还有CD44结合位点,可以和肠上皮细胞上的CD44受体结合实现OPN及其肽段的跨膜转运[7-8,57]。膳食中牛乳OPN在8~24 h内被吸收并从循环中清除,ELISA试剂盒检测结果显示牛乳OPN占血浆总OPN的一小部分(<5%)。对人乳OPN研究表明,3 h后,完整或消化的OPN被吸收到胴体(62%)、小肠(23%)、胃(5%)和小肠灌流(4%)中,盲肠、肝脏、大脑、心脏和脾脏中均<2%[42]。
表2 全长与片段化OPN的生物活性功能对比
Table 2 Comparison of bioactivity between full-length and fragmented OPN
片段类型吸收效率核心功能全长OPN中等免疫调节N端片段高抗炎、屏障修复10 kDa消化物低NF-κB抑制(剂量依赖)
3.3 翻译后修饰对消化吸收特性的影响
磷酸化修饰是OPN功能调控的重要机制之一。磷酸化通过调节OPN折叠状态增强稳定性,增加表面负电荷形成空间位阻,同时改变构象暴露酶切位点,提升局部灵活性及结构伸长特性,从而影响其酶降解敏感性和消化动力学[45,58]。OPN的磷酸化对其生物利用度的影响是一个复杂且多层次调控的过程。例如,磷酸化程度与生物学效应密切相关,低磷酸化增强细胞黏附能力,高磷酸化则降低黏附性,C末端修饰特异性削弱αVβ3整合素结合能力,而去磷酸化OPN可通过CD44受体触发不同生物效应[26,59-61]。不同磷酸化位点主要通过电荷调控、空间构象改变和信号通路特异性激活等机制影响OPN的生物利用度。在受体结合与信号传导方面,磷酸化可能通过电荷排斥间接增强RGD与整合素结合,酪蛋白激酶II(casein kinase II,CKII)靶点(如Ser101)的磷酸化可激活FAKSrc-Rho通路以驱动细胞迁移与抗凋亡,而Ser46/Ser47/Thr50磷酸化簇则通过静电稳定CD44结合构象促进肿瘤转移[62-64]。磷酸化可降低OPN与肝素的结合亲和力,减少其在血管或细胞表面的滞留[45]。磷酸化对OPN的矿化具有抑制功能。Ser8-Ser11双磷酸化通过静电屏蔽钙离子显著延长羟基磷灰石(hydroxyapatite,HAP)成核诱导时间并抑制晶体相转变[65-66],而CKII靶点(如Ser107)磷酸化增强OPN与草酸钙晶体面结合,发挥抑制作用,减少结石形成[67]。从细胞类型到病理状态,OPN的磷酸化呈现显著异质性。成骨细胞(含21 个磷酸化位点)较成纤维细胞(4 个位点)的OPN具有更强的骨细胞黏附能力[60];乳腺癌微环境中OPN磷酸化水平与表皮生长因子受体磷酸化正相关,介导化疗耐药[64];辅助性T细胞17极化中,Ser179磷酸化可能通过增强与可诱导共刺激分子配体互作加剧炎症反应[68]。因此,磷酸化在OPN的胃肠道转运效率以及生物学功能发挥过程中扮演着重要角色,探索磷酸化在OPN消化吸收特性中的作用机制,对于OPN的功能性开发以及提高其生物利用度具有重要意义。
糖基化修饰为OPN功能调控的另一关键机制。糖基化(包括O-/N-糖型)通过改变OPN空间结构增强热稳定性,调节其与细胞表面受体结合能力,介导细胞内信号传导以调控增殖、迁移及炎症反应[69]。消化稳定性方面,糖链通过增加分子质量及构象保护显著提升抗酶解能力[57,70],延长消化道存留时间[9,42],其中特定糖型结构(如高甘露糖型、唾液酸化)可通过精细调控酶-底物互作和信号通路激活,实现功能多样性[71-72]。消化产物调控中,不同糖链结构导致差异化的生物活性产物生成,部分糖基化形式可保留或增强消化后产物的功能潜力。例如,高甘露糖型OPN消化产物激活磷脂酰肌醇3-激酶/蛋白激酶B(phosphatidylinositol 3-kinase/protein kinase B signaling pathway,PI3K/Akt)信号通路的效率是复杂型产物的1.8 倍,促进肿瘤细胞上皮-间质转化[73-74]。肠道吸收层面,糖基化通过N-糖型介导受体特异性结合促进胞吞内化[75],同时调节细胞膜流动性及表面电荷以优化吸收效率,其中受体介导途径为肠道吸收的核心机制[76]。这些表明,糖基化不仅维持OPN的结构稳定性,还通过动态调控其消化-吸收级联过程拓展其生物医学应用价值。
磷酸化与糖基化修饰通过空间构象重塑、电荷分布调控及分子间相互作用形成动态协同网络在OPN功能调控中发挥协同调控作用。磷酸化与糖基化修饰位点选择性互作。磷酸化(Ser8-Ser11/Ser101-Ser107簇)与O-糖基化(Thr/Pro-rich区)因空间分离形成动态平衡,磷酸化诱导构象伸展促进糖基转移酶识别远端Thr位点[1,20,45],而N-糖基化(Asn63、Asn90)通过空间位阻降低邻近激酶活性[77]。电荷层面,磷酸化强负电荷抑制糖链延伸(如唾液酸化),糖基化则通过中性糖链中和电荷减少蛋白酶识别[77-78]。磷酸化与糖基化通过空间屏蔽效应与电荷中和发挥抗酶解协同机制。磷酸化通过钙螯合形成致密纳米簇屏蔽切割位点(如RGD附近的非磷酸化区域)[58],糖基化则以体积效应覆盖蛋白酶识别基序(如Arg/Lys区)[1]。磷酸化区域的强负电荷(如Ser10-Ser11双磷酸化)与糖基化区域的弱负/中性电荷形成电荷梯度削弱切割位点处的酶静电吸引效应[46,78]。此外,磷酸化能增强局部刚性(如Ser101-Ser107氢键锁定),O-糖基化则通过熵效应稳定OPN的无序区(如N端),减少因构象波动产生的酶切位点暴露[45,78]。磷酸化与糖基化修饰在病理与生理环境中具有协同调控。例如,乳腺癌中Ser179磷酸化与Asn63糖基化协同增强其与整合素αVβ3的结合,减少尿激酶型纤溶酶原激活物对OPN的降解作用[60]。骨重塑时高磷酸化OPN与低糖基化协同抵抗Cathepsin K的降解[60,79]。矿化抑制中磷酸化OPN通过Ser8簇结合至HAP表面,其糖基化区域(如Thr136)通过氢键稳定结合构象,形成HAP保护层抑制酶解[46,78]。在此基础上,磷酸化通过整合素受体激活FAK磷酸化[80-81],糖基化调控CD44介导的细胞黏附[82-84],共同促进肠道上皮修复与免疫稳态等[85]。此外,磷酸化与糖基化修饰可协同调节OPN消化速度及产物功能活性(如免疫调控与信号传导)[60,86-87],使OPN的酶解产物根据修饰状态呈现差异化功能活性,为定向开发提供策略。这些多修饰协同作用揭示了OPN消化-吸收-功能效应的动态调控机制。
4 营养功能
OPN主要是靠其核心RGD基序与细胞表面整合素受体家族结合而发挥各种生理作用,这些整合素家族包括αVβ1、αVβ3、αVβ5、αVβ6、α5β1和α8β1整合素[88-89]。而α4β1和α9β1整合素通过其隐蔽的SVVYGLR序列结合OPN[90-91]。自然杀伤细胞通过OPN上的负电荷结合OPN[92-93]。OPN在Lys154-Ser155位点被纤溶酶裂解,产生一个N末端片段,与全长OPN相比,该片段与α5β1和αVβ3整合素亲和力更强[32]。此外,OPN还能与CD44受体相互作用。这些结构特征赋予了OPN在免疫细胞调控、炎症反应控制和组织修复中的重要生物学功能[7-8]。
4.1 免疫调节功能
乳中OPN的浓度比身体其他组织表达的OPN高几个数量级,这表明OPN作为乳中先天免疫系统的一部分在新生儿和婴儿免疫反应调控中发挥作用。乳OPN不仅通过直接与免疫细胞相互作用调控免疫反应,还通过其在消化系统中的代谢产物(活性肽)发挥抗炎、抗感染等作用。
OPN能够通过与巨噬细胞表面的整合素和CD44受体结合,激活巨噬细胞,促进其分泌多种炎症因子和抗微生物分子。激活后的巨噬细胞可以有效吞噬和清除病原体,同时通过分泌细胞因子如IL-12,调节后续的适应性免疫反应。OPN可结合无乳链球菌和金黄色葡萄球菌这两种细菌的所有已知血清型,并调理这些细菌以进行吞噬作用[92]。在另一项体外实验中,添加牛乳OPN的无菌脱脂奶通过抑制表皮链球菌的生长显示出剂量依赖性抗菌活性[94],表皮链球菌是一种常见的新生儿病原体,可在肠道易位后引起迟发性败血症[95]。总的来说,这些研究表明,牛乳OPN可以作为婴儿肠道中细胞因子产生的诱导剂、作为调理素标记细菌以供巨噬细胞清除或作为针对特定病原菌的抗菌剂发挥重要作用。
OPN在T细胞免疫反应中起关键作用。通过与整合素和CD44结合,OPN能够直接促进T细胞的活化,特别是在感染或免疫挑战时,它通过增强T细胞的增殖和细胞毒性,提升免疫系统的应答能力。OPN在调节T辅助细胞(T helper,Th)1型/Th2免疫反应平衡中起着重要作用。研究发现,OPN可以促进Th1型免疫反应,增强干扰素-γ的分泌,从而提高机体对细胞内病原体(如病毒和某些细菌)的抵抗能力。此外,OPN通过抑制Th2型反应减少过敏性和炎症性疾病的发生。牛乳OPN已被证明可在从肠道活检中分离的培养人固有层单核细胞中诱导T辅助细胞1细胞因子IL-12的表达[4]。进一步婴配粉添加牛乳OPN喂养婴儿研究表明,OPN强化配方奶粉组的肿瘤坏死因子α(tumor necrosis factor alpha,TNF-α)水平显著降低,发热的天数少于未添加OPN的配方奶粉组的婴儿,这表明牛乳OPN下调了人类婴儿的炎性细胞因子,OPN对婴儿的免疫系统有影响[96]。早产仔猪喂养OPN实验也表明,OPN猪的肠道绒毛与隐窝比高于饲喂牛奶对照组的猪,并且在第8天时单核细胞和淋巴细胞计数更高[94]。这些研究表明,膳食补充OPN可以影响肠道的免疫过程,促进婴儿健康。OPN在B细胞的发育和抗体生成中也发挥重要作用。研究发现,OPN能够促进B细胞的增殖和抗体生成,尤其在急性炎症和感染状态下,OPN可以增强抗体介导的免疫反应。
OPN通过多种途径调节炎症反应,具体表现为对促炎因子和抗炎因子的平衡调控。在急性炎症过程中,OPN消化产生的片段具有显著的抗炎作用,能够抑制炎症因子如TNF-α、IL-1β和IL-6的分泌,从而减轻炎症反应。Guo Zhengtao等[97]用人喉癌细胞株HEP-2进行OPN抗流感病毒实验,结果表明其半抑制浓度值为1.65 μmol/L,具有较好的抗病毒能力。与3’-唾液基乳糖联合使用,抑制率达到75%。其原因和细胞因子TNF-α、IL-6和诱导型一氧化氮合酶与mRNA表达相关的水平降低有关。这些抗炎作用在慢性炎症性疾病如肠炎、关节炎等病理状态中具有潜在的治疗价值。此外,OPN通过调节巨噬细胞和中性粒细胞的活性,有效限制炎症的扩展。OPN在炎症反应中具有双重作用,既可以促进炎症,又能在某些情况下起到抗炎作用。例如,OPN在自身免疫性疾病中表现出促进炎症的作用,而在感染性疾病中则可能具有保护作用。OPN在多种感染状态下表现出抗感染活性。通过增强免疫细胞的活化和迁移,OPN能够帮助机体更有效地清除病毒、细菌和其他病原体。尤其在肠道感染中,OPN通过增强肠道屏障功能,减少病原体穿透和感染。
4.2 促进大脑发育和认知功能
OPN被证明在动物的脑干、神经节中表达[98-99],OPN基因敲除小鼠模型幼崽的学习和记忆能力受损[13,100],在野生型小鼠喂养的幼仔的大脑中,观察到髓鞘形成相关蛋白的表达水平更高,神经胶质细胞向少突胶质细胞的分化和增殖增加[13]。这些研究表明,OPN可以改善小鼠幼崽大脑中的髓鞘形成,促进大脑发育,进而提高小鼠的认知能力发育[101]。
膳食补充OPN实验表明,注射外源性OPN诱导了暴露于缺氧缺血性损伤的大鼠的内源性OPN表达,并促进了神经系统发育[102]。仔猪补充OPN日粮实验神经影像学结果显示接受OPN饮食的猪的多个脑区体积增加[103],这些研究说明,添加牛乳OPN的婴配粉有助于促进婴儿的认知功能[104]。但目前这方面研究较少,也有研究补充OPN对早产猪的认知能力没有提升作用[94],因此还需要更多研究。
4.3 促进肠道健康功能
OPN能够通过调节肠道免疫环境诱导产生细胞因子[92],或调节肠道菌群促进有益微生物的增殖[105-106],或作为调理素标记细菌以供巨噬细胞清除或作为针对特定病原菌的抗菌剂,从而促进肠道的健康发育和功能维护。
研究表明,OPN在免疫细胞或肠上皮细胞中的内源性表达变化会影响正常和患病组织中肠道屏障的状态[107],例如,克罗恩病患者的肠上皮细胞中的OPN低表达与上皮屏障的破坏有关,血浆中OPN的水平与克罗恩病患者的炎症程度有关[108]。给葡聚糖硫酸钠诱导的急性结肠炎小鼠模型饲喂牛乳OPN,降低了疾病活动指数和肠道中性粒细胞活性,并增加了红细胞的数量,减少了T细胞,自然杀伤细胞和树突状细胞的数量也显著减少,结肠中转化生长因子β-1的表达较高,而促炎细胞因子的水平较低[56,109]。Aasmul-Olsen等[94]发现与饲喂不添加OPN的饮食的猪相比,饲喂补充牛乳OPN日粮的早产猪的小肠绒毛与隐窝比增加。这些研究表明,牛乳OPN会影响肠道细胞因子的产生和肠道细胞形态,包括肠道表面积,从而增强营养吸收,并对肠道炎症性疾病有缓解作用。
膳食OPN有可能影响肠道微生物组[105-106],乳OPN已被证明与乙醇饮食治疗小鼠中的细菌脂多糖结合,从而降低TNF-α表达和随后乙醇诱导的肝损伤发展[110-111]。OPN可以刺激色氨酸代谢和短链脂肪酸(short-chain fatty acids,SCFA)合成细菌的生长,包括双歧杆菌、真杆菌、普雷沃氏菌、别洛普雷沃菌、脱硫菌、丁酸球菌、丁酸单胞菌等,这些细菌从未消化的碳水化合物中产SCFA,从而增加肠膜中紧密连接蛋白的表达,被认为对肠道健康有益[110]。Han Lihua等[112]以6 mg/kg体质量的OPN剂量给高脂饮食(high-fat diet,HFD)妊娠大鼠补充牛乳OPN,发现OPN可减轻HFD引起的结肠炎症反应,提高了结肠闭锁小带蛋白-1和闭合蛋白-4的表达,提高了粪中拟杆菌门的相对丰度,而降低了变形菌门、幽门杆菌科和脱硫弧菌科的相对丰度。分析表明,牛乳OPN部分通过调节胆汁酸的生物合成改善HFD妊娠大鼠的肠道健康。而Chen Jianing等[105]研究发现,OPN可能通过引起肠道微生物组的改变而加剧HFD诱导的代谢功能障碍,OPN水平与人类身体质量指数之间呈强烈正相关。
口服牛乳OPN通过上调整合素αβ3和CD44的表达,促进肠道增殖和分化[7]。OPN在消化系统中的代谢产物(如小分子肽)能够增强肠上皮细胞的紧密连接和屏障功能,减少肠道渗透性,防止病原体的入侵。这种功能对于维持肠道稳态和减少炎症性肠病的发生具有重要意义[94]。
4.4 促进骨健康功能
OPN在骨代谢中起关键作用,参与骨生成、矿化和骨吸收等过程。它通过与整合素受体结合,促进成骨细胞的黏附和迁移,调节骨的生成和再吸收[113]。
OPN是骨基质的重要组成部分,主要由成骨细胞和骨细胞分泌。在骨生成过程中发挥重要作用,能够促进成骨细胞的黏附和迁移。它通过与整合素(如αVβ3和αVβ5)和CD44受体结合,激活下游信号通路(如PI3K/Akt通路和丝裂原活化蛋白激酶信号通路),调节成骨细胞的增殖和分化[21,114-115]。研究表明,OPN缺乏的小鼠表现出成骨细胞黏附和迁移能力的显著降低,导致骨形成受损[116]。
OPN在骨的矿化过程中也起重要作用。OPN通过与HAP结合,调节矿物质沉积和晶体生长,促进矿物质在骨基质中的沉积,从而增强骨的机械强度[21,114,117]。OPN的磷酸化状态对其与矿物质的结合能力具有重要影响,高度磷酸化增加了其与钙离子的亲和力,更有利于骨矿化过程[115]。在矿化过程中,OPN既可以作为促进剂,也可以作为抑制剂,具体作用取决于其局部浓度和微环境[118]。OPN通过其磷酸化位点与矿物质结合,稳定矿物质沉积,防止矿化过度和异常矿化[24]。此外,OPN还可以通过调节基质金属蛋白酶的活性,影响骨基质的降解和重塑[119]。
OPN在骨吸收中也扮演着重要角色。破骨细胞是负责骨吸收的主要细胞类型,OPN通过与破骨细胞表面的整合素αVβ3结合,调控破骨细胞的形成和活性,促进破骨细胞的黏附和活化[120],从而增强骨吸收的效率[121]。研究表明,OPN缺乏会导致破骨细胞的形成和活性受损,进而影响骨的再吸收过程[122-123]。此外,OPN还可以通过调控破骨细胞分化过程中关键信号通路(如NF-κB受体活化因子/NF-κB受体活化因子配体/骨保护素)的表达,调节破骨细胞的形成和功能,维持骨重塑的动态平衡[123],间接影响骨代谢。
研究发现,骨质疏松症患者的OPN表达水平显著升高[116],可能通过调节成骨细胞和破骨细胞的活性,影响骨的生成和吸收过程[124]。通过膳食补充OPN,可以调节成骨细胞和破骨细胞的活性,促进骨的形成和抑制骨的再吸收,提高骨密度,从而预防和治疗骨质疏松症,减少骨折风险[118,125-127]。同样,在骨折早期,OPN的表达显著增加,OPN通过促进成骨细胞的黏附和迁移,加速骨折部位的新骨形成,从而促进骨折的愈合[118]。OPN还可以调节骨髓间充质干细胞的分化,进一步支持骨折修复[128]。此外,OPN还可以通过调节炎症反应,促进愈合环境的优化,进一步加速骨折愈合。研究表明,缺乏OPN的小鼠在骨折愈合过程中表现出显著的延迟,提示OPN在骨折愈合中的关键作用。
5 新食品原料的应用与前景展望
目前,商业化乳源性OPN主要通过从牛乳中分离纯化获得,代表企业为欧洲Arla食品公司。该公司生产的基于牛乳源OPN的产品Lacprodan® OPN-10已完成较为全面的安全性评估[129],并且通过EFSA的新型食品安全认证,获准作为婴儿配方乳粉中的食品添加剂使用。EFSA建议其在重组即饮型婴儿配方乳粉中的最大添加量为151 mg/L,相当于每升配方乳粉中含有约109 mg的牛乳OPN。在毒理学评估方面,乳OPN已通过多项标准化实验验证其安全性,包括细菌回复突变试验、体外哺乳动物细胞染色体畸变试验和体内微核试验,均未发现其具有遗传毒性。同时,亚慢性毒性和致畸性研究结果也未发现显著不良反应,支持其作为新食品原料的应用前景[10]。动物模型[37,94,130]及婴儿临床研究[5,96]进一步证实了牛乳OPN的生物学功能和安全性。牛乳OPN对婴儿生长无不良影响,未改变免疫系统发育轨迹,亦未对胃肠道或脑部发育造成不良影响。然而,为进一步完善其安全性证据,仍需开展更多高质量临床研究,重点评估其在吸收、分布、代谢和排泄方面的特征,以及其在免疫和认知等关键发育指标上的长期作用[42]。
尽管牛乳OPN已获得欧盟新型食品认证,我国尚未出台针对OPN使用的国家标准或监管法规,相关提取技术及功能性研究尚处于起步阶段。未来,应加强对OPN生物功能与安全性的系统研究,推动其在婴幼儿配方乳粉等特殊人群食品中的科学应用,助力我国乳品行业实现高质量、规范化发展。
6 结 语
近年来,乳OPN作为一种功能性蛋白质,因其在免疫调节、促进大脑发育和认知功能、肠道健康、骨健康等方面的重要作用而受到广泛关注。在营养食品(如婴幼儿奶粉、功能性食品)、骨骼健康、肠道健康维护,以及可能的医疗领域如炎症调节和神经发育支持等方面具有优秀的应用前景。随着欧盟批准了牛乳OPN作为新食品原料用于婴配粉等食品中,未来关于OPN提取工艺、结构性质、消化吸收以及营养健康功能等研究也将愈来愈受到重视。在结构性质方面,目前关于OPN在乳中以及胃肠道体内消化水解的肽段种类特征还不清楚,不同肽段吸收特性及功能研究缺乏,尤其是磷酸化糖基化修饰对肽段功能影响机制有待研究。在消化吸收方面,尽管已有大量关于OPN在消化道中吸收机制的研究,未来的工作仍需深入探讨不同大小和修饰形式的OPN肽段在体内的吸收动力学及其在不同器官中的分布。在营养功能方面,OPN在免疫调节、大脑发育和认知功能、肠道健康和骨骼健康方面有重要作用。未来需要更多的临床研究验证OPN作为食品添加剂的长期健康效应。特别是在婴幼儿和老年人群中的应用,需要通过大规模的临床试验评估其安全性和有效性,以及通过工艺优化和配方调整提高OPN的生物利用度以最大化其营养功能。此外,由于牛乳中OPN含量很低,提取工艺复杂,成本高,因此利用新的合成生物学技术开发基于发酵工程的OPN制备工艺将成为未来发展趋势。
[1] SØRENSEN E S, PETERSEN T E, HØJRUP P. Posttranslational modifications of bovine osteopontin: identification of twenty-eight phosphorylation and three O-glycosylation sites[J]. Protein Science,1995, 4(10): 2040-2049. DOI:10.1002/pro.5560041009.
[2] FRANZÉN A, HEINEGÅRD D. Isolation and characterization of two sialoproteins present only in bone calcified matrix[J]. Biochemical Journal, 1985, 232(3): 715-724. DOI:10.1042/bj2320715.
[3] SENGER D R, PERRUZZI C A, PAPADOPOULOS A, et al.Purification of a human milk protein closely similar to tumor-secreted phosphoproteins and osteopontin[J]. Biochimica et Biophysica Acta(BBA): Protein Structure and Molecular Enzymology, 1989, 996(1/2):43-48. DOI:10.1016/0167-4838(89)90092-7.
[4] SCHACK L, LANGE A, KELSEN J, et al. Considerable variation in the concentration of osteopontin in human milk, bovine milk, and infant formulas[J]. Journal of Dairy Science, 2009, 92(11): 5378-5385.DOI:10.3168/jds.2009-2360.
[5] JIANG R L, LÖNNERDAL B. Osteopontin in human milk and infant formula affects infant plasma osteopontin concentrations[J]. Pediatric Research, 2019, 85(4): 502-505. DOI:10.1038/s41390-018-0271-x.
[6] SØRENSEN E S, PETERSEN T E. Purification and characterization of three proteins isolated from the proteose peptone fraction of bovine milk[J]. The Journal of Dairy Research, 1993, 60(2): 189-197.DOI:10.1017/s0022029900027503.
[7] JIANG R L, LO J, PRELL C, et al. Milk osteopontin promotes intestinal development by up-regulating the expression of integrin αvβ3 and CD44[J]. FASEB Journal, 2023, 37(6): e22988. DOI:10.1096/fj.202300092R.
[8] JIANG R L, LÖNNERDAL B. Effects of milk osteopontin on intestine,neurodevelopment, and immunity[J]. Nestle Nutrition Institute Workshop Series, 2020, 94: 152-157. DOI:10.1159/000505067.
[9] SØRENSEN E S, CHRISTENSEN B. Milk osteopontin and human health[J]. Nutrients, 2023, 15(11): 2423. DOI:10.3390/nu15112423.
[10] EFSA Panel on Nutrition, Novel Foods and Food Allergens (NDA),TURCK D, et al. Safety of bovine milk osteopontin as a Novel food pursuant to Regulation (EU) 2015/2283[J]. EFSA Journal, 2022, 20(5):e07137. DOI:10.2903/j.efsa.2022.7137.
[11] CHRISTENSEN B, ZACHARIAE E D, POULSEN N A, et al. Factors influencing milk osteopontin concentration based on measurements from Danish Holstein cows[J]. The Journal of Dairy Research, 2021,88(1): 89-94. DOI:10.1017/S0022029921000054.
[12] HU B, ZHANG J S, JIANG Y R, et al. Quantitative determination of osteopontin in bovine, buffalo, yak, sheep and goat milk by ultrahigh performance liquid chromatography-tandem mass spectrometry and stable isotope dimethyl labeling[J]. Food Chemistry, 2021, 343:128489. DOI:10.1016/j.foodchem.2020.128489.
[13] JIANG R L, PRELL C, LÖNNERDAL B. Milk osteopontin promotes brain development by up-regulating osteopontin in the brain in early life[J]. The FASEB Journal, 2019, 33(2): 1681-1694. DOI:10.1096/fj.201701290RR.
[14] ZOU Z Z, DULEY J A, COWLEY D M, et al. Physicochemical properties and whey proteomes of camel milk powders produced by different concentration and dehydration processes[J]. Foods, 2022,11(5): 727. DOI:10.3390/foods11050727.
[15] ZHU J, YU X, WANG Y R, et al. Longitudinal changes of lactopontin(milk osteopontin) in term and preterm human milk[J]. Frontiers in Nutrition, 2022, 9: 962802. DOI:10.3389/fnut.2022.962802.
[16] AKSAN A, ERDAL I, YALCIN S S, et al. Osteopontin levels in human milk are related to maternal nutrition and infant health and growth[J].Nutrients, 2021, 13(8): 2670. DOI:10.3390/nu13082670.
[17] BRUUN S, JACOBSEN L N, ZE X L, et al. Osteopontin levels in human milk vary across countries and within lactation period: data from a multicenter study[J]. Journal of Pediatric Gastroenterology and Nutrition, 2018, 67(2): 250-256. DOI:10.1097/MPG.0000000000002004.
[18] DUDEMAINE P L, THIBAULT C, ALAIN K, et al. Genetic variations in the SPP1 promoter affect gene expression and the level of osteopontin secretion into bovine milk[J]. Animal Genetics, 2014,45(5): 629-640. DOI:10.1111/age.12176.
[19] MASUDA K, TAKAHASHI N, TSUKAMOTO Y, et al. N-Glycan structures of an osteopontin from human bone[J]. Biochemical and Biophysical Research Communications, 2000, 268(3): 814-817.DOI:10.1006/bbrc.2000.2224.
[20] CHRISTENSEN B, NIELSEN M S, HASELMANN K F, et al.Post-translationally modified residues of native human osteopontin are located in clusters: identification of 36 phosphorylation and five O-glycosylation sites and their biological implications[J]. The Biochemical Journal, 2005, 390(Pt 1): 285-292. DOI:10.1042/BJ20050341.
[21] SODEK J, GANSS B, MCKEE M D. Osteopontin[J]. Critical Reviews in Oral Biology & Medicine, 2000, 11(3): 279-303. DOI:10.1177/10454411000110030101.
[22] 罗元理, 于雪, 窦宇琪, 等. 牛乳与山羊乳中乳桥蛋白的比较研究[J]. 中国乳品工业, 2023, 51(2): 10-14; 31. DOI:10.19827/j.issn1001-2230.2023.02.002.
[23] KLÄNING E, CHRISTENSEN B, SØRENSEN E S, et al. Osteopontin binds multiple calcium ions with high affinity and independently of phosphorylation status[J]. Bone, 2014, 66: 90-95. DOI:10.1016/j.bone.2014.05.020.
[24] HOLM E, GLEBERZON J S, LIAO Y Y, et al. Osteopontin mediates mineralization and not osteogenic cell development in vitro[J]. Biochemical Journal, 2014, 464(3): 355-364. DOI:10.1042/bj20140702.
[25] ERIKSON D W, BURGHARDT R C, BAYLESS K J, et al. Secreted phosphoprotein 1 (SPP1, osteopontin) binds to integrin αvβ6 on porcine trophectoderm cells and integrin αvβ3 on uterine luminal epithelial cells, and promotes trophectoderm cell adhesion and migration[J].Biology of Reproduction, 2009, 81(5): 814-825. DOI:10.1095/biolreprod.109.078600.
[26] CHRISTENSEN B, KLÄNING E, NIELSEN M S, et al. C-Terminal modification of osteopontin inhibits interaction with the αVβ3-integrin[J]. Journal of Biological Chemistry, 2012, 287(6): 3788-3797.DOI:10.1074/jbc.M111.277996.
[27] BOSKEY A L, CHRISTENSEN B, TALEB H, et al. Posttranslational modification of osteopontin: effects on in vitro hydroxyapatite formation and growth[J]. Biochemical and Biophysical Research Communications, 2012, 419(2): 333-338. DOI:10.1016/j.bbrc.2012.02.024.
[28] CHRISTENSEN B, SØRENSEN E S. Structure, function and nutritional potential of milk osteopontin[J]. International Dairy Journal, 2016, 57: 1-6. DOI:10.1016/j.idairyj.2016.02.034.
[29] WEBER G F. The phylogeny of osteopontin-analysis of the protein sequence[J]. International Journal of Molecular Sciences, 2018, 19(9):2557. DOI:10.3390/ijms19092557.
[30] BAYLESS K J, MEININGER G A, SCHOLTZ J M, et al. Osteopontin is a ligand for the α4β1 integrin[J]. Journal of Cell Science, 1998, 111 (Pt 9):1165-1174. DOI:10.1242/jcs.111.9.1165.
[31] CHRISTENSEN B, SØRENSEN E S. Osteopontin is highly susceptible to cleavage in bovine milk and the proteolytic fragments bind the αVβ3-integrin receptor[J]. Journal of Dairy Science, 2014,97(1): 136-146. DOI:10.3168/jds.2013-7223.
[32] CHRISTENSEN B, SCHACK L, KLÄNING E, et al. Osteopontin is cleaved at multiple sites close to its integrin-binding motifs in milk and is a novel substrate for plasmin and cathepsin D[J]. Journal of Biological Chemistry, 2010, 285(11): 7929-7937. DOI:10.1074/jbc.M109.075010.
[33] BISSONNETTE N, DUDEMAINE P L, THIBAULT C, et al.Proteomic analysis and immunodetection of the bovine milk osteopontin isoforms[J]. Journal of Dairy Science, 2012, 95(2): 567-579. DOI:10.3168/jds.2011-4750.
[34] CHRISTENSEN B, NIELSEN N R, SØRENSEN M R, et al. Naturally occurring N-terminal fragments of bovine milk osteopontin are transported across models of the intestinal barrier[J]. Biomedicines,2023, 11(3): 893. DOI:10.3390/biomedicines11030893.
[35] AZUMA N, MAETA A, FUKUCHI K, et al. A rapid method for purifying osteopontin from bovine milk and interaction between osteopontin and other milk proteins[J]. International Dairy Journal,2006, 16(4): 370-378. DOI:10.1016/j.idairyj.2005.03.012.
[36] YAMNIUK A P, BURLING H, VOGEL H J. Thermodynamic characterization of the interactions between the immunoregulatory proteins osteopontin and lactoferrin[J]. Molecular Immunology, 2009,46(11/12): 2395-2402. DOI:10.1016/j.molimm.2009.04.024.
[37] JIANG R L, LIU L, DU X G, et al. Evaluation of bioactivities of the bovine milk lactoferrin-osteopontin complex in infant formulas[J].Journal of Agricultural and Food Chemistry, 2020, 68(22): 6104-6111.DOI:10.1021/acs.jafc.9b07988.
[38] LIU L, JIANG R L, LIU J X, et al. The bovine lactoferrin-osteopontin complex increases proliferation of human intestinal epithelial cells by activating the PI3K/Akt signaling pathway[J]. Food Chemistry, 2020,310: 125919. DOI:10.1016/j.foodchem.2019.125919.
[39] DALL’ASTA C, FLORIO P, LAMMARDO A M, et al. Development of an in vitro digestive model for studying the peptide profile of breast milk[J]. International Journal of Food Sciences and Nutrition, 2015,66(4): 409-415. DOI:10.3109/09637486.2015.1042846.
[40] LIU L, JIANG R L, LÖNNERDAL B. Assessment of bioactivities of the human milk lactoferrin-osteopontin complex in vitro[J]. The Journal of Nutritional Biochemistry, 2019, 69: 10-18. DOI:10.1016/j.jnutbio.2019.03.016.
[41] GOULDING D A, BONNET N, HORCAJADA M N, et al. The impact of complexation or complex coacervation of lactoferrin and osteopontin on simulated infant gastrointestinal digestion, intestinal inflammation, and in vivo bone development[J]. Food & Function,2024, 15(19): 9928-9940. DOI:10.1039/d4fo02790f.
[42] FLEMING S A, REYES S M, DONOVAN S M, et al. An expert panel on the adequacy of safety data and physiological roles of dietary bovine osteopontin in infancy[J]. Frontiers in Nutrition, 2024, 11:1404303. DOI:10.3389/fnut.2024.1404303.
[43] LEVY E, MARCIL V, BAUMEL S T É, et al. Lactoferrin, osteopontin and lactoferrin-osteopontin complex: a critical look on their role in perinatal period and cardiometabolic disorders[J]. Nutrients, 2023,15(6): 1394. DOI:10.3390/nu15061394.
[44] CHEN Y, QU S, HUANG Z, et al. Analysis and comparison of key proteins in Maiwa yak and bovine milk using high-performance liquid chromatography mass spectrometry[J]. Journal of Dairy Science, 2021,104(8): 8661-8672. DOI:10.3168/jds.2021-20269.
[45] MATEOS B, HOLZINGER J, CONRAD-BILLROTH C, et al.Hyperphosphorylation of human osteopontin and its impact on structural dynamics and molecular recognition[J]. Biochemistry, 2021,60(17): 1347-1355. DOI:10.1021/acs.biochem.1c00050.
[46] AZZOPARDI P V, O’YOUNG J, LAJOIE G, et al. Roles of electrostatics and conformation in protein-crystal interactions[J]. PLoS ONE, 2010, 5(2): e9330. DOI:10.1371/journal.pone.0009330.
[47] BAI W L, YANG R J, YIN R H, et al. Molecular characterization and expression analysis of osteopontin cDNA from lactating mammary gland in yak (Bos grunniens)[J]. Molecular Biology Reports, 2012,39(4): 3627-3635. DOI:10.1007/s11033-011-1137-z.
[48] DU J M, HOU S, ZHONG C, et al. Molecular basis of recognition of human osteopontin by 23C3, a potential therapeutic antibody for treatment of rheumatoid arthritis[J]. Journal of Molecular Biology,2008, 382(4): 835-842. DOI:10.1016/j.jmb.2008.07.075.
[49] LYU Y P, WEN X, HU J Q, et al. Compendium of lactopontin:molecular structure, manufacturing process and biological functions[J].Food Bioscience, 2025, 65: 106155. DOI:10.1016/j.fbio.2025.106155.
[50] GOULDING D A, BOVETTO L, O’REGAN J, et al. Rheological and microstructural properties of heteroprotein complex coacervates formed by lactoferrin and osteopontin[J]. Food Hydrocolloids, 2024,147: 109231. DOI:10.1016/j.foodhyd.2023.109231.
[51] MARCANO O A, MARKUSHIN Y, MELIKECHI N, et al. Fourier transform infrared spectroscopy of deuterated proteins[C]//Linear and Nonlinear Optics of Organic Materials VIII. SPIE, 2008, 7049: 201-208. DOI:10.1117/12.794878.
[52] LENTON S, SEYDEL T, NYLANDER T, et al. Dynamic footprint of sequestration in the molecular fluctuations of osteopontin[J]. Journal of the Royal Society, Interface, 2015, 12(110): 0506. DOI:10.1098/rsif.2015.0506.
[53] KURZBACH D, PLATZER G, SCHWARZ T C, et al. Cooperative unfolding of compact conformations of the intrinsically disordered protein osteopontin[J]. Biochemistry, 2013, 52(31): 5167-5175.DOI:10.1021/bi400502c.
[54] CHATTERTON D E W, RASMUSSEN J T, HEEGAARD C W,et al. In vitro digestion of novel milk protein ingredients for use in infant formulas: research on biological functions[J]. Trends in Food Science & Technology, 2004, 15(7/8): 373-383. DOI:10.1016/j.tifs.2003.12.004.
[55] RITTLING S R, WEJSE P L, YAGIZ K, et al. Suppression of tumour growth by orally administered osteopontin is accompanied by alterations in tumour blood vessels[J]. British Journal of Cancer, 2014,110(5): 1269-1277. DOI:10.1038/bjc.2014.10.
[56] DA SILVA A P B, ELLEN R P, SØRENSEN E S, et al. Osteopontin attenuation of dextran sulfate sodium-induced colitis in mice[J].Laboratory Investigation, 2009, 89(10): 1169-1181. DOI:10.1038/labinvest.2009.80.
[57] CHRISTENSEN B, KARLSEN N J, JØRGENSEN S D S, et al.Milk osteopontin retains integrin-binding activity after in vitro gastrointestinal transit[J]. Journal of Dairy Science, 2020, 103(1): 42-51. DOI:10.3168/jds.2019-17212.
[58] LENTON S, GRIMALDO M, ROOSEN-RUNGE F, et al. Effect of phosphorylation on a human-like osteopontin peptide[J]. Biophysical Journal, 2017, 112(8): 1586-1596. DOI:10.1016/j.bpj.2017.03.005.
[59] CHEN C, ZHAO S J, KARNAD A, et al. The biology and role of CD44 in cancer progression: therapeutic implications[J]. Journal of Hematology & Oncology, 2018, 11(1): 64. DOI:10.1186/s13045-018-0605-5.
[60] CHRISTENSEN B, KAZANECKI C C, PETERSEN T E, et al. Cell type-specific post-translational modifications of mouse osteopontin are associated with different adhesive properties[J]. The Journal of Biological Chemistry, 2007, 282(27): 19463-19472. DOI:10.1074/jbc.M703055200.
[61] SCHYTTE G N, CHRISTENSEN B, BREGENOV I, et al. FAM20C phosphorylation of the RGDSVVYGLR motif in osteopontin inhibits interaction with the αvβ3 integrin[J]. Journal Of Cellular Biochemistry,2020, 121(12): 4809-4818. DOI:10.1002/jcb.29708.
[62] DAS R, MAHABELESHWAR G H, KUNDU G C. Osteopontin induces AP-1-mediated secretion of urokinase-type plasminogen activator through c-Src-dependent epidermal growth factor receptor transactivation in breast cancer cells[J]. Journal of Biological Chemistry, 2004, 279(12): 11051-11064. DOI:10.1074/jbc.M310256200.
[63] HSIEH Y H, VAN DER HEYDE H, OH E S, et al. Osteopontin mediates tumorigenic transformation of a preneoplastic murine cell line by suppressing anoikis: an Arg-Gly-Asp-dependent-focal adhesion kinase-caspase-8 axis[J]. Molecular Carcinogenesis, 2015, 54(5): 379-392. DOI:10.1002/mc.22108.
[64] KARIYA Y, OYAMA M, KARIYA Y, et al. Phosphorylated osteopontin secreted from cancer cells induces cancer cell motility[J].Biomolecules, 2021, 11(9): 1323. DOI:10.3390/biom11091323.
[65] 李诗燕. 磷酸化Osteopontin抑制磷酸钙和草酸钙结晶的动力学研究[D].武汉: 华中农业大学, 2015.
[66] DE BRUYN J R, GOIKO M, MOZAFFARI M, et al. Dynamic light scattering study of inhibition of nucleation and growth of hydroxyapatite crystals by osteopontin[J]. PLoS ONE, 2013, 8(2):e56764. DOI:10.1371/journal.pone.0056764.
[67] WANG L J, GUAN X Y, TANG R K, et al. Phosphorylation of osteopontin is required for inhibition of calcium oxalate crystallization[J]. The Journal of Physical Chemistry. B, 2008,112(30): 9151-9157. DOI:10.1021/jp804282u.
[68] INOUE M, SHINOHARA M L. Intracellular osteopontin (iOPN)and immunity[J]. Immunologic Research, 2011, 49(1/2/3): 160-172.DOI:10.1007/s12026-010-8179-5.
[69] 刘中静, 乔里, 叶朝阳, 等. Opsin3糖基化位点的鉴定及糖基化修饰功能[J]. 生物工程学报, 2022, 38(3): 1173-1182. DOI:10.13345/j.cjb.210488.
[70] MIWA H E, GERKEN T A, JAMISON O, et al. Isoform-specific O-glycosylation of osteopontin and bone sialoprotein by polypeptide N-acetylgalactosaminyltransferase-1[J]. Journal of Biological Chemistry, 2010, 285(2): 1208-1219. DOI:10.1074/jbc.M109.035436.
[71] WANG L B, NIU X Y. Immunoregulatory roles of osteopontin in diseases[J]. Nutrients, 2024, 16(2): 312. DOI:10.3390/nu16020312.
[72] MINAI-TEHRANI A, CHANG S H, PARK S B, et al. The O-glycosylation mutant osteopontin alters lung cancer cell growth and migration in vitro and in vivo[J]. International Journal of Molecular Medicine, 2013, 32(5): 1137-1149. DOI:10.3892/ijmm.2013.1483.
[73] MOREMEN K W, TIEMEYER M, NAIRN A V. Vertebrate protein glycosylation: diversity, synthesis and function[J]. Nature Reviews.Molecular Cell Biology, 2012, 13(7): 448-462. DOI:10.1038/nrm3383.
[74] THIBODEAUX C, III C M, PROF H L. Natural-product sugar biosynthesis and enzymatic glycodiversification[J]. Angewandte Chemie International Edition, 2008, 47(51): 9814-9859. DOI:10.1002/anie.200801204.
[75] REGGIORI F, GABIUS H J, AURELI M, et al. Glycans in autophagy,endocytosis and lysosomal functions[J]. Glycoconjugate Journal, 2021,38(5): 625-647. DOI:10.1007/s10719-021-10007-x.
[76] FENG G N, ZHOU Y, YAN J B, et al. Proteomic and N-glycoproteomic analyses of total subchondral bone protein in patients with primary knee osteoarthritis[J]. Journal of Proteomics, 2023, 280: 104896.DOI:10.1016/j.jprot.2023.104896.
[77] 陈万方. OPN N-糖基化修饰对子宫内膜容受性建立的调控机制研究[D]. 大连: 大连医科大学, 2019. DOI:10.26994/d.cnki.gdlyu.2019.000797.
[78] HOLZINGER J, KOTISCH H, RICHTER K W, et al. Binding mode characterization of osteopontin on hydroxyapatite by solution NMR spectroscopy[J]. ChemBioChem, 2021, 22(13): 2300-2305.DOI:10.1002/cbic.202100139.
[79] SALIH E, ASHKAR S, GERSTENFELD L C, et al. Identification of the phosphorylated sites of metabolically 32P-labeled osteopontin from cultured chicken osteoblasts[J]. Journal of Biological Chemistry,1997, 272(21): 13966-13973. DOI:10.1074/jbc.272.21.13966.
[80] 李菁菁, 温进坤, 韩梅. 骨桥蛋白趋化和趋触作用对FAK和ILK磷酸化修饰的影响[J]. 细胞生物学杂志, 2007, 29(4): 550-554.DOI:10.3969/j.issn.1674-7666.2007.04.019.
[81] 杨萍萍, 张微, 迟立君. 骨桥蛋白在免疫相关性疾病中作用的分子机制新进展[J]. 免疫学杂志, 2017, 33(3): 263-267. DOI:10.13431/j.cnki.immunol.j.20170047.
[82] LIAO C C, WANG Q, AN J X, et al. CD44 glycosylation as a therapeutic target in oncology[J]. Frontiers in Oncology, 2022, 12:883831. DOI:10.3389/fonc.2022.883831.
[83] WEBER G F, ASHKAR S, GLIMCHER M J, et al. Receptor-ligand interaction between CD44 and osteopontin (Eta-1)[J]. Science, 1996,271: 509-512. DOI:10.1126/science.271.5248.509.
[84] ASHKAR S, WEBER G F, PANOUTSAKOPOULOU V, et al.Eta-1 (osteopontin): an early component of type-1 (cell-mediated)immunity[J]. Science, 2000, 287(5454): 860-864. DOI:10.1126/science.287.5454.860.
[85] 孙海艳, 李岩, 刘银坤. 骨桥蛋白表达和翻译后修饰与肿瘤生物学行为的关系[J]. 生命的化学, 2010, 30(6): 885-888. DOI:10.13488/j.smhx.2010.06.029.
[86] CASTELLO M L, RAINERI D, SALMI L, et al. Osteopontin at the crossroads of inflammation and tumor progression[J]. Mediators of Inflammation, 2017, 282(27): 4049098. DOI:10.1155/2017/4049098 .
[87] SINGH A, GILL G, KAUR H, et al. Role of osteopontin in bone remodeling and orthodontic tooth movement: a review[J]. Progress in Orthodontics, 2018, 19(1): 18. DOI:10.1186/s40510-018-0216-2.
[88] YOKOSAKI Y, TANAKA K, HIGASHIKAWA F, et al. Distinct structural requirements for binding of the integrins αvβ6, αvβ3, αvβ5,α5β1 and α9β1 to osteopontin[J]. Matrix Biology, 2005, 24(6): 418-427.DOI:10.1016/j.matbio.2005.05.005.
[89] ICER M A, GEZMEN-KARADAG M. The multiple functions and mechanisms of osteopontin[J]. Clinical Biochemistry, 2018, 59: 17-24.DOI:10.1016/j.clinbiochem.2018.07.003.
[90] BAYLESS K J, DAVIS G E. Identification of dual α4β1 integrin binding sites within a 38 amino acid domain in the N-terminal thrombin fragment of human osteopontin[J]. Journal of Biological Chemistry, 2001, 276(16):13483-13489. DOI:10.1074/jbc.M011392200.
[91] YOKOSAKI Y, MATSUURA N, SASAKI T, et al. The integrin α9β1 binds to a novel recognition sequence (SVVYGLR) in the thrombincleaved amino-terminal fragment of osteopontin[J]. Journal of Biological Chemistry, 1999, 274(51): 36328-36334. DOI:10.1074/jbc.274.51.36328.
[92] SCHACK L, STAPULIONIS R, CHRISTENSEN B, et al. Osteopontin enhances phagocytosis through a novel osteopontin receptor, the αXβ2 integrin[J]. Journal of Immunology, 2009, 182(11): 6943-6950.DOI:10.4049/jimmunol.0900065.
[93] KLÄNING E, CHRISTENSEN B, BAJIC G, et al. Multiple low-affinity interactions support binding of human osteopontin to integrin αXβ2[J]. Biochimica et Biophysica Acta (BBA)-Proteins and Proteomics, 2015, 1854(8): 930-938. DOI:10.1016/j.bbapap.2015.03.008.
[94] AASMUL-OLSEN K, HENRIKSEN N L, NGUYEN D N, et al.Milk osteopontin for gut, immunity and brain development in preterm pigs[J]. Nutrients, 2021, 13(8): 2675. DOI:10.3390/nu13082675.
[95] GOLIŃSKA E, STRUS M, TOMUSIAK-PLEBANEK A, et al.Coagulase-negative staphylococci contained in gut microbiota as a primary source of sepsis in low- and very low birth weight neonates[J].Journal of Clinical Medicine, 2020, 9(8): 2517. DOI:10.3390/jcm9082517.
[96] LÖNNERDAL B, KVISTGAARD A S, PEERSON J M, et al. Growth,nutrition, and cytokine response of breast-fed infants and infants fed formula with added bovine osteopontin[J]. Journal of Pediatric Gastroenterology and Nutrition, 2016, 62(4): 650-657. DOI:10.1097/MPG.0000000000001005.
[97] GUO Z T, XIE Q G, REN Q Q, et al. Enhancing immune regulation in vitro: the synergistic impact of 3’-sialyllactose and osteopontin in a nutrient blend following influenza virus infection[J]. Frontiers in Immunology, 2024, 15: 1271926. DOI:10.3389/fimmu.2024.1271926.
[98] CHOI J S, CHA J H, PARK H J, et al. Transient expression of osteopontin mRNA and protein in amoeboid microglia in developing rat brain[J]. Experimental Brain Research, 2004, 154(3): 275-280.DOI:10.1007/s00221-003-1657-4.
[99] LEE M Y, CHOI J S, LIM S W, et al. Expression of osteopontin mRNA in developing rat brainstem and cerebellum[J]. Cell and Tissue Research, 2001, 306(2): 179-185. DOI:10.1007/s004410100456.
[100] JIANG R L, LÖNNERDAL B. Evaluation of bioactivities of bovine milk osteopontin using a knockout mouse model[J]. Journal of Pediatric Gastroenterology and Nutrition, 2020, 71(1): 125-131.DOI:10.1097/MPG.0000000000002702.
[101] SELVARAJU R, BERNASCONI L, LOSBERGER C, et al.Osteopontin is upregulated during in vivo demyelination and remyelination and enhances myelin formation in vitro[J]. Molecular and Cellular Neuroscience, 2004, 25(4): 707-721. DOI:10.1016/j.mcn.2003.12.014.
[102] CHEN W Q, MA Q Y, SUZUKI H, et al. Osteopontin reduced hypoxia-ischemia neonatal brain injury by suppression of apoptosis in a rat pup model[J]. Stroke, 2011, 42(3): 764-769. DOI:10.1161/STROKEAHA.110.599118.
[103] JOUNG S, FIL J E, HECKMANN A B, et al. Earlylife supplementation of bovine milk osteopontin supports neurodevelopment and influences exploratory behavior[J]. Nutrients,2020, 12(8): 2206. DOI:10.3390/nu12082206.
[104] HORTA B L, DE MOLA C L, VICTORA C G. Breastfeeding and intelligence: a systematic review and meta-analysis[J]. Acta Paediatrica, 2015, 104: 14-19. DOI:10.1111/apa.13139.
[105] CHEN J N, ZENG P, GONG L, et al. Osteopontin exacerbates high-fat diet-induced metabolic disorders in a microbiome-dependent manner[J].mBio, 2022, 13(6): e0253122. DOI:10.1128/mbio.02531-22.
[106] SMITH B N, HANNAS M, ORSO C, et al. Dietary osteopontinenriched algal protein as nutritional support in weaned pigs infected with F18-fimbriated enterotoxigenic Escherichia coli[J]. Journal of Animal Science, 2020, 98(10): skaa314. DOI:10.1093/jas/skaa314.
[107] GASSLER N, AUTSCHBACH F, GAUER S, et al. Expression of osteopontin (Eta-1) in Crohn disease of the terminal ileum[J].Scandinavian Journal of Gastroenterology, 2002, 37(11): 1286-1295.DOI:10.1080/003655202761020560.
[108] AGNHOLT J, KELSEN J, SCHACK L, et al. Osteopontin, a protein with cytokine-like properties, is associated with inflammation in Crohn’s disease[J]. Scandinavian Journal of Immunology, 2007, 65(5):453-460. DOI:10.1111/j.1365-3083.2007.01908.x.
[109] KANWAR J R, KANWAR R K, STATHOPOULOS S, et al.Comparative activities of milk components in reversing chronic colitis[J]. Journal of Dairy Science, 2016, 99(4): 2488-2501.DOI:10.3168/jds.2015-10122.
[110] DAS S, SONG Z L, HAN H, et al. Intestinal osteopontin protects from alcohol-induced liver injury by preserving the gut microbiome and the intestinal barrier function[J]. Cellular and Molecular Gastroenterology and Hepatology, 2022, 14(4): 813-839. DOI:10.1016/j.jcmgh.2022.06.012.
[111] GE X D, LEUNG T M, ARRIAZU E, et al. Osteopontin binding to lipopolysaccharide lowers tumor necrosis factor-α and prevents early alcohol-induced liver injury in mice[J]. Hepatology, 2014, 59(4): 1600-1616. DOI:10.1002/hep.26931.
[112] HAN L H, LI Q Q, DU M, et al. Bovine milk osteopontin improved intestinal health of pregnant rats fed a high-fat diet through improving bile acid metabolism[J]. Journal of Dairy Science, 2024, 107(1): 24-39. DOI:10.3168/jds.2023-23802.
[113] STANDAL T, BORSET M, SUNDAN A. Role of osteopontin in adhesion, migration, cell survival and bone remodeling[J].Experimental Oncology, 2004, 26(3): 179-184.
[114] DENHARDT D T, GUO X J. Osteopontin: a protein with diverse functions[J]. The FASEB Journal, 1993, 7(15): 1475-1482.DOI:10.1096/fasebj.7.15.8262332.
[115] GIACHELLI C M, STEITZ S. Osteopontin: a versatile regulator of inflammation and biomineralization[J]. Matrix Biology, 2000, 19(7):615-622. DOI:10.1016/S0945-053X(00)00108-6.
[116] RITTLING S R, SINGH R. Osteopontin in immune-mediated diseases[J]. Journal of Dental Research, 2015, 94(12): 1638-1645.DOI:10.1177/0022034515605270.
[117] ITO S, SAITO T, AMANO K. In vitro apatite induction by osteopontin:interfacial energy for hydroxyapatite nucleation on osteopontin[J].Journal of Biomedical Materials Research: Part A, 2004, 69(1): 11-16.DOI:10.1002/jbm.a.20066.
[118] DENHARDT D T, NODA M, O’REGAN A W, et al. Osteopontin as a means to cope with environmental insults: regulation of inflammation,tissue remodeling, and cell survival[J]. The Journal of Clinical Investigation, 2001, 107(9): 1055-1061. DOI:10.1172/JCI12980.
[119] MCKEE M D, NANCI A. Osteopontin: an interfacial extracellular matrix protein in mineralized tissues[J]. Connective Tissue Research,1996, 35(1/2/3/4): 197-205. DOI:10.3109/03008209609029192.
[120] LIAW L, ALMEIDA M, HART C E, et al. Osteopontin promotes vascular cell adhesion and spreading and is chemotactic for smooth muscle cells in vitro[J]. Circulation Research, 1994, 74(2): 214-224.DOI:10.1161/01.res.74.2.214.
[121] RITTLING S R, CHAMBERS A F. Role of osteopontin in tumour progression[J]. British Journal of Cancer, 2004, 90(10): 1877-1881.DOI:10.1038/sj.bjc.6601839.
[122] REINHOLT F P, HULTENBY K, OLDBERG A, et al. Osteopontin: a possible anchor of osteoclasts to bone[J]. Proceedings of the National Academy of Sciences of the United States of America, 1990, 87(12):4473-4475. DOI:10.1073/pnas.87.12.4473.
[123] SCATENA M, LIAW L, GIACHELLI C M. Osteopontin: a multifunctional molecule regulating chronic inflammation and vascular disease[J]. Arteriosclerosis, Thrombosis, and Vascular Biology, 2007,27(11): 2302-2309. DOI:10.1161/ATVBAHA.107.144824.
[124] FISHER L W, FEDARKO N S. Six genes expressed in bones and teeth encode the current members of the SIBLING family of proteins[J]. Connective Tissue Research, 2003, 44(Suppl 1): 33-40.DOI:10.1080/03008200390152061.
[125] SI J Y, WANG C W, ZHANG D H, et al. Osteopontin in bone metabolism and bone diseases[J]. Medical Science Monitor, 2020, 26:e919159. DOI:10.12659/MSM.919159.
[126] BOUDIN E, FIJALKOWSKI I, HENDRICKX G, et al. Genetic control of bone mass[J]. Molecular and Cellular Endocrinology, 2016,432: 3-13. DOI:10.1016/j.mce.2015.12.021.
[127] STAINES K A, MACRAE V E, FARQUHARSON C. The importance of the SIBLING family of proteins on skeletal mineralisation and bone remodelling[J]. The Journal of Endocrinology, 2012, 214(3): 241-255.DOI:10.1530/JOE-12-0143.
[128] CHEN Q, SHOU P S, ZHANG L Y, et al. An osteopontin-integrin interaction plays a critical role in directing adipogenesis and osteogenesis by mesenchymal stem cells[J]. Stem Cells, 2014, 32(2):327-337. DOI:10.1002/stem.1567.
[129] KVISTGAARD A S, MATULKA R A, DOLAN L C, et al. Preclinical in vitro and in vivo safety evaluation of bovine whey derived osteopontin, Lacprodan® OPN-10[J]. Food and Chemical Toxicology,2014, 73: 59-70. DOI:10.1016/j.fct.2014.07.026.
[130] DONOVAN S M, MONACO M H, DRNEVICH J, et al. Bovine osteopontin modifies the intestinal transcriptome of formula-fed infant rhesus monkeys to be more similar to those that were breastfed[J].The Journal of Nutrition, 2014, 144(12): 1910-1919. DOI:10.3945/jn.114.197558.