抗菌脂肽起源于真核生物[1],脂肽类化合物是一类具有显著结构多样性的生物表面活性物质[2-3],其分子结构由亲水性组分(环状或短链线性寡肽)与疏水性组分(长链脂肪酸)共同构成,具有广谱抗菌活性[4]。脂肽类化合物主要包括以下典型代表:环状结构的表面活性素(Surfactin)、具有抑菌特性的芬荠素(Fengycin)以及呈现显著表面活性的伊枯草菌素(Iturin)[5-6]。抗菌脂肽无毒无副作用,对天然食品没有危害[7-8],可作为天然防腐剂有效抑制食品致病菌等,延长食品货架期,且其与常规抗生素的联合使用也被证明可以协同提高抗菌效果[9-10],为应对多重耐药菌提供了新的策略,成为微生物学和生物技术领域的研究热点[11]。
贝莱斯芽孢杆菌(Bacillus velezen)隶属于枯草芽孢杆菌群[12],是一种兼性厌氧的革兰氏阳性菌,可在严峻环境下产生孢子[13]。贝莱斯芽孢杆菌基因组中大约5%~8%的基因用于合成抗菌化合物,这些基因簇编码了非核糖体肽合成酶(nonribosomal peptide synthetas,NRPS)和聚酮合酶,可用于合成抗菌肽和多酮类化合物[14-15]。Jayakumar等[16]利用含有氧化锌纳米颗粒和枯草芽孢杆菌来源的脂肽制备PVOH(PVA)纳米复合膜,发现其对金黄色葡萄球菌、肺炎克雷伯菌和铜绿假单胞菌的抗菌活性显著增强。Ambrico等[17]研究表明,枯草芽孢杆菌ET-1菌株上清液能够有效抑制草莓和柠檬的轮状病真菌的菌丝扩展。陈成等[18]研究发现,枯草芽孢杆菌发酵上清液对桑椹鲜果采后主要致腐菌具有明显的抑制作用,可显著降低果实霉变率。尽管枯草芽孢杆菌已被证实具有合成抗菌脂肽的能力,但其天然产量仍存在较大局限,因此,通过定向选育获得高产抗菌脂肽的优良菌株,并降低生产成本,推动抗菌脂肽在食品加工、饲料等领域的应用。
微生物诱变育种因其操作简便、成本低廉且效果显著等优势,已成为工业菌种改良的重要手段,常用的物理诱变方法包括紫外辐射和常压室温等离子体(atmospheric and room temperature plasma,ARTP)诱变技术[19]。Bouassida等[20]采用紫外线辐射诱变技术,成功选育出遗传稳定的枯草芽孢杆菌突变株,其Surfactin产量较野生型菌株提高了3 倍。Wang Yaxin等[21]利用ARTP诱变技术,使枯草芽孢杆菌A3菌株的产量显著提升了202.0%。然而,传统单一诱变方式往往伴随明显的适应性衰减现象,整合物理与化学两种不同作用机制的复合诱变技术,可有效扩大突变谱并增强遗传多样性[22]。陈尚里等[23]通过复合诱变(紫外诱变、ARTP-LiCl诱变)选育获得一株高产Fengycin突变株UA397,经发酵优化后暹罗芽孢杆菌UA-397的Fengycin产量为517.09 mg/L,是野生型在未进行发酵条件优化时Fengycin产量(113.02 mg/L)的4.575 倍。
现有研究多聚焦于诱变前后抗菌脂肽产量的表型变化,而对其分子机制特别是关键功能基因的遗传变异与表达调控网络缺乏深入解析。随着高通量测序技术的快速发展,基于多组学联用的生物信息学分析已成为揭示微生物代谢调控机制和环境适应的重要手段。本研究采用ARTP-LiCl复合诱变技术,成功选育出抗菌脂肽产量显著提升的贝莱斯芽孢杆菌突变株BV227。通过整合全基因组重测序与转录组分析,系统鉴定参与脂肽生物合成的关键功能基因及其调控网络,旨在从分子水平阐明菌株的高产机制,为通过代谢工程手段构建高效表达工程菌奠定分子基础,对开发高效、安全的生物源食品抗菌剂具有重要的理论指导。
1 材料与方法
1.1 材料与试剂
初始菌株贝莱斯芽孢杆菌BVQ121筛自发酵豆粕,由实验室保藏,保藏号:CCTCC M 20211570。
Surfactin标准品 上海源叶生物科技有限公司。
1.2 仪器与设备
ARTP-M等离子体诱变仪 上海非利加实业有限公司;RE-52AA旋转蒸发器 上海亚荣生化仪器厂;LDCP1000超声波破碎仪 山东莱恩德智能科技有限公司;Atlantis T3色谱柱(100 mm×3.0 mm,3.0 µm) 美国Waters科技有限公司;Q Exactive质谱仪 美国赛默飞世尔科技公司。
1.3 方法
1.3.1 致死率曲线的制作
1.3.1.1 紫外诱变致死率曲线的制作
紫外线诱变处理采用20 W紫外光源,设置辐照距离为20 cm,分别设置0、30、60、90、120、150、180、210、240、270 s这10 个不同辐照时间梯度。完成辐照处理后,将菌液用灭菌生理盐水进行107 倍稀释,吸取100 µL稀释液均匀涂布于LB琼脂平板表面。以未经辐照处理的样品作为阴性对照,所有平板避光条件下37 ℃倒置培养24 h后,统计各平板菌落形成单位,按照下式计算致死率:
1.3.1.2 ARTP-化学复合诱变致死率曲线的制作
首先将标准浓度菌液10 µL均匀涂布于无菌载玻片表面。随后将载玻片置于ARTP诱变仪中,设置0~270 s范围内共10 个梯度(间隔30 s)的处理时间。完成诱变后,用无菌生理盐水将菌液稀释107 倍,取100 µL均匀涂布于添加0.3% LiCl的LB琼脂平板。设置未诱变组作为对照,所有平板避光条件下37 ℃倒置培养24 h后统计菌落数。致死率根据1.3.1.1节公式计算,通过分析不同处理时间下的微生物存活率,绘制致死曲线,最终确定最佳诱变时长。
1.3.2 突变菌株的筛选
对经诱变处理的平板菌落进行系统编号后,选取形态良好的单菌落分别转接至含10 mL LB液体培养基的试管中。在37 ℃恒温条件下振荡培养24 h。培养完成后,将菌液于4 ℃低温条件下以8 000 r/min离心10 min,收集上清液。采用氯化十六烷基吡啶-溴百里酚蓝(cetylpyridinium chloride-bromothymol blue,CPCBTB)比色法快速筛选发酵上清液中的抗菌脂肽产量显著提高的突变菌株。将0.2 mmol/L CPC和0.2 mmol/L BTB等体积混合在0.2 mol/L磷酸缓冲溶液(NaH2PO4/Na2HPO4,pH 8.0)中,配制成CPC-BTB溶液。对方法进行改变,在酶标板内分别加入25 µL不同质量浓度Surfactin标准品(50、100、150、200、250、300、350、400、450、500 µg/mL),每孔加入100 µL CPC-BTB溶液,25 ℃条件下反应5 min,使用酶标仪测定其OD600值,绘制标准曲线。
1.3.3 发酵条件的优化
1.3.3.1 单因素优化试验
本研究采用单因素变量法系统考察了培养基组成及培养条件对发酵工艺的影响,具体考察参数包括:碳源种类及其添加量、氮源种类及其添加量、发酵时间、培养基初始pH值以及发酵温度。基于单因素试验结果筛选最优培养条件。
1.3.3.2 Box-Behnken设计优化条件
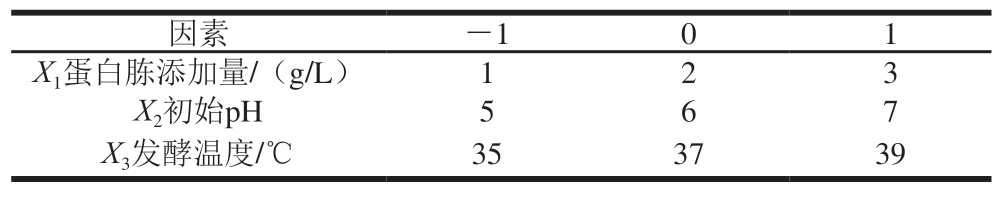
基于单因素试验结果,采用3因素3水平的Box-Behnken试验设计体系,考察关键因素(蛋白胨添加量X1、初始pH值X2、发酵温度X3)对突变菌株抗菌活性的影响。脂肽粗提产量(Y)作为评价指标,通过响应面分析法系统评估各因素及其交互作用对抗菌脂肽产量的综合效应。试验设计方案如表1所示。
表1 Box-Behnken试验设计因素与水平
Table 1 Code and level of independent variables used for Box-Behnken design
?
1.3.4 抗菌脂肽产量的测定
在无菌发酵培养基中加入预培养的种子液(接种量3%)进行发酵,将培养体系置于200 r/min、37 ℃的恒温振荡器中持续发酵48 h。发酵结束后,4 ℃低温条件下8 000 r/min离心10 min,保留上清液组分。使用6 mol/L盐酸溶液将上清液pH值调节至4.0,4 ℃静置沉淀12 h。再次于同样条件离心10 min,收集沉淀物。将所得沉淀充分溶解于过量甲醇中,经0.22 µm有机相滤膜真空抽滤去除不溶性杂质。最后,将滤液在45 ℃水浴条件下进行旋转蒸发浓缩处理,旋蒸后得到的沉淀溶于蒸馏水中。然后冻干收集抗菌脂肽提取物。
1.3.5 液相色谱-质谱(liquid chromatograph-mass spectrometry,LC-MS)分析
LC条件:样品经色谱柱Atlantis T3分离,采用Q Exactive质谱仪对正离子进行检测。流动相A为0.1%甲酸水溶液;流动相B为乙腈。进样量为10 µL,柱温为40 ℃,流速为0.4 mL/min。
MS条件:样品质谱信号采集采用正负离子扫描模式,加热电喷雾离子源,鞘气速率40 arb,辅助气速率10 arb,喷雾电压正离子3.8 kV,毛细管温度320 ℃,辅助气温度350 ℃,S-lens 50%,扫描模式为先进行一级全扫描,之后选取信号强度最高的前10 个离子进行碎裂分析并进行二级扫描,一级扫描分辨率70 000,范围m/z 120~1 700,二级扫描分辨率17 500,起始离子m/z 50,二级碎裂采用高能碰撞解离,归一化碰撞能量设为NCE 27。
1.3.6 菌株的全基因组测序与变异分析
菌株的全基因组测序与变异分析参考文献[24]的方法。
初始菌株的基因组测序与组装:取-80 ℃保存的初始菌株,融化后划线活化24 h,挑取单菌落接种于LB液体培养基,37 ℃振荡培养12~16 h。菌体经8 000 r/min离心10 min收集后,用无菌水洗涤两次。提取高质量DNA,经Covaris超声随机片段化处理后,进行文库构建,包括末端修复、3’端加A尾、接头连接、聚合酶链式反应(polymerase chain reaction,PCR)扩增及片段筛选纯化。对原始测序数据进行质控,去除低质量、含接头及PolyG序列的reads,获得高质量Clean Data。随后采用SOAPdenovo、SPAdes和ABySS进行独立组装,并通过CISA整合优化,利用gapclose填补scaffold缺口,最终获得完整基因组序列(去除<500 bp片段及污染序列),并进行组装质量评估。
诱变菌株的DNA提取、文库构建及测序流程与初始菌株一致。将Clean Data比对至参考基因组,检测以下遗传变异:1)单核苷酸多态性(single nucleotide polymorphism,SNP);2)短片段插入缺失;3)基因组结构变异;4)拷贝数变化,通过生物信息学方法对这些变异位点进行功能注释和影响预测。
1.3.7 转录组分析
在相同培养条件下(如对数生长期或特定胁迫环境),分别收集原始菌株(对照组)和诱变菌株(实验组)的菌体样本,每组设置3 个生物学重复。采用TRIzol法或RNA提取试剂盒提取总RNA,并进行质检。随后,通过磁珠法富集mRNA(真核生物)或去除rRNA(原核生物),并将其随机打断为200~500 bp片段。以mRNA为模板合成双链cDNA,经末端修复、加A尾、接头连接及PCR扩增构建测序文库。最终,使用Illumina NovaSeq平台进行高通量测序。对原始测序数据进行质控,去除低质量(Q score<20)、含接头及N碱基比例>5%的reads,获得高质量Clean Data。基于比对结果筛选差异表达基因,并进行功能富集分析。
1.3.8 抗菌脂肽的抑菌活性及热稳定性评价
1.3.8.1 抗菌脂肽对食源性致病菌的抑菌效果研究
取鸡肠炎沙门氏菌、鮰鱼爱德华氏菌SZJL-5的菌株冻存管,划线于LB固体平板上,挑取单菌落加入10 mL LB液体培养基中,37 ℃摇床活化12 h。分别向LB固体平板中加入50 µL不同的指示菌菌液,用一次性涂布棒将指示菌涂抹均匀。每组设置4 个浓度,第1个为空白组,第2、3、4组分别添加50、100、150 µL发酵上清液。于37 ℃摇床培养24 h,测量抑菌圈大小并拍照记录,实验重复3 次,取平均值。
1.3.8.2 脂肽水溶液热稳定性研究
制备含10%、20%的抗菌脂肽水溶液,分别在-20、-4、25、45 ℃条件下保存,待处理组发酵液恢复至常温状态,在0 h和24 h时进行牛津杯实验,每孔分别加入100 µL不同温度处理的脂肽水溶液,测量其抑菌圈直径,重复3 次。
1.4 数据分析处理
所有实验均重复3 次,数据用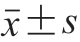 表示。使用方差分析(ANOVA)和T检验对多重平均值进行显著性分析。P<0.05表示具有统计意义。
表示。使用方差分析(ANOVA)和T检验对多重平均值进行显著性分析。P<0.05表示具有统计意义。
2 结果与分析
2.1 致死率曲线
如图1a所示,紫外诱变处理下菌株致死率呈现先升高后降低的变化趋势。值得注意的是,即使在最高剂量处理(120 s)条件下,致死率仅达到82.86%。这一现象与芽孢杆菌特有的抗逆机制密切相关,其芽孢结构能够有效抵御紫外线辐射,导致在高剂量照射下仍能保持部分细胞的存活能力[25],从而限制了致死率的进一步提升。基于此,本研究未采用紫外诱变进行高产菌株选育。图1b展示了ARTP-LiCl复合诱变的时间-效应关系。实验数据显示,致死率随处理时间延长呈显著上升趋势,处理90 s时致死率达99.14%,60 s处理组的致死率为92.85%。考虑到过高致死率(>95%)可能导致有效突变体数量不足,本研究最终确定采用60 s处理时间(致死率92.85%)进行后续筛选实验。该条件既保证了足够的诱变强度,又保留了充足的可筛选突变群体。
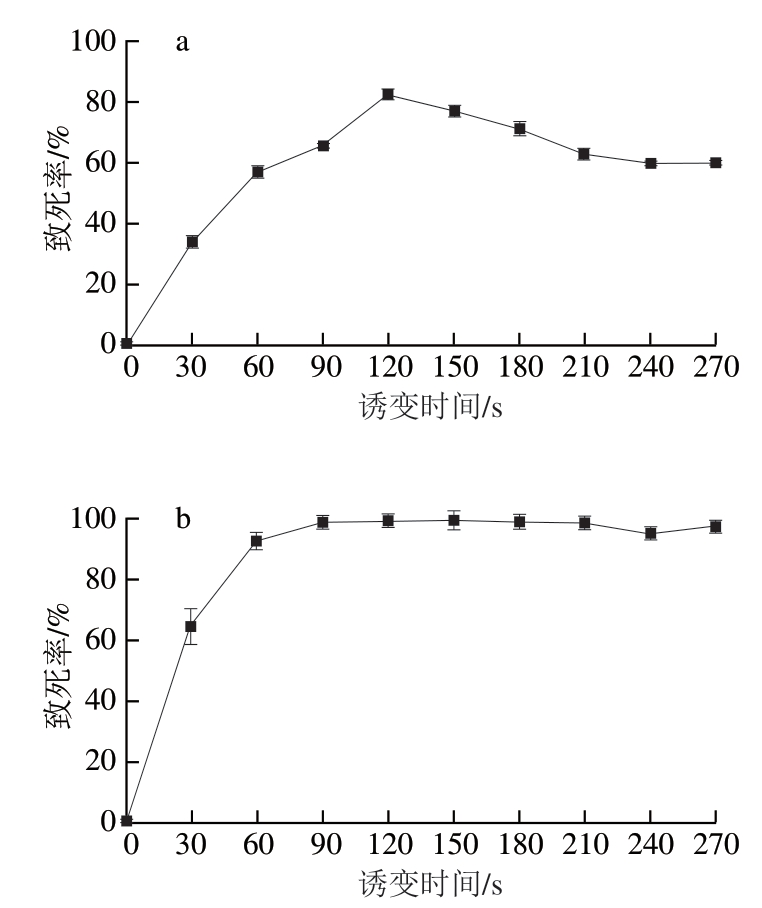
图1 紫外诱变(a)和ARTP-LiCl诱变(b)致死率与诱变时间的关系
Fig. 1 Relationship between mortality rate and mutagenesis time for ultraviolet radiation (a) and combined ARTP-LiCl treatment (b)
2.2 ARTP-化学复合诱变突变菌株的筛选
通过CPC-BTB高通量筛选结合牛津杯法,从诱变菌群中初步筛选出7 株抑菌效果显著的突变株(BV112、BV156、BV227、BV289、BV358、BV422、BV487)。采用酸沉淀法提取各菌株发酵液中的脂肽,测定其产量并进行抑菌活性评价。抑菌圈直径测定结果显示(图2),各突变株的抗菌活性与其脂肽粗提产量呈正相关,进一步验证了脂肽是主要的抗菌活性物质。通过产量测定发现,原始菌株BVQ121的脂肽产量为1.22 g/L,突变株BV227的产量达1.89 g/L,较原始菌株提高52.83%。谢定刚等[26]基于紫外诱变方法选育,抗菌脂肽产量较原始菌提高了40%,因此协同诱变策略可能可以克服单一诱变局限性。基于产量和活性综合评价,选择BV227作为后续实验材料。该菌株不仅产量提升显著,且表现出良好的遗传稳定性(连续传代10 代后产量波动<5%)。
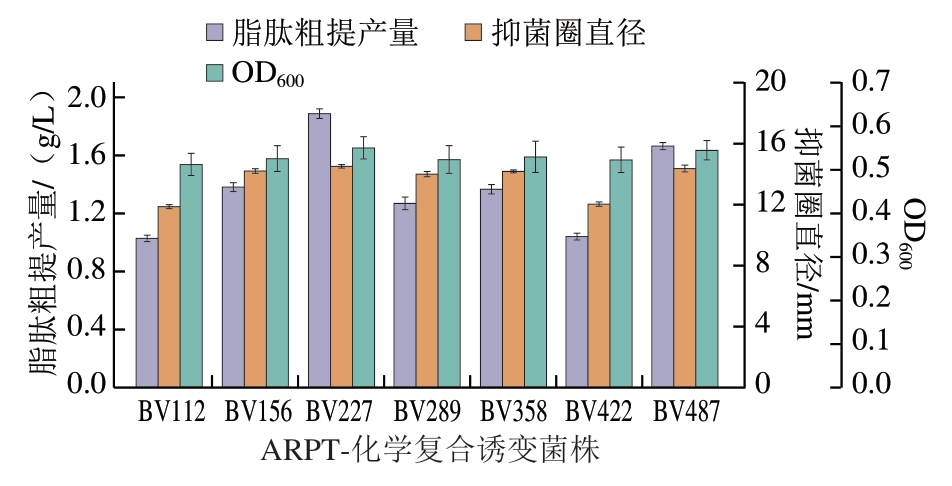
图2 ARTP-化学复合诱变法菌株筛选
Fig. 2 Strain screening by ARTP-chemical mutagenesis
2.3 发酵条件优化
2.3.1 单因素优化试验
实验结果表明,碳源种类对脂肽合成具有明显影响(图3a),以可溶性淀粉为单一碳源时,脂肽粗提产量和抑菌圈直径均达到最大值,这可能是由于其多糖结构能提供稳定的碳源供应;而D-半乳糖组则表现最差,推测与诱变菌株缺乏相关代谢酶有关。通过碳源添加量优化发现,可溶性淀粉的添加量与抑菌圈直径呈正相关,综合考虑到成本及抑菌效果,最终选择30 g/L作为最佳碳源添加量(图3b)。氮源筛选显示蛋白胨能最大程度促进脂肽合成,最佳添加量为2 g/L(图3c、d),故在后期响应面设计中设置1~3 g/L的考察范围。由图3e发现,脂肽产量和抑菌活性随发酵时间延长呈现先增大后减小的趋势,48 h时脂肽粗提产量和抑菌圈直径达到峰值,72 h时降至最低,故确定48 h为最佳发酵时间。在不同发酵pH值下培养发现,培养基初始pH值为6时产量和抑菌活性最高,pH 9时最低(图3f),表明碱性环境会抑制菌体生长和脂肽合成,可能是由于高pH值改变了细胞膜通透性和酶活性,这与刘伟等[27]的研究结论相符,最终选择pH 6为最佳发酵条件。由图3g可知,温度对脂肽合成的影响呈现单峰曲线,37 ℃时产量和抑菌活性最佳,41 ℃时显著降低,这与高温抑制菌体生长的现象一致。所有实验数据均表明,脂肽合成效率与菌体生长状况密切相关,适宜的环境参数对维持代谢活性至关重要。基于上述结果,响应面试验设计选取发酵时间48 h、pH 5~7和发酵温度35~39 ℃进行后续优化研究。
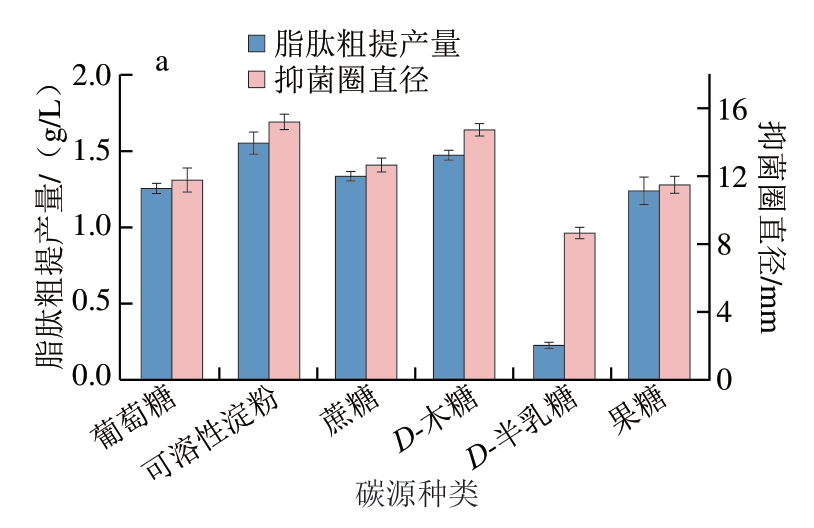
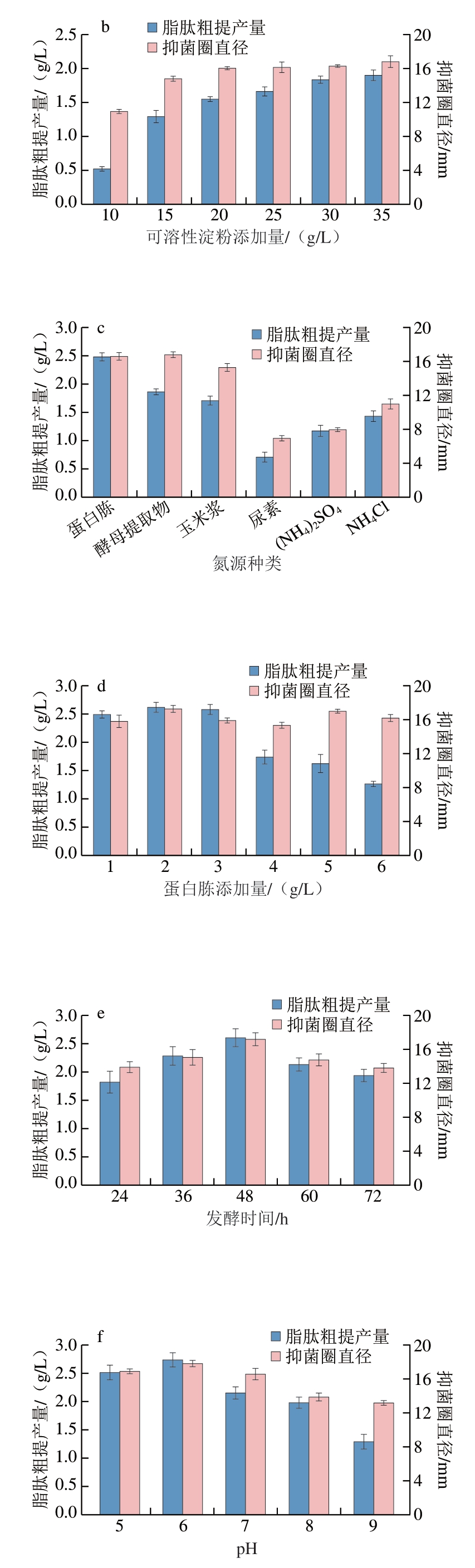
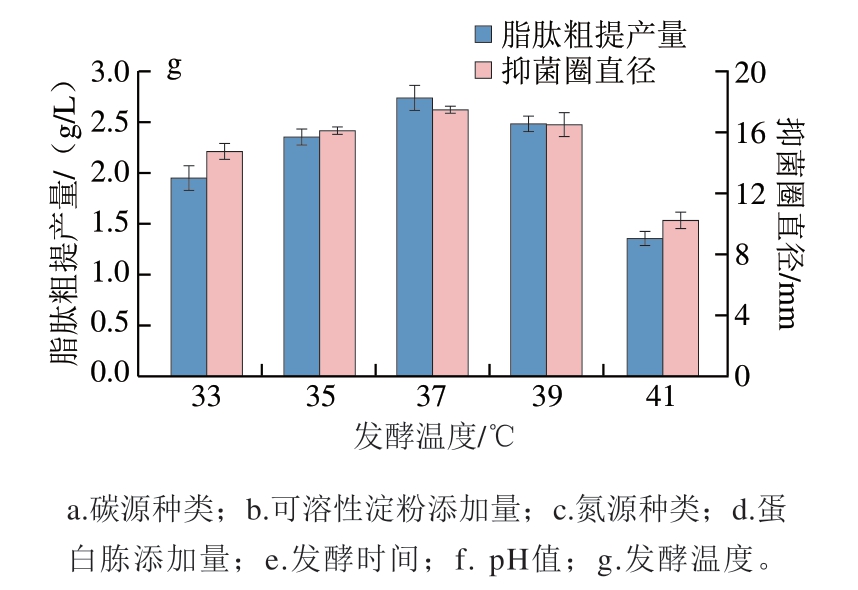
图3 发酵条件单因素优化
Fig. 3 Results of single factor experiments for the optimization of fermentation conditions
2.3.2 响应面设计优化
本研究采用Design-Expert 10.0软件对脂肽发酵条件进行响应面优化分析,并建立了蛋白胨添加量(X1)、初始pH值(X2)、发酵温度(X3)三因素的二次多项式回归模型:Y=2.72―0.057X1+0.096X2―0.14X3―![]()
![]() 。
。
基于建立的回归模型,采用Design-Expert分析平台生成工艺参数优化响应面,成功构建了蛋白胨添加量、发酵温度和环境pH值三因素交互作用的立体响应模型(图4)。对回归模型进行方差分析与显著性分析检验,方差分析表明该模型具有高度显著性(F=212.40,P<0.001),决定系数R2=0.996 4,调整决定系数![]() =0.965 3,证实模型可靠性良好。各因素对脂肽产量的影响程度依次为:发酵温度(X3)>初始pH值(X2)>蛋白胨添加量(X1),其中X1X2和X2X3交互作用极显著(P<0.000 1),二次项
=0.965 3,证实模型可靠性良好。各因素对脂肽产量的影响程度依次为:发酵温度(X3)>初始pH值(X2)>蛋白胨添加量(X1),其中X1X2和X2X3交互作用极显著(P<0.000 1),二次项![]() 均达极显著水平(P<0.000 1)。模型预测最优条件为:蛋白胨添加量1.9 g/L、pH 6.1、发酵温度36.5 ℃,预期产量2.739 6 g/L。经实验验证,实际产量为(2.722 3±0.09)g/L(n=3),达到预测值的99.31%,相对误差低于3%。经发酵优化,脂肽粗提物的产量获得显著提升,较优化前的诱变菌株提高了44.97%,与原始菌株相比增幅达122.31%。纪帅奇等[28]同样针对高产抗菌脂肽的芽孢杆菌进行了发酵优化,但仅提高20%左右,这可能是因为本研究发酵优化条件更为丰富,凸显了培养基组分与环境参数对脂肽生物合成的协同调控作用,同时进一步证明了该模型能准确反映各工艺参数与脂肽产量的定量关系,为工业化生产提供了可靠的理论依据。
均达极显著水平(P<0.000 1)。模型预测最优条件为:蛋白胨添加量1.9 g/L、pH 6.1、发酵温度36.5 ℃,预期产量2.739 6 g/L。经实验验证,实际产量为(2.722 3±0.09)g/L(n=3),达到预测值的99.31%,相对误差低于3%。经发酵优化,脂肽粗提物的产量获得显著提升,较优化前的诱变菌株提高了44.97%,与原始菌株相比增幅达122.31%。纪帅奇等[28]同样针对高产抗菌脂肽的芽孢杆菌进行了发酵优化,但仅提高20%左右,这可能是因为本研究发酵优化条件更为丰富,凸显了培养基组分与环境参数对脂肽生物合成的协同调控作用,同时进一步证明了该模型能准确反映各工艺参数与脂肽产量的定量关系,为工业化生产提供了可靠的理论依据。
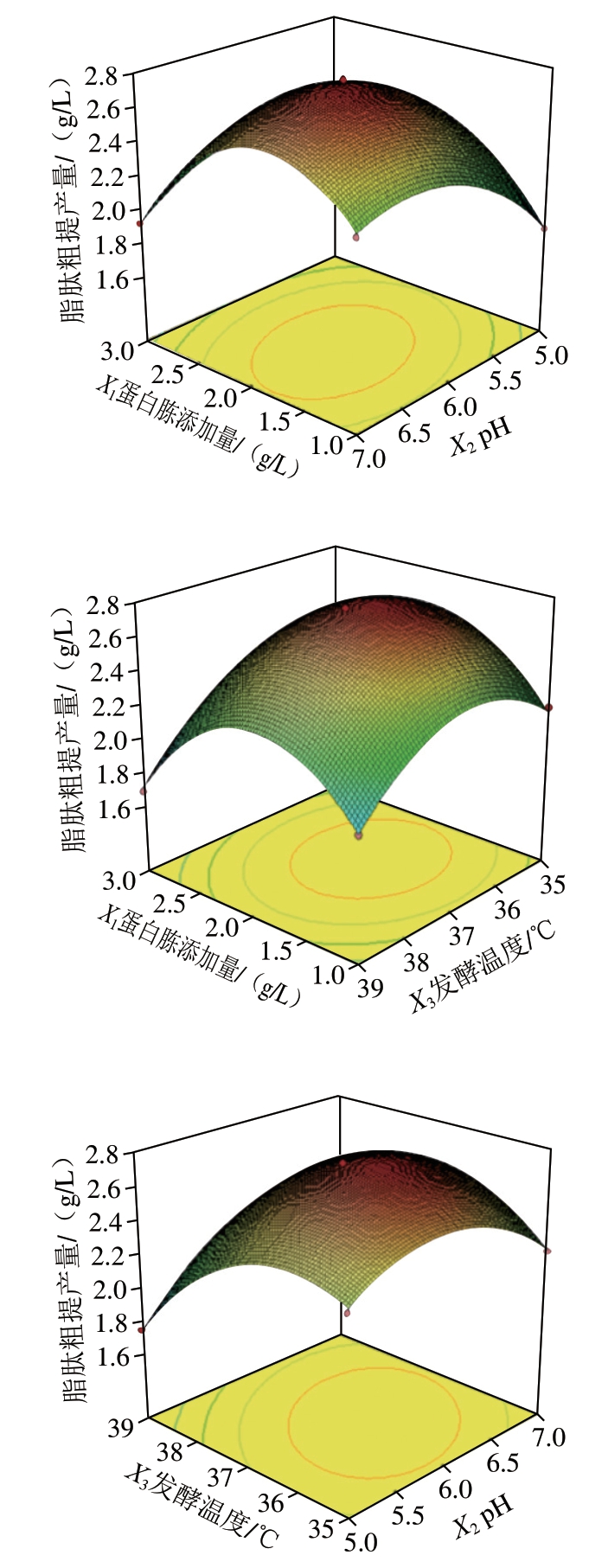
图4 多因素交互效应与响应面分析
Fig. 4 Response surface plots showing the interactive effects of variables on the production of lipopeptides
2.4 菌株诱变前后的LC-MS分析
基于LC-MS技术的脂肽鉴定主要依据其离子化后形成的特征性质谱峰。不同结构脂肽因氨基酸组成差异、肽链长度变化、脂肪酸链长度及饱和度不同会产生独特的质荷比(m/z)分布,从而在质谱图上呈现出特定的峰型。3 类典型脂肽的[M+H]+离子特征峰分布为Surfactin:m/z 993~1 053、Iturin:m/z 1 044.6~1 058.7、Fengycin:m/z 1 410~1 570[29-30]。诱导前后菌株脂肽粗提物的LC-MS如图5所示,可见其产出的主要脂肽成分未发生明显变化,具体分析结果见表2,根据已知的m/z作参照,诱变菌株粗提物中的活性成分均由3 类抗菌脂肽类物质共同组成。与Sui Xiaona[31]、Hammad[32]、Zhang Li[33]等在对贝莱斯芽孢杆菌脂肽链的LC-MS分析中[M+H]+的质荷比,突变株BV227的Iturin、Iturin与Surfactin同系物均增多,表明突变株BV227中脂肽的合成能力得到明显提升。其中,对比发现诱变前后Surfactin组分保持稳定,种类未发生显著改变,而Iturin同系物组成出现明显变异。值得注意的是,突变株BV227在m/z 1 410~1 570区间的峰数量显著增加,表明其生产的Fengycin类脂肽具有更高多样性。进一步使BV227菌株的乳化性能得到提升,并具有更宽的pH值耐受范围,在工业上更适用于食品级生物表面活性剂的生产、石油污染的生物修复等。
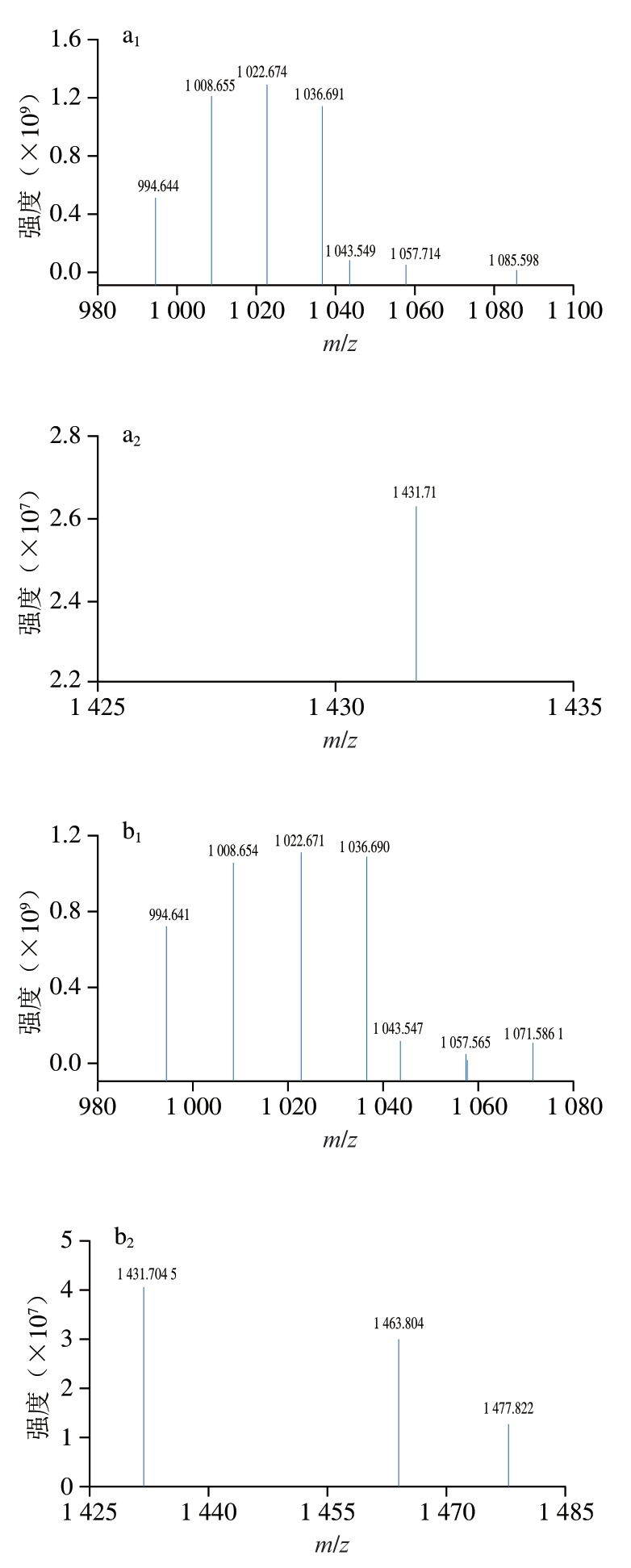
图5 BVQ121(a)和BV227(b)的脂肽提取物LC-MS图
Fig. 5 LC-MS spectra of lipopeptide extracts from strains BVQ121 (a) and BV227 (b)
表2 抗菌脂肽提取物LC-MS结果
Table 2 LC-MS results of antimicrobial lipopeptide extracts
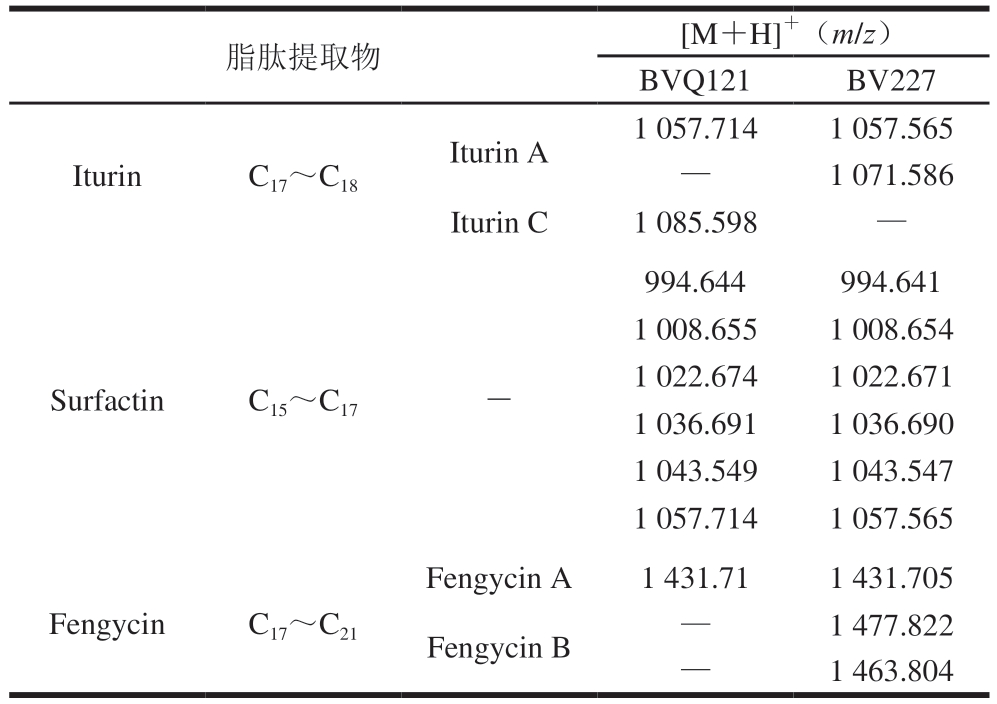
注:—.未检测到对应的脂肽。
脂肽提取物[M+H]+(m/z)BVQ121BV227 IturinC17~C18 Iturin A1 057.7141 057.565—1 071.586 Iturin C1 085.598—SurfactinC15~C17―994.644994.641 1 008.6551 008.654 1 022.6741 022.671 1 036.6911 036.690 1 043.5491 043.547 1 057.7141 057.565 Fengycin A1 431.711 431.705 Fengycin B—1 477.822—1 463.804 FengycinC17~C21
2.5 诱变前后菌株的全基因组测序及变异分析
采用Illumina平台对诱变前后的贝莱斯芽孢杆菌进行全基因组测序,经fastp质控过滤后获得高质量Clean Data,有效数据量为1.616 Gb。测序数据显示:基因组大小为4 038 252 bp,GC相对含量为46.45%,测序深度>50×,N50为586 433 bp,Q30碱基占比>95%。15-kmer分布符合泊松分布,GC-depth分析显示数据点集中分布于40%~60%区间,符合芽孢杆菌G+C含量分布特点,证实样品无污染且数据可靠,可用于后续分析。
SNP是基因组中最常见的遗传变异类型之一,其本质为DNA序列中单个碱基位点发生的核苷酸替换现象[34]。通过GATK检测发现的SNP位点中,主要包括编码区变异:非同义突变4 个(可能影响脂肽合成相关基因功能)、同义突变7 个;非编码区变异:基因下游1 kb区域6 个,基因间区8 个。关键突变示例如表3所示,其中Scaffold7: 7936位点(T→G)的突变质量值最高(变异检测质量=396.77),深度达10×,提示该位点变异可靠性较高。这些遗传变异为解析菌株表型改良的分子机制提供了重要线索。
表3 SNP 注释结果示例
Table 3 Examples of SNP annotation results

注:CHROM.该突变所在的染色体ID;POS.该突变所在CHROM(序列)的位置;REF.参考基因组碱基类型。
测序深度(×)Scaffold511112AGSNP236.846 Scaffold511133TASNP152.034 Scaffold511139TCSNP152.033 Scaffold77936TGSNP396.7710 Scaffold77962AGSNP195.905 CHROMPOSREF样本中的变异的碱基类型类型可信度评分
2.6 转录组分析
通过基因本体论(Gene Ontology,GO)富集分析发现(图6a),诱变菌株中细胞分解代谢过程相关基因显著下调,促使碳源等前体物质向脂肽合成途径重分配,为脂肽产量增加提供了物质基础。同时,细胞结构和蛋白质结合相关基因的表达改变,可能影响了细胞内蛋白质-蛋白质相互作用,重塑了细胞内环境,削弱了脂肽合成的负调控机制。GO分析结果显示(图6b),差异表达基因在细胞组分和部分生物过程(如细胞大分子生物合成过程)中显著富集。这表明诱变主要影响了细胞结构组成及相关生物过程,但对分子功能相关基因的影响较小。
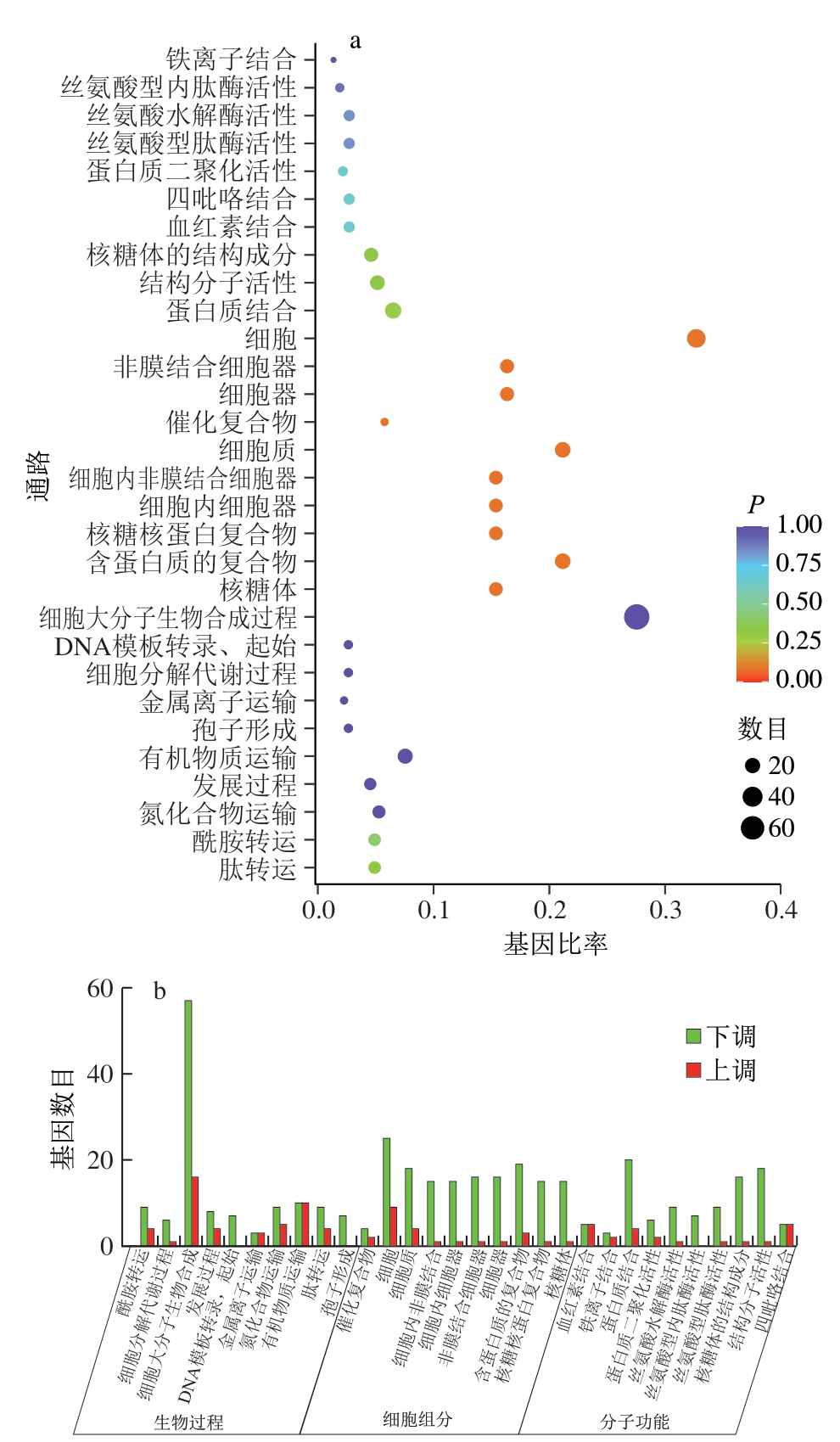
图6 GO富集分析图(a)和分类柱状图(b)
Fig. 6 GO enrichment analysis plot (a) and bar chart (b) of GO enrichment classification
2.7 代谢通路整合分析
图7a结果显示,群体感应富集到超过40 个基因,并且与诱变前具有显著差异(P<0.01),表明其富集程度最为显著。作为调控微生物生理行为的关键系统,群体感应可影响次级代谢产物的合成。在芽孢杆菌中,该系统的基因突变可能改变了信号分子的合成、感知或传导过程,从而解除对脂肽合成的抑制或激活相关基因表达。此外,ABC转运体也显示出一定的富集显著性,这类转运体通过提高前体物质的运输效率或促进脂肽外排,可能减少了产物反馈抑制,进而提升脂肽产量。根据代谢网络分析(图7b)揭示,脂肪酸降解途径中乙醇脱氢酶(alcohol dehydrogenase,ADH,1.1.1.1)和脂肪酸羟化酶(cytochromeP450,CYP450,1.14.14.1)的表达均呈现显著上调。其中ADH(编码基因BK_GM003379、BK_GM002199)可以催化乙醇氧化为乙醛,并进一步生成乙酰CoA,而乙酰CoA作为脂肪酸β-氧化的关键起始物质,为脂肽的疏水脂肪酸链(如Surfactin的C13~C15链、Iturin的β-氨基脂肪酸)提供碳骨架,ADH反应还可以调节细胞内NAD+/NADH比例,影响三羧酸循环和能量代谢,从而间接支持NRPS的高能耗合成过程。Fengycin和部分Surfactin的脂肪酸链需β-羟基化修饰,代谢路径中CYP450(编码基因BK_GM003604、BK_GM003746)可以催化长链脂肪酸(如C16~C18)的羟化反应,生成β-羟基脂肪酸前体。此外,CYP450还可修饰脂肪酸链的长度和氧化状态,影响脂肽的生物活性(如增强抗真菌性能)。由此认为BK_GM003379和BK_GM002199基因的上调为脂肪酸链合成提供更多前体并支持NRPS能量需求,BK_GM003604和BK_GM003746基因的上调增加了脂肽结构多样性和生物活性。这些基因的协同作用为脂肽的理性设计和产量提升提供了关键靶点,尤其在脂肪酸链工程化改造方面具有潜力。
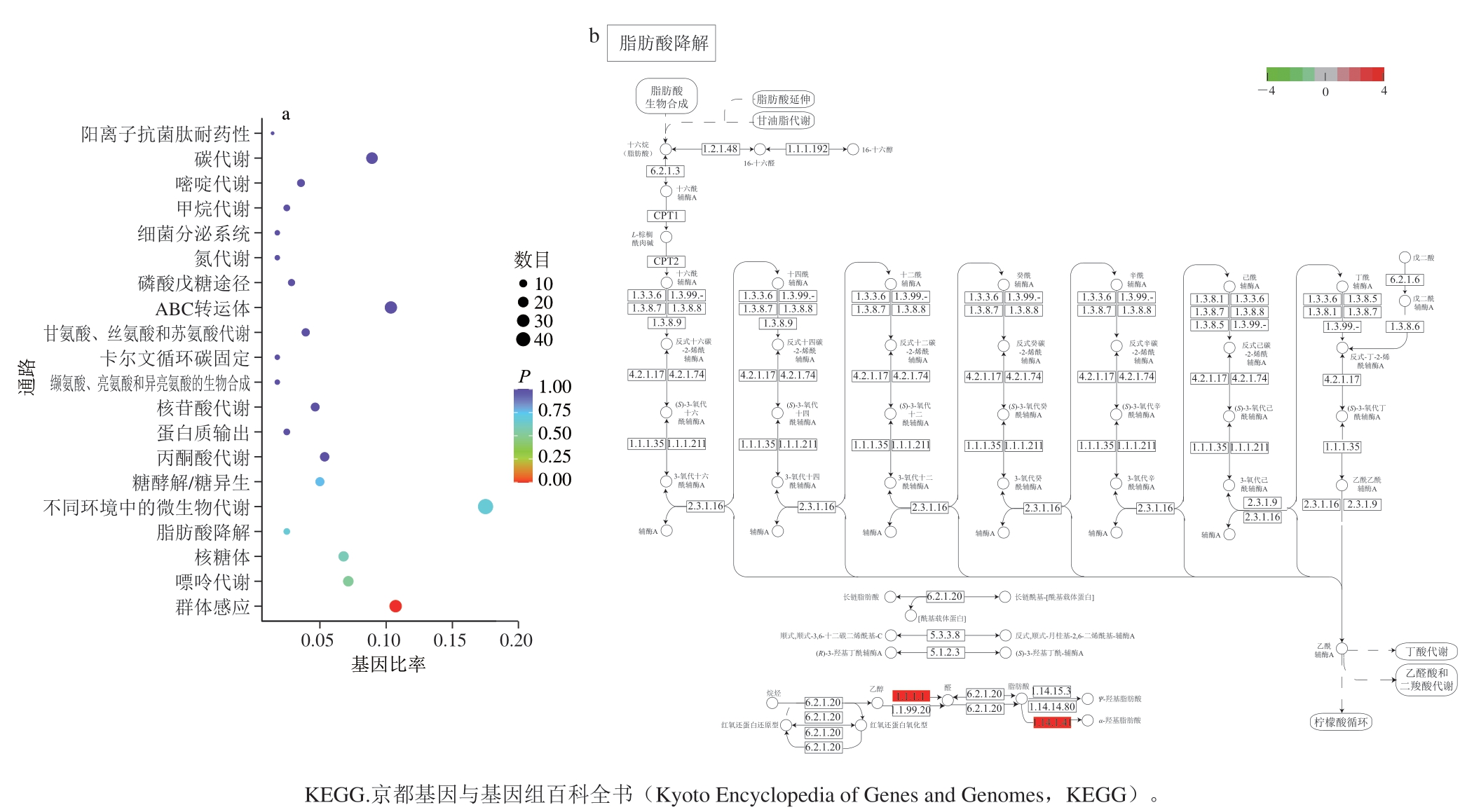
图7 差异表达前20的基因KEGG富集分析图(a)和差异表达代谢通路图(b)
Fig. 7 KEGG enrichment analysis plot of the top 20 differentially expressed genes (a) and metabolic pathways of the differentially expressed genes (b)
2.8 抗菌脂肽对食源性致病菌的抑菌效果
当前对抗菌脂肽的抑菌效果研究主要集中在金黄色葡萄球菌、大肠杆菌和铜绿假单胞菌等常见致病菌株[35],而沙门氏菌和鮰鱼爱德华氏菌也是典型的致病菌,对家禽、水产等具有不可小觑的危害[36-37],因此本研究选择沙门氏菌和鮰鱼爱德华氏菌作为抑菌效果研究的主要对象。通过对比抗菌脂肽对沙门氏菌和鮰鱼爱德华氏菌的牛津杯实验(图8),观察记录其抑菌圈直径并进行显著性分析(表4),发现脂肽添加量与抑菌圈直径之间具有高度显著性(P<0.000 1),即随着脂肽添加量的增加,其对沙门氏菌和爱德华氏菌的抑制效果均呈现剂量依赖性增强趋势。当添加量为50 µL时,脂肽对沙门氏菌和爱德华氏菌的抑菌圈直径分别为(9.15±0.13)mm和(8.92±0.11)mm;当添加量增至150 µL时,抑菌圈直径分别达到(14.32±0.18)mm和(12.87±0.13)mm。值得注意的是,在低添加量(50~100 µL)条件下,脂肽对两种病原菌的抑制效果相近;而当添加量达到150 µL时,对沙门氏菌的抑制效果明显优于爱德华氏菌。这种差异可能源于两种病原菌细胞膜结构的特异性差异,导致其对脂肽类抗菌物质的敏感性不同。研究结果表明,抗菌脂肽对食源性病原菌具有显著的抑制作用,且其抑菌效果与添加剂量呈正相关。沙门氏菌和爱德华氏菌分别是禽肉和水产品中的重要食源性病原体,可能导致产品召回、食源性疾病及养殖的经济损失。基于本研究,抗菌脂肽可用于扩展养殖业抗生素替代品市场,开发家禽和水产饲料添加剂,并优化禽肉加工及冷链运输中的防腐方案,以提升食品安全。
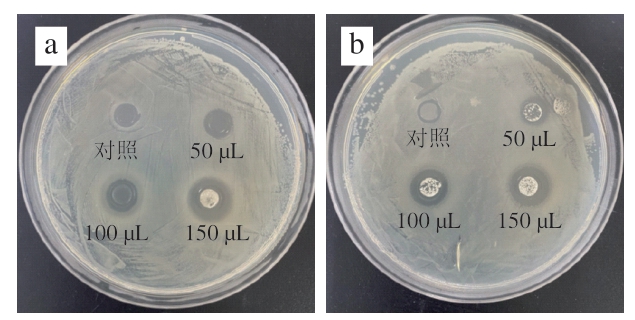
图8 抗菌脂肽对沙门氏菌(a)和鮰鱼爱德华氏菌(b)的抑菌效果
Fig. 8 Antibacterial effects of antimicrobial lipopeptides on Salmonella (a) and E. ictalurid (b)
表4 抗菌脂肽对食源性致病菌的抑菌圈直径及其差异性分析
Table 4 Antimicrobial activity analysis of lipopeptides against foodborne pathogens: diameter of inhibition zones and statistical significance test

指示菌名称抑菌圈直径/mm方差检验FP对照50 µL100 µL150 µL沙门氏菌09.15±0.1310.12±0.1214.32±0.181 066.534<0.000 1鮰鱼爱德华氏菌08.92±0.1111.24±0.2112.87±0.13485.041<0.000 1
2.9 脂肽的热稳定性
在不同温度处理下观察脂肽水溶液的外观颜色,根据图9a发现其无明显变化,表明脂肽分子在测试温度范围内未发生明显的聚集或沉淀,物理性质较为稳定。根据不同质量分数脂肽溶液在不同温度下处理不同时间的抑菌效果及独立样本T检验(图9b、c和表5)发现,除45 ℃条件下处理48 h条件外,在所有测试温度范围内,20%溶液的抑菌效果均显著优于10%溶液(P<0.001),这一结果与2.7节中关于脂肽添加量与抑菌活性之间呈正相关的结论相互印证。此外,在不同温度下,以处理时间为自变量做差异性分析时发现,在低温(-20 ℃至-4 ℃)范围内,各质量分数脂肽水溶液处理48 h过程中金黄色葡萄球菌的抑菌圈直径无显著差异(P>0.05),这表明在低温储存条件下,抗菌脂肽能够长期保持良好稳定的抗菌性能。这些数据充分证明,本研究开发的抗菌脂肽在低温下具有良好的稳定性,能够满足冷链运输中对防腐剂储存条件和加工稳定性的严格要求,为其工业化应用提供了重要的实验依据。
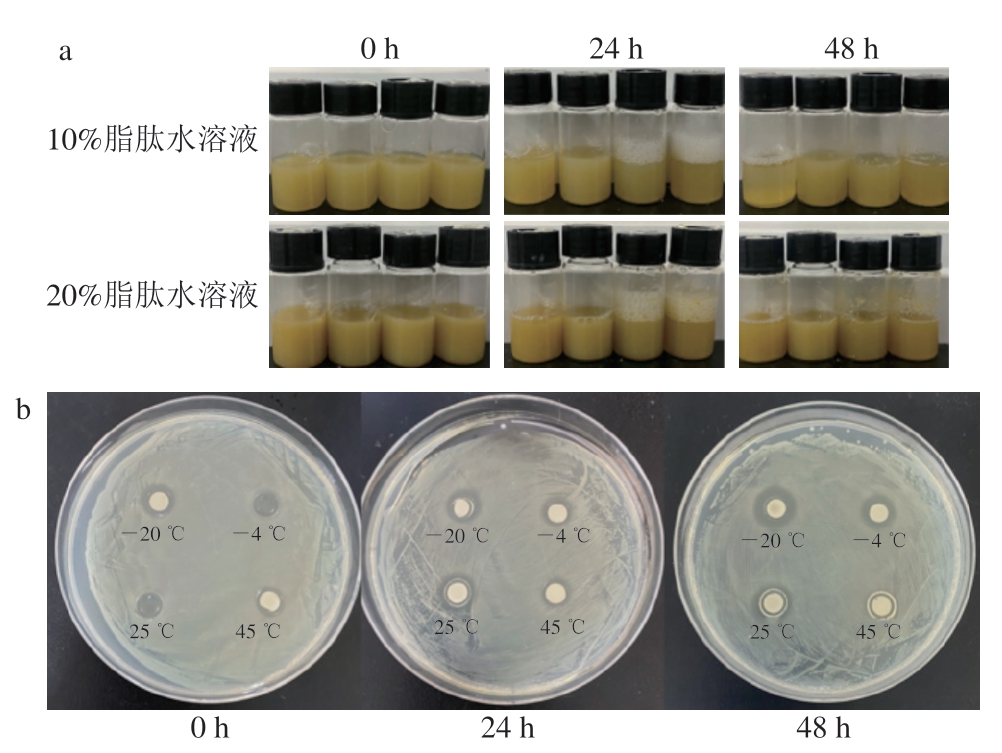
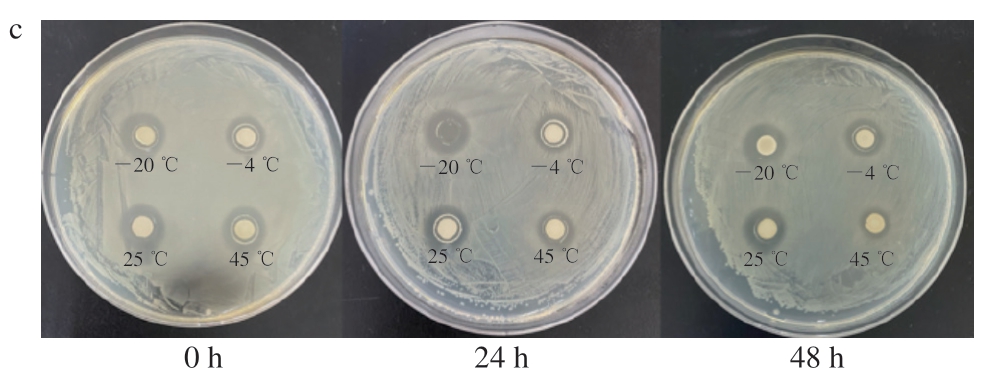
图9 脂肽水溶液的外观(a)和10%(b)、20%(c)脂肽水溶液在不同温度处理下的抑菌圈大小
Fig. 9 Appearance of lipopeptide aqueous solutions (a) and inhibition zones of 10% (b) and 20% (c) lipopeptide aqueous solutions after treatment at different temperatures
表5 10%、20%脂肽水溶液在不同温度下处理不同时间的抑菌圈大小及差异性
Table 5 Diameter of inhibition zones of 10% and 20% lipopeptide aqueous solutions at different combinations of treatment temperature and duration and significance test
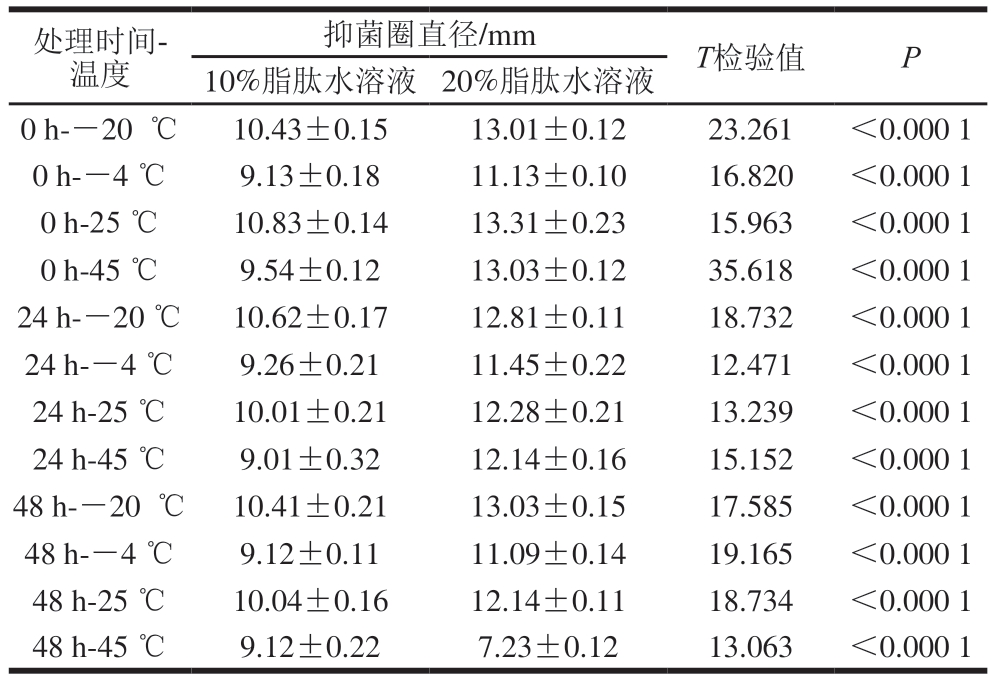
抑菌圈直径/mmT检验值P 10%脂肽水溶液20%脂肽水溶液0 h--20 ℃10.43±0.1513.01±0.1223.261<0.000 1 0 h--4 ℃9.13±0.1811.13±0.1016.820<0.000 1 0 h-25 ℃10.83±0.1413.31±0.2315.963<0.000 1 0 h-45 ℃9.54±0.1213.03±0.1235.618<0.000 1 24 h--20 ℃10.62±0.1712.81±0.1118.732<0.000 1 24 h--4 ℃9.26±0.2111.45±0.2212.471<0.000 1 24 h-25 ℃10.01±0.2112.28±0.2113.239<0.000 1 24 h-45 ℃9.01±0.3212.14±0.1615.152<0.000 1 48 h--20 ℃10.41±0.2113.03±0.1517.585<0.000 1 48 h--4 ℃9.12±0.1111.09±0.1419.165<0.000 1 48 h-25 ℃10.04±0.1612.14±0.1118.734<0.000 1 48 h-45 ℃9.12±0.227.23±0.1213.063<0.000 1处理时间-温度
3 结 论
本研究对具有生产抗菌脂肽功能的B. velezens BVQ212进行诱变,并通过CPC-BTB比色法测定发酵液中抗菌脂肽的含量以筛选诱导菌株。先对其进行了紫外诱变,发现其芽孢结构能够有效抵御紫外线辐射,诱变效果不佳,随后采用ARTP-LiCl复合诱变得到优势菌株BV227,其抗菌脂肽产量达1.89 g/L,较原始菌株提高52.83%。通过系统的单因素试验和响应面优化设计,建立了可靠的脂肽发酵工艺模型(R2=0.996 4),在最优条件下(蛋白胨1.9 g/L、pH 6.1、36.5 ℃)使脂肽产量达到(2.722 3±0.09)g/L,较原始菌株提高122.31%,显著优于文献报道值,为抗菌脂肽的工业化生产提供了优化的工艺参数和理论基础。此外,BV227还具有良好的遗传稳定性,在工业化生产中更具优势。为分析影响抗菌脂肽生产的关键基因,本研究通过全基因组测序结合多组学分析,发现诱变菌株中细胞结构组成及相关生物过程均发生了改变,系统揭示了诱变菌株中关键酶(如ADH和CYP450)的显著上调及其协同作用机制,不仅为脂肽产量提升提供了分子层面的解释,更通过SNP变异分析、GO功能富集和代谢网络整合,阐明了群体感应调控和脂肪酸前体供应在脂肽生物合成中的核心作用,促使更多资源和条件向有利于脂肽合成的方向发展,凸显了多组学联用技术在解析微生物次级代谢产物合成机制中的独特优势。最后对产生的抗菌脂肽进行抑菌效果和热稳定性检测,不仅证实了抗菌脂肽对沙门氏菌和爱德华氏菌的显著抑制效果,更通过温度稳定性(-20~25 ℃保持活性)与剂量依赖性(150 µL时抑菌效果最佳)的作用规律,为开发针对禽肉加工厂、水产冷链运输防腐剂提供了坚实的理论基础和应用依据。本研究利用ARTP-LiCl复合诱变得到突变菌株,再通过抗菌脂肽的产量筛选出产出效果最好的诱变菌株BV227,通过生物信息技术分析其基因表达水平的改变,并最终验证抗菌脂肽的抑菌效果及热稳定性。未来可将本研究得到的突变种BV227进行大规模投产试验以验证其实际应用效果,以及后续可进一步研究菌株的诱变的机制,为菌株的定向筛选提供参考,从而提高选育效率。
[1] SANI A, QIN W Q, LI J Y, et al. Structural diversity and applications of lipopeptide biosurfactants as biocontrol agents against phytopathogens: a review[J]. Microbiological Research, 2024, 278:127518. DOI:10.1016/j.micres.2023.127518.
[2] 杨晨远, 于子川, 秦迪, 等. 抗菌肽的结构分析、抗菌机制及改造应用的研究进展[J]. 微生物学报, 2024, 64(7): 2242-2259.DOI:10.13343/j.cnki.wsxb.20230812.
[3] 刘敏, 黄湘宇, 吴昊, 等. 植物源抗菌肽的筛选及其在食品中的应用进展[J]. 食品与机械, 2024, 40(7): 200-207; 215. DOI:10.13652/j.spjx.1003.5788.2024.80476.
[4] MNIF I, GHRIBI D. Review lipopeptides biosurfactants: mean classes and new insights for industrial, biomedical, and environmental applications[J]. Peptide Science, 2015, 104(3): 129-147. DOI:10.1002/bip.22630.
[5] 李道明, 王瑛, 陈超, 等. 芽孢杆菌几种重要抗菌脂肽研究进展[J].生物工程学报, 2022, 38(5): 1768-1783. DOI:10.13345/j.cjb.220001.
[6] BERNHEIMER A W, AVIGAD L S. Nature and properties of a cytolytic agent produced by Bacillus subtilis[J]. Journal of General Microbiology,1970, 61(3): 361-369. DOI:10.1099/00221287-61-3-361.
[7] CHEN X Y, LU Y J, SHAN M Y, et al. A mini-review: mechanism of antimicrobial action and application of surfactin[J]. World Journal of Microbiology & Biotechnology, 2022, 38(8): 143. DOI:10.1007/s11274-022-03323-3.
[8] SUTHAR H, HINGURAO K, DESAI A, et al. Selective plugging strategy-based microbial-enhanced oil recovery using Bacillus licheniformis TT33[J]. Journal of Microbiology and Biotechnology,2009, 19(10): 1230-1237.
[9] NAUGHTON P J, MARCHANT R, NAUGHTON V, et al. Microbial biosurfactants: current trends and applications in agricultural and biomedical industries[J]. Journal of Applied Microbiology, 2019,127(1): 12-28. DOI:10.1111/jam.14243.
[10] INÈS M, DHOUHA G. Lipopeptide surfactants: production,recovery and pore forming capacity[J]. Peptides, 2015, 71: 100-112.DOI:10.1016/j.peptides.2015.07.006.
[11] MANDAL S M, BARBOSA A E A D, FRANCO O L. Lipopeptides in microbial infection control: scope and reality for industry[J].Biotechnology Advances, 2013, 31(2): 338-345. DOI:10.1016/j.biotechadv.2013.01.004.
[12] FAN B, WANG C, SONG X F, et al. Bacillus velezensis FZB42 in 2018: the Gram-positive model strain for plant growth promotion and biocontrol[J]. Frontiers in Microbiology, 2018, 9: 2491. DOI:10.3389/fmicb.2018.02491.
[13] KHAN M S, GAO J L, CHEN X Q, et al. The endophytic bacteria Bacillus velezensis Lle-9, isolated from Lilium leucanthum, harbors antifungal activity and plant growth-promoting effects[J]. Journal of Microbiology and Biotechnology, 2020, 30(5): 668-680. DOI:10.4014/jmb.1910.10021.
[14] KENFAOUI J, DUTILLOY E, BENCHLIH S, et al. Bacillus velezensis: a versatile ally in the battle against phytopathogens:insights and prospects[J]. Applied Microbiology and Biotechnology,2024, 108(1): 439. DOI:10.1007/s00253-024-13255-7.
[15] ALETI G, SESSITSCH A, BRADER G. Genome mining: prediction of lipopeptides and polyketides from Bacillus and related Firmicutes[J].Computational and Structural Biotechnology Journal, 2015, 13: 192-203. DOI:10.1016/j.csbj.2015.03.003.
[16] JAYAKUMAR A, RADOOR S, C NAIR I, et al. Polyvinyl alcoholnanocomposite films incorporated with clay nanoparticles and lipopeptides as active food wraps against food spoilage microbes[J].Food Packaging and Shelf Life, 2021, 30: 100727. DOI:10.1016/j.fpsl.2021.100727.
[17] AMBRICO A, TRUPO M. Efficacy of cell free supernatant from Bacillus subtilis ET-1, an Iturin A producer strain, on biocontrol of green and gray mold[J]. Postharvest Biology and Technology, 2017,134: 5-10. DOI:10.1016/j.postharvbio.2017.08.001.
[18] 陈成, 方银, 金超, 等. 枯草芽孢杆菌对桑椹采后致腐微生物的抑菌作用[J]. 蚕业科学, 2016, 42(1): 118-123. DOI:10.13441/j.cnki.cykx.2016.01.017.
[19] ANIMASAUN D A, OGUNTOYE E O. Mutagenesis in crop improvement: methods and applications[J]. Journal of Crop Improvement, 2024, 38(3): 156-178. DOI:10.1080/15427528.2024.2336257.
[20] BOUASSIDA M, GHAZALA I, ELLOUZE-CHAABOUNI S, et al.Improved biosurfactant production by Bacillus subtilis SPB1 mutant obtained by random mutagenesis and its application in enhanced oil recovery in a sand system[J]. Journal of Microbiology and Biotechnology, 2018, 28(1): 95-104. DOI:10.4014/jmb.1701.01033.
[21] WANG Y X, WU S H, WANG H Y, et al. Optimization of conditions for a surfactant-producing strain and application to petroleum hydrocarbon-contaminated soil bioremediation[J]. Colloids and Surfaces B: Biointerfaces, 2022, 213: 112428. DOI:10.1016/j.colsurfb.2022.112428.
[22] MEHANDJIEV A, KOSTURKOVA G, MIHOV M. Enrichment of Pisum sativum gene resources through combined use of physical and chemical mutagens[J]. Israel Journal of plant sciences, 2001, 49(4):280-284. DOI:10.1560/UQPC-NNXP-GU0L-P3X4.
[23] 陈尚里, 于福田, 沈圆圆, 等. 高产抗菌脂肽Fengycin芽孢杆菌的诱变育种和发酵条件优化[J]. 食品工业科技, 2023, 44(23): 134-143.DOI:10.13386/j.issn1002-0306.2023020239.
[24] SCHÜRCH A C, ARREDONDO-ALONSO S, WILLEMS R L, et al.Whole genome sequencing options for bacterial strain typing and epidemiologic analysis based on single nucleotide polymorphism versus gene-by-gene-based approaches[J]. Clinical Microbiology and Infection, 2018, 24(4): 350-354. DOI:10.1016/j.cmi.2017.12.016.
[25] SETLOW P. Resistance of spores of Bacillus species to ultraviolet light[J]. Environmental and Molecular Mutagenesis, 2001, 38(2/3): 97-104. DOI:10.1002/em.1058.
[26] 谢定刚, 丛丽娜, 李若凡, 等. 原生质体紫外诱变选育高产抗菌脂肽菌株及其活性物质的研究[J]. 工业微生物, 2020, 50(1): 1-7.DOI:10.3969/j.issn.1001-6678.2020.01.001.
[27] 刘伟, 李英, 杜春梅. 微生物源脂肽的生物合成和分子调控[J]. 中国生物化学与分子生物学报, 2022, 38(12): 1630-1639. DOI:10.13865/j.cnki.cjbmb.2022.05.1571.
[28] 纪帅奇, 乌日娜, 张淘崴, 等. 高产抗菌脂肽芽孢杆菌的分离鉴定筛选及发酵工艺优化[J]. 食品工业科技, 2024, 45(4): 101-108.DOI:10.13386/j.issn1002-0306.2023040051.
[29] MA Y X, KONG Q, QIN C, et al. Identification of lipopeptides in Bacillus megaterium by two-step ultrafiltration and LC-ESI-MS/MS[J].AMB Express, 2016, 6(1): 79. DOI:10.1186/s13568-016-0252-6.
[30] LIN L Z, ZHENG Q W, WEI T, et al. Isolation and characterization of fengycins produced by Bacillus amyloliquefaciens JFL21 and its broad-spectrum antimicrobial potential against multidrug-resistant foodborne pathogens[J]. Frontiers in Microbiology, 2020, 11: 579621.DOI:10.3389/fmicb.2020.579621.
[31] SUI X N, HAN X B, CAO J M, et al. Biocontrol potential of Bacillus velezensis EM-1 associated with suppressive rhizosphere soil microbes against tobacco bacterial wilt[J]. Frontiers in Microbiology, 2022, 13:940156. DOI:10.3389/fmicb.2022.940156.
[32] HAMMAD M, ALI H, HASSAN N, et al. Food safety and biological control; genomic insights and antimicrobial potential of Bacillus velezensis FB2 against agricultural fungal pathogens[J]. PLoS ONE,2023, 18(11): e0291975. DOI:10.1371/journal.pone.0291975.
[33] ZHANG L, LIU Z R, PU Y L, et al. Antagonistic strain Bacillus velezensis JZ mediates the biocontrol of Bacillus altitudinis M-1, a cause of leaf spot disease in strawberry[J]. International Journal of Molecular Sciences, 2024, 25(16): 8872. DOI:10.3390/ijms25168872.
[34] SHAW G. Polymorphism and single nucleotide polymorphisms (SNPs)[J].BJU International, 2013, 112(5): 664-665. DOI:10.1111/bju.12298.
[35] DAS B, SARKAR C, DAS D, et al. Telavancin: a novel semisynthetic lipoglycopeptide agent to counter the challenge of resistant Grampositive pathogens[J]. Therapeutic Advances in Infectious Disease,2017, 4(2): 49-73. DOI:10.1177/2049936117690501.
[36] RAJAN K, SHI Z H, RICKE S C. Current aspects of Salmonella contamination in the US poultry production chain and the potential application of risk strategies in understanding emerging hazards[J].Critical Reviews in Microbiology, 2017, 43(3): 370-392. DOI:10.1080/1040841X.2016.1223600.
[37] XU T T, ZHANG X H. Edwardsiella tarda: an intriguing problem in aquaculture[J]. Aquaculture, 2014, 431: 129-135. DOI:10.1016/j.aquaculture.2013.12.001.