小麦低聚肽是由小麦蛋白经过酶解而成的一种具有生物活性的小分子质量肽混合物。通常由2~6 个氨基酸组成,分子质量主要分布在1 000 Da以下[1]。小麦低聚肽由于具有较高的营养价值,深受广大消费者的喜爱。近年来,小麦低聚肽在制备、营养功能、产品加工等方面受到国内外学者的广泛关注,并取得了一定的进展。研究发现,小麦低聚肽具有多种生物活性功能[2],如抗氧化[3]、抗炎[4]、降血糖[5]等,充分了解小麦低聚肽的功能和作用机制,才能合理加工和利用小麦低聚肽。本文综述小麦低聚肽在抗氧化、抗炎、调节免疫、降血压、降血糖、保护神经等功能和相关作用机制,以及在食品添加剂、功能性食品、医药和化学产品等方面的加工应用,并展望小麦低聚肽的发展前景,旨在为未来小麦低聚肽的开发和利用提供参考。
1 小麦低聚肽的制备
小麦低聚肽的制备方法主要包括蛋白酶酶解法、微生物发酵法等,目前最常用的制备方法是蛋白酶酶解法[6]。酶解法制备小麦低聚肽通常以小麦蛋白为原料,经过前处理(温度、pH值调节等)、酶解、灭酶、分离、纯化、喷雾干燥制得小分子肽混合物。常用于水解小麦蛋白的酶包括碱性蛋白酶、中性蛋白酶、风味蛋白酶、胰蛋白酶和木瓜蛋白酶等,不同蛋白酶作用于小麦蛋白的作用位点不同,水解程度也不同,因此得到的小麦低聚肽种类不同[7]。An Guangjie等[8]采用碱性蛋白酶水解小麦蛋白制备小麦低聚肽,发现固液比1∶7(g/mL)、酶解时间2 h、酶添加量1.2%的条件下小麦蛋白水解度最高(19.4%),且分子质量低于1 kDa的小麦低聚肽比例最高(78.8%)。于笛等[9]采用单一酶水解和双酶复合水解两种方法制备小麦低聚肽,发现由5种蛋白酶(碱性蛋白酶、中性蛋白酶、风味蛋白酶、胰蛋白酶、木瓜蛋白酶)单独制备的小麦低聚肽水解度不同,其中碱性蛋白酶水解度最高(18.3%),而采用碱性蛋白酶和胰蛋白酶复合水解小麦蛋白后水解度提升至37.72%,得到的小麦低聚肽分子质量更低(445~1 374 Da)。由此可见,采用复合酶法制备小麦低聚肽可显著提高小麦蛋白的水解度,但是小麦低聚肽的生产仍存在利用率低等问题,因此进一步提升小麦蛋白的水解度、提高小麦低聚肽的产出率具有重要的研究意义。
除蛋白酶酶解法外,微生物发酵法也是一种有效的制备小麦低聚肽的方法,微生物(如乳酸菌、曲霉等)会产生和利用蛋白酶催化小麦蛋白水解,生成分子质量较小的低聚肽和氨基酸[10]。彭睆睆[11]采用米曲霉和乳酸菌混合制曲结合发酵技术处理小麦蛋白制备得到呈味肽Asp-Cys-Gly,该肽能够显著增强鲜味。Niu Liya等[12]利用枯草芽孢杆菌B1发酵小麦蛋白,在最佳条件下小麦低聚肽的最大产量为8.69 mg/mL,分子质量主要分布在1 000 Da以下。但值得注意的是,采用微生物发酵法制备小麦低聚肽的相关研究较少,发酵过程中可能会产生有机酸、挥发性化合物以及其他次生代谢副产物,发酵工艺需优化,发酵机制也有待进一步探究。
2 小麦低聚肽的功能
近年来研究发现,小麦低聚肽具有抗氧化、抗炎、调节免疫、降血压、降血糖、保护神经等功能,图1展示了小麦低聚肽对人体各组织的常见功能以及其体内外相关作用机制。
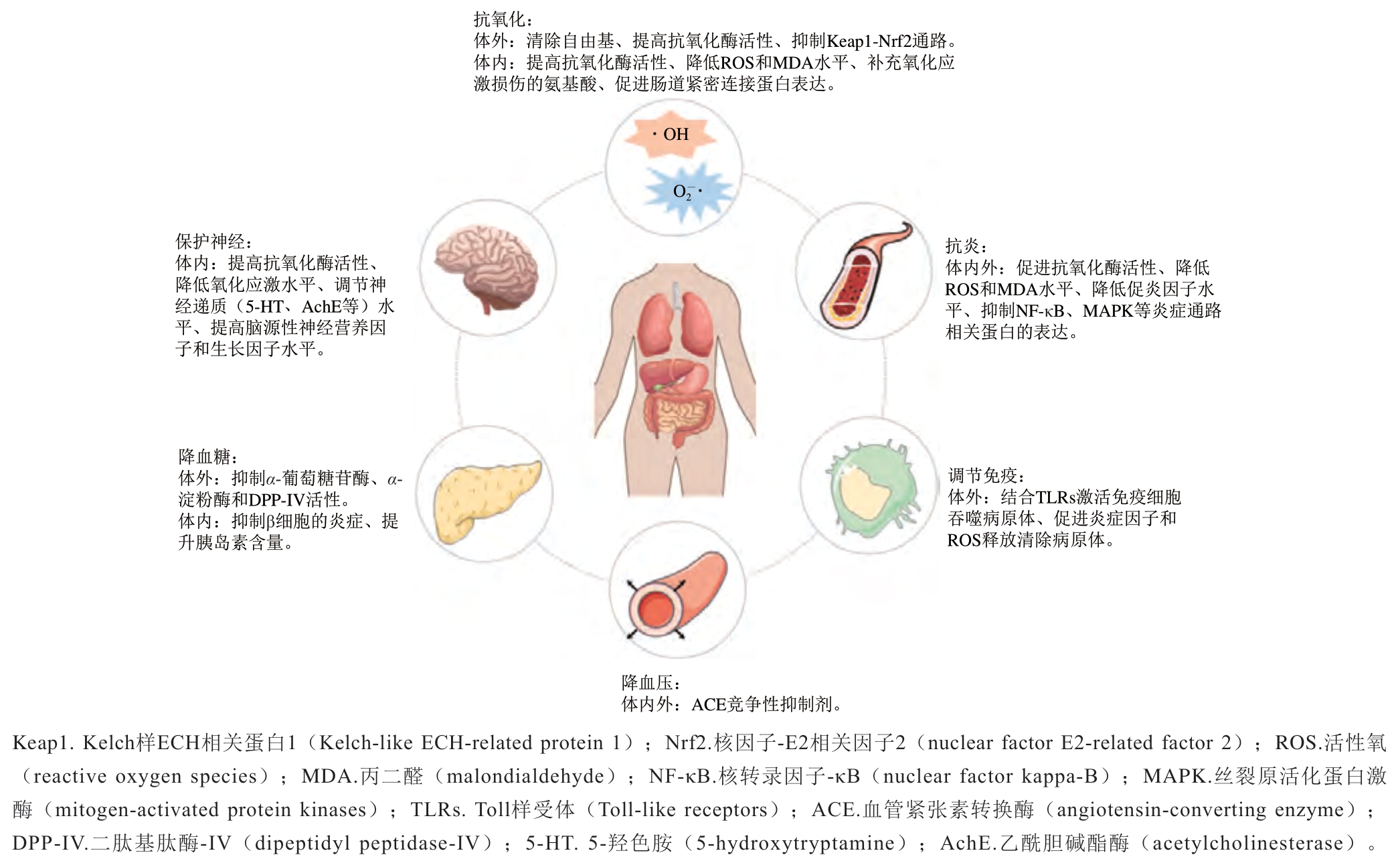
图1 小麦低聚肽的主要功能
Fig. 1 Primary functions of wheat oligopeptides
2.1 小麦低聚肽的抗氧化功能
小麦蛋白经过不同蛋白酶水解后得到的小麦低聚肽末端氨基酸残基主要含有苯酚基团、NH-基团和咪唑等特殊结构,可以为自由基提供氢原子使其还原为稳定的分子,对抗氧化活性有积极的影响[13-14]。体外研究表明,小麦低聚肽具有1,1-二苯基-2-苦基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)自由基、2,2’-联氮-二(3-乙基-苯并噻唑-6-磺酸)(2,2’-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS)阳离子自由基、羟自由基等的清除能力[15-19](表1)。Zhang Jixian等[15]研究发现碱性蛋白酶水解制备分子质量<1 kDa的小麦低聚肽具有较强的DPPH自由基清除能力,半数抑制浓度(half maximal inhibitory concentration,IC50)为2.77 mg/mL,经过分离发现,由Gly-Pro-Phe、Gly-Pro-Glu、Phe-Gly-Glu组成的小麦低聚肽抗氧化活性最高,IC50为1.17 mg/mL。Wang Fang等[16]发现中性蛋白酶水解小麦蛋白得到分子质量为948 Da的小麦低聚肽(ADWGGPLPH)也具有较好的DPPH自由基清除能力,IC50为3.76 mmol/L。凌空等[17]发现采用胃肠液消化小麦低聚肽,消化前后的DPPH自由基、羟自由基、总抗氧化能力(total-antioxidant capacity,T-AOC)没有显著差异。以上研究可见,不同蛋白酶水解小麦蛋白得到的小麦低聚肽肽段不同,体外抗氧化能力也不同,中性蛋白酶和碱性蛋白酶复合水解得到的小麦低聚肽抗氧化能力更强[17-18]。
表1 小麦低聚肽体外清除自由基活性
Table 1 In vitro free radical scavenging activity of wheat oligopeptides
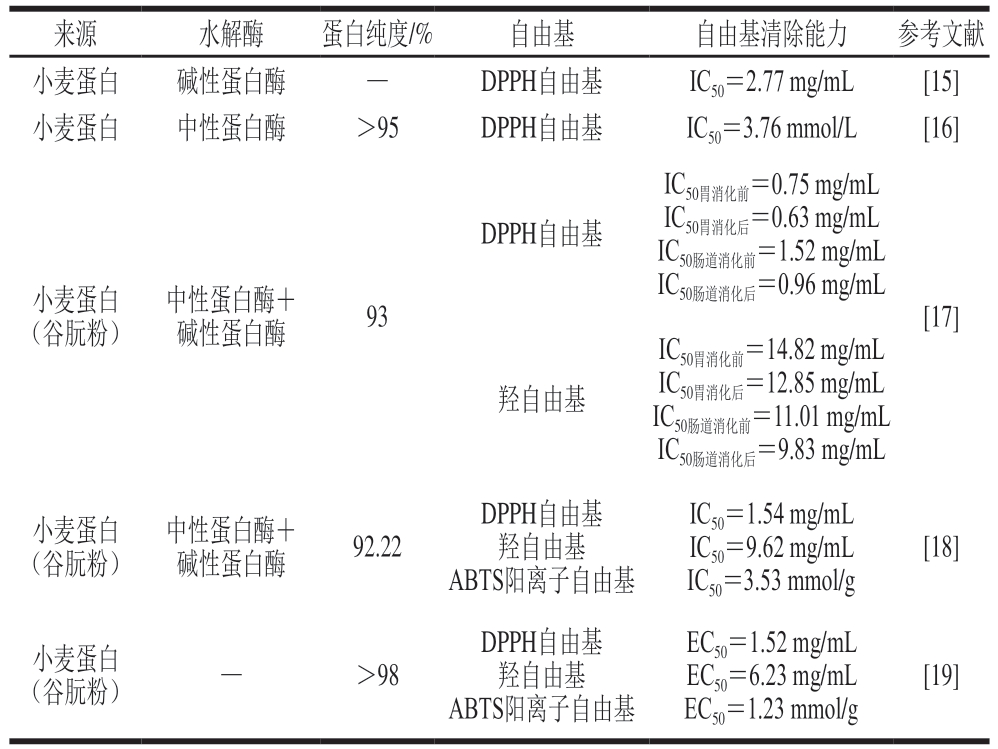
注:—.文献未说明,下同;EC50.半数有效浓度(median effect concentration)。
来源水解酶蛋白纯度/%自由基自由基清除能力参考文献小麦蛋白碱性蛋白酶—DPPH自由基IC50=2.77 mg/mL[15]小麦蛋白中性蛋白酶>95DPPH自由基IC50=3.76 mmol/L[16]DPPH自由基小麦蛋白(谷朊粉)中性蛋白酶+碱性蛋白酶93 IC50胃消化前=0.75 mg/mL IC50胃消化后=0.63 mg/mL IC50肠道消化前=1.52 mg/mL IC50肠道消化后=0.96 mg/mL[17]羟自由基IC50胃消化前=14.82 mg/mL IC50胃消化后=12.85 mg/mL IC50肠道消化前=11.01 mg/mL IC50肠道消化后=9.83 mg/mL小麦蛋白(谷朊粉)中性蛋白酶+碱性蛋白酶92.22 DPPH自由基羟自由基ABTS阳离子自由基IC50=1.54 mg/mL IC50=9.62 mg/mL IC50=3.53 mmol/g[18]小麦蛋白(谷朊粉)—>98 DPPH自由基羟自由基ABTS阳离子自由基EC50=1.52 mg/mL EC50=6.23 mg/mL EC50=1.23 mmol/g[19]
体外细胞实验解释了小麦低聚肽抗氧化能力的作用机制。Liu Wenying等[20-21]研究了小麦低聚肽中分离出的5种肽段(Leu-Tyr、Pro-Tyr、Tyr-Gln、Ala-Pro-Ser-Tyr、Arg-Gly-Gly-Tyr)对2,2’-偶氮二异丁基脒二盐酸盐(2,2’-azobis(2-methylpropionamidine) dihydrochloride,AAPH)处理下氧化应激的人胚胎肾细胞HEK-293的影响。5种小麦肽能与胞质接头蛋白Keap1抗体活性位点结合,阻止Keap1与Nrf2结合,因此激活的Nrf2能够进入细胞核促进抗氧化酶相关蛋白的表达,提高了超氧化物歧化酶(superoxide dismutase,SOD)、过氧化氢酶(catalase,CAT)、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)的活性,显著降低AAPH诱导细胞产生的脂肪过氧化产物MDA的水平。张羽等[22]研究了小麦低聚肽LNYPPY(分子质量为765 Da)对H2O2诱导的人肝肿瘤细胞和血管平滑肌细胞氧化应激模型的影响,发现LNYPPY能显著降低细胞内ROS的水平,提高细胞的存活率,有效缓解细胞的氧化应激。张亚卓等[23]使用1、5、10 mg/mL的小麦低聚肽对氧化损伤后的肠上皮细胞(Caco-2)进行修复,可显著提高细胞内SOD活性,降低MDA水平。综上,小麦低聚肽可以对氧化应激损伤的细胞起到修复作用,主要通过促进抗氧化酶蛋白表达,提升抗氧化酶活性,从而起到抗氧化作用。
体内实验进一步验证了小麦低聚肽的抗氧化作用。于兰兰等[3]采用低、中、高(0.4、0.8、1.6 g/(kg·d))3 个剂量组的小麦低聚肽(分子质量200~1 000 Da)灌胃一次性乙醇处理引起的急性酒精性肝损伤ICR小鼠,结果显示,低剂量小麦低聚肽处理能够显著提高小鼠肝脏的总SOD活力、血清和肝脏的谷胱甘肽(glutathione,GSH)水平,以及降低肝脏中蛋白质羰基含量,高剂量小麦低聚肽灌胃能够显著降低小鼠血清中MDA水平,这可能归因于小麦低聚肽片段中谷氨酸的质量分数最高,为肝脏合成GSH提供了来源,也为机体补充了由于氧化应激损伤的氨基酸,从而起到抗氧化作用。Feng Zhiyuan等[24]采用纯度为92.6%小麦低聚肽低中高剂量组(0.3、0.6、0.9 g/(kg·d))灌胃昆明雄性小鼠14 d,发现高剂量组能够有效缓解双氯芬酸钠导致的肠道黏膜损伤,其作用机制是通过提高SOD活性降低氧化应激水平(MDA和一氧化氮),以及增加肾上腺素E2水平和促进小鼠肠道紧密连接蛋白ZO-1和Occludin的表达,减轻肠道屏障受损和增加肠道黏膜的修复性,有效缓解氧化应激带来的肠黏膜损伤。由此可见,小麦低聚肽通过提升血清和肝脏中抗氧化酶活性、补充损伤氨基酸以及修复氧化应激导致的肠黏膜损伤,从而在体内起到抗氧化作用。
综上,小麦低聚肽的末端大部分含有疏水性和芳香族氨基酸,可以作为氢供体体外清除自由基,也可以在体内提供丰富的谷氨酸等氨基酸来源促进GSH的合成、减少自由基对蛋白质的损伤,以及通过抑制Keap1-Nrf2通路提升抗氧化酶的活性起到抗氧化作用。
2.2 小麦低聚肽的抗炎活性
炎症往往是由微生物污染、物理或化学损伤引起,通过刺激炎症介质如细胞因子、趋化因子和前列腺素的释放,激活NF-κB、MAPK等多种炎症信号传递途径,增强炎症反应使得血管舒张、血管渗透性增加,并且引起巨噬细胞、中性粒细胞等趋向病原体和损伤的细胞,通过释放自由基对病原体和受损细胞进行清除,但过量的炎症介质和自由基会导致细胞功能障碍和组织损伤,进一步引发心血管疾病、糖尿病等慢性疾病[25-26]。小麦低聚肽能够在体外和体内抑制炎症介质的产生、抑制炎症相关信号通路、减缓氧化应激水平从而起到抗炎作用(表2)。
表2 小麦低聚肽的抗炎作用
Table 2 Anti-inflammation effects of wheat oligopeptides
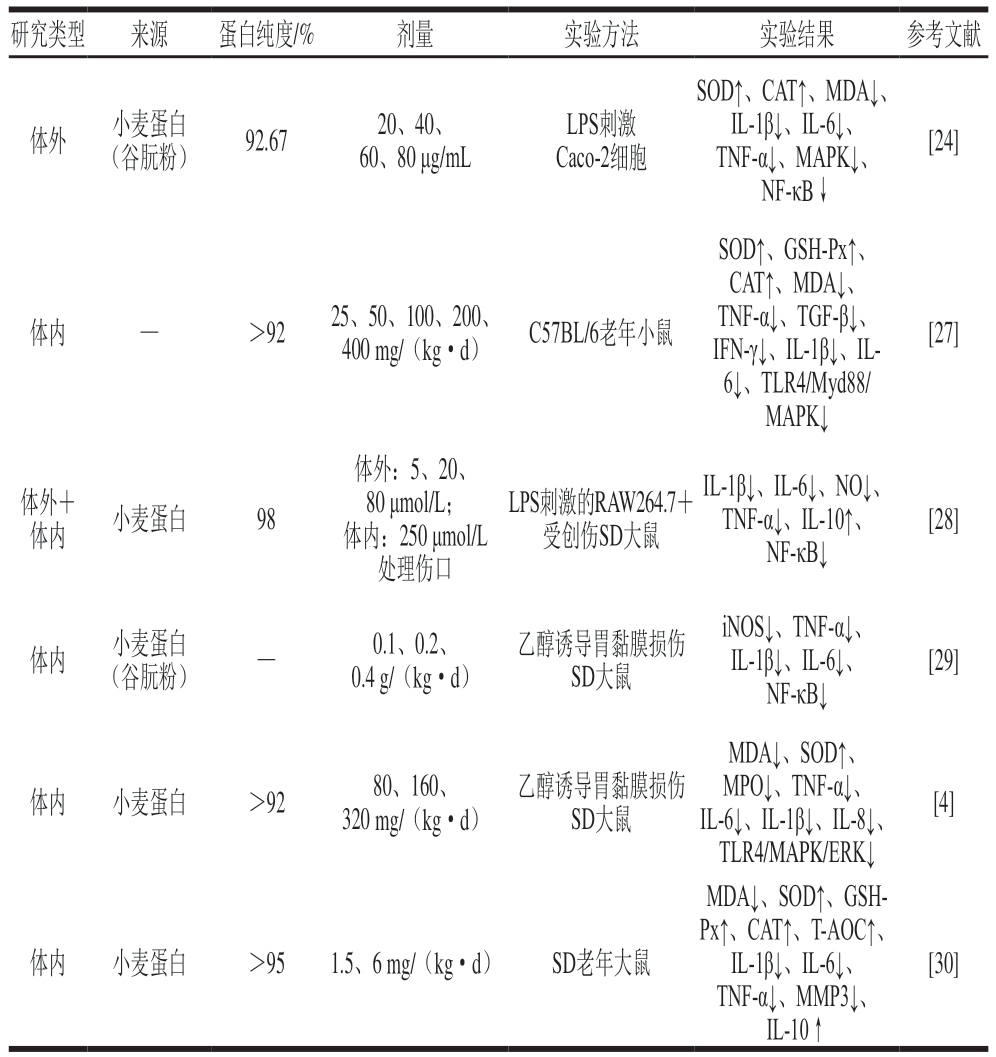
注:TGF-β.转化生长因子β(transforming growth factor-β);IFN-γ.干扰素-γ(interferon-γ);MMP3.基质金属蛋白酶3(matrix metalloproteinase 3)。
研究类型来源蛋白纯度/%剂量实验方法实验结果参考文献体外小麦蛋白(谷朊粉)92.6720、40、60、80 μg/mL LPS刺激Caco-2细胞SOD↑、CAT↑、MDA↓、IL-1β↓、IL-6↓、TNF-α↓、MAPK↓、NF-κB↓[24]体内—>9225、50、100、200、400 mg/(kg·d)C57BL/6老年小鼠SOD↑、GSH-Px↑、CAT↑、MDA↓、TNF-α↓、TGF-β↓、IFN-γ↓、IL-1β↓、IL-6↓、TLR4/Myd88/MAPK↓[27]体外+体内小麦蛋白98体外:5、20、80 μmol/L;体内:250 μmol/L处理伤口LPS刺激的RAW264.7+受创伤SD大鼠IL-1β↓、IL-6↓、NO↓、TNF-α↓、IL-10↑、NF-κB↓[28]体内小麦蛋白(谷朊粉)—0.1、0.2、0.4 g/(kg·d)乙醇诱导胃黏膜损伤SD大鼠iNOS↓、TNF-α↓、IL-1β↓、IL-6↓、NF-κB↓[29]体内小麦蛋白>9280、160、320 mg/(kg·d)乙醇诱导胃黏膜损伤SD大鼠MDA↓、SOD↑、MPO↓、TNF-α↓、IL-6↓、IL-1β↓、IL-8↓、TLR4/MAPK/ERK↓[4]体内小麦蛋白>951.5、6 mg/(kg·d)SD老年大鼠MDA↓、SOD↑、GSHPx↑、CAT↑、T-AOC↑、IL-1β↓、IL-6↓、TNF-α↓、MMP3↓、IL-10↑[30]
Feng Zhiyuan等[24]研究了小麦低聚肽对脂多糖(lipopolysaccharide,LPS)刺激Caco-2细胞的影响,发现将刺激后的细胞暴露于小麦低聚肽24 h后,显著增加细胞内SOD、CAT的活性,降低MDA水平,缓解细胞氧化应激水平,同时降低细胞内白细胞介素(interleukin,IL)-1β、IL-6和肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)的表达,抑制MAPK和NF-κB p65炎症相关信号通路的磷酸化水平,因此起到缓解炎症的作用。
随着年龄增长,体内氧化应激水平上升,炎症逐渐增加,且机体抗炎能力下降。Yang Xian等[27]研究了分子质量集中在140~1 000 Da的小麦低聚肽对C57BL/6老年小鼠体内炎症和氧化应激状况的影响,发现给老年小鼠连续灌胃小麦低聚肽30 d,能够显著增加小鼠血清内SOD等抗氧化酶的活性,降低MDA水平,从而起到减轻氧化应激的作用,还可以减少TNF-α、TGF-β、IL-1β等促炎因子的释放,以及抑制TLR4、髓样分化因子88(myeloid differentiation primary response protein 88,Myd88)和MAPK蛋白的表达,有效阻断了TLR4/Myd88/MAPK炎症通路。因此,小麦低聚肽起到抗氧化和缓解炎症的作用。Sui Huilin等[28]研究了小麦低聚肽(YDWPGGRN)对伤口创伤引起的炎症影响,小麦低聚肽处理能显著降低SD雄性大鼠伤口创面IL-1β、IL-6等多种促炎因子的水平,并且促进抗炎因子IL-10的释放。小麦低聚肽还能够刺激成纤维细胞和角质形成细胞的增殖和分化,刺激血管生成和胶原沉积,促进伤口愈合,有效缓解炎症水平。Yu Lanlan等[29]研究发现对乙醇诱导的急性胃黏膜损伤SD大鼠灌胃小麦低聚肽4 周可以通过抑制乙醇触发的NF-κB信号通路p65蛋白表达,显著降低诱导型一氧化氮合酶(inductive nitric oxide synthase,iNOS)和TNF-α、IL-6等促炎因子的水平,且灌胃低剂量小麦低聚肽的效果最优。Yang Xian等[4]研究同样发现,使用小麦低聚肽对SD雄性大鼠进行30 d治疗,可以有效缓解无水乙醇导致的胃黏膜损伤,减少大鼠体内TNF-α、IL-6、IL-1β等促炎因子的水平,同时降低TLR4、MAPK和细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK)蛋白表达,阻断TLR4/MAPK/ERK信号通路。汪芳等[30]研究了小麦低聚肽ADWGGPLPH对老化导致的SD大鼠肝脏损伤的影响,发现采用小麦低聚肽灌胃老年大鼠12 个月可以显著增加大鼠血清和肝脏中SOD、CAT等抗氧化酶的活性,降低MDA含量,以及减少IL-6、IL-1β等促炎因子的水平,增加抗炎因子IL-10的分泌,缓解老化导致的肝脏炎症。
综上,小麦低聚肽可以降低IL-1β、IL-6等促炎因子水平,促进抗氧化酶的活性,有效缓解氧化应激水平,抑制氧化应激导致的炎症损伤,以及抑制NF-κB、MAPK等炎症相关通路的蛋白表达,在体内外对炎症起到调控作用,因此,小麦低聚肽具有加工成抗炎药物的潜在应用价值。
2.3 小麦低聚肽的免疫调节活性
人体的免疫系统可以识别和清除体内的各种有害物质,起到抗炎、抗癌、修复组织损伤等作用。小麦低聚肽可以通过增加免疫细胞活性、调节炎症因子等调节机体的免疫系统[31]。Wu Wenjia等[32]研究了小麦低聚肽对免疫细胞的影响,发现相比于中性蛋白酶、胃蛋白酶、木瓜蛋白酶等水解酶,碱性蛋白酶水解得到的分子质量集中在300~1 450 Da的小麦低聚肽对淋巴细胞增殖、巨噬细胞吞噬作用和促炎细胞因子分泌的免疫调节活性最强。Wu Wenjia等[33]进一步研究发现碱性蛋白酶水解小麦蛋白得到的小麦肽ECFSTA(Glu-Cys-Phe-Ser-Thr-Ala)可通过与TLRs结合,激活RAW264.7巨噬细胞对病原体进行清除和吞噬,并显著促进炎症因子NO、IL-6、TNF-α和ROS的分泌,起到免疫调节的作用。以上研究表明,不同的酶解方法导致小麦低聚肽的免疫调节活性差异显著,其中碱性蛋白酶水解得到的小麦低聚肽调节免疫功能更强。小麦低聚肽通过结合TLRs激活免疫细胞对微生物进行清除,促进促炎因子和自由基的释放从而调控免疫功能。但近年来小麦低聚肽免疫调节活性相关研究较少,其激活免疫细胞的作用机制还有待深入研究。
2.4 小麦低聚肽的降血压活性
ACE是一种锌蛋白酶,广泛分布于人体的各个组织,可以通过调节肾素-血管紧张素系统起到调节血压的作用。ACE可以催化血管紧张素I转化为血管紧张素II。血管紧张素II可以结合血管壁的受体促进血管收缩,以及促进肾上腺皮质释放醛固酮提高血压。ACE还可以催化具有降压作用的缓激肽水解失活,进一步增加高血压的风险[34-36]。小麦低聚肽是一种ACE抑制肽,通过静电、疏水、氢键和范德华力作用于ACE的活性位点,阻止血管转化素I和ACE的相互作用,进而阻止血管紧张素I转化为血管紧张素II,作为ACE的竞争性抑制剂起到降血压的作用。
Liu Wenying等[19]研究了从小麦低聚肽混合物中分离出的5种肽段(Leu-Tyr、Leu-Val-Ser、Tyr-Gln、Ala-Pro-Ser-Tyr、Arg-Gly-Gly-Tyr)的ACE抑制活性,5种ACE抑制肽的IC50分别为0.09、0.19、0.62、0.64、0.67 mg/mL,小麦低聚肽混合物ACE抑制活性(IC50=0.68 mg/mL)分别是5种ACE抑制肽IC50的7.56、3.58、1.10、1.06、1.01 倍。Zhang Peng等[37]研究发现,通过铜绿假单胞菌蛋白酶和碱性蛋白酶协同作用水解小麦蛋白(谷朊粉),得到分子质量<1 kDa的小麦低聚肽具有较高的ACE抑制活性(IC50=0.21 mg/mL)。从小麦低聚肽中分离得到的7种具有不同ACE抑制活性的组分,其中,两种羧基末端含有色氨酸的ACE抑制肽(SAGGYIW、APATPSFW)抑制活性最高,IC50分别为0.002 mg/mL和0.036 mg/mL。因此,小麦低聚肽肽段C末端的色氨酸可能适当增强了ACE抑制作用,起到降血压的作用。Zou Zhipeng等[38]研究表明,在碱性蛋白酶水解小麦蛋白(谷朊粉)后得到的不同分子质量的肽段中,分子质量<1 kDa的肽段对ACE抑制活性最高,抑制率为84.25%,其较高的降血压活性可能归因于小麦低聚肽中N和C末端疏水和芳香族残基的存在,可以与ACE活性位点相结合。Zou Zhipeng等[38]还通过体内研究证明,给高血压大鼠灌胃小麦低聚肽(100 mg/(kg·d))可以有效降低其收缩压,且与卡托普利这类降压药起到的效果相似,进一步证实了体外实验得到的小麦低聚肽ACE抑制活性,证明了小麦低聚肽的降血压功能。
综上,小麦低聚肽可以作为ACE竞争性抑制剂起到降血压功能,且经过分离后得到的有效肽段的抑制活性更高,这可能是由于其含有的疏水性和芳香族氨基酸残基能更好的作用于ACE的活性位点。但是,大多数研究为体外实验,因此不能确定小麦低聚肽的ACE抑制活性能否会受到人体消化吸收的影响。
2.5 小麦低聚肽的降血糖活性
α-葡萄糖苷酶和α-淀粉酶可以将碳水化合物分解为葡萄糖,葡萄糖通过小肠上皮细胞吸收进入血液,因此提升了餐后的血糖水平[39]。小麦低聚肽可以作用于这两种酶的活性位点,阻止其与底物结合,减缓葡萄糖的生成和吸收,从而控制餐后血糖水平。Liu Weiwei等[5]发现胰蛋白酶水解小麦蛋白得到分子质量<1、1~3、3~5、5~10 kDa和>10 kDa的小麦肽中,分子质量<1 kDa的小麦低聚肽α-葡萄糖苷酶抑制活性最高,IC50为2.1 mg/mL。通过外翻肠囊模型法也测得小麦低聚肽可以显著抑制肠道葡萄糖的生成,且具有剂量依赖性。此外,经过活性肽段分析得出,LDLQR、AGGFR、LDNFR肽段具有较强的α-葡萄糖苷酶抑制活性(IC50=8.59、8.66、9.21 mmol/L),它们的C末端氨基酸残基大多为精氨酸,可以与α-葡萄糖苷酶活性位点上的关键氨基酸残基(ASP203、THR205、ASP542、ARG526)结合,起到竞争性抑制作用[40]。Mousavi等[41]使用猕猴桃酶水解小麦蛋白(谷朊粉)得到小麦肽,通过体外实验得出小麦低聚肽具有抑制α-葡萄糖苷酶和α-淀粉酶的活性,相比于分子质量为1~10、10~100 kDa和>100 kDa的小麦肽,分子质量<1 kDa的小麦低聚肽(WGLYH)抑制活性最高,抑制率分别为18.4%和53.3%,经过肽段分析得出,小麦低聚肽的α-葡萄糖苷酶和α-淀粉酶抑制活性可能归因于它们含有较高的羟基氨基酸(酪氨酸、苏氨酸、丝氨酸)、碱性氨基酸(精氨酸)和脯氨酸,在酶活性位点存在竞争性抑制作用,起到降血糖功能。以上研究证明,小麦肽可以作为α-葡萄糖苷酶和α-淀粉酶竞争性抑制剂起到降血糖作用,且分子质量<1 kDa的小麦低聚肽降血糖效果最为明显,这可能归因于小麦低聚肽含有更多能与酶活性关键位点结合的氨基酸残基,但是不同研究得到的小麦低聚肽酶抑制活性不同,这与使用的水解蛋白酶、得到的氨基酸残基不同有关,具有精氨酸残基的肽段与酶活性位点作用力可能更强,抑制效果更好。
DPP-IV是一种丝氨酸蛋白酶,可以在人体多个组织如肠道、肝脏和胰腺等表达。胰高血糖素样态-1(glucagon-like peptide-1,GLP-1)作为一种调节血糖的激素可以促进胰岛素分泌,抑制胰高血糖素分泌以及抑制胃排空,起到降血糖的作用。DPP-IV会引起GLP-1降解,从而提高餐后血糖水平,进而引发糖尿病[42]。先前研究表明小麦低聚肽可以作为DPP-IV竞争性抑制剂起到调控血糖的作用。Ding Long等[43]研究了不同蛋白酶水解小麦蛋白(谷朊粉)得到的分子质量<1 kDa小麦低聚肽的DPP-IV抑制活性,发现风味蛋白酶水解得到的小麦低聚肽对DPP-IV抑制活性最高,IC50为1.25 mg/mL,进一步分离后发现MPF和VAVPV肽段的抑制活性最高(抑制率分别为57.33%、56.08%)。Taga等[44]研究了生姜蛋白酶水解小麦蛋白(谷朊粉)得到的三肽(Gln-Pro-Gln、Gln-Pro-Gly、Gln-Pro-Phe、Leu-Pro-Gln、Ser-Pro-Gln)具有较好的DPP-IV抑制活性,IC50为20~30 μg/mL。此外,研究均发现小麦低聚肽N端的倒数第2个氨基酸(脯氨酸)通过与DPP-IV的S1和S2活性口袋的氨基酸残基(Tyr631、Val656、Trp659、Tyr662、Tyr666、Val711、Arg125、Glu205、Glu206、Ser 209、Phe357、Arg358)形成氢键、电荷吸引和疏水相互作用,起到竞争性抑制作用。由此可见,N端的倒数第2个氨基酸(脯氨酸)具有DPP-IV抑制活性。
β细胞可以通过感知血糖浓度,调节离子通道释放胰岛素,促进组织对葡萄糖的摄取和利用,从而调节人体血糖水平[45]。而炎症的发生和氧化应激可能会导致β细胞功能障碍和凋亡,从而引发糖尿病。MIN-6细胞是从糖尿病小鼠胰岛素瘤细胞中提取出来,保持了正常β细胞的生理特性[46]。Sun Suling等[47]研究了32种混合小麦低聚肽(Ala-Ala-Pro、Glu-Glu-Pro-Lys、Leu-Ala-Leu-Leu等)对非肥胖糖尿病(nonobese diabetic,NOD)小鼠β细胞功能的影响,给NOD小鼠灌胃小麦低聚肽20 周,随后提取其MIN-6细胞,并通过LPS刺激使其发生炎症反应后发现,小麦低聚肽可以显著抑制小鼠MIN-6细胞IL-6 mRNA的表达,减少小鼠血清中IL-6的水平,并显著提高小鼠体内的胰岛素水平。因此,小麦低聚肽可以通过抑制β细胞的炎症水平,维持正常的生理功能,促进胰岛素的分泌,起到降低血糖的作用。
综上,小麦低聚肽可以作为α-葡萄糖苷酶、α-淀粉酶和DPP-IV的竞争性抑制剂起到降血糖的功效,也可以通过缓解β细胞的炎症水平间接调控血糖平衡。值得注意的是,对于不同蛋白酶水解得到的小麦低聚肽降血糖活性不同,今后可以进一步研究肽段结构特点与降糖效果的关系。
2.6 小麦低聚肽的保护神经活性
5-HT是一种重要的神经递质,参与神经系统调节,AchE主要具有水解乙酰胆碱、终止突触膜上神经递质的兴奋性功能,较低水平的5-HT和AchE容易出现焦虑、抑郁等疾病[48-49]。小麦低聚肽可以调控多种神经递质起到保护神经的作用。
Zheng Zhiqiang等[50]研究表明,补充小麦肽显著增强了4 个月增量游泳训练下SD大鼠骨骼肌GSH-Px、SOD的活性,降低了MDA水平。同时增加脑组织中5-HT和AchE的水平,缓解大鼠疲劳带来的压力情绪。刘辉等[51]研究了小麦低聚肽对慢性疲劳综合症引起的认知障碍影响,发现给慢性疲劳综合症的SD雄性大鼠灌胃小麦低聚肽8 周后可以显著提升大鼠海马组织的SOD活力和降低MDA水平,降低大鼠脑组织中5-HT含量,以及提高脑源性神经营养因子和神经生长因子的水平,缓解大鼠的认知功能障碍。
小麦低聚肽可以促进抗氧化酶活性从而抑制氧化应激水平、调控神经递质等因子缓解疲劳带来的神经系统紊乱,起到保护神经系统的作用。但神经系统相关疾病不同,对神经递质起到的调节作用不同,且涉及到的研究较少,因此小麦低聚肽的神经保护功能还需要大量研究的验证。
2.7 小麦低聚肽在其他方面的活性
随着年龄的增长,机体代谢功能和抗氧化能力下降,肌肉蛋白质吸收和合成功能下降,以及产生大量的ROS自由基,造成氧化应激、脂肪过氧化等问题,会导致肌肉衰减、萎缩[52-53]。Pan Da等[54]研究了小麦低聚肽的摄入对肌肉老化和萎缩的影响,发现给SD老年大鼠灌胃小麦低聚肽(100、200、400 mg/(kg·d))可以显著上调吡咯啉-5-羧酸还原酶3、前纤维蛋白1的表达,抑制骨骼肌肉的萎缩,上调RNA结合基序蛋白3、蛋白激酶B的表达,促进肌肉中蛋白质的合成以及骨骼肌的重组,以及上调肌球蛋白和骨骼肌慢肌肌钙蛋白T的表达,增强老年大鼠的骨骼肌力量。同时,小麦低聚肽还可以显著降低大鼠体内ROS、MDA的水平,并提高SOD活性,有效抑制老年大鼠体内氧化应激水平,以及降低IL-6、TNF-α等促炎因子的释放,抑制肌肉炎症,提升肌肉的质量和功能,证明了小麦低聚肽缓解肌肉老化萎缩的潜力。
Liu Wenying等[55]研究了小麦低聚肽对血管疾病的影响,发现碱性蛋白酶和中性蛋白酶水解后得到的15种小麦低聚肽肽段具有抗血栓、血管舒张和降胆固醇活性,其中,Ile-Leu-Arg和Ile-Leu-Pro-Arg通过抑制凝血酶活性起到抗血栓的作用,Val-Asn、Phe-Pro-Gln和Phe-Arg通过增加NOx浓度起到促进血管舒张活性,而Gln-Arg-Gln、Ile-Leu-Arg、Phe-Pro-Gln和Ile-Leu-Pro-Arg通过促进胆固醇7α羟化酶的mRNA表达有效抑制胆固醇的合成,起到降低胆固醇的作用。
剧烈运动会导致肌肉中肌糖原被消耗生成乳酸,蛋白质被消耗引起尿素含量升高,同时肌肉会产生大量的ROS自由基,进而引起炎症、肌肉酸痛等问题,导致疲劳的产生[56]。钱平等[57]研究了小麦低聚肽对运动导致的SD大鼠疲劳的影响,发现通过灌胃4 周20 mg/(kg·d)和100 mg/(kg·d)的小麦低聚肽能够显著缩短大鼠力竭游泳时间,增加大鼠骨骼肌糖原的含量,以及增强大鼠骨骼肌SOD和GSH-Px的活性,降低骨骼肌MDA的水平,发挥抗疲劳的作用。
3 小麦低聚肽的应用
小麦低聚肽富含人体必要氨基酸,是日常饮食中优质蛋白的来源,且小麦低聚肽具有抗氧化、抗炎、增加免疫力等生物活性,受到人们的喜爱,并被广泛应用于食品、医药和化学产品的加工应用中。
3.1 食品添加剂
小麦低聚肽富含大量的谷氨酸以及亲水性氨基酸残基,可以与面制品中的淀粉分子以及水分子结合,因此可以作为一种天然食品添加剂改善面制品的流变特性和面筋网络结构,从而提高面制品的质地和口感。Liu Hongyan等[58]研究了添加(0.5%、1%、1.5%,质量分数)小麦低聚肽制成的面团品质和特性,发现小麦低聚肽与淀粉分子通过分子间氢键交联,形成较强的谷蛋白网络结构(淀粉-淀粉、淀粉-蛋白质、蛋白质-蛋白质),降低了面团中水的流动性,显著增强面团的黏弹性、稳定性、延伸性和强度,提高面团的发酵高度和持气率,降低面团的峰值黏度、崩解值和消减值,抑制淀粉的糊化,提升了面团产品的品质。Zhang Yuting等[59]研究发现,添加1%的小麦低聚肽制成的面包卷品质更好,这主要也归因于小麦低聚肽与面粉形成的谷蛋白网络结构,改善了面包卷的比容和内部结构,小麦低聚肽还阻碍了淀粉的双螺旋结构形成,降低了淀粉结晶度等,从而有效抑制了面包卷的变质。单传龙等[60]研究发现,碱性蛋白酶水解得到的小麦低聚肽加入酸奶中可以有效减少其发酵周期,改善酸奶的感官和结构特征,且富含的亮氨酸、异亮氨酸和缬氨酸丰富了酸奶的营养价值。以上研究为今后更好地将小麦低聚肽应用于食品质量改善和加工提供了良好的理论基础,并进一步拓展了其作为新型食品添加剂的应用领域。
3.2 功能性食品
小麦低聚肽具有抗氧化、抗炎以及调控免疫系统等功能,将小麦低聚肽作为原料加工成功能性保健食品,在市场上具有广阔应用前景。袁媛等[61]根据小麦低聚肽的免疫调节活性研制出3种不同剂量的小麦低聚肽(1.0、2.5、5.0 g/kg)固体饮料,体内研究发现可以通过增强细胞免疫、体液免疫以及自然杀伤细胞活性从而增强ICR小鼠的免疫功能。高畅等[62]根据小麦低聚肽抗疲劳活性研究发明了牛磺酸-小麦肽复合饮料(0.9%牛磺酸、1.0%小麦低聚肽、1.8%木糖醇、0.4%菊粉),并通过体内实验证明该饮料可以显著降低小鼠血液乳酸、MDA及尿素氮的含量,增加SOD活力及糖原含量,能有效地促进小鼠体能恢复,起到抗疲劳的作用。小麦低聚肽与金属螯合也可以作为一种功能性食品。Liu Wenying等[63]研究制备了钙螯合小麦低聚肽产品,发现14种小麦低聚肽螯合钙肽段的生物利用率较高,在强酸环境下具有较强的稳定性,可以作为有效的钙补充剂。关桦楠等[64]研究了一种小麦低聚肽-纳米二氧化硅蛋白冠复合物,发现小麦低聚肽中氨基酸残基作为氢供体可以起到抗氧化作用,以及与金属螯合形成的三维网状结构有利于泡沫的形成和稳定,具有较强的抗氧化性、起泡性和乳化性,可以添加到冲调类粉末状食物中等。由此可见,小麦低聚肽的功能和相关作用机制为研发小麦低聚肽功能性产品提供了重要依据,以小麦低聚肽为基础原料制备功能性食品,在未来具有巨大的应用价值。
3.3 药物载体
小麦低聚肽的水溶性、抗氧化性等特点,使其具有加工为药物载体的应用价值,刘睿等[65]将小麦低聚肽作为微胶囊壁材,VD作为芯材,制备小麦肽-VD微胶囊,小麦低聚肽中脯氨酸的存在可以有效提高微胶囊的稳定性,谷氨酸、丙氨酸、天冬氨酸和亮氨酸等提供了抗氧化功能,保护VD活性和延长货架期。卢知浩等[66]也发现小麦低聚肽作为壁材,VD3作为芯材制作出的微胶囊具有较高的热稳定性、溶解性以及胃环境稳定性。
3.4 化学产品加工
Li Wanchun等[67]通过小麦低聚肽和月桂酰氯反应,研发了一种新型表面活性剂(月桂酰小麦肽钾),其具有较强的发泡性能且无刺激性,被证明在洗发水、洗面奶等产品中具有潜在的应用前景。
综上,小麦低聚肽可以加工为功能性添加剂应用到食品和化学产品中;加工成保健品起到抗疲劳、提高免疫力等作用;加工成药物载体起到抗氧化作用。尽管小麦低聚肽在多种产品的研发中具有广泛的应用潜力,但是小麦低聚肽的多种加工产品目前还没有广泛应用于市场,这需要进一步拓展应用场景,并加强产品的市场推广。
4 结 语
小麦低聚肽可以作为氢供体起到清除自由基的作用,激活抗氧化酶的活性,起到抗氧化作用;阻碍炎症相关通路,降低促炎因子水平,有效抑制炎症的发生;激活免疫细胞调控免疫系统清除病原体;作为ACE抑制肽起到降血压的作用、抑制碳水化合物消化吸收相关酶活性,起到降血糖活性;通过调节神经递质的水平起到保护神经的作用。由于小麦低聚肽具有多种生物活性功能,可以充分应用于食品的加工中,作为食品添加剂改善加工食品的品质和保质期,作为功能性食品起到相应的生物活性作用,以及作为药物载体帮助药物更好的储存和吸收。总体来说,小麦低聚肽具有广阔的发展前景和加工应用方向,但是在未来应从以下方面进行深入研究:1)小麦低聚肽功能研究涉及的实验大多为体外和动物实验,很少应用到人体实验中,很难保证小麦低聚肽在人体消化吸收后是否还具有相应的功能。因此,未来应将小麦低聚肽应用于人群膳食干预实验中,进一步检测其生物活性功能。2)小麦低聚肽功能相关研究主要通过测量相对应的生物指标进行判断,但具体机理仍需要进一步的深入研究。3)小麦低聚肽的产品加工目前仍处于研发和探索中,未来应进一步研究产品的生物活性机制,更好地加工和利用小麦低聚肽资源,进一步扩大消费市场。
[1] 方磊, 李诒光, 陈亮, 等. 小麦低聚肽营养成分和特征功能肽段研究[J]. 食品与发酵工业, 2023, 49(11): 178-182. DOI:10.13995/j.cnki.11-1802/ts.031455.
[2] WENG Z B, CHEN Y R, LIANG T T, et al. A review on processing methods and functions of wheat germ-derived bioactive peptides[J].Critical Reviews in Food Science and Nutrition, 2023, 63(22): 5577-5593. DOI:10.1080/10408398.2021.2021139.
[3] 于兰兰, 刘伟, 周雅琳, 等. 小麦低聚肽对急性酒精中毒小鼠抗氧化功能的影响[J]. 食品科学, 2020, 41(7): 159-163. DOI:10.7506/spkx1002-6630-20190321-285.
[4] YANG X, YANG L G, PAN D, et al. Wheat peptide protects against ethanol-induced gastric mucosal damage through downregulation of TLR4 and MAPK[J]. Journal of Functional Foods, 2020, 75: 104271.DOI:10.1016/j.jff.2020.104271.
[5] LIU W W, LI H Y, WEN Y Y, et al. Molecular mechanism for the α-glucosidase inhibitory effect of wheat germ peptides[J]. Journal of Agricultural and Food Chemistry, 2021, 69(50): 15231-15239.DOI:10.1021/acs.jafc.1c06098.
[6] 康连虎, 曹川. 小麦低聚肽酶解方法及生物活性研究进展[J]. 粮食与油脂, 2019, 32(5): 1-3. DOI:10.3969/j.issn.1008-9578.2019.05.001.
[7] 赵泽龙. 小麦低聚肽制备工艺的优化及性质与抗氧化能力测试[D].大庆: 黑龙江八一农垦大学, 2016.
[8] AN G J, WEI M Y, WANG Z C, et al. Effects of enzymolysis method on the preparation of peptides from wheat flour[J]. Food Bioscience,2022, 49: 101956. DOI:10.1016/j.fbio.2022.101956.
[9] 于笛, 赵泽龙, 张丽萍. 复合酶法制备小麦低聚肽的工艺研究[J].中国食品添加剂, 2017(6): 170-177.
[10] ZHANG J Y, XIAO X, DONG Y, et al. Effect of fermented wheat germ extract with Lactobacillus plantarum Dy-1 on HT-29 cell proliferation and apoptosis[J]. Journal of Agricultural and Food Chemistry, 2015,63(9): 2449-2457. DOI:10.1021/acs.jafc.5b00041.
[11] 彭睆睆. 利用小麦面筋蛋白制备呈味基料及呈味肽的分离鉴定[D].广州: 华南理工大学, 2014.
[12] NIU L Y, JIANG S T, PAN L J. Preparation and evaluation of antioxidant activities of peptides obtained from defatted wheat germ by fermentation[J]. Journal of Food Science and Technology, 2013,50(1): 53-61. DOI:10.1007/s13197-011-0318-z.
[13] MEMARPOOR-YAZDI M, ASOODEH A, CHAMANI J. A novel antioxidant and antimicrobial peptide from hen egg white lysozyme hydrolysates[J]. Journal of Functional Foods, 2012, 4(1): 278-286.DOI:10.1016/j.jff.2011.12.004.
[14] MARDANI M, BADAKNÉ K, FARMANI J, et al. Antioxidant peptides: overview of production, properties, and applications in food systems[J]. Comprehensive Reviews in Food Science and Food Safety,2023, 22(1): 46-106. DOI:10.1111/1541-4337.13061.
[15] ZHANG J X, WEN C T, LI C Z, et al. Antioxidant peptide fractions isolated from wheat germ protein with subcritical water extraction and its transport across Caco-2 cells[J]. Journal of Food Science, 2019,84(8): 2139-2146. DOI:10.1111/1750-3841.14720.
[16] WANG F, WENG Z B, LYU Y, et al. Wheat germ-derived peptide ADWGGPLPH abolishes high glucose-induced oxidative stress via modulation of the PKCζ/AMPK/NOX4 pathway[J]. Food & Function,2020, 11(8): 6843-6854. DOI:10.1039/d0fo01229g.
[17] 凌空, 张铭晧, 高丽辉, 等. 体外模拟消化对小麦低聚肽抗氧化活性影响[J]. 食品工业, 2021, 42(4): 82-86.
[18] 刘文颖, 冯晓文, 程青丽, 等. 小麦低聚肽的结构特征及其体外抗氧化活性[J]. 现代食品科技, 2021, 37(12): 72-79. DOI:10.13982/j.mfst.1673-9078.2021.12.0075.
[19] LIU W Y, ZHANG J T, MIYAKAWA T, et al. Antioxidant properties and inhibition of angiotensin-converting enzyme by highly active peptides from wheat gluten[J]. Scientific Reports, 2021, 11(1): 5206.DOI:10.1038/s41598-021-84820-7.
[20] LIU W Y, REN J, WU H S, et al. Inhibitory effects and action mechanism of five antioxidant peptides derived from wheat gluten on cells oxidative stress injury[J]. Food Bioscience, 2023, 56: 103236.DOI:10.1016/j.fbio.2023.103236.
[21] LIU W Y, LIU R, QIN Q Y, et al. Molecular docking and molecular dynamics simulation of wheat gluten-derived antioxidant peptides acting through the Keap1-Nrf2 pathway[J]. Journal of the Science of Food and Agriculture, 2024, 104(13): 8150-8161. DOI:10.1002/jsfa.13647.
[22] 张羽, 汪芳, 翁泽斌, 等. 麦胚清蛋白抗氧化肽的筛选及对细胞氧化损伤的保护作用[J]. 食品科学, 2021, 42(17): 10-18. DOI:10.7506/spkx1002-6630-20200901-012.
[23] 张亚卓, 姜思萌, 魏颖, 等. 小麦低聚肽对体外肠上皮细胞氧化应激损伤的保护作用[J]. 食品与发酵工业, 2015, 41(1): 46-50.DOI:10.13995/j.cnki.11-1802/ts.201501009.
[24] FENG Z Y, WEI Y, ZHANG Z R, et al. Wheat peptides inhibit the activation of MAPK and NF-κB inflammatory pathways and maintain epithelial barrier integrity in NSAID-induced intestinal epithelial injury[J]. Food & Function, 2024, 15(2): 823-837. DOI:10.1039/d3fo03954d.
[25] SCHULZE-OSTHOFF K, FERRARI D, RIEHEMANN K, et al.Regulation of NF-kappa B activation by MAP kinase cascades[J].Immunobiology, 1997, 198(1/2/3): 35-49. DOI:10.1016/s0171-2985(97)80025-3.
[26] GALLO K A, ELLSWORTH E, STOUB H, et al. Therapeutic potential of targeting mixed lineage kinases in cancer and inflammation[J].Pharmacology & Therapeutics, 2020, 207: 107457. DOI:10.1016/j.pharmthera.2019.107457.
[27] YANG X, PAN D, YANG C, et al. Wheat oligopeptides enhance the intestinal mucosal barrier and alleviate inflammation via the TLR4/Myd88/MAPK signaling pathway in aged mice[J]. Food & Nutrition Research, 2022, 66: 66. DOI:10.29219/fnr.v66.5690.
[28] SUI H L, WANG F, WENG Z B, et al. A wheat germ-derived peptide YDWPGGRN facilitates skin wound-healing processes[J].Biochemical and Biophysical Research Communications, 2020,524(4): 943-950. DOI:10.1016/j.bbrc.2020.01.162.
[29] YU L L, LI R J, LIU W, et al. Protective effects of wheat peptides against ethanol-induced gastric mucosal lesions in rats: vasodilation and anti-inflammation[J]. Nutrients, 2020, 12(8): 2355. DOI:10.3390/nu12082355.
[30] 汪芳, 罗涛, 陈烩铃, 等. 小麦胚芽活性肽通过AMPK/SIRT1改善大鼠肝脏衰老损伤的作用机制研究[J]. 中国科学: 生命科学, 2024,54(3): 537-547. DOI:10.1360/SSV-2023-0200.
[31] SZERSZUNOWICZ I, KOZICKI S. Plant-derived proteins and peptides as potential immunomodulators[J]. Molecules, 2023, 29(1):209. DOI:10.3390/molecules29010209.
[32] WU W J, ZHANG M M, SUN C Z, et al. Enzymatic preparation of immunomodulatory hydrolysates from defatted wheat germ (Triticum Vulgare) globulin[J]. International Journal of Food Science &Technology, 2016, 51(12): 2556-2566. DOI:10.1111/ijfs.13238.
[33] WU W J, ZHANG M M, REN Y, et al. Characterization and immunomodulatory activity of a novel peptide, ECFSTA, from wheat germ globulin[J]. Journal of Agricultural and Food Chemistry, 2017,65(27): 5561-5569. DOI:10.1021/acs.jafc.7b01360.
[34] GUANG C E, PHILLIPS R D, JIANG B, et al. Three key proteasesangiotensin-I-converting enzyme (ACE), ACE2 and renin: within and beyond the renin-angiotensin system[J]. Archives of Cardiovascular Diseases, 2012, 105(6/7): 373-385. DOI:10.1016/j.acvd.2012.02.010.
[35] ZHANG Y Q, LIU H G, HONG H, et al. Purification and identification of dipeptidyl peptidase IV and angiotensin-converting enzyme inhibitory peptides from silver carp (Hypophthalmichthys molitrix)muscle hydrolysate[J]. European Food Research and Technology,2019, 245(1): 243-255. DOI:10.1007/s00217-018-3157-6.
[36] ALUKO R E. Food protein-derived renin-inhibitory peptides: in vitro and in vivo properties[J]. Journal of Food Biochemistry, 2019, 43(1):e12648. DOI:10.1111/jfbc.12648.
[37] ZHANG P, CHANG C, LIU H J, et al. Identification of novel angiotensin I-converting enzyme (ACE) inhibitory peptides from wheat gluten hydrolysate by the protease of Pseudomonas aeruginosa[J]. Journal of Functional Foods, 2020, 65: 103751.DOI:10.1016/j.jff.2019.103751.
[38] ZOU Z P, WANG M J, WANG Z G, et al. Antihypertensive and antioxidant activities of enzymatic wheat bran protein hydrolysates[J]. Journal of Food Biochemistry, 2020, 44(1): e13090. DOI:10.1111/jfbc.13090.
[39] GONG L X, FENG D N, WANG T X, et al. Inhibitors of α-amylase and α-glucosidase: potential linkage for whole cereal foods on prevention of hyperglycemia[J]. Food Science & Nutrition, 2020,8(12): 6320-6337. DOI:10.1002/fsn3.1987.
[40] SIM L, QUEZADA-CALVILLO R, STERCHI E E, et al. Human intestinal maltase-glucoamylase: crystal structure of the N-terminal catalytic subunit and basis of inhibition and substrate specificity[J].Journal of Molecular Biology, 2008, 375(3): 782-792. DOI:10.1016/j.jmb.2007.10.069.
[41] MOUSAVI B, AZIZI M H, ABBASI S. Antidiabetic bio-peptides of soft and hard wheat glutens[J]. Food Chemistry: Molecular Sciences,2022, 4: 100104. DOI:10.1016/j.fochms.2022.100104.
[42] ZHAO R, LU S W, LI S Z, et al. Enzymatic preparation and processing properties of DPP-IV inhibitory peptides derived from wheat gluten:effects of pretreatment methods and protease types[J]. Foods, 2024,13(2): 216. DOI:10.3390/foods13020216.
[43] DING L, MA R D, YOU H X, et al. Identification and characterization of dipeptidyl peptidase IV inhibitory peptides from wheat gluten proteins[J]. Journal of Cereal Science, 2022, 103: 103396.DOI:10.1016/j.jcs.2021.103396.
[44] TAGA Y, HAYASHIDA O, KUSUBATA M, et al. Production of a novel wheat gluten hydrolysate containing dipeptidyl peptidase-IV inhibitory tripeptides using ginger protease[J]. Bioscience Biotechnology and Biochemistry, 2017, 81(9): 1823-1828. DOI:10.1080/09168451.2017.1345615.
[45] EIZIRIK D L, PASQUALI L, CNOP M. Pancreatic β-cells in type 1 and type 2 diabetes mellitus: different pathways to failure[J]. Nature Reviews Endocrinology, 2020, 16(7): 349-362. DOI:10.1038/s41574-020-0355-7.
[46] SOBEL D O, RAMASUBRAMANIAN B, MITNAUL L.Characterization of a mouse model of islet transplantation using MIN-6 cells[J]. Islets, 2020, 12(4): 71-86. DOI:10.1080/19382014.2020.1763719.
[47] SUN S L, ZHANG H, SHAN K, et al. Effect of different cereal peptides on the development of type 1 diabetes is associated with their anti-inflammatory ability: in vitro and in vivo studies[J]. Molecular Nutrition & Food Research, 2019, 63(11): 1800987. DOI:10.1002/mnfr.201800987.
[48] JANS L A W, RIEDEL W J, MARKUS C R, et al. Serotonergic vulnerability and depression: assumptions, experimental evidence and implications[J]. Molecular Psychiatry, 2007, 12(6): 522-543.DOI:10.1038/sj.mp.4001920.
[49] MODESTO K A, MARTINEZ C B R. Roundup® causes oxidative stress in liver and inhibits acetylcholinesterase in muscle and brain of the fish Prochilodus lineatus[J]. Chemosphere, 2010, 78(3): 294-299.DOI:10.1016/j.chemosphere.2009.10.047.
[50] ZHENG Z Q, YANG X X, LIU J, et al. Effects of wheat peptide supplementation on anti-fatigue and immunoregulation during incremental swimming exercise in rats[J]. RSC Advances, 2017, 7(69):43345-43355. DOI:10.1039/C7RA07860A.
[51] 刘辉, 周安妮, 胡胜男, 等. 小麦肽改善慢性疲劳综合征大鼠认知功能障碍[J]. 食品科学, 2022, 43(19): 137-143. DOI:10.7506/spkx1002-6630-20220610-098.
[52] DAO T, GREEN A E, KIM Y A, et al. Sarcopenia and muscle aging: a brief overview[J]. Endocrinology and Metabolism, 2020, 35(4): 716-732. DOI:10.3803/EnM.2020.405.
[53] GREVENDONK L, CONNELL N J, MCCRUM C, et al. Impact of aging and exercise on skeletal muscle mitochondrial capacity, energy metabolism, and physical function[J]. Nature Communications, 2021,12(1): 4773. DOI:10.1038/s41467-021-24956-2.
[54] PAN D, YANG L G, YANG X, et al. Potential nutritional strategies to prevent and reverse sarcopenia in aging process: role of fish oilderived ω-3 polyunsaturated fatty acids, wheat oligopeptide and their combined intervention[J]. Journal of Advanced Research, 2024, 57:77-91. DOI:10.1016/j.jare.2023.04.005.
[55] LIU W Y, MIYAKAWA T, LU J, et al. Isolation and characterization of oligopeptides with vascular disease suppression effects derived from wheat gluten[J]. Journal of Food Science and Technology, 2021, 58(9):3504-3513. DOI:10.1007/s13197-021-05040-5.
[56] WANG P X, WANG D H, HU J M, et al. Natural bioactive peptides to beat exercise-induced fatigue: a review[J]. Food Bioscience, 2021, 43:101298. DOI:10.1016/j.fbio.2021.101298.
[57] 钱平, 邵剑钢, 刘晋, 等. 小麦低聚肽抗疲劳活性研究[J]. 中国食物与营养, 2019, 25(12): 64-68. DOI:10.19870/j.cnki.11-3716/ts.2019.12.013.
[58] LIU H Y, WAN L Y, XIAO S S, et al. Changes in the physicochemical and protein distribution properties of dough with the wheat oligopeptide incorporation[J]. Food Bioscience, 2023, 52: 102354.DOI:10.1016/j.fbio.2023.102354.
[59] ZHANG Y T, LIU X R, YU J B, et al. Effects of wheat oligopeptide on the baking and retrogradation properties of bread rolls: evaluation of crumb hardness, moisture content, and starch crystallization[J]. Foods,2024, 13(3): 397. DOI:10.3390/foods13030397.
[60] 单传龙, 李欣悦, 许博能, 等. 小麦低聚肽制备凝固型酸奶及其发酵特性的研究[J]. 农产品加工, 2024(10): 39-42. DOI:10.16693/j.cnki.1671-9646(X).2024.10.010.
[61] 袁媛, 贾福怀, 熊菲菲, 等. 小麦低聚肽固体饮料对小鼠免疫功能的影响[J]. 农产品加工, 2019(9): 39-42. DOI:10.16693/j.cnki.1671-9646(X).2019.05.012.
[62] 高畅, 葛永喆, 魏月, 等. 牛磺酸-小麦肽复合饮料的研制及其体能恢复功效的研究[J]. 中国食品添加剂, 2022, 33(9): 104-112.DOI:10.19804/j.issn1006-2513.2022.09.015.
[63] LIU W Y, WU H S, LIU R, et al. Structural identification, stability and combination mechanism of calcium-chelating wheat gluten peptides[J].International Journal of Food Engineering, 2024, 20(5): 303-313.DOI:10.1515/ijfe-2023-0288.
[64] 关桦楠, 迟振东, 王东旭. 小麦低聚肽-纳米二氧化硅蛋白冠复合物的制备及其性能研究[J]. 食品与发酵工业, 2024, 50(11): 216-224.DOI:10.13995/j.cnki.11-1802/ts.035896.
[65] 刘睿, 王华蕾, 吴晗硕, 等. 小麦肽-维生素D微胶囊的稳定性及结构鉴定[J]. 食品科技, 2024, 49(5): 258-265; 274. DOI:10.13684/j.cnki.spkj.2024.05.035.
[66] 卢知浩, 刘放, 李嘉兴, 等. 玉米低聚肽-维生素D3和小麦低聚肽-维生素D3微胶囊的制备与表征[J]. 食品与发酵工业, 2023, 49(10):108-113; 121. DOI:10.13995/j.cnki.11-1802/ts.032083.
[67] LI W C, SHEN J, XU H J. Wheat protein-derived surfactants: synthesis and properties[J]. Journal of Surfactants and Detergents, 2024, 27(4):511-522. DOI:10.1002/jsde.12753.