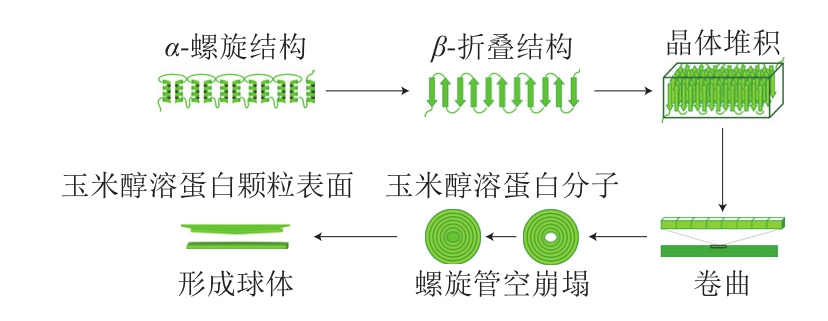
图1 玉米醇溶蛋白从单个分子自组装成微球的可能机制[17]
Fig. 1 Possible mechanism for zein self-assembly from single molecule to nanospheres[17]
随着食品工业的不断进步和生活水平的不断提高,人们对食品健康和营养更加关注,并尝试开发具有超出正常营养价值的创新型功能食品。功能性食品的开发依赖于通过生物活性物质的添加来赋予其独特的功能、保健性及期望的质地特性[1],如多酚、植物甾醇、维生素、矿物质、功能性脂类、生物活性肽、益生菌等[2-7]。然而,疏水性生物活性物质存在低水溶性、低生物利用度、在食品加工过程中易氧化或降解、在人类胃肠道消化反应中不稳定等局限性。因此应用食物载体对生物活性物质进行包埋来提高其稳定性和利用率尤为重要。
生物活性物质输送系统包括纳米颗粒、微球、微胶、脂质体、水凝胶、纤维、乳液、膜等类型,通过构建这些输送载体,可实现对包封物质的保护、提高难溶物质的溶解度和生物利用率、在食品中的兼容性[8]。载体材料主要包括合成的生物可降解高分子材料和天然高分子材料[9-10]。合成的高分子材料包括聚乳酸、DL-聚乳酸、聚乳酸-羟基乙酸共聚物等,但是这些通过化学合成的大部分载体在生物相容性、可降解性及细胞毒性等方面存在一些不足。用于包埋营养物质的天然生物材料主要包括蛋白质、糖类和脂质[11],其具有良好的生物兼容性、可降解性和低毒性,并且来源广泛,可被生物吸收,在营养递送领域具有广阔前景。
醇溶蛋白是禾本科作物种子中的一种主要贮存蛋白,是种子萌发时的主要碳源和氮源[12],它包括玉米醇溶蛋白、小麦醇溶蛋白、大麦醇溶蛋白和高粱醇溶蛋白等。这些醇溶蛋白不仅自身耐受消化、具有独特的自组装能力,而且对疏水性生物活性物质有较好亲和力。这些醇溶蛋白作为植物来源的天然生物高分子物质,因氨基酸组成不平衡,导致其不溶于水而溶于体积分数50%~90%乙醇溶液,因其具有的良好生物相容性和可降解性而成为现阶段食物载体的一大热点。
玉米醇溶蛋白是玉米中主要的贮存蛋白[13],玉米醇溶蛋白的平均分子质量约为44 000 Da,是由具有不同分子质量、溶解能力和电荷的肽链通过二硫键聚合而成的非均相混合物[14];其因含有大于50%的疏水氨基酸基团和较低含量的亲水性氨基酸,而表现出两亲特性[15]。
玉米醇溶蛋白由于两亲特性能够自组装成多种有序结构,了解玉米醇溶蛋白的自组装机制是探索其构建生物活性物质递送系统实际应用的关键。玉米醇溶蛋白的两亲特性是其进行自组装的主要驱动力[16]。Wang Yi等[17]发现玉米醇溶蛋白能够在醇溶液中自组装形成纳米粒、微球结构,并采用高分辨率透射电子显微镜(transmission electron microscope,TEM)研究其自组装过程,发现随着溶液极性的增强,玉米醇溶蛋白分子从α-螺旋结构转变为β-折叠构象,随着蒸发的继续,在疏水作用下β-折叠构象反向排列,自组装形成首尾相连的条带,条带通过卷曲最终形成纳米颗粒(图1)。

图1 玉米醇溶蛋白从单个分子自组装成微球的可能机制[17]
Fig. 1 Possible mechanism for zein self-assembly from single molecule to nanospheres[17]
小麦醇溶蛋白是一种天然的糖蛋白,约占小麦胚乳贮存蛋白总量的50%~60%,分子质量约为28~55 kDa,通过氢键、二硫键和分子内的疏水相互作用形成三维球状结构[18],含有大量的亲脂性氨基酸和中性氨基酸[19]。中性氨基酸可以促进其与黏膜的氢键相互作用,而亲脂性氨基酸可以与生物组织通过疏水相互作用而作用[20]。
小麦醇溶蛋白可分为α、β、γ、ω 4 种主要类型,其所占的比例分别为20%、30%、30%、15%。α、β、γ-醇溶蛋白结构相似,主要包括1 个含有大量脯氨酸和谷氨酸的N-端、1 个由半胱氨酸和带电残基组成的C-端以及中间重复区域;α-醇溶蛋白包含6 个半胱氨酸,可以形成3 个分子内二硫键;γ-醇溶蛋白包含8 个半胱氨酸,可以形成4 个分子内二硫键。ω-醇溶蛋白不含半胱氨酸,其结构主要以β转角为主,几乎没有α-螺旋和β-折叠结构,而α、β、γ-醇溶蛋白均存在该结构(表1)。小麦醇溶蛋白在水溶液中的溶解度很低,在体积分数70%的乙醇溶液中溶解性较好,这种低水溶性被认为是因为二硫键协同疏水相互作用导致蛋白质链呈折叠状[21]。小麦醇溶蛋白可与疏水性生物活性物质特异性结合,在消化道中以氢键、二硫键和疏水相互作用的方式与消化道内的黏蛋白结合,并且更甚趋向于黏附在上消化道黏膜上,因此使生物活性物质在消化道内的停留时间延长,吸收率提高[22]。此外,小麦醇溶蛋白中存在一定含量的色氨酸、亮氨酸等疏水性氨基酸,因此具有两亲性,该特性是小麦醇溶蛋白自组装的重要依据。
表1 小麦醇溶蛋白的性质[23]
Table 1 Some properties of gliadins[23]
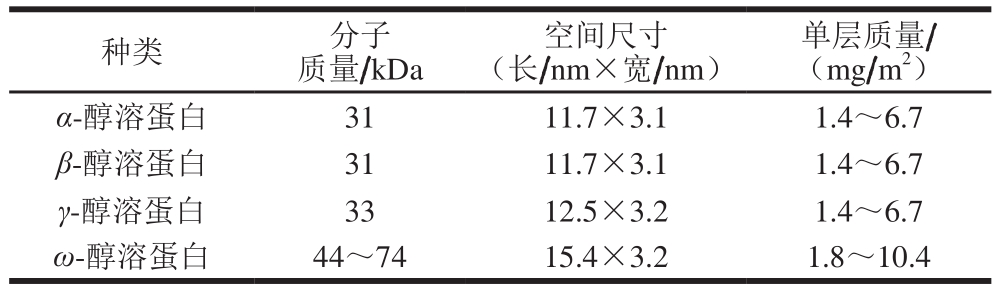
单层质量/(mg/m2)α-醇溶蛋白 31 11.7×3.1 1.4~6.7 β-醇溶蛋白 31 11.7×3.1 1.4~6.7 γ-醇溶蛋白 33 12.5×3.2 1.4~6.7 ω-醇溶蛋白 44~74 15.4×3.2 1.8~10.4种类 分子质量/kDa空间尺寸(长/nm×宽/nm)
大麦醇溶蛋白是大麦的主要贮存蛋白质,约占籽粒总蛋白含量的30%~50%,分子质量约为30~50 kDa[24]。大麦醇溶蛋白是从大麦中提取的疏水性蛋白质,存在大量的疏水性基团,在水中的溶解性低,能较好地溶解于70%乙醇溶液中,这些疏水性氨基酸残基易与二硫键形成局部疏水中心,水分子难以破坏蛋白质分子内部氢键,导致其易于形成稳定的高级结构区域[25-26],可应用于缓释材料载体。曹威[27]用X射线小角散射、动态光散射和动态流变仪研究了大麦醇溶蛋白在溶液中的构象和聚集行为,结果表明:在体积分数60%乙醇溶液中,大麦醇溶蛋白为细长的棒状结构,内部结构或聚集体构象呈高斯分布;蛋白结构紧凑、外部倾向于部分解折叠;随浓度增加,大麦醇溶蛋白有轻微的聚集现象;扫描电子显微镜(scanning electron microscope,SEM)观察结果显示大麦醇溶蛋白微粒呈光滑、扁平的球状,粒径在8~15 μm范围内(图2)。

图2 大麦醇溶蛋白的SEM图[27]
Fig. 2 Scanning electron microscope image of hordein[27]
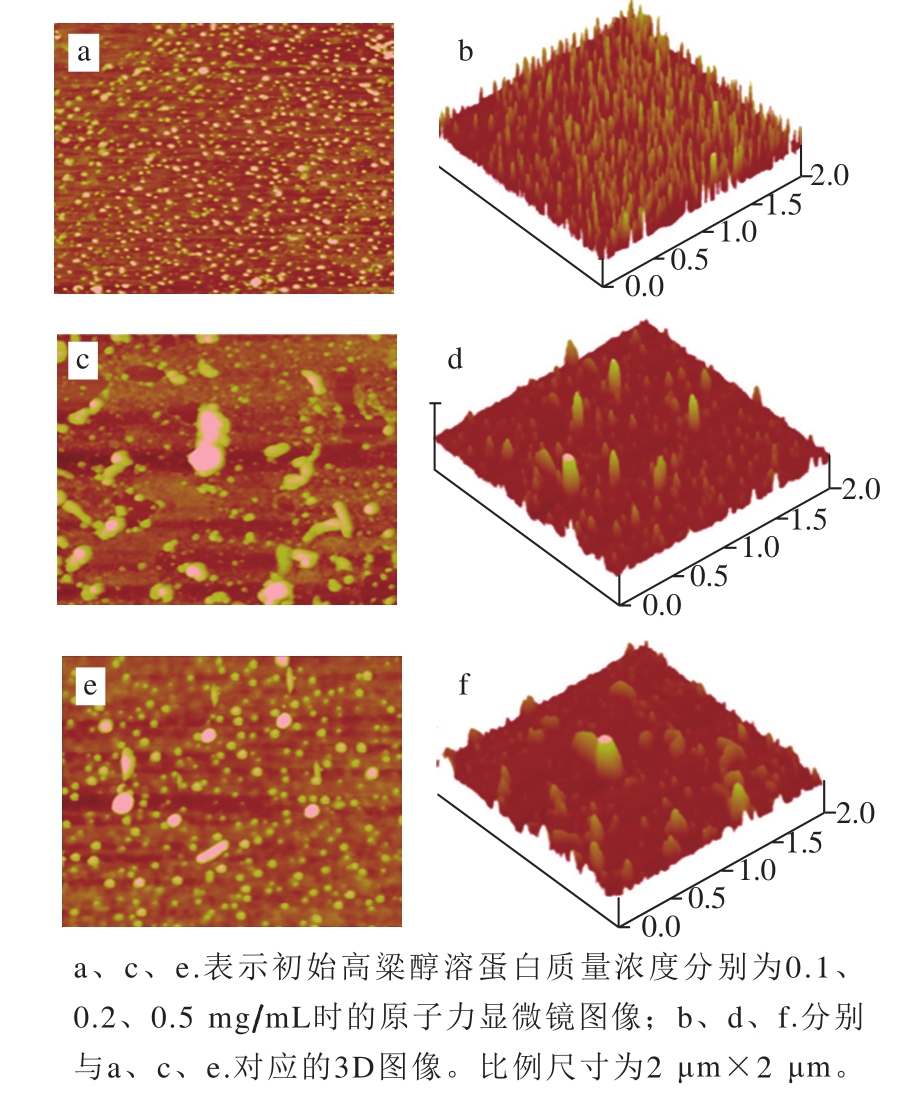
图3 高粱醇溶蛋白的形态[30]
Fig. 3 Morphology of kafirin[30]
高粱醇溶蛋白是高粱的主要贮存蛋白,约占高粱总蛋白的77%~82%[28]。高粱醇溶蛋白具有良好的生物相容性和可降解性[29],它与玉米醇溶蛋白在结构上有很大的相似性,Xiao Jie等[30]从高粱谷物中提取了高粱醇溶蛋白,其中α、β、γ-高粱醇溶蛋白和交联-高粱醇溶蛋白分别占总高粱醇溶蛋白的68%、14%、6%和12%,并用原子力显微镜观察高粱醇溶蛋白的形态和自组装过程,结果显示:在初始蛋白质量浓度为0.1 mg/mL时,高粱醇溶蛋白以椭球或圆盘状颗粒的形式均匀分散(图3a、b);当初始蛋白质量浓度增加到0.2 mg/mL时,除了单个球形颗粒外,开始出现大的圆盘状和棒状颗粒(图3c、d);当初始蛋白质量浓度进一步增加到0.5 mg/mL时,蛋白颗粒继续聚集,形成更大的圆盘状或杆状结构(图3e、f)。蛋白质的质量浓度和溶剂的极性可以影响高粱醇溶蛋白的自组装,因此通过改变蛋白质量浓度和溶剂极性是调节醇溶性生物材料原纤化的一种简便方式。
谷物醇溶蛋白诸多功能性质是蛋白质两大分子特性的体现,即表面性质和水动力学特性。表面性质包括吸湿特性、分散性、溶解性、起泡性、乳化性、保水性与保油性等,其由蛋白质表面的亲水/疏水及立体特征所决定;水动力学特性主要包括黏度、增稠、凝胶及组织化等功能特性,其主要与蛋白质分子质量、形状及分子柔顺性有关。醇溶蛋白的表面性质主要受氨基酸组成、分布以及折叠方式的影响,而水动力学特性更容易受到醇溶蛋白的物理形状和分子质量的制约(表2)。
表2 醇溶蛋白的功能特性
Table 2 Functional properties of prolamines

种类 功能特性玉米醇溶蛋白 溶解性、成膜性、黏结性、抗氧化性、阻油保水性、凝胶性[31]小麦醇溶蛋白 黏弹性、延展性及成膜性[32]大麦醇溶蛋白 水不溶性、流变性、延伸性、膨胀性、成膜性和胶凝性[33]高粱醇溶蛋白 弹性、成形性、高韧性、持油性、持水性[34]
醇溶蛋白的提取多采用有机溶剂提取法,利用在特定溶剂中溶解度的差异而完全或部分分离。常用的方法有超声辅助法、微波法、Obsorne法、超声波-微波辅助法等。任婷婷[35]采用超声辅助法提取玉米醇溶蛋白,通过正交试验确定其最优提取条件为:乙醇体积分数70%、超声波处理时间120 min、料液比1∶12、pH 11,玉米醇溶蛋白的提取率为86.6%。侯菲菲等[32]采用微波法提取小麦醇溶蛋白,通过设计单因素试验和正交优化试验确定微波法提取小麦醇溶蛋白的最佳工艺条件为:乙醇体积分数75%、料液比1∶25、微波提取时间120 s、微波功率450 W。刘丹等[34]采用超声辅助酶法制备高粱醇溶蛋白,通过建立二次多项的数学模型,优化得出高粱醇溶蛋白超声辅助酶法提取的最佳工艺条件为:加酶量1%、酶作用时间3 h、乙醇体积分数60%、超声波作用时间19 min。曹威等[36]采用Obsorne法提取大麦醇溶蛋白,结果表明最佳提取条件为:乙醇体积分数70%、液料比6∶1、温度25 ℃、提取时间2.0 h,所得大麦醇溶蛋白纯度为82.1%,提取率为2.95%。耿存花[37]利用超声波-微波辅助技术提取高粱醇溶蛋白,通过正交试验优化确定最佳提取条件为:超声功率、温度和时间分别是410 W、63 ℃和31 min,在此条件下高粱醇溶蛋白得率为7.80%。
醇溶蛋白微粒制备的方法主要反溶剂法、液-液分散法,新型方法有超临界反溶剂(supercritical antisolvent,SAS)法、电喷雾法、静电纺丝等方法。
反溶剂法是指在溶剂中加入反溶剂,使溶质溶解度下降,从而聚集成颗粒的方法。将醇溶蛋白溶解在体积分数55%~90%乙醇溶液中,混合溶液再均匀分散到水相中,使醇相浓度迅速降低,醇溶蛋白过饱和形成颗粒,关键影响因素有搅拌速度、时间、超声参数、醇溶蛋白浓度等。主要机理是:醇溶蛋白在不同溶剂条件下溶解度不同,当醇相浓度降低时,醇溶蛋白的溶解度降低,从而产生聚集和沉淀。液-液分散法是将醇溶蛋白溶解在某种溶剂中,使用超声或者磁力搅拌使其溶解完全,然后逐滴分散到分散液中,可自组装成纳米颗粒。
李晓晖等[38]采用反溶剂法制备姜黄素-高粱醇溶蛋白复合颗粒,对其理化性质及稳定性进行研究,结果表明:最佳芯壁比为1∶10,此条件下制备的复合纳米颗粒的平均粒径为13.17 μm,Zeta电位为19.38 mV,得率、包封率和负载率分别为87.51%、62.61%、6.51%,颗粒粒径均一、表面多微孔结构,并且紫外光稳定性提高了33%,用高粱醇溶蛋白包埋姜黄素不仅可以增强其自身抗氧化活性,而且提高了复合颗粒的稳定性。孔祥珍等[39]采用反溶剂法制备白藜芦醇-小麦醇溶蛋白纳米粒子,研究了乙醇体积分数、蛋白质量分数、分散液pH值、分散液盐浓度等因素对复合纳米粒子的粒径及Zeta电位的影响,结果表明:在乙醇体积分数为65%、蛋白质量分数为4%、分散液pH值为4.5、分散液盐浓度为0.00 mol/L时得到的小麦醇溶蛋白纳米粒子较理想,用其包埋白藜芦醇,发现芯壁比为1∶40时包埋率最高,为55.0%,载药率为1.5%;负载的白藜芦醇复合纳米粒子表面光滑、颗粒较小,表明小麦醇溶蛋白具有较好的包埋特性。朱美如等[40]采用反溶剂法制备芦丁-玉米醇溶蛋白复合颗粒,并以此为稳定剂制备Pickering乳液,研究了乳液的稳定性和抗氧化性,结果表明此方法可以有效使玉米醇溶蛋白对疏水活性物质芦丁进行高效包埋,不仅实现了复合纳米级颗粒的制备,还保留了芦丁的抗氧化活性,且玉米醇溶蛋白-芦丁纳米复合颗粒可以提高Pickering乳液的稳定性和抗氧化能力。王思琦等[41]采用液-液分散法制备阿魏酸-大麦醇溶蛋白复合纳米粒子,对复合颗粒进行多项表征,结果发现,当阿魏酸、大麦醇溶蛋白质量比为1∶5时,制得的复合纳米颗粒的粒径为(446.2±12.6)nm,Zeta电位为(16.65±0.20)mV,粒子的分散性良好,呈均匀规则的圆球状,包封率及负载率分别为28.35%、5.37%。
SAS法是一种制备醇溶蛋白传递系统的新型方法,相较于传统制备方法,SAS制备的醇溶蛋白颗粒粒径小、粒度分布可控、残余有机溶剂少、反应条件温和、包封率高。其原理是将溶质先溶于有机溶剂中形成溶液,再将溶液迅速喷洒在超临界流体(supercritical fluid,SCF)中,由于此溶液的溶质不溶于SCF,但溶剂却能与SCF互溶;因此,当溶液与SCF接触时,极短时间内可使溶液形成极大的过饱和度,促使溶质以纳米或微米颗粒析出(图4)。该法的关键控制因素是调节过程参数如温度、压力、流速等,从而可以达到控制颗粒粒径和晶型的目的。
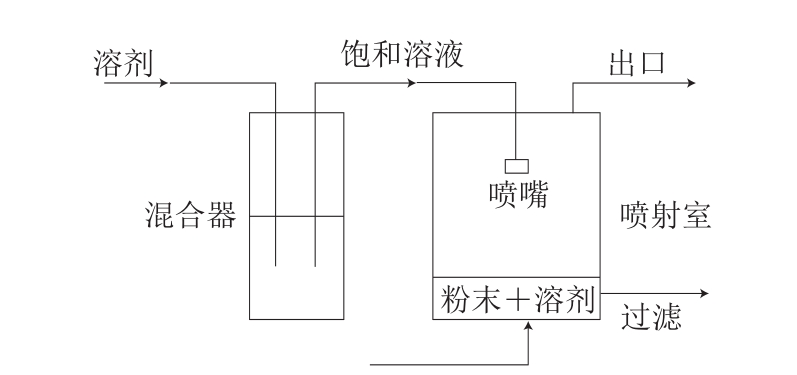
图4 SAS过程流程示意图
Fig. 4 Schematic diagram of supercritical anti-solvent process
Zhong Qixin等[42]使用玉米醇溶蛋白用作载体材料,并且使用体积分数90%乙醇溶液作为溶剂,采用SAS法微囊化鸡蛋清溶菌酶,所制得的复合微胶囊表面光滑、基质连续,置室温下36 d内可以观察到溶菌酶的释放规律,其中在pH 2~8磷酸盐缓冲液下释放较慢。研究表明SAS法可能是制备一般认为安全输送系统以提高抗菌功效的可行方法。
电喷雾法又称电流体驱动雾化法,可用来制备单分散纳米颗粒,与其他制备微胶囊的技术相比,电喷雾法具有诸多优势,如包埋率高、不需要耗时长的相分离过程,且易于获得较均一的不同粒径的颗粒。电喷雾的原理如下:流体在电场力和机械力的作用下发生喷射,分裂成细小的沉积滴,当电流体表面加上足够的电场力时,电场剪切力可以把在喷嘴外的液滴延长,从而形成射流和锥柱,由于流体表面电荷的加速,射流会进一步分裂成细小沉积滴。
Gomez-Estaca等[43]用电喷雾法制备了负载姜黄素的玉米醇溶蛋白纳米复合颗粒,包封效率约为85%~90%,姜黄素均匀分布在玉米醇溶蛋白基质中;X射线衍射图显示,姜黄素在纳米颗粒中保持无定形状态,证明其与玉米醇溶蛋白紧密接触;将得到的复合颗粒在23 ℃、相对湿度43%的黑暗条件中贮存3 个月后,颗粒的尺寸、形态及姜黄素含量的变化都不明显。
静电纺丝是一种利用高压电场产生的静电力形成射流,并快速固化制备纳米纤维的技术,其中高压电源输出电压为1~30 kV,聚合物溶液通过电场力从一个注射器针头引入收集器中,注射器中的溶液在静电场的作用下开始充电,并形成“泰勒锥”。当静电作用力能够克服液体表面张力的束缚时,“泰勒锥”流体开始喷出,形成射流。在静电作用力、表面张力、注射器推力以及重力等相互作用下,射流开始拉伸并发生旋转。随着溶剂的快速挥发,射流射向收集板并固化形成纳米纤维[44],具体原理见图5。
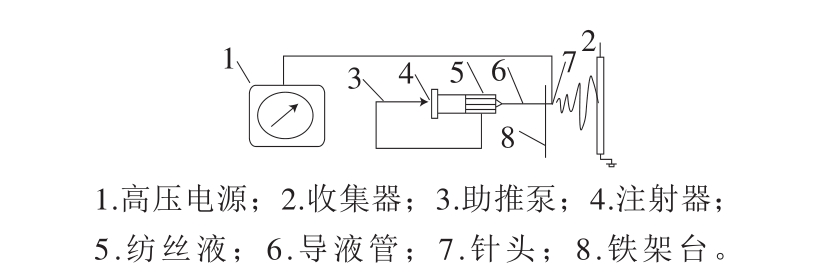
图5 静电纺丝过程原理图
Fig. 5 Schematic diagram of electrospinning process
Altan等[45]成功地通过静电纺丝将高挥发性香芹酚包埋在玉米醇溶蛋白和聚乳酸复合载体中,傅里叶变换红外光谱和热重分析结果表明,香芹酚被包埋在电纺玉米醇溶蛋白和聚乳酸纤维复合载体中;负载香芹酚的玉米醇溶蛋白纤维的抗氧化活性为62%~75%,而聚乳酸纤维的抗氧化活性仅为53%~65%。复合纤维膜显示出持续的扩散控制释放能力。因此,静电纺丝技术在食品和营养保健品、生物活性食品包装和食品加工行业具有良好的潜力。
类似于药物性质,通常所述的营养素具有疏水性。醇溶蛋白应用于营养物质输送体系优势体现在:提高食品生物活性成分的生物利用度、增强营养素的稳定性、提高精油的抗菌活性、保持食品着色剂的功效等方面。
3.1.1 多酚类物质
多酚类物质是植物化学成分中含量较丰富的一类化合物,具有较强的抗氧化活性,是人和动物膳食中所必需的营养物质,但其对氧气、光、酶、湿度、pH值等因素敏感,在贮藏环境或者胃肠道中易降解。多酚可以通过非共价相互作用,如氢键和疏水相互作用,与脯氨酸含量丰富的蛋白质发生强烈的相互作用[46-48],醇溶蛋白的包埋可以为其提供保护。
黄旭琳等[49]利用反溶剂法和静电沉积法制备负载姜黄素的核/壳型复合纳米颗粒,得到的纳米颗粒为表面光滑的球形,平均粒径为133 nm,对1,1-二苯基-2-三硝基苯肼自由基的清除率明显高于姜黄素乙醇溶液,但纳米颗粒的抑菌效果较差;纳米颗粒包埋的姜黄素消化吸收率较与纳米颗粒组分完全相同的姜黄素-玉米醇溶蛋白-果胶的混合物中姜黄素消化吸收率提高了4 倍。因此,纳米颗粒包埋的姜黄素具有较高的抗氧化活性及消化吸收率,在功能性食品及药物方面有良好的应用前景。Yang Shufang等[50]采用反溶剂沉淀法制备了负载姜黄素的小麦醇溶蛋白和卵磷脂的复合纳米颗粒,结果表明小麦醇溶蛋白-卵磷脂复合纳米粒子明显提高了纳米粒子中姜黄素的包封效率、紫外光和热稳定性、抗氧化活性。
3.1.2 油脂
油脂难溶于水,且通常不稳定,易氧化造成风味损失、生物活性降低,甚至产生有毒有害物质。醇溶蛋白不溶于水,能够吸附油脂,可用于包埋油脂,提高其生物利用率。
Chen Yu等[51]用反溶剂法制备柠檬烯-玉米醇溶蛋白-酪蛋白酸钠微胶囊,观察到在微胶囊的破壁释放阶段,柠檬烯的释放速率明显低于柠檬烯-乳清分离蛋白微胶囊中柠檬烯的释放速率;在持续释放阶段,柠檬烯的释放速率趋于平缓,符合零级动力学;微胶囊在加速贮存条件(室温搅拌)下,柠檬烯的保留率高于乳清分离蛋白稳定乳液中的柠檬烯的保留率,这是由于微胶囊的玉米醇溶蛋白-酪蛋白酸钠壳层存在固体阻隔作用。Wu Yunpeng等[52]使用液-液分散方法将具有相似化学结构的两种精油(百里酚和香芹酚)包封在玉米醇溶蛋白的纳米颗粒中,在玉米醇溶蛋白纳米颗粒中包封精油可以将其溶解度提高14 倍,且不会降低它们清除自由基和抑制大肠杆菌生长的能力。在另一项研究中,用玉米醇溶蛋白包裹的百里酚纳米粒子在酪蛋白酸盐和盐酸壳聚糖盐的双层稳定作用下,在较长时间内具有更强的抗微生物作用[53]。
3.1.3 益生菌
益生菌是一类对宿主有益的活性微生物,定植于人体肠道、生殖系统内,对改善宿主肠道微生态具有重要作用作用。在食品工业中,牛奶、饮料、冷冻酸奶、奶酪、冰淇淋、乳酱、发酵豆制品的生产中常伴随着大量益生菌的生产。由于益生菌对环境敏感,不易存活,因此,在生产过程中需要对益生菌提供一定的保护,有研究报道包埋技术能实现这一目的[54]。
Laelorspoen等[55]将益生菌包埋在通过电喷雾形成的藻酸盐微胶囊中,提高了嗜酸乳杆菌在胃液中的存活率,再用柠檬酸改性的玉米醇溶蛋白包埋,从而形成含有嗜酸乳杆菌的藻酸盐-玉米醇溶蛋白核-壳微胶囊;研究了柠檬酸浓度以及电喷雾条件对获得的核壳微胶囊形态、包封细胞计数和孵化后存活细胞数的影响。结果表明,柠檬酸浓度的增加不影响核-壳微胶囊粒径大小及粒径分布,但包封的嗜酸乳杆菌活细胞数显著降低,然而,随着玉米醇溶蛋白溶液酸度的增加,存活细胞数显著减少。将包埋微粒在模拟胃液中消化2 h,包埋的嗜酸乳杆菌仅减少1(lg(CFU/mL)),而未包埋的细菌数量减少约5(lg(CFU/mL))。
近年来,制备聚合物-聚合物复合物的递送系统也备受关注[56-57]。聚合物-聚合物复合物递送系统涉及不同作用机制,包括静电相互作用、疏水相互作用、氢键和范德华力。醇溶蛋白作为弱聚合电解质,与其他生物聚合物(多糖或蛋白质)通过疏水相互作用和氢键形成复合物。研究人员在制备微米级玉米醇溶蛋白输送体系,或在不同pH值下采用悬浮剂制备玉米醇溶蛋白纳米粒子时,发现冷冻干燥后的纳米粒子复溶会产生大量聚集的现象[42]。此外有研究发现,相对于微米级别的粒子,纳米粒子更易受pH值、温度以及盐离子浓度等条件的影响,这些因素会导致蛋白质发生聚集,粒子变得不稳定[58-59];酪蛋白酸钠具有乳化活性、热稳定性、水溶性等特性,其与小麦醇溶蛋白、玉米醇溶蛋白等混合可形成具有良好形态特征的粒子,被视作荷载活性物质的潜力材料。Xue Jinli等[60]采用液-液分散法制备了玉米醇溶蛋白-酪蛋白酸钠复合纳米颗粒,并成功包埋姜黄素,分别使用粒径和Zeta电位仪、TEM、差示扫描量热仪等对复合纳米粒子进行表征,结果表明,复合纳米颗粒呈球状,平均粒径、多分散指数、Zeta电位分别为187.16 nm、0.13、36.43 mV,在水中具有理想的再分散性;玉米醇溶蛋白酪蛋白酸钠复合纳米粒子能够改善姜黄素的水溶性,提高其对热和紫外线照射的稳定性和生物利用度。有研究者加入酪蛋白或表面活性剂来改善复合纳米体系的稳定性与再分散性,Liu Chengzhen等[61]制备小麦醇溶蛋白和酪蛋白混合蛋白负载原花青素的复合纳米颗粒,探究了蛋白和原花青素的比例、蛋白浓度、氯化钠浓度、pH值和时间对复合纳米颗粒表征的影响,结果表明,在最优条件下,通过TEM观察到复合纳米粒子呈现粒径约30 nm的规则形状,其抗氧化能力分别比纯原花青素在氯化钠(0.8 mol/L)、紫外线辐射(10 W)和加热处理(80 ℃、30 min)条件下提高了12%、26%和14%;因此醇溶蛋白和酪蛋白的聚合物可以作为原花青素的保护性载体。
一些研究表明多糖与蛋白质相互作用可用于改善蛋白质纳米粒子对环境的稳定性。Li Hao等[62]在pH 4.0时成功制备了玉米醇溶蛋白-可溶性大豆多糖(soluble soybean polysaccharide,SSPS)负载槲皮素的复合纳米粒子,结果发现,SSPS可以在pH 2.0~8.0下有效稳定玉米醇溶蛋白纳米颗粒的聚集;复合纳米颗粒通过静电、氢键和疏水相互作用形成,在盐、热和长期贮存中表现出良好的稳定性;SSPS作为一种稳定剂能够调节玉米醇溶蛋白纳米粒子的表面疏水性;SSPS的存在显著提高了纳米粒子的包封效率和光化学稳定性,玉米醇溶蛋白-SSPS纳米粒子具有很大的潜力,可用作生物活性化合物的纳米递送系统。黄旭琳等[49]利用静电沉积法将果胶吸附到纳米颗粒表面,利用果胶羧基基团的静电排斥稳定纳米颗粒,制得的纳米颗粒具有较好的水分散性,用海藻酸钠替代部分果胶,制备负载姜黄素的玉米醇溶蛋白-多糖复合纳米颗粒,研究纳米颗粒包埋的姜黄素清除自由基能力及抗菌活性,并以模拟消化液研究姜黄素的生物利用度。结果表明,纳米颗粒负载的姜黄素比乙醇溶解的姜黄素具有更高的清除1,1-二苯基-2-三硝基苯肼自由基能力,从而说明纳米颗粒负载姜黄素对提高其抗氧化活性是有效的。
为改善醇溶蛋白/壳聚糖复合物输送体系,常采用水溶性壳聚糖衍生物即羧甲基壳聚糖取代壳聚糖。Xiao Jie等[30]分别制备了负载姜黄素的高粱醇溶蛋白纳米颗粒和负载姜黄素的羧甲基壳聚糖-高粱醇溶蛋白复合纳米颗粒,两种纳米颗粒都呈球形,通过动态光散射和原子力显微镜观察,羧甲基壳聚糖-高粱醇溶蛋白负载姜黄素的纳米颗粒平均粒径较大,这两种颗粒包封率和负载率分别为(55.0±1.1)%、(5.0±0.1)%和(86.1±2.1)%、(6.1±0.2)%。与天然姜黄素相比,添加羧甲基壳聚糖复合纳米颗粒光稳定性显着改善,并且在胃肠道中有较好的溶出曲线以及有效的细胞摄取行为(表3)。
表3 不同聚合物与醇溶蛋白形成的复合体系
Table 3 Composite systems of different polymers and prolamines

醇溶蛋白种类 聚合物 包埋物质 参考文献玉米醇溶蛋白 酪蛋白酸钠 姜黄素 Xue Jinli等[60]小麦醇溶蛋白 酪蛋白 原花青素 Liu Chengzhen等[61]玉米醇溶蛋白 SSPS 槲皮素 Li Hao等[62]玉米醇溶蛋白 多糖 姜黄素 黄旭琳等[49]高粱醇溶蛋白 羧甲基壳聚糖 姜黄素 Xiao Jie等[30]
疏水性生物活性物质由于其溶解度低而不易被人体吸收,可通过构建醇溶蛋白荷载食品功能组分的微粒来提高其在人体胃肠道中的消化率,并且探究其释放规律。田倚凡等[63]采用反溶剂法制备萝卜硫素-玉米醇溶蛋白纳米水分散体,对其理化性质及萝卜硫素的释放特性进行了研究,结果显示,在模拟胃液中时,萝卜硫素、玉米醇溶蛋白质量比为1:25的纳米水分散体在0~60 min内,萝卜硫素的累计释放率接近50%,0~120 min内累计释放率接近80%,此释放类型为快速释放型;120~240 min,在模拟小肠液中,纳米水分散体中萝卜硫素的累计释放率将近95%,释放实验结果表明,玉米醇溶蛋白纳米颗粒中的萝卜硫素为快速释放型。Cheng等[64]制备了包埋叶黄素的玉米醇溶蛋白纳米颗粒,并且对其进行体外胃肠模拟消化。结果表明,叶黄素包埋到玉米醇溶蛋白纳米颗粒中后,消化稳定性提高。黄旭琳等[49]采用反溶剂法和静电沉积法制备负载姜黄素的核/壳型复合纳米颗粒,采用模拟体外消化实验测定消化吸收率,结果显示,纳米颗粒包埋的姜黄素经消化后在消化液中的浓度是未进行包埋的同组分混合物消化后的4 倍,这充分说明经过纳米颗粒包埋的姜黄素能更有效地释放到消化液中从而被人体吸收。
醇溶蛋白在开发具有应用前景的食物载体、保护各种疏水性生物活性物质以及提高这些生物活性物质的稳定性和生物利用率方面具有巨大潜力。醇溶蛋白可以被广泛用于制备多种微米或纳米颗粒、纤维、薄膜、水凝胶等。随着人们对功能性食品的广泛关注,基于醇溶蛋白的先进传递系统的发展将扩大其应用范围。然而,对于功能性成分复杂的食物系统中制备传递系统具有一定的挑战性,因为这不仅需要考虑到功能性食品复杂基质的稳定性和生物利用度,还需保证食品的质地、味道、外观和成分。此外,尽管用于制备传递系统的方法在实验室规模上取得了成功,但在食品工业大规模生产中仍然存在局限性和困难;因此,大规模生产纳米级输送系统的新技术是未来研究的另一个问题。未来该领域的发展方向是设计多种稳定剂与醇溶蛋白制成复合颗粒,该颗粒可同时用于多种目的,如功能性成分传递和食品分散(如乳剂和泡沫)界面稳定。最后,醇溶蛋白载体材料在体内的毒性还不明确,需要对这些醇溶蛋白传递系统进行更多的体内评估,以了解它们在人类胃肠道中的生物学命运以及它们在生理条件下的有效性和安全性。
[1] ZUIDAM N J, VELIKOV K P. Choosing the right delivery systems for functional ingredients in foods: an industrial perspective[J].Current Opinion in Food Science, 2018, 21: 15-25. DOI:10.1016/j.cofs.2018.04.007.
[2] GHAYOUR N, HOSSEINI S M H, ESKANDARI M H, et al.Nanoencapsulation of quercetin and curcumin in casein-based delivery systems[J]. Food Hydrocolloids, 2018, 87: 394-403. DOI:10.1016/j.foodhyd.2018.08.031.
[3] REINECCIUS G. Use of proteins for the delivery of flavours and other bioactive compounds[J]. Food Hydrocolloids, 2018, 86: 62-69.DOI:10.1016/j.foodhyd.2018.01.039.
[4] OZKAN G, FRANCO P, DE MARCO I, et al. A review of microencapsulation methods for food antioxidants: principles,advantages, drawbacks and applications[J]. Food Chemistry, 2019,272: 494-506. DOI:10.1016/j.foodchem.2018.07.205.
[5] ADITYA N P, ESPINOSA Y G, NORTON I T. Encapsulation systems for the delivery of hydrophilic nutraceuticals: food application[J].Biotechnology Advances, 2017, 35(4): 450-457. DOI:10.1016/j.biotechadv.2017.03.012.
[6] DHAVAL A, YADAV N, PURWAR S. Potential applications of food derived bioactive peptides in management of health[J]. International Journal of Peptide Research and Therapeutics, 2016, 22(3): 377-398.DOI:10.1007/s10989-016-9514-z.
[7] ZHU F. Encapsulation and delivery of food ingredients using starch based systems[J]. Food Chemistry, 2017, 229: 542-552. DOI:10.1016/j.foodchem.2017.02.101.
[8] 王丽娟. 玉米醇溶蛋白胶体颗粒的制备及应用研究[D]. 广州: 华南理工大学, 2014: 1-5.
[9] ZHAO J, WENG G J, LI J J, et al. Polyester-based nanoparticles for nucleic acid delivery[J]. Materials Science and Engineering: C, 2018,92(1): 983-994. DOI:10.1016/j.msec.2018.07.027.
[10] KUMAR B, JALODIA K, KUMAR P, et al. Recent advances in nanoparticle-mediated drug delivery[J]. Journal of Drug Delivery Science and Technology, 2017, 41: 260-268. DOI:10.1016/j.jddst.2017.07.019.
[11] 蒋姗姗. 玉米醇溶蛋白微粒的制备工艺研究[D]. 杭州: 浙江大学,2017: 1-4.
[12] 臧珉, 单承莺, 马翼飞, 等. 谷物醇溶蛋白研究进展[J]. 中国野生植物资源, 2017, 36(4): 46-49. DOI:10.3969/j.issn.1006-9690.2017.04.010.
[13] DAI L, SUN C X, WANG D, et al. The interaction between zein and lecithin in ethanol-water solution and characterization of zein-lecithin composite colloidal nanoparticles[J]. PLoS ONE, 2016, 11(11): 167-172. DOI:10.1371/journal.pone.0167172.
[14] SHUKLA R, CHERYAN M. Zein: the industrial protein from corn[J].Industrial Crops and Products, 2001, 13(3): 171-192. DOI:10.1016/S0926-6690(00)00064-9.
[15] 许辰琪, 袁芳, 高彦祥. 玉米醇溶蛋白作为传递载体研究进展[J]. 中国食品添加剂, 2015, 6(7): 156-161. DOI:10.3969/j.issn.1006-2513.2015.07.018.
[16] LÖWIK D W P M, VAN HEST J C M. Peptide based amphiphiles[J].Chemical Society Reviews, 2004, 33(4): 234-245. DOI:10.1039/B212638A.
[17] WANG Yi, PADUA G W. Nanoscale characterization of zein self-assembly[J]. Langmuir, 2012, 28(5): 2429-2435. DOI:10.1021/la204204j.
[18] 马永强, 韩春然, 石忠志. 小麦醇溶蛋白的研究进展[J]. 食品科学,2006, 27(12): 813-817. DOI:10.3321/j.issn:1002-6630.2006.12.212.
[19] ARANGOA M A, CAMPANERO M A, RENEDO M J, et al. Gliadin nanoparticles as carriers for the oral administration of lipophilic drugs. relationships between bioadhesion and pharmacokinetics[J].Pharmaceutical Research, 2002, 18(11): 1521-1527. DOI:10.1023/A:1013018111829.
[20] ARANGOA M A, PONCHEL G, ORECCHIONI A M, et al.Bioadhesive potential of gliadin nanoparticulate systems[J].European Journal of Pharmaceutical Sciences, 2000, 11(4): 333-341.DOI:10.1016/S0928-0987(00)00121-4.
[21] WU W H, KONG X Z, ZHANG C M, et al. Improving the stability of wheat gliadin nanoparticles: effect of gum arabic addition[J]. Food Hydrocolloids, 2018, 80: 78-87. DOI:10.1016/j.foodhyd.2018.01.042.
[22] EZPELETA I, ARANGOA M A, IRACHE J M, et al. Preparation of Ulex europaeus lectin-gliadin nanoparticle conjugates and their interaction with gastrointestinal mucus[J]. International Journal of Pharmaceutics, 1999, 191(1): 25-32. DOI:10.1016/S0378-5173(99)00232-X.
[23] ORNEBRO J, WAHLGREN M, ELIASSON A C, et al. Adsorption of α-, β-, γ- and ω-gliadins onto hydrophobic surfaces[J]. Journal of Cereal Science,1999, 30(2): 105-114. DOI:10.1006/jcrs.1999.0270.
[24] ZHAO J, TIAN Z, CHEN L. Effects of deamidation on structure and functional properties of barley hordein[J]. Journal of Agricultural and Food Chemistry, 2010, 58(21): 11448-11455. DOI:10.1021/jf102307f.
[25] WEDEMEYER W J, WELKER E, NARAYAN M, et al. Disulfide bonds and protein folding[J]. Biochemistry, 2000, 39(15): 4207-4216.DOI:10.1021/bi005111p.
[26] HOGG P J. Disulfide bonds as switches for protein function[J]. Trends in Biochemical Sciences, 2003, 28(4): 210-214. DOI:10.1016/S0968-0004(03)00057-4.
[27] 曹威. 大麦醇溶蛋白的提取、性质及成膜研究[D]. 武汉: 武汉轻工大学, 2015: 27-40.
[28] BELTON P S, DELGADILLO I, HALFORD N G, et al. Kafirin structure and functionality[J]. Journal of Cereal Science, 2006, 44(3):272-286. DOI:10.1016/j.jcs.2006.05.004.
[29] 张伟敏, 谭小蓉, 钟耕. 高粱蛋白质研究进展[J]. 粮食与油脂,2005(1): 7-9. DOI:10.3969/j.issn.1008-9578.2005.01.002.
[30] XIAO Jie, LI Yunqi, LI Ji, et al. Structure, morphology, and assembly behavior of kafirin[J]. Journal of Agricultural and Food Chemistry,2015, 63(1): 216-224. DOI:10.1021/jf504674z.
[31] 王香丽, 刘洁, 吕宁, 等. 玉米醇溶蛋白在食品中的应用[J]. 粮食与饲料工业, 2018(1): 33-36; 45.
[32] 侯菲菲, 张泽英. 微波法提取小麦醇溶蛋白的工艺优化[J]. 现代食品, 2018(16): 147-150.
[33] ZHAO J, TIAN Z G, CHEN L Y. Effects of deamidation on the molecular structures and functional properties of barley hordein[J].Journal of Chinese Institute of Food Science and Technology, 2010,58(21): 11448-11455.
[34] 刘丹, 刘剑利, 王帅, 等. 高粱醇溶蛋白提取工艺及其功能特性研究[J].食品与机械, 2017, 33(11): 173-178.
[35] 任婷婷. 玉米蛋白的提取、功能特性及应用研究[D]. 石家庄: 河北科技大学, 2014: 11-21. DOI:10.7666/d.Y2534326.
[36] 曹威, 李芳, 黄庆荣. 大麦醇溶蛋白的提取及其理化性质研究[J]. 粮食加工, 2015, 40(4): 40-43.
[37] 耿存花. 高粱醇溶蛋白的提取及应用研究[D]. 长春: 吉林农业大学,2014: 9-18.
[38] 李晓晖, 黄文娟, 周伟, 等. 反溶剂法制备姜黄素-高粱醇溶蛋白复合颗粒及其特性分析[J]. 食品科学, 2018, 39(6): 7-12. DOI:10.7506/spkx1002-6630-201806002.
[39] 孔祥珍, 黄飞, 周治彤, 等. 小麦醇溶蛋白自组装纳米粒子负载白藜芦醇的性质研究[J]. 中国粮油学报, 2017, 32(11): 21-25.DOI:10.3969/j.issn.1003-0174.2017.11.004.
[40] 朱美如, 潘贯珠. 玉米醇溶蛋白-芦丁复合纳米颗粒制备Pickering乳液及其特性研究[J]. 粮食与油脂, 2018, 31(5): 43-47. DOI:10.3969/j.issn.1008-9578.2018.05.013.
[41] 王思琦, 李律. 阿魏酸-大麦醇溶蛋白复合纳米粒子的制备及其性质的研究[J]. 食品与发酵科技, 2016, 52(3): 11-14.
[42] ZHONG Qixin, JIN Minfeng, DAVIDSON P M, et al. Sustained release of lysozyme from zein microcapsules produced by a supercritical anti-solvent process[J]. Food Chemistry, 2009, 115(2):697-700. DOI:10.1016/j.foodchem.2008.12.063.
[43] GOMEZ-ESTACA J, BALAGUER M P, GAVARA R, et al. Formation of zein nanoparticles by electrohydrodynamic atomization: effect of the main processing variables and suitability for encapsulating the food coloring and active ingredient curcumin[J]. Food Hydrocolloids, 2012,28(1): 82-91. DOI:10.1016/j.foodhyd.2011.11.013.
[44] LIU G D, GU Z B, HONG Y, et al. Electrospun starch nanofibers:Recent advances, challenges, and strategies for potential pharmaceutical applications[J]. Journal of Controlled Release, 2017,252: 95-107. DOI:10.1016/j.jconrel.2017.03.016.
[45] ALTAN A, AYTAC Z, UYAR T. Carvacrol loaded electrospun fibrous films from zein and poly(lactic acid) for active food packaging[J]. Food Hydrocolloids, 2018, 81: 48-59. DOI:10.1016/j.foodhyd.2018.02.028.
[46] LU Y, BENNICK A. Interaction of tannin with human salivary proline-rich proteins[J]. Archives of Oral Biology, 1998, 43(9): 717-728.DOI:10.1016/S0003-9969(98)00040-5.
[47] SIEBERT K J, TROUKHANOVA N V, LYNN P Y. Nature of polyphenol-protein interactions[J]. Journal of Agricultural and Food Chemistry, 1996, 44(1): 80-85. DOI:10.1021/jf9502459.
[48] EMMAMBUX N M, TAYLOR J R N. Sorghum kafirin interaction with various phenolic compounds[J]. Journal of the Science of Food and Agriculture, 2003, 83(5): 402-407. DOI:10.1002/jsfa.1379.
[49] 黄旭琳, 黄晓霞, 钟南京, 等. 负载姜黄素的玉米醇溶蛋白-多糖纳米颗粒的制备及生物活性研究[J]. 广东药学院学报, 2016, 32(5):545-549.
[50] YANG Shufang, DAI Lei, SUN Cuixia, et al. Characterization of curcumin loaded gliadin-lecithin composite nanoparticles fabricated by antisolvent precipitation in different blending sequences[J]. Food Hydrocolloids, 2018, 85: 185-194. DOI:10.1016/j.foodhyd.2018.07.015.
[51] CHEN Yu, SHU Meng, YAO Xiaoxue, et al. Effect of zein-based microencapsules on the release and oxidation of loaded limonene[J]. Food Hydrocolloids, 2018, 84: 330-336. DOI:10.1016/j.foodhyd.2018.05.049.
[52] WU Yunpeng, LUO Yaguang, WANG Qin. Antioxidant and antimicrobial properties of essential oils encapsulated in zein nanoparticles prepared by liquid-liquid dispersion method[J].LWT-Food Science and Technology, 2012, 48(2): 283-290.DOI:10.1016/j.lwt.2012.03.027.
[53] ZHANG Y Q, NIU Y G, LUO Y C, et al. Fabrication, characterization and antimicrobial activities of thymol-loaded zein nanoparticles stabilized by sodium caseinate-chitosan hydrochloride double layers[J]. Food Chemistry, 2014, 142: 269-275. DOI:10.1016/j.foodchem.2013.07.058.
[54] CRITTENDEN R, SANGUANSRI L, AUGUSTIN M A. Probiotic storage and delivery: US8871266[P/OL]. 2014-10-28[2018-08-11].http://www.google.co.in/patents/US8871266.
[55] LAELORSPOEN N, WONGSASULAK S, YOOVIDHYA T, et al.Microencapsulation of Lactobacillus acidophilus in zein-alginate core-shell microcapsules via electrospraying[J]. Journal of Functional Foods, 2014, 7: 342-349. DOI:10.1016/j.jff.2014.01.026.
[56] LUO Y C, WANG Q. Recent advances of chitosan and its derivatives for novel applications in food science[J]. Journal of Food Processing &Beverages, 2013, 1(1): 1-13.
[57] LUO Y C, WANG Q. Recent development of chitosan-based polyelectrolyte complexes with natural polysaccharides for drug delivery[J]. International Journal of Biological Macromolecules, 2014,64: 353-367. DOI:10.1016/j.ijbiomac.2013.12.017.
[58] JOYE I J, NELIS V A, MCCLEMENTS D J. Gliadin-based nanoparticles: fabrication and stability of food-grade colloidal delivery systems[J]. Food Hydrocolloids, 2015, 44: 86-93. DOI:10.1016/j.foodhyd.2014.09.008.
[59] JOYE I J, NELIS V A, MCCLEMENTS D J. Gliadin-based nanoparticles: stabilization by post-production polysaccharide coating[J]. Food Hydrocolloids, 2015, 43: 236-242. DOI:10.1016/j.foodhyd.2014.05.021.
[60] XUE Jinli, ZHANG Yaqiong, HUANG Guoren, et al. Zein-caseinate composite nanoparticles for bioactive delivery using curcumin as a probe compound[J]. Food Hydrocolloids, 2018, 83: 25-35.DOI:10.1016/j.foodhyd.2018.04.037.
[61] LIU Chengzhen, LI Man, YANG Jie, et al. Fabrication and characterization of biocompatible hybrid nanoparticles from spontaneous co-assembly of casein/gliadin and proanthocyanidin[J].Food Hydrocolloids, 2017, 73: 74-89. DOI:10.1016/j.foodhyd.2017.06.036.
[62] LI Hao, WANG Dongfeng, LIU Chengzhen, et al. Fabrication of stable zein nanoparticles coated with soluble soybean polysaccharide for encapsulation of quercetin[J]. Food Hydrocolloids, 2018, 87: 342-351.DOI:10.1016/j.foodhyd.2018.08.002.
[63] 田倚凡, 陈芳, 谭小路, 等. 萝卜硫素-玉米醇溶蛋白纳米水分散体制备及性质[J]. 食品与发酵工业, 2019, 45(1): 121-127. DOI:10.13995/j.cnki.11-1802/ts.017077.
[64] CHENG C J, MARIOF, JONES O G. Fate of lutein-containing zein nanoparticles following simulated gastric and intestinal digestion[J]. Food Hydrocolloids, 2019, 87: 229-236. DOI:10.1016/j.foodhyd.2018.08.013.
Recent Progress in Prolamines as a Food Nutrient Carrier
黄慧, 李学艳, 王君文, 等. 醇溶蛋白荷载食品功能组分的研究进展[J]. 食品科学, 2019, 40(19): 318-325. DOI:10.7506/spkx1002-6630-20181008-049. http://www.spkx.net.cn
HUANG Hui, LI Xueyan, WANG Junwen, et al. Recent progress in prolamines as a food nutrient carrier[J]. Food Science, 2019,40(19): 318-325. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-20181008-049. http://www.spkx.net.cn